Holger Petri, Bad Wildungen*
In der immunsuppressiven Therapie werden zur Verstärkung der Wirksamkeit bei gleichzeitiger Reduktion der Nebenwirkungen Arzneimittel mit unterschiedlichem Wirkprofil kombiniert [22]. Bei Autoimmunerkrankungen und Organtransplantationen werden im Wesentlichen Glucocorticoide und Hemmstoffe der DNA-Biosynthese (Zytostatika) sowie selektiv wirkende Inhibitoren der Calcineurin-Aktivierung und mTOR-Inhibtoren (mTOR: mechanistic [synonym: mammalian] target of rapamycin) eingesetzt.
Calcineurin-Inhibitoren (CNI)
Ciclosporin
Ciclosporin wird hauptsächlich über das Cytochrom-P450(CYP)-Isoenzym 3A4 abgebaut [10].
In Studien an transplantierten Patienten reduzierten die beiden starken CYP3A4-Inhibitoren (Abb. 1) Ketoconazol und Clarithromycin den Dosisbedarf von Ciclosporin um 85 % bzw. 59 % [14, 17]. Telaprevir erhöhte bei gesunden Probanden die AUC (Fläche unter der Konzentrations-Zeit-Kurve) von Ciclosporin um das 4,6-Fache [13]. Unter Erythromycin stiegen die AUC-Werte in einer Untersuchung um durchschnittlich das 2,4-Fache, gemäß Herstellerangabe kann der Ciclosporin-Plasmaspiegel um das 4- bis 7-Fache steigen [10, 12]. Fluconazol und Voriconazol können die AUC-Werte des Calcineurin-Inhibitoren um das 1,8- bzw. 1,7-Fache erhöhen [5, 29]. Ritonavir in niedriger Dosis erhöht als pharmakokinetischer Booster die Plasmaspiegel anderer antiretroviraler Arzneimittel, indem es deren Abbau durch die starke CYP3A4-Hemmung verzögert. Die Kombination aus Paritaprevir, Ritonavir, Ombitasvir und Dasabuvir erhöhte den AUC-Wert von Ciclosporin um das 5,8-Fache. In einer anderen Studie mit HIV-infizierten Patienten wurde die Ciclosporin-Tagesdosis in Kombination mit Lopinavir und Ritonavir auf 5 bis 20 % der ursprünglichen Dosis gesenkt [1, 33]. Bei einem Patienten unter der Kombination Amprenavir/Ritonavir wurde die Ciclosporin-Dosis auf ein Zwölftel der ursprünglichen Dosis (von 600 mg auf 50 mg täglich) reduziert [15]. Die Fachinformationen Ciclosporin-haltiger Arzneimittel weisen auf die Wechselwirkung mit Ritonavir-haltigen Virustatika jedoch nicht hin [10].
Inhaltsstoffe des Grapefruitsafts hemmen intestinale CYP-Enzyme [28]. In einer Studie erhöhte sich die Bioverfügbarkeit des oral eingenommenen Immunsuppressivums um 62 % [6].
Ciclosporin ist ein Substrat des Effluxtransporters P-Glykoprotein (P-gp). Die beiden Calciumkanalblocker Diltiazem und Verapamil sind moderate CYP3A4-Inhibitoren, Verapamil hemmt zusätzlich P-gp [27]. Diltiazem kann die Ciclosporin-Plasmakonzentration um 50 % erhöhen, Verapamil um das 2- bis 3-Fache [10].
Ein Abfall der Plasmaspiegel um durchschnittlich 50 % ist durch die potenten CYP3A4-Induktoren (Abb. 1) Carbamazepin und Johanniskraut möglich und es drohen subtherapeutische Spiegel mit der Gefahr von Abstoßungsreaktionen nach Organtransplantationen bei gleichbleibender CNI-Dosis [3, 4, 31].
Zusätzliche Interaktionen von Ciclosporin sind möglich durch seine hemmende Wirkung auf P-Glykoprotein (P-gp) und OATP1B1 (organisches Anionen-Transporter-Polypeptid 1B1). Kombinationen mit Substraten dieser Arzneimitteltransporter sind zu meiden, wenn durch erhöhte Plasmakonzentrationen schwere und/oder lebensbedrohliche Ereignisse drohen [10]. Zu diesen Arzneimitteln gehören beispielsweise Bosentan, Colchicin, Dabigatranetexilat, Digitoxin und Digoxin sowie HMG-CoA-Reductasehemmer.
Tacrolimus
Tacrolimus wird weitgehend durch CYP3A4 metabolisiert [8]. Dabei sind im Vergleich zu Ciclosporin stärkere Änderungen der AUC-Werte unter CYP3A4-Modulatoren möglich. Telaprevir und Posaconazol erhöhten bei gesunden Probanden die AUC-Werte von Tacrolimus um das 70- bzw. 4,6-Fache [13, 30]. Die Kombination mit Ritonavir-geboosterten antiretroviralen Therapien bedarf einer deutlichen Senkung der Dosis. Mit Tagesdosen von nur 0,06 bis 0,08 mg konnten empfohlene Zielspiegel des CNI in zwei Fallbeispielen erreicht werden [2]. Clarithromycin steigerte bei einem Patienten die Talspiegel von Tacrolimus um das 13-Fache trotz Dosisreduktion des Immunsuppressivums um 64 % [34]. Erythromycin erhöhte die Exposition von Tacrolimus in einer Kasuistik um mehr als das 6-Fache [26]. Der Konsum von Grapefruitsaft steigerte die Bioverfügbarkeit von Tacrolimus bei lebertransplantierten Patienten mit der Folge, dass der tägliche Bedarf des Immunsuppressivums um durchschnittlich 2,3 mg gesenkt wurde [23].
Johanniskraut führte bei zehn nierentransplantierten Patienten zu einer Senkung der Tacrolimusspiegel um im Schnitt 58 % [24]. Andere Fallbespiele und Studien belegen diesen Effekt von Johanniskraut [3, 16]. Das pflanzliche Antidepressivum ist folglich bei gleichzeitiger Tacrolimus-Therapie kontraindiziert [8]. Für andere ähnlich potente CYP3A4-Induktoren wie Carbamazepin und ältere, konventionelle Antikonvulsiva (Abb. 1) sollte dies ebenso gelten.
mTOR-Inhibitoren
Everolimus
Everolimus wird primär über CYP3A4 abgebaut [7]. In Studien mit gesunden Probanden erhöhten CYP3A4-Hemmer die Everolimus-Plasmaspiegel (Ketoconazol um das 15-Fache, Erythromycin um das 4,4-Fache und Verapamil um das 3,5-Fache). Der CYP3A4-Induktor Rifampicin senkte den AUC-Wert um 63 % [18–21]. Es wird empfohlen, starke CYP3A4-Modulatoren in Kombination mit dem mTOR-Hemmer zu meiden, es sei denn, der Nutzen überwiegt das Risiko. CYP3A4-Modulatoren sollten nur mit entsprechender Vorsicht und unter Monitoring der Vollblut-Talspiegel angewandt werden [7].
Sirolimus
Sirolimus wird in beträchtlichem Umfang über CYP3A4 metabolisiert [9]. Ketoconazol und Voriconazol erhöhten die Sirolimus-Plasmaspiegel um das 11-Fache bei gesunden Probanden, Verapamil um das 2,2-Fache, Rifampicin senkte sie um 82 % [25, 32, 35]. Patienten, deren Sirolimus-Dosis um 90 % gesenkt wurde, hatten in Kombination mit Voriconazol vergleichbare Talspiegel wie in der Monotherapie [25]. Die Kombination ist daher kontraindiziert [11].
Fazit
Selektive Immunsuppressiva sind Arzneimittel mit enger therapeutischer Breite. Unter Calcineurin-Inhibitoren drohen bei Überdosierung neuro- und vor allem nephrotoxische Nebenwirkungen [22]. Somit ist ein therapeutisches Drug-Monitoring (TDM) nach An- und Absetzen von klinisch relevanten CYP3A4-Modulatoren obligat. Vorzugsweise sollte eine Kombination von vorneherein vermieden werden. Die Auswaschphase des CYP3A4-Hemmers von drei bis fünf Halbwertszeiten und die (De-)Induktionszeiten des CYP3A4-Induktors sind zu beachten [28]. Es empfiehlt sich, soweit Daten vorhanden sind, schon bei Beginn einer Therapie die Dosis des Immunsupressivums anzupassen, wie es beispielsweise der Fachinformation Voriconazol-haltiger Arzneimittel für die Kombination mit Ciclosporin und Tacrolimus zu entnehmen ist, die konkrete Dosisvorgaben liefert [11]. Wünschenswert wäre, wenn die Fachinformationen der jeweiligen Immunsuppressiva diese Informationen auch enthielten.
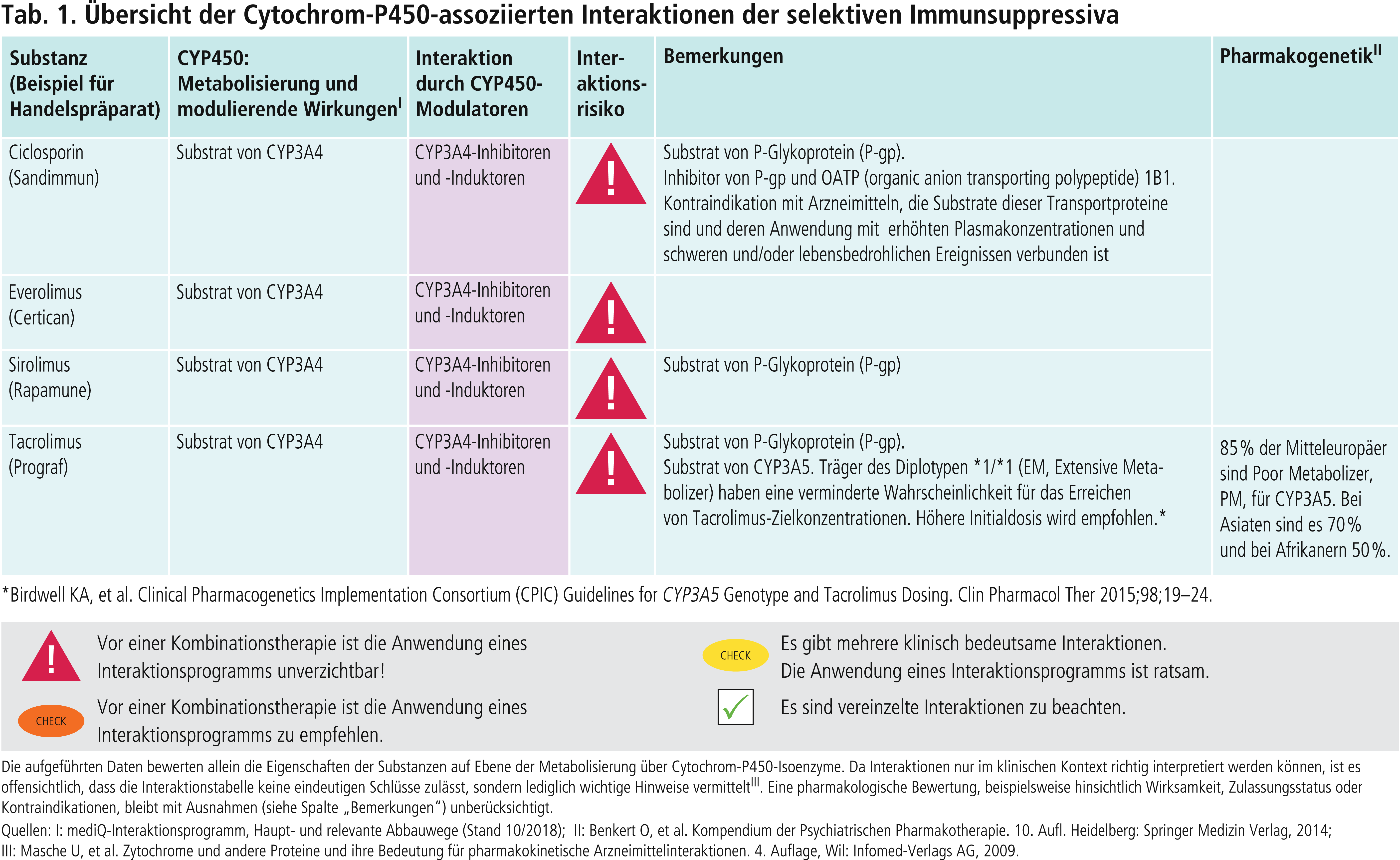
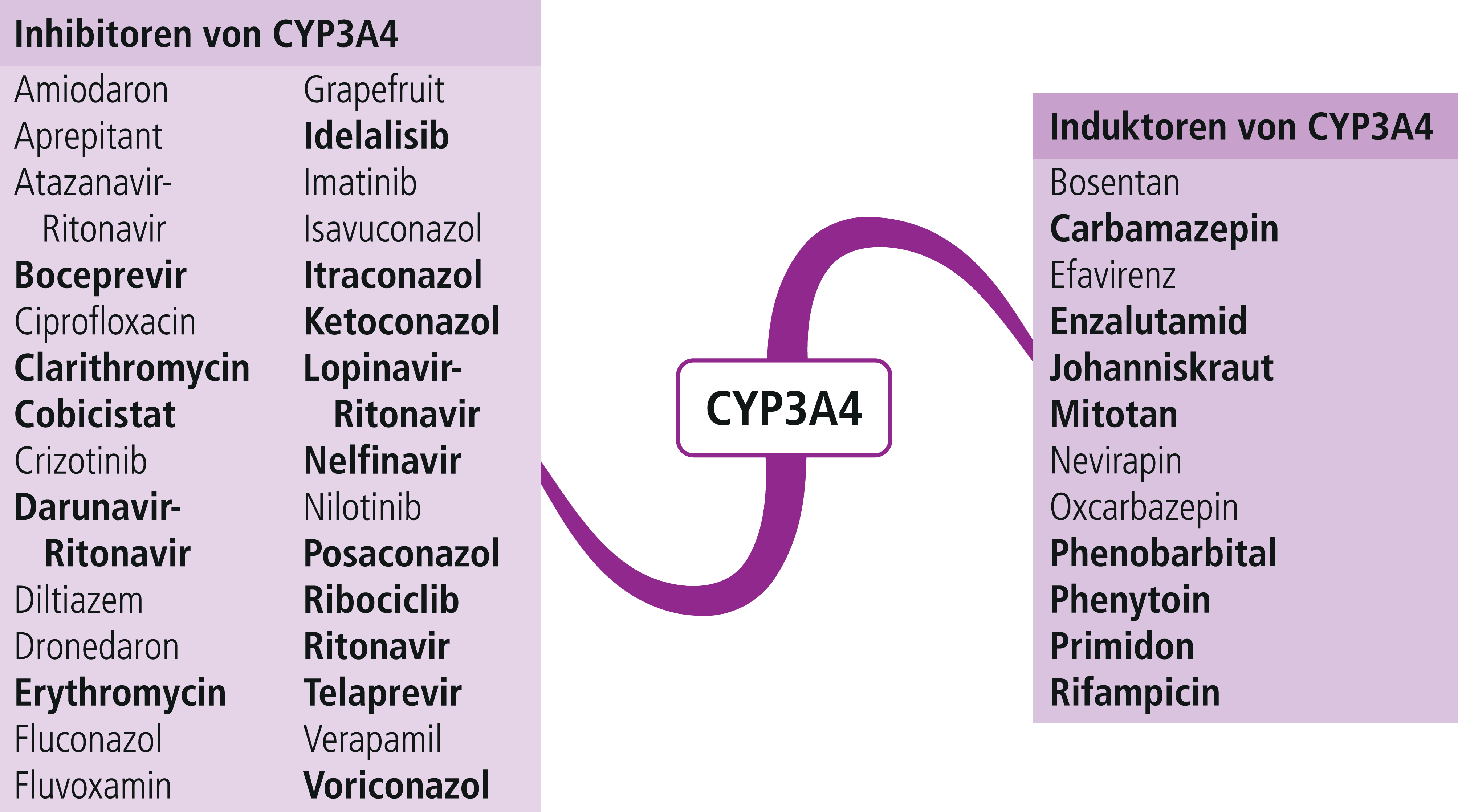
Abb. 2. Auswahl von modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf Cytochrom P450 (CYP) 2C9 und 3A4 (Stand 8/2018) [Quelle: mediQ-Interaktionsprogramm]
Literatur
1. Badri P, Dutta S, Coakley E, et al. Pharmacokinetics and dose recommendations for cyclosporine and tacrolimus when coadministered with ABT-450, ombitasvir, and dasabuvir. AM J Transplant 2015;15:1313–22.
2. Bickel M, Anadol E, Vogel M, et al. Daily dosing of tacrolimus in patients treated with HIV-1 therapy containing a ritonavir-boosted protease inhibitor or raltegravir. J Antimicrob Chemother 2010;65:999–1004.
3. Borrelli F, Izzo AA. Herb-drug interactions with St John’s wort (Hypericum perforatum): an update on clinical observations. AASP J 2009;11:710–27.
4. Breidenbach T, Hoffmann MW, Becker T, et al. Drug interaction of St John’s wort with cyclosporin. Lancet 2000;355:1912.
5. Canafax DM, Graves NM, Hilligoss DM, et al. Interaction between cyclosporine and fluconazole in renal allograft recipients. Transplantation 1991;51:1014–8.
6. Ducharme MP, Warbasse LH, Edwards DJ. Disposition of intravenous and oral cyclosporine after administration with grapefruit juice. Clin Pharmacol Ther 1995;57:485–91.
7. Fachinformation Certican®. Stand: Dezember 2016.
8. Fachinformation Prograf®. Stand: Mai 2018.
9. Fachinformation Rapamune®. Stand: August 2018.
10. Fachinformation Sandimmun®. Stand: Juli 2015.
11. Fachinformation Vfend®. Stand: Juni 2018.
12. Freeman DJ, Martell R, Carruthers SG, et al. Cyclosporin-erythromycin interaction in normal subjects. Br J Clin Pharmacol 1987;23:776–8.
13. Garg V, van Heeswijk R, Lee JE, et al. Effect of telaprevir on the pharmacokinetics of cyclosporine and tacrolimus. Hepatology 2011;54:20–7.
14. Gerntholz T, Pascoe MD, Botha JF, et al. The use of a cyclosporin-ketoconazole combination: making renal transplantation affordable in developing countries. Eur J Clin Pharmacol 2004;60:143–8.
15. Guaraldi G, Cocchi S, Codeluppi M, et al. Pharmacokinetic interaction between Amprenavir/Ritonavir and FosAmprenavir on cyclosporine in two patients with human immunodeficiency virus infection undergoing orthotopic liver transplantation. Transplant Proc 2006;38:1138–40.
16. Hebert MF, Park JM, Chen YL, et al. Effects of St. John’s wort (Hypericum perforatum) on tacrolimus pharmacokinetics in healthy volunteers. J Clin Pharmacol 2004;44:89–94.
17. Knower MT, Labella-Walker K, McFadden PM, et al. Clarithromycin for safe and cost-effective reduction of cyclosporine doses in lung allograft recipients. South Med J 2000;93:1087–92.
18. Kovarik JM, Beyer D, Bizot MN, et al. Blood concentrations of everolimus are markedly increased by ketoconazole. J Clin Pharmacol 2005;45:514–8.
19. Kovarik JM, Beyer D, Bizot ME, et al. Effect of multiple-dose erythromycin on everolimus pharmacokinetics. Eur J Clin Pharmacol 2005;61:35–8.
20. Kovarik JM, Beyer D, Bizot MN, et al. Pharmacokinetic interaction between verapamil and everolimus in healthy subjects. Br J Clin Pharmacol 2005;60:434–7.
21. Kovarik JM, Hartmann S, Figueiredo J, et al. Effect of rifampin on apparent clearance of everolimus. Ann Pharmacother 2002;36:981–5.
22. Kroy D, Trautwein C. Immunsuppression nach Lebertransplantation. Gastroenterologe 2018;13:198–8.
*Nachruck aus Krankenhauspharmazie 2018;39:496–9.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2018; 25(06):313-316
