Abdol A. Ameri, Weidenstetten
Die Fortschritte im Verständnis der komplexen Pathomechanismen der MS führten zur Entwicklung neuer Wirkstoffe, die spezifisch in das Krankheitsgeschehen eingreifen, und damit auch zur Formulierung neuer Therapieziele. Das oberste Ziel der MS-Therapie ist heute die langfristige Freiheit von klinischer und kernspintomographisch nachweisbarer Krankheitsaktivität [4]. Um es zu erreichen, sollte unter Berücksichtigung der individuellen Patientenbedürfnisse bereits unmittelbar nach der Diagnosestellung eine möglichst effektive Therapie eingeleitet werden [4]. Bei Wiederauftreten von Krankheitsaktivität ist rechtzeitig eine Anpassung der Therapie vorzunehmen [4]. Mit den monoklonalen Antikörpern Natalizumab (Tysabri®) [2] und Daclizumab (Zinbryta®) [3] stehen zwei hochwirksame Therapieoptionen zur Behandlung der aktiven MS zur Verfügung.
Natalizumab: individuelles Patientenmanagement
Der humanisierte monoklonale Anti-α4-Integrin-Antikörper Natalizumab ist seit mehr als zehn Jahren zur Therapie der hochaktiven schubförmig remittierenden MS zugelassen. In kontrollierten Studien wie auch unter den Bedingungen des klinischen Alltags zeigte Natalizumab ein günstiges Nutzen-Risiko-Verhältnis [7, 8]. In der Zulassungsstudie AFFIRM reduzierte die Substanz die jährliche Schubrate um 68%, die Wahrscheinlichkeit einer Behinderungsprogression (bestätigt nach 24 Wochen) um 54% und die Zahl der Gadolinium-aufnehmenden (Gd+-)Läsionen um 92% (jeweils p<0,001 vs. Placebo) [7].
Neue Daten aus der offenen, prospektiven TOP-(Tysabri observational program-)Studie bestätigen die Wirksamkeit von Natalizumab im klinischen Alltag und den Vorteil einer Frühtherapie: Bei frühzeitigem Beginn der Natalizumab-Therapie, das heißt bei einer vor weniger als einem Jahr diagnostizierten MS, zeigten 49,3% der Patienten im Verlauf von drei Jahren eine EDSS-Verbesserung, bei späterem Therapiebeginn hingegen nur 38,1% (MS-Dauer 1 bis 5 Jahre) bzw. 26,3% (>5 Jahre) [8].
Um den potenziellen Nutzen von Natalizumab optimal auszuschöpfen und das Risiko für die Entwicklung einer progressiven multifokalen Leukenzephalopathie (PML) zu minimieren, ist ein regelmäßiges Monitoring erforderlich. Nach einem Update der Europäischen Arzneimittelbehörde (EMA) kann das individuelle PML-Risiko noch differenzierter ermittelt werden. Patienten mit einem JCV-Antikörperindex von >1,5 haben ein hohes Risiko und sollten die Natalizumab-Therapie nach zwei Jahren nur dann fortsetzen, wenn das Nutzen-Risiko-Verhältnis als positiv eingestuft wird. Bei ihnen sollte alle drei bis sechs Monate ein MRT-Monitoring mit vereinfachtem Protokoll erfolgen. Bei einem niedrigen JCV-Antikörperindex (≤0,9) wird das PML-Risiko als gering angesehen. Bei diesen Patienten sowie bei Patienten mit negativem JCV-Antikörperstatus soll der Test halbjährlich wiederholt werden, um gegebenenfalls einen Anstieg des Index auf >1,5 rechtzeitig zu erkennen [5].
Daclizumab: Suppression der Krankheitsaktivität durch reversiblen Wirkungsmechanismus
Der einmal monatlich subkutan injizierte humanisierte, monoklonale Antikörper Daclizumab bindet selektiv an die Alpha-Untereinheit (CD25) des hochaffinen Interleukin(IL)-2-Rezeptors und führt zu einer reversiblen Reduktion aktivierter T-Zellen, ohne eine generelle Immunzelldepletion zu bewirken [1]. Da der hochaffine IL-2-Rezeptor nicht mehr für IL-2 zugänglich ist, steht das Zytokin in erhöhten Mengen für die Interaktion mit dem intermediär-affinen IL-2-Rezeptor auf immunregulatorischen CD56bright-Natural-Killer(NK)-Zellen zur Verfügung, was zu deren Expansion und Aktivierung führt [1].
Die randomisierte, doppelblinde Phase-III-Studie DECIDE (n=1841) untersuchte die Wirksamkeit und Sicherheit von Daclizumab (150 mg alle vier Wochen) im Vergleich zu Interferon beta-1a (IFN-β 1a, 30 µg/Woche i.m.) [6]. In Bezug auf die Reduktion der jährlichen Schubrate über einen Behandlungszeitraum von zwei bis drei Jahren (primärer Endpunkt), war Daclizumab gegenüber IFN-β 1a signifikant überlegen (Abb. 1). Die Zahl neuer oder vergrößerter hyperintenser T2-Läsionen über 96 Wochen (sekundärer Endpunkt) war im Daclizumab-Arm um 54% gegenüber dem IFN-β-1a-Arm reduziert (4,3 vs. 9,4; p<0,0001) und das Risiko für eine anhaltende Behinderungsprogression (bestätigt nach 24 Wochen, tertiärer Endpunkt) um 27% (13 vs. 18%; p=0,033) [6].
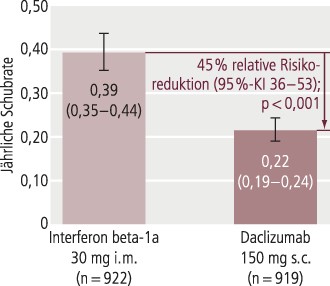
Abb. 1. DECIDE-Studie: Reduktion der jährlichen Schubrate unter Daclizumab versus Interferon beta-1a (nach [6]); 95%-KI: 95%-Konfidenzintervall
Die häufigsten Nebenwirkungen von Daclizumab waren Hautreaktionen und Leberwertveränderungen [6]. Daher ist ein regelmäßiges Monitoring erforderlich. Die Leberwerte (Alanin-Aminotransferase [ALT], Aspartat-Aminotransferase [AST]) und gegebenenfalls Serumbilirubin werden vor Therapiebeginn und während der Therapie einmal pro Monat bestimmt. Nach dem Therapieende sollten die Transaminasen für weitere vier Monate kontrolliert werden. Alle drei Monate wird ein großes Blutbild empfohlen [3]. Bei einer ALT- oder AST-Erhöhung über das 3-Fache des oberen Normwerts (>3×OGN) sollte die Behandlung unterbrochen werden. Sie kann wieder aufgenommen werden, wenn die Werte auf <2×OGN sinken. Zudem ist der Patient darüber zu informieren, dass er bei Hautreaktionen einen Arzt aufsucht [3].
Quelle
Priv.-Doz. Dr. Björn Tackenberg, Marburg, Prof. Dr. Tjalf Ziemssen, Dresden, Pressegespräch „Aktive MS frühzeitig, wirksam und individuell behandeln – Exklusive Einblicke in den Klinikalltag“, Berlin, 18. Mai 2017, veranstaltet von Biogen.
Literatur
1. Bielekova B. Daclizumab therapy for multiple sclerosis. Neurotherapeutics 2013;10:55–67.
2. Fachinformation Tysabri®; Stand: Februar 2017.
3. Fachinformation Zinbryta®, Stand: Juli 2016.
4. Gold R, et al. Therapieziele und Therapiemanagement bei schubförmig-remittierender Multipler Sklerose. Nervenheilkunde 2015; 34:915–22.
5. www.ema.europa.eu/ema/index.jsp?curl=pages/news_and_events/news/2016/02/news_detail_002476.jsp&mid=WC0b01ac058004d5c1 (Zugriff am 26.05.2017).
6. Kappos L, et al. Daclizumab HYP versus interferon beta-1a in relapsing multiple sclerosis. N Engl J Med 2015;373:1418–28.
7. Polman CH, et al. A randomized, placebo-controlled trial of natalizumab for relapsing multiple sclerosis. N Engl J Med 2006;354:899–910.
8. Spelman T, et al. AAN 2017; P350.
Anwendungsbeschränkungen für Daclizumab
Die europäische Arzneimittelbehörde EMA hat Anfang Juli wegen Sicherheitsbedenken bezüglich der Leberfunktion die Anwendungsgebiete für Daclizumab eingeschränkt, und zwar auf die Behandlung von Patienten
- mit hochaktiver schubförmiger MS trotz Behandlung mit mindestens einem anderen Basistherapeutikum (Disease modifying drug) oder
- mit sich rasch entwickelnder schwerer schubförmiger MS, für die ein anderes Basistherapeutikum nicht geeignet ist.
Bei vorbestehender Lebererkrankung oder Leberinsuffizienz ist Daclizumab jetzt kontraindiziert.
Bei ALT- oder AST-Werten >2×OGN wird ein Therapiebeginn nicht empfohlen. Der Serumbilirubinspiegel ist jetzt fester Bestandteil des Monitorings vor, während und nach der Therapie.
Die Risikobewertung durch das Pharmacovigilance Risik Assessment Committee (PRAC) wird fortgesetzt. (Red.)
[EMA. Pressemitteilung vom 07.07.2017. www.ema.europa.eu/docs/en_GB/document_library/Press_release/2017/07/WC500230922.pdf]
Psychopharmakotherapie 2017; 24(04)
