Priv.-Doz. Dr. Dieter Angersbach, Wolfratshausen
Nach Schätzungen weisen 25 bis 40% der Patienten mit einer Depression auch unterschwellige manische Symptome auf (Depression mit gemischten Merkmalen). Im Unterschied zu Patienten mit einer reinen Depression sind diese Patienten schwerer krank, haben häufiger Rückfälle, größere funktionelle Störungen und eine schlechtere Prognose. Mehrere klinische Berichte legen nahe, dass eine Behandlung mit Antidepressiva wenig wirksam und mit behandlungsbedingten Komplikationen verbunden ist, wie vermehrten Suizidgedanken, manischem Switch, Agitiertheit und Sprunghaftigkeit. Antipsychotika werden als Behandlungsalternative diskutiert, jedoch gibt es bisher keinerlei klinische Untersuchungen.
Ziel der vorliegenden Studie ist die Untersuchung der Wirksamkeit und Verträglichkeit von Lurasidon, einem atypischen Antipsychotikum, bei depressiven Patienten mit unterschwelligen hypomanen Symptomen. In Europa ist Lurasidon (Latuda®) zur Behandlung der Schizophrenie bei Erwachsenen ab 18 Jahren zugelassen [1]. Im Kontext der frühen Nutzenbewertung hat Takeda Lurasidon 2015 aus dem deutschen Markt genommen.
Lurasidon ist ein selektiver Hemmer dopaminerger (D) und serotonerger (5-HT) Effekte und bindet stark an D2-, 5-HT2A- und 5-HT7-Rezeptoren (Ki=0,994, 0,47 bzw. 0,495 nmol/l). Weiterhin ist Lurasidon ein partieller Agonist des 5-HT1A-Rezeptors (Ki=6,38 nmol/l) und ein Blocker adrenerger Alpha-2c- und Alpha-2a-Rezeptoren (Ki=10,8 bzw. 40,7 nmol/l). Die antidepressive Wirksamkeit wird im Zusammenhang mit der Hemmung des 5-HT7-Rezeptors gesehen. Die Eliminationshalbwertszeit beträgt 20 bis 40 Stunden, deshalb wird die Substanz einmal täglich eingenommen.
Die Studie wurde im Zeitraum zwischen September 2011 und Oktober 2014 in 18 Zentren in den USA und 26 Zentren in Europa durchgeführt.
Methoden
Eingeschlossen wurden ambulante Patienten zwischen 18 und 75 Jahren mit der Diagnose einer Major Depression nach DSM-IV-TR-Kriterien, bestätigt durch ein strukturiertes klinisches Interview für DSM-IV-Störungen, das für die Erfassung gemischter Symptome modifiziert war. Bei Screening und Einschluss musste eine akute depressive Episode mit einem Score auf der MADRS von ≥26 (von maximal 60) vorliegen. Zusätzlich mussten wenigstens zwei, aber nicht mehr als drei der folgenden manischen Symptome seit wenigstens zwei Wochen vorhanden sein: expansive Stimmung, übersteigertes Selbstwertgefühl bzw. Selbstüberschätzung, Redseligkeit, Ideenflucht, Gedankenrasen, erhöhte Energie, ausgiebige Aktivitäten mit unter Umständen negativen Konsequenzen und geringes Schlafbedürfnis.
Nach einer Auswaschphase von wenigstens drei Tagen wurden die Patienten randomisiert im Verhältnis von 1:1 einer Behandlung mit Lurasidon (20–60 mg/Tag) oder Placebo zugewiesen. Die Lurasidon-Behandlung begann mit 20 mg/Tag über sieben Tage. Ab Tag 8 konnte die Dosis schrittweise bis auf 60 mg einmal täglich gesteigert werden.
Primärer Wirksamkeitsparameter war die Änderung des MADRS-Scores vom Einschluss bis Woche 6, sekundäre Parameter waren Änderungen des CGI-S-Scores (Schlüsselparameter) sowie die Responder-Rate (≥50% Reduktion des MADRS-Scores) und die Remitter-Rate (MADRS-Score ≤12). Ferner wurden die YMRS, die Hamilton Anxiety Scale (HAM-A) und die Sheehan Disability Scale ausgewertet. Zur Erfassung der Verträglichkeit wurden die unerwünschten Ereignisse registriert, Vitalparameter gemessen, Labortests durchgeführt und ein EKG abgeleitet. Zur Erfassung extrapyramidaler Wirkungen wurden die Simpson-Angus Rating Scale, die Abnormal Involuntary Movement Scale (AIMS) und die Barnes Akathisia Rating Scale herangezogen. Die Assessments zur Beurteilung der Wirksamkeit und von unerwünschten Ereignissen fanden wöchentlich statt.
Ergebnisse
Patienten: Insgesamt wurden 327 Patienten gescreent, 211 von ihnen wurden eingeschlossen und 209 erhielten wenigstens eine Dosis der Prüfsubstanzen (Lurasidon n=109; Placebo n=100). Die Abschlussquote war hoch (Lurasidon-Gruppe: 93,6%, Placebo-Gruppe: 85,3%). Die mittlere Tagesdosis von Lurasidon betrug 36,2 mg, die höchste Tagesdosis von 60 mg nahmen 39% der Lurasidon-Patienten ein.
Wirksamkeit: Die mittlere Änderung des MADRS-Scores zu Woche 6 war unter Lurasidon signifikant größer als unter Placebo (–20,5 vs. –13,0; p<0,001; Effektstärke 0,8; Abb. 1). Auch die mittlere Änderung des Scores der CGI-S war unter Lurasidon signifikant größer als mit Placebo (p<0,001; Effektstärke 0,6). Sowohl die Responder- als auch die Remitter-Rate waren in der Lurasidon-Gruppe im Vergleich zu Placebo signifikant höher (Response: 64,8% vs. 30%; p<0,001; Remitter: 49,1% vs. 23%; p<0,001); daraus ergab sich eine Number needed to treat (NNT) von 3 für eine Response und von 4 für eine Remission. Auch die Änderungen der Scores der YMRS, der HAM-A und der Sheehan Disability Scale waren unter Lurasidon stärker als unter Placebo (jeweils p<0,001).
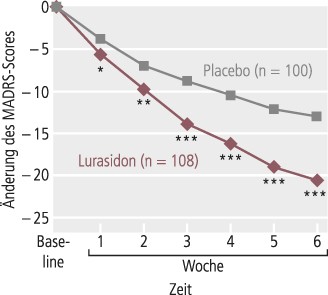
Abb. 1. Mittlere Änderung des MADRS-Scores unter Lurasidon und Placebo vom Einschluss bis zum Endpunkt (Woche 6) in der Behandlung einer Major Depression mit gemischten Merkmalen [nach Suppes et al.]. * p<0,05; ** p<0,01; *** p<0,001
Verträglichkeit: Der Anteil der Patienten, die wenigstens ein behandlungsbezogenes unerwünschtes Ereignis meldeten, betrug unter Lurasidon 40,4% und unter Placebo 38%. Die häufigsten unerwünschten Ereignisse unter Lurasidon waren Übelkeit (6,4%) und Somnolenz (5,5%). Akathisie und Parkinsonismus traten unter Lurasidon etwas häufiger auf als unter Placebo (3,7% vs. 2,0%, bzw. 2,8% vs. 1%). Gewichtsänderungen waren in beiden Gruppen gering (+0,7% vs. +0,4%). Klinisch signifikante Änderungen der Laborparameter wurden in keiner der beiden Gruppen gefunden. Schwerwiegende unerwünschte Ereignisse wurden in der Studie nicht gemeldet.
Nach Ansicht der Autoren war Lurasidon in dieser Studie eine wirksame Therapie, unter der sich sowohl die depressiven als auch die manischen Symptome gebessert haben. Zudem war Lurasidon gut verträglich und zeigte ein günstiges Nutzen-Risiko-Profil.
Kommentar
In der vorliegenden Studie war die Prüfsubstanz in allen Wirksamkeitsparametern der Placebo-Behandlung hochsignifikant überlegen. Diese gute Wirksamkeit zeigte sich nicht unerwartet, da Lurasidon zuvor in zwei Placebo-kontrollierten Untersuchungen eine gute Wirksamkeit in der Behandlung der bipolaren Depression gezeigt hatte. Es gibt Hinweise darauf, dass sich Patienten mit einer Depression mit gemischten Merkmalen möglicherweise im Übergang von der reinen Depression zur bipolaren Störung befinden und damit ein ähnliches Krankheitsprofil haben wie bipolare Patienten. Auch wird diskutiert, ob die erstmals mit DSM 5 in die Klassifikation aufgenommene „mixed Depression“ tatsächlich eine von der bipolaren Depression abgrenzbare Entität darstellt [2].
Wie der vorliegenden Arbeit zu entnehmen ist, war die Diagnose „Major Depression mit gemischten Merkmalen“ nicht ganz einfach zu stellen, denn die Eignung jedes Patienten wurde anhand des Interview-Protokolls von einer externen Expertenkommission überprüft. Im klinischen Alltag dürfte es allerdings für die Behandlung kein Nachteil sein, wenn sich die zu behandelnden Patienten weiter fortgeschritten auf dem Übergang zur bipolaren Erkrankung befinden als die Teilnehmer dieser Studie.
Lurasidon zeigte nicht nur eine gute Wirksamkeit, sondern auch eine sehr gute Verträglichkeit, wie die hohe Abschlussquote (93,6%) zeigt. Für eine kritische Bewertung ist eine Behandlungsdauer von nur sechs Wochen zwar nicht lang genug. Bemerkenswert ist aber in diesem Zusammenhang, dass Lurasidon in der vorliegenden Studie zur Behandlung der Depression deutlich niedriger dosiert wurde als vom Hersteller zur Behandlung der Schizophrenie empfohlen wird (37 bis 143 mg/Tag).
Quelle
Suppes T, et al. Lurasidon for the treatment of major depressive disorder with mixed features: A randomized, double-blind, placebo-controlled study. Am J Psychiatry 2016;173:400–7.
Literatur
1. Fachinformation Latuda® 37 mg Filmtabletten (Stand Juli 2014).
2. Weibel S, Bertschy G. Mixed depression and DSM-5: A critical review. Encephale 2016; 42:90–8.
Psychopharmakotherapie 2017; 24(03)
