Dr. Jürgen Sartorius, Eitorf
Kinder mit einer Duchenne-Muskeldystrophie zeigen vom Säuglingsalter an Entwicklungs- und progressive Bewegungseinschränkungen, die letztlich in der dritten oder spätestens vierten Lebensdekade zum Tod führen. Meist wird die Krankheit erst bei Kleinkindern erkannt, da die von Mutationen im X-Chromosom betroffenen Jungen besonders durch Störungen beim Aufstehen und im Vergleich mit Gleichaltrigen auffallen.
Orphan-Disease Duchenne-Muskeldystrophie
Die Duchenne-Muskeldystrophie gehört zu den seltenen Erkrankungen. In Deutschland leben nach Angaben der Deutschen Gesellschaft für Muskelkranke etwa 1500 bis 2000 Betroffene. Den Patienten fehlt das Protein Dystrophin, das Muskelmembranen stabilisiert und den Muskel vor Schädigungen schützt. Zugrunde liegen verschiedene Mutationen im Dystrophin-Gen, am häufigsten Deletionen, seltener Duplikationen oder Punktmutationen. Zu Letzeren zählen die Nonsense-Mutationen. (Red.)
Bei etwa 10 bis 15% der Betroffenen wird die Muskeldystrophie durch eine Nonsense-Mutation im Dystrophin-Gen hervorgerufen; infolge eines frühzeitigen Stopp-Codons in der mRNA entsteht ein funktionsloses Dystrophin-Bruchstück. Der oral verfügbare Wirkstoff Ataluren (Abb. 1) ermöglicht das Durchlesen vorzeitiger Stopp-Codons und damit die korrekte Translation. Somit steht den Patienten das funktionsfähige Protein Dystrophin wieder zur Verfügung. Zur eindeutigen Identifikation geeigneter Kinder muss eine Nonsense-Mutation im Dystrophin-Gen nachgewiesen werden. Zugelassen wurde Ataluren (TranslarnaTM) für Patienten ab fünf Jahren, die noch gehfähig sind. Die Nutzenbewertung durch den G-BA (2015) geht hier von bis zu 110 Patienten in Deutschland aus.
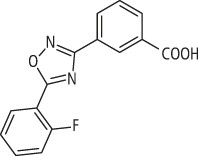
Abb. 1. Ataluren
In prospektiven Studien signifikante Verbesserungen gegenüber Placebo
Der Grund für die Zulassungseinschränkung liegt darin, dass nur bei noch gehfähigen Patienten die Wirksamkeit von Ataluren in prospektiven Studien nachgewiesen werden konnte. Besonders aussagekräftig waren die Ergebnisse von Patienten, deren Erkrankung sich in einem Übergangsstadium von erhaltener Gehfähigkeit zu einer Abnahme der 6-Minuten-Gehstrecke befindet. In diesem Zeitraum können die Betroffenen noch 300 bis 400 Meter gehen, tragen aber ein hohes Risiko, dass ihre Gehfähigkeit ohne Behandlung beschleunigt abnimmt. Andererseits reicht in diesem Stadium die Muskelmasse noch aus, um einen Arzneieffekt über 48 Wochen im 6-Minuten-Gehstreckentest zu zeigen.
Subgruppen genau dieser Patienten zeigten in beiden zulassungsrelevanten Studien signifikant verlangsamte Abnahmen der 6-Minuten-Gehstrecke durch Ataluren im Vergleich mit Placebo (Tab. 1). Auch bei den sekundären Endpunkten, darunter Verlust der Gehfähigkeit, Aufstehen und Stufensteigen, zeigten Patienten unter Ataluren deutlich bessere Ergebnisse.
Tab. 1. Verlangsamung der Abnahme (somit ein positiver Wert) der Gehstrecke unter Ataluren in 48 Wochen
|
Art der Studie, n [Quelle] |
Primärer Endpunkt 6MWD, ITT |
Subgruppe 300–400 m [Quelle] Ausgangswert im 6MWD (n, p) |
|
RCT Phase IIb, n=114 [1] |
+31,3 m vs. Placebo |
+49 m vs. Placebo [2] (n=22, p=0,0262) |
|
RCT Phase III, n=228 [3] |
+15 m vs. Placebo |
+47 m vs. Placebo [3] (n=99, p=0,007) |
RCT: Randomisierte kontrollierte Studie, 6MWD: 6-Minuten-Gehstreckentest; ITT: Intention-to-treat
Wesentlich ist die korrekte Dosierung von 40 mg Ataluren/kg Körpergewicht, verteilt auf drei regelmäßige Gaben morgens, mittags und abends, als Granulat in Flüssigkeit getrunken. Klinische Erfahrungen mit mittlerweile über 600 Patienten zeigen eine gute Verträglichkeit. Ataluren kann mit der bisher vorherrschenden Glucocorticoid-Therapie kombiniert werden.
Quelle
Prim. Univ.-Prof. Dr. Günther Bernert, Wien, Dr. med. Jessika Johannsen, Hamburg, Prof. Dr. med. Janbernd Kirschner, Freiburg, Symposium „TranslarnaTM (Ataluren) in der Therapie der DMD mit zugrundeliegender Nonsense-Mutation – Eine Standortbestimmung“, veranstaltet von PTC Therapeutics im Rahmen der 43. Jahrestagung der Gesellschaft für Neuropädiatrie, Bad Nauheim, 28. April 2017.
Literatur
1. Bushby K, et al. Muscle Nerve 2014;50:477–87.
2. Haas M, et al. Neuromuskul Disord 2015;25: 5–13.
3. McDonald CM, et al. Presentation at American Academy of Neurology (AAN) 68th Annual Meeting, 15.–21. April 2016, Vancouver, Canada, #P3.121.
Psychopharmakotherapie 2017; 24(03)
