Jürgen Fritze, Frankfurt am Main, Claudia Riedel, Angelika Escherich, Peggy Beinlich, Karl Broich und Thomas Sudhop, Bonn
Der am 28. August 2013 von der Bundesregierung akzeptierte „Nationale Aktionsplan für Menschen mit Seltenen Erkrankungen“ des Nationalen Aktionsbündnisses für Menschen mit Seltenen Erkrankungen (NAMSE) enthält unter anderen im Maßnahmenvorschlag 7 die Empfehlung, eine „Studie zur Erfassung des Umfangs des Off-Label-Use bei Seltenen Krankheiten anhand der Daten nach §303a ff. SGB V […]“ durchzuführen. Zu den Initiatoren des NAMSE gehört die Allianz Chronischer Seltener Erkrankungen (ACHSE e.V.), sodass die Selbsthilfeorganisationen die vorgeschlagenen Maßnahmen entscheidend geprägt haben. Ein wesentliches Problem in der Off-Label-Verordnung von Arzneimitteln liegt in der Schwierigkeit der Erstattung durch die gesetzliche Krankenversicherung (GKV). Zugelassene Arzneimittel dürfen gemäß einem Urteil des Bundessozialgerichts vom 19. März 2002 (Az.: B 1 KR 37/00 R) grundsätzlich nicht zulasten der GKV in einem Anwendungsgebiet verordnet werden, auf das sich die Zulassung nicht erstreckt („Off-Label-Use“). Andererseits kann ein Off-Label-Use aber auch rechtlich geboten sein, um eine unterlassene Hilfeleistung zu verhindern. In jedem Fall ist ein Off-Label-Use mit erhöhten Anforderungen an Aufklärung und Dokumentation und gegebenenfalls mit erhöhten Haftungsrisiken des Arztes verbunden.
Das Bundesministerium für Gesundheit (BMG) hat gemäß §35c Absatz 1 Sozialgesetzbuch V (SGB V) Expertenkommissionen beim Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) berufen, die im Auftrag des Gemeinsamen Bundesausschusses (G-BA) oder des BMG „Bewertungen zum Stand der wissenschaftlichen Erkenntnis über die Anwendung von zugelassenen Arzneimitteln für Indikationen und Indikationsbereiche, für die sie nach dem Arzneimittelgesetz nicht zugelassen sind“ abgeben. Der G-BA entscheidet auf deren Basis, ob eine nicht zugelassene Indikation in die Anlage VI zum Abschnitt K der Arzneimittel-Richtlinie (Verordnungsfähigkeit von zugelassenen Arzneimitteln in nicht zugelassenen Anwendungsgebieten) aufgenommen wird, sofern die betroffenen pharmazeutischen Unternehmer einer Aufnahme ihrer Arzneimittel zugestimmt haben.
Obwohl häufig diskutiert, fehlen bisher weitgehend Daten zur epidemiologischen Relevanz des jeweiligen Off-Label-Use. Vor den Hintergründen des NAMSE-Aktionsplans und des Verfahrens nach §35c SGB V untersucht das vorliegende Projekt – aus zwei Perspektiven – zum einen den Umfang des Off-Label-Use häufig verordneter Wirkstoffe nach Art und Häufigkeit und zum anderen mögliche sich daraus ableitende Implikationen für die Verbesserung der Therapie seltener Erkrankungen.
Untersuchte Arzneimittel
Unter der Annahme, Wirkstoffe mit nosologisch unspezifischer Pharmakodynamik könnten eher außerhalb des zugelassenen Anwendungsgebiets eingesetzt werden, wurden folgende Arzneimittelgruppen gemäß dem anatomisch-therapeutisch-chemischen Klassifikationssystem (ATC-System) ausgewählt:
- B01AC Thrombozytenaggregationshemmer, außer Heparin
- B01AE Direkte Thrombin-Inhibitoren
- B01AF Direkte Faktor-Xa-Inhibitoren
- L01 Antineoplastische Mittel
- L03 Immunstimulanzien
- L04 Immunsuppressiva
- N03 Antiepileptika
- N05 Psycholeptika
- N06 Psychoanaleptika
Da eine Priorisierung nach der Art der Krankheit ethisch unvertretbar erschien, wurden aus diesen Wirkstoffgruppen die gemäß Arzneiverordnungsreport 2013 im Jahr 2012 am häufigsten (nach definierten Tagesdosen, DDD) verordneten Wirkstoffe einbezogen, die grundsätzlich in der genannten Reihenfolge abzuarbeiten sind. In der vorliegenden Untersuchung wurden also ausdrücklich ohne jedwede Priorisierungsmotive und grundsätzlich hypothesenfrei die vier am häufigsten verordneten Thrombozytenaggregationshemmer Acetylsalicylsäure (ASS), Clopidogrel, Prasugrel und Ticagrelor analysiert. Die Anwendungsgebiete der verschiedenen Thrombozytenaggregationshemmer unterscheiden sich und sind nachfolgend dargestellt.
Acetylsalicylsäure (ASS)
Die zugelassenen Anwendungsgebiete von ASS unterscheiden sich zwischen den verschiedenen Zulassungen und Stärken und umfassen in der Regel folgende Anwendungsgebiete:
- Symptomatische Behandlung bei leichten bis mäßig starken Schmerzen
- Symptomatische Behandlung von Fieber
- Instabile Angina pectoris – als Teil der Standardtherapie
- Akuter Myokardinfarkt – als Teil der Standardtherapie
- Reinfarktprophylaxe nach arteriellen gefäßchirurgischen oder interventionellen Eingriffen (z.B. nach aortokoronarem venösem Bypass [ACVB], bei perkutaner transluminaler Koronarangioplastie [PTCA])
- Vorbeugung von transitorischen ischämischen Attacken (TIA)
- Vorbeugung von Hirninfarkten, nachdem Vorläuferstadien aufgetreten sind
- Kawasaki-Syndrom:
- Zur Entzündungshemmung für die Dauer der febrilen Phase
- Zur prophylaktischen Thrombozytenaggregationshemmung bei koronar-arteriellen Aneurysmen
- Zur Reinfarktprophylaxe
Mindestalter
Ein Mindestalter für die Behandlung mit ASS ist nicht vorgegeben, allerdings ist die Anwendung bei Kindern und Jugendlichen mit fieberhaften Erkrankungen aufgrund des seltenen Reye-Syndroms auf eine strengste Indikationsstellung zu beschränken.
Clopidogrel
Entsprechend der Fachinformationen der meisten Präparate ist Clopidogrel zur Prävention atherothrombotischer Ereignisse indiziert bei:
- Erwachsenen Patienten mit Herzinfarkt (wenige Tage bis weniger als 35 Tage zurückliegend), mit ischämischem Schlaganfall (7 Tage bis weniger als 6 Monate zurückliegend) oder mit nachgewiesener peripherer arterieller Verschlusskrankheit,
- Erwachsenen Patienten mit akutem Koronarsyndrom:
- Akutes Koronarsyndrom ohne ST-Strecken-Hebung (instabile Angina pectoris oder Non-Q-Wave-Myokardinfarkt), einschließlich Patienten, denen bei einer perkutanen Koronarintervention ein Stent implantiert wurde, in Kombination mit ASS
- Akuter Myokardinfarkt mit ST-Strecken-Hebung, in Kombination mit ASS bei medizinisch behandelten Patienten, für die eine thrombolytische Therapie infrage kommt.
Weiterhin ist Clopidogrel indiziert zur Prävention atherothrombotischer und thromboembolischer Ereignisse bei Vorhofflimmern. Hier gilt:
Bei erwachsenen Patienten mit Vorhofflimmern, bei denen wenigstens ein Risikofaktor für vaskuläre Ereignisse vorliegt, die keine Vitamin-K-Antagonisten-Therapie erhalten können und die ein geringes Blutungsrisiko aufweisen, ist Clopidogrel in Kombination mit ASS angezeigt zur Prophylaxe atherothrombotischer und thromboembolischer Ereignisse, einschließlich Schlaganfall.
Mindestalter
Clopidogrel ist nicht zur Behandlung von Kindern und Jugendlichen zugelassen. Das Mindestalter beträgt 18 Jahre.
Prasugrel
Gemäß Fachinformation ist Prasugrel in Kombination mit ASS angezeigt zur Prävention atherothrombotischer Ereignisse bei Patienten mit akutem Koronarsyndrom (d.h. instabiler Angina pectoris, Nicht-ST-[Strecken-]Hebungsinfarkt [UA/NSTEMI] oder ST-[Strecken-]Hebungsinfarkt [STEMI]) mit primärer oder verzögerter perkutaner Koronarintervention (PCI).
Mindestalter
Prasugrel ist nicht zur Behandlung von Kindern und Jugendlichen zugelassen. Das Mindestalter beträgt 18 Jahre.
Ticagrelor
Gemäß Fachinformation ist Ticagrelor gleichzeitig eingenommen mit ASS indiziert zur Prävention atherothrombotischer Ereignisse bei erwachsenen Patienten mit einem akuten Koronarsyndrom (instabile Angina pectoris, Myokardinfarkt ohne ST-Strecken-Hebung [NSTEMI] oder Myokardinfarkt mit ST-Strecken-Hebung [STEMI]), und zwar sowohl bei medikamentös behandelten Patienten als auch bei Patienten, bei denen eine perkutane Koronarintervention (PCI) oder eine aortokoronare Bypass-Operation (CABG) durchgeführt wurde.
Mindestalter
Ticagrelor ist nicht zur Behandlung von Kindern und Jugendlichen zugelassen. Das Mindestalter beträgt 18 Jahre.
Methoden der Datenanalyse
Grundlage bilden die Daten nach §§303a ff. SGBV, also die Abrechnungsdaten der gesetzlichen Krankenkassen. Gemäß §303b SGBV handelt es sich um die Daten, die das Bundesversicherungsamt (BVA) der Kalkulation des morbiditätsorientierten Risikostrukturausgleichs zugrunde zu legen hat und an die Datenaufbereitungsstelle nach §303e SGBV übermittelt hat, die gemäß §2 Datentransparenzverordnung beim Deutschen Institut für Medizinische Dokumentation und Information (DIMDI) angesiedelt ist. Während die Daten nach §§303a ff. SGBV die Diagnosen aus vertragsärztlicher und stationärer Behandlung enthalten, entstammen die Informationen über die Arzneimitteltherapie grundsätzlich nur der vertragsärztlichen Versorgung. Diese Daten enthalten unter anderen Angaben zu Geschlecht und Alter, Diagnosedaten (Codes der Diagnosenklassifikation ICD-10-GM) und Arzneimittelkennzeichen (Pharmazentralnummer [PZN]), wobei über die Pseudonymisierung der Patienten grundsätzlich auch ein Versichertenbezug über längere Zeiträume hergestellt werden kann. Den PZN wurden mithilfe einer Mapping-Tabelle, die anhand der „Arzneimittel-Stammdatei“ des Wissenschaftlichen Instituts der AOK (WIdO) erstellt wurde, die entsprechenden ATC-Codes zugeordnet, wodurch die als PZN kodierten Verordnungsdaten der Datenbank als Wirkstoffe identifiziert wurden.
Die arzneimittelrechtliche Zulassung gilt dem Fertigarzneimittel, kann sich also zwischen Fertigarzneimitteln mit identischem Wirkstoff unterscheiden. Die Zulassung erstreckt sich nicht nur auf die medizinische Indikation, die Diagnose, sondern auch auf Kontraindikationen, Darreichungsform/Applikationsweg, Dosis und Behandlungsdauer sowie Alter und Geschlecht des Patienten. Soweit das Anwendungsgebiet auf Diagnosen Bezug nimmt, sind diese als Freitext formuliert, dem keine expliziten ICD-Codes zugeordnet sind. Darüber hinaus kann die arzneimittelrechtliche Beschreibung des Anwendungsgebiets Klarstellungen enthalten, mit denen Anwendungseinschränkungen bei einer Diagnose, zum Beispiel das vorherige Versagen einer anderen Therapie, festgelegt werden.
Um in den Daten nach §§303a ff. SGBV Analysen des Off-Label-Use nach Art und Häufigkeit durchführen zu können, wurden die als Freitext formulierten Anwendungsgebiete der Wirkstoffe bezüglich der Diagnosen mit Codes der amtlichen ICD-10-GM operationalisiert. Anwendungseinschränkungen, wie bei Thrombozytenaggregationshemmern gegeben, und Kontraindikationen konnten nicht gewürdigt werden, weil sich das Projekt auf Standardabfragen beim DIMDI beschränken musste.
Für alle gesetzlich Versicherten, denen in den Jahren 2010 und 2011 mindestens einmal Thrombozytenaggregationshemmer gemäß den ATC-Codes B01AC06, B01AC04, B01AC22 und B01AC24 verordnet worden waren, wurden sämtliche in diesem Beobachtungszeitraum übermittelten ICD-10-GM-Codes erfasst. Die beiden damals zugänglichen Berichtsjahre wurden einbezogen, um die Sensitivität für seltene Off-Label-Indikationen zu erhöhen. Dadurch musste in Kauf genommen werden, dass eine Differenzierung zwischen diesen beiden Jahren nicht mehr möglich war. Dies wurde als akzeptabel angesehen, da sich aus zwei benachbarten Datenjahrgängen ohnehin kaum Erkenntnisse über Trends im Zeitverlauf würden gewinnen lassen.
Als In-Label-Use wurden diejenigen pseudonymisierten Patienten identifiziert, bei denen mindestens eine der im Datensatz übermittelten Diagnosen einer der zugelassenen Diagnosen gemäß Operationalisierung entsprach, als Off-Label-Use jene Versicherten, bei denen keine Diagnose den zugelassenen Indikationsdiagnosen entsprach. Um gegebenenfalls Mängel der Operationalisierung zu kompensieren, wurde die sich ergebende Gruppe mit apparentem Off-Label-Use darauf geprüft, inwieweit möglicherweise doch ein In-Label-Use vorlag und durch Rekonstruktionen entsprechend korrigiert. Die Rekonstruktionen konnten immer dann nur semiquantitativ gelingen, wenn die mutmaßlich dem Off-Label-Use geltenden Diagnosen nicht disjunkt waren. Das galt insbesondere bei unspezifischen ICD-Codes (z.B. Xxx.9).
Um Off-Label-Use in Form eines Verstoßes gegen mögliche Altersbeschränkungen näherungsweise erkennen zu können, erfolgten die Zählungen differenziert nach den Altersgruppen <1 Jahr, 1<14 Jahre (Kinder), 14<18 Jahre (Jugendliche) und Erwachsene nach Dekaden.
Der In-Label-Use der Thrombozytenaggregationshemmer wurde mit den in Tabelle 1 präsentierten Codes operationalisiert.
Tab. 1. ICD-10-GM-Codes, die zur Klassifikation eines In-Label-Use der analysierten Thrombozytenaggregationshemmer verwendet wurden
|
Operationalisierende ICD-Codes |
ASS |
Clopidogrel |
Prasugrel |
Ticagrelor |
|
E11.50 Nicht primär insulinabhängiger Diabetes mellitus [Typ-2-Diabetes] mit peripheren vaskulären Komplikationen, nicht als entgleist bezeichnet |
+ |
+ |
||
|
I20.0 Instabile Angina pectoris |
+ |
+ |
+ |
|
|
I21.- Akuter Myokardinfarkt |
+ |
+ |
+ |
+ |
|
I22.- Rezidivierender Myokardinfarkt |
+ |
+ |
+ |
+ |
|
I24.- Sonstige akute ischämische Herzkrankheit |
+ |
|||
|
I24.9 Akute ischämische Herzkrankheit, nicht näher bezeichnet |
+ |
+ |
||
|
I25.- Chronische ischämische Herzkrankheit |
+ |
|||
|
I25.21 Alter Myokardinfarkt 4 Monate bis unter 1 Jahr zurückliegend |
+ |
|||
|
I48.- Vorhofflimmern und Vorhofflattern |
+ |
+ |
||
|
I63.- Hirninfarkt |
+ |
+ |
||
|
I65.- Verschluss und Stenose präzerebraler Arterien ohne resultierenden Hirninfarkt |
+ |
+ |
||
|
I66.- Verschluss und Stenose zerebraler Arterien ohne resultierenden Hirninfarkt |
+ |
+ |
||
|
I69.3 Folgen eines Hirninfarkts |
+ |
+ |
||
|
I70.2 Atherosklerose der Extremitätenarterien |
+ |
+ |
||
|
I73.9 Periphere Gefäßkrankheit, nicht näher bezeichnet |
+ |
+ |
||
|
I79.2 Periphere Angiopathie bei anderenorts klassifizierten Krankheiten |
+ |
+ |
||
|
M30.3 Mukokutanes Lymphknotensyndrom (Kawasaki-Krankheit) |
+ |
|||
|
Z95.1 Vorhandensein eines aortokoronaren Bypasses |
+ |
+ |
||
|
Z95.5 Vorhandensein eines Implantats oder Transplantats nach koronarer Gefäßplastik |
+ |
+ |
||
|
Z95.88 Vorhandensein von sonstigen kardialen oder vaskulären Implantaten oder Transplantaten |
+ |
+ |
Einschränkungen der Operationalisierungen
Die Übersetzung der Formulierung der Anwendungsgebiete in Codes der ICD-10-GM (Operationalisierung) erfolgte durch nur eine Person (J.F.) und wurde durch nur eine Person (A.E.) auf Plausibilität im Sinne einer Qualitätssicherung geprüft. Für eine parallele Operationalisierung durch mindestens zwei Personen standen keine Ressourcen zur Verfügung. Die Operationalisierungen konnten wegen der aus Effizienzgründen standardisierten Datenbankabfragen die teilweise gemäß der jeweiligen Zulassungsbedingungen geforderten – unzureichend erfolgreichen – Vorbehandlungen und weiteren Vorbedingungen nicht würdigen. Die Indikationen „Schmerz“ bzw. „Fieber“ für ASS wurden bewusst nicht in die Operationalisierung einbezogen und damit das Risiko einer falsch häufigeren Off-Label-Use-Ermittlung in Kauf genommen, da – auch wenn in ICD-Kapitel XVIII die Codes R50ff. zur Verfügung stehen – unzureichend antizipierbar erschien, ob diese Codes überhaupt verwendet werden oder ob nicht eher die den Symptomen Schmerz bzw. Fieber zugrunde liegenden Krankheiten kodiert worden waren. Diese aber waren offensichtlich nicht antizipierbar. Hier war also zu erwarten, dass Versicherte der Off-Label-Use-Gruppe post hoc als In-Label-Use zu reklassifizieren sein würden. Ebenso konnten beispielhaft im Anwendungsgebiet der Fachinformationen genannte Risikofaktoren nicht als Risikofaktoren gewürdigt werden. Auch gegebenenfalls optionale Kopplungen an eine perkutane Koronarintervention (PCI) mit Stenting wurden nicht gewürdigt, weil entsprechende OPS-Codes nicht berücksichtigt werden konnten. Der Code „I25.21 Alter Myokardinfarkt 4 Monate bis unter 1 Jahr zurückliegend“ wurde zwar in die Operationalisierung des In-Label-Use von Clopidogrel einbezogen, stellt aber eigentlich eine relative Kontraindikation für die Initiierung von Clopidogrel dar. Obligate Komedikationen wurden nicht durch ATC-Codes als Bedingung einbezogen, weil dies mit dem Konzept von auf alle Wirkstoffe anwendbaren Standardabfragen unvereinbar gewesen wäre.
Als weitere Limitation ist bei der Interpretation der Ergebnisse zu berücksichtigen, dass jeder Versicherte in jedem der einbezogenen acht Quartale von einer nicht identifizierbaren Anzahl konsultierter Vertragsärzte bzw. bei einer nicht identifizierbaren Anzahl von Krankenhausaufenthalten mindestens eine Diagnose erhalten haben konnte, sodass die Häufigkeit der In-Label-Diagnosen die Anzahl der Versicherten, denen der Wirkstoff verordnet worden war, infolge wechselnder In-Label-Diagnosen, beispielsweise infolge unterschiedlicher Kodiergewohnheiten, erheblich übersteigen kann, wenn mehrere ICD-Codes zur Operationalisierung des Anwendungsgebiets infrage kommen. Derselbe Effekt war erst recht und in stärkerem Maße bei Off-Label-Indikationen zu erwarten.
Limitationen aufgrund des Datenschutzes
Aus Gründen des Datenschutzes wurde für alle Einzeldiagnosen (ICD-Codes) mit einer Anzahl von Versicherten zwischen 1 und 30 vom DIMDI für solche Diagnosen eine Anzahl von 30 ausgewiesen, um sicherzustellen, dass keine Re-Identifikation der Versicherten erfolgen kann. In diesen Fällen wurden zur Kompensation jeweils Spannweiten mit einem hypothetischen Minimum, bei dem n=1 Versicherter pro Gruppe angenommen wurde, und einem Maximum, bei dem hypothetisch n=30 angenommen wurden, errechnet und in den Auswertungen in Form eines Intervalls mit jeweils unterer und oberer Grenze angegeben.
Weitere Limitationen
Die Auswahl, Interpretation und Bewertung mutmaßlich beabsichtigter Off-Label-Indikationen konnte unausweichlich letztlich nur durch manuelle Sichtung jeder einzelnen Diagnose gemäß medizinischer Plausibilität erfolgen. Sie erfolgte durch nur eine Person (J.F.) und wurde durch nur eine Person (A.E.) auf Plausibilität im Sinne einer Qualitätssicherung geprüft. Für eine parallele Auswahl, Interpretation und Bewertung durch mindestens zwei Personen standen keine Ressourcen zur Verfügung.
Die Häufigkeiten der im Beobachtungszeitraum kodierten Komorbiditäten werden zu illustrativen Zwecken – also im Bewusstsein der methodischen Schwächen – vergleichend präsentiert, auch wenn die Kollektive zum Beispiel bezüglich der Verteilung von Alter und Geschlecht nicht zwangsläufig vergleichbar sind. Bei jedem Wirkstoff gilt, dass die Versicherten im Beobachtungszeitraum auch mit anderen Thrombozytenaggregationshemmern (und zahlreichen anderen Wirkstoffen) behandelt worden sein konnten.
Ergebnisse
Jeweils deutlich mehr als 99% der analysierten Behandlungsfälle im Beobachtungszeitraum stammten aus ambulanten Behandlungsfällen (Tab. 2). Zwischen den verschiedenen Thrombozytenaggregationshemmern bestanden Unterschiede in der Verteilung von Geschlecht (Tab. 2) und Alter (Abb. 1). In allen Fällen dominierte das männliche Geschlecht (Tab. 2). Das Mindestalter (Tab. 2) wurde unter Clopidogrel bei 125 bis 212 Versicherten (Minimum und Maximum aufgrund der Datenschutzregelung) unterschritten, unter Prasugrel bei 1 bis 30 Versicherten, unter Ticagrelor bei 3 bis 90 Versicherten.
Angesichts der Grenzen einer praktikablen Operationalisierung war für Acetylsalicylsäure ein falsch häufiger apparenter Off-Label-Use in Kauf genommen worden, den es durch Rekonstruktionen zu korrigieren galt. Unter den häufig kodierten ICD-Codes in dieser Off-Label-Use-Gruppe fanden sich die Codes I64 (Schlaganfall, nicht als Blutung oder Infarkt bezeichnet) mit 69204 Nennungen und I69.4 (Folgen eines Schlaganfalls, nicht als Blutung oder Infarkt bezeichnet) mit 22199 Nennungen. Diese Codes waren wegen ihrer Unspezifität nicht in die Operationalisierung einbezogen worden. Die Codes I64 und I69.4 dürften aber zu den unter Erhaltungstherapie verwendeten Codes gehören. Wurden auch Codes, die mit Schmerz bzw. Fieber verbunden sind, einbezogen (Tab. 3), dann erwies sich der apparente Off-Label-Use nominal vollständig als In-Label-Use. Allerdings sind die Codes insbesondere bezüglich der Codes zum Symptom „Schmerz“ nicht disjunkt. Schließt man diese aus, bleibt es bei einer vollen Ausschöpfung der Off-Label-Use-Gruppe. Dies gilt erst recht, wenn die aus ICD-Kapitel I (A00–B99 Bestimmte infektiöse und parasitäre Krankheiten) kodierten 322641 Nennungen einbezogen würden, bei denen ASS zum Beispiel der Fiebersenkung gegolten haben könnte. Andererseits können die Versicherten im Beobachtungszeitraum aber auch mehrere der hier berücksichtigten Krankheiten erlitten haben. Dennoch erscheint zumindest möglich, dass Acetylsalicylsäure vollständig konform mit den zugelassenen Anwendungsgebieten verordnet wurde.
Tab. 2. Verordnung von Thrombozytenaggregationshemmern: Synopse der Ergebnisse (OLU =Off-Label-Use); infolge der Datenschutzregelung kann sich ergeben, dass die Maxima rechnerisch unter den Minima liegen
|
ASS |
Clopidogrel |
Prasugrel |
Ticagrelor |
|
|
Total min. |
2793359 |
854109 |
37907 |
9854 |
|
Total max. |
2793388 |
854196 |
38023 |
10057 |
|
Ausschließlich ambulant min. |
99,90% |
99,87% |
99,87% |
99,95% |
|
Ausschließlich ambulant max. |
99,90% |
99,87% |
99,87% |
99,37% |
|
Anteil weiblich min. |
45,7% |
37,7% |
23,0% |
29,6% |
|
Anteil weiblich max. |
45,7% |
37,7% |
23,3% |
31,2% |
|
OLU vor Rekonstruktion min. |
18,5% |
24,8% |
14,1% |
3,6% |
|
OLU vor Rekonstruktion max. |
18,5% |
24,8% |
14,3% |
4,7% |
|
OLU nach Rekonstruktion |
0% |
2% |
1% |
1% |
|
Alter <18 Jahre min. |
0,230% |
0,015% |
0,003% |
0,010% |
|
Alter <18 Jahre max. |
0,231% |
0,025% |
0,079% |
0,298% |
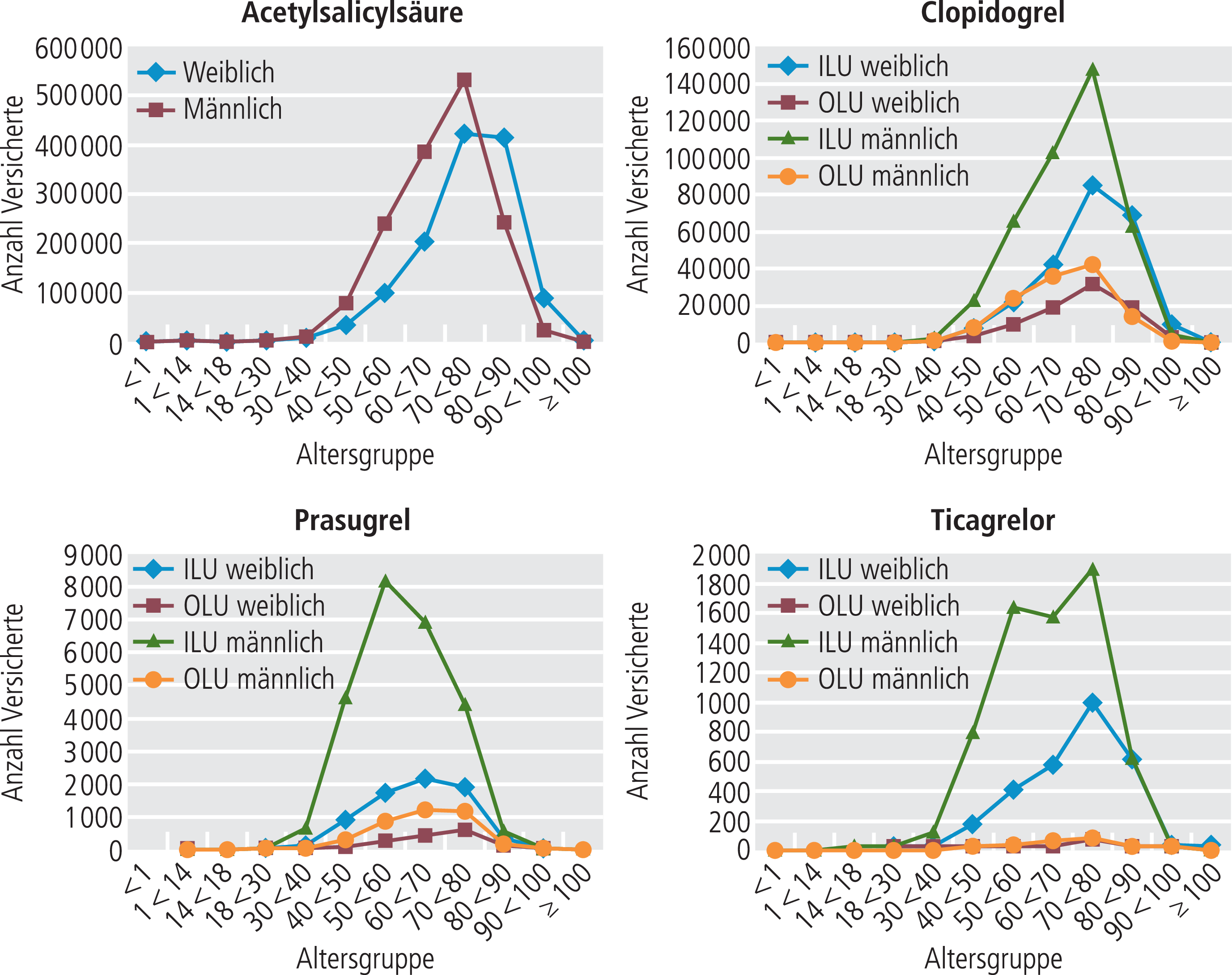
Abb. 1. Verordnung von Acetylsalicylsäure, Clopidogrel, Prasugrel und Ticagrelor nach Altersgruppen und Geschlecht (ILU: In-Label-Use; OLU: Off-Label-Use)
Tab. 3. In der Off-Label-Use-Gruppe der mit Acetylsalicylsäure (ASS) Behandelten genannte, ausgewählte Diagnosen, die mit einem In-Label-Use vereinbar sind
|
In-Label-Use |
Off-Label-Use |
|||
|
Vor Rekonstruktion min. |
2277574 |
515785 |
||
|
Vor Rekonstruktion max. |
2277603 |
515785 |
||
|
Total min. |
2793359 |
|||
|
Total max. |
2793388 |
|||
|
Total min. |
81,5% |
18,5% |
||
|
Total max. |
81,5% |
18,5% |
||
|
G43.- Migräne |
20810 |
|||
|
G44.- Kopfschmerz |
11052 |
|||
|
G45 bis G46.8 Hirnischämien, TIA |
86964 |
|||
|
G50 bis G54 Neuralgien, Phantomschmerz |
6138 |
|||
|
I64 Schlaganfall, nicht als Blutung oder Infarkt bezeichnet |
69204 |
|||
|
I69.4 Folgen eines Schlaganfalls, nicht als Blutung oder Infarkt bezeichnet |
22199 |
|||
|
M16.9 Koxarthrose, nicht näher bezeichnet |
47578 |
|||
|
M17.9 Gonarthrose, nicht näher bezeichnet |
78573 |
|||
|
M19.91 Arthrose, nicht näher bezeichnet: Schulterregion [Klavikula, Skapula, Akromioklavikular-, Schulter-, Sternoklavikulargelenk] |
13584 |
|||
|
M25.5 bis M25.59 Gelenkschmerzen |
35116 |
|||
|
M48.2 Baastrup-Syndrom |
2302 |
|||
|
M54.2 bis M54.99 Neuralgien, Rückenschmerz |
181418 |
|||
|
M79.1 bis M79.70 Myalgien, Neuralgien |
37093 |
|||
|
R50.8 bis R50.9 Fieber |
7298 |
|||
|
R51 bis R52.9 Schmerz |
65767 |
|||
|
In-Label-Use |
Off-Label-Use |
|||
|
Nach Rekonstruktion min. |
2962670 |
–169311 |
||
|
Nach Rekonstruktion max. |
2962699 |
–169311 |
||
|
Total min. |
2793359 |
|||
|
Total max. |
2793388 |
|||
|
Total min. |
106,1% |
–6,1% |
||
|
Total max. |
106,1% |
–6,1% |
||
Bei der Aufklärung des apparenten Off-Label-Use von Ticagrelor war zu berücksichtigen, dass es sich hier um nur 353 bis 469 Versicherte handelte, woraus infolge der Datenschutzregelung Verzerrungen resultierten. Der Einschluss von Vorhofflattern (Tab. 4) als den In-Label-Use operationalisierend war überinklusiv. Die nicht als operationalisierend berücksichtigten Codes aus dem Bereich I25.- (Chronische ischämische Herzkrankheit) dürften die unter Erhaltungstherapie verwendeten Codes sein. Bei Clopidogrel erklärten sie etwa 60% bis 100% des apparenten Off-Label-Use, bei Prasugrel und Ticagrelor war unter Berücksichtigung der aus der Datenschutzregelung resultierenden Unschärfen möglich, dass der Off-Label-Use vollständig erklärt wurde. Dieser scheinbare Off-Label-Use wäre also unvollständigen Operationalisierungen anzulasten. Die Codes sind nicht disjunkt, daran exemplifiziert, dass unter den drei Wirkstoffen bei mehr als 50% (Tab. 4) der unspezifische Code I25.9 (Chronische ischämische Herzkrankheit, nicht näher bezeichnet) mindestens einmal im Beobachtungszeitraum kodiert worden war, sowohl bei apparentem In-Label-Use als auch bei Off-Label-Use als Signal eines generellen Trends zu unspezifischem Kodieren.
Tab. 4. Synopse der den In-Label-Use operationalisierenden ICD-10-GM-Codes mindestens eines der vier Thrombozytenaggregationshemmer mit den Häufigkeiten in der jeweiligen Gruppe
|
ICD-Code |
ICD-Titel 2010/2011 |
Anteil an |
Anteil an Clopidogrel ILU |
Anteil an Clopidogrel OLU |
Anteil an Prasugrel ILU |
Anteil an Prasugrel OLU |
Anteil an Ticagrelor ILU |
Anteil an Ticagrelor OLU |
|
E11.50 |
Nicht primär insulinabhängiger Diabetes mellitus (Typ-2-Diabetes): Mit peripheren vaskulären Komplikationen: Nicht als entgleist bezeichnet |
3,34% |
6,72% |
3,19% |
6,31% |
4,12% |
42,49% |
|
|
I20.0 |
Instabile Angina pectoris |
5,61% |
13,01% |
16,35% |
28,10% |
24,69% |
||
|
I21.0 |
Akuter transmuraler Myokardinfarkt der Vorderwand |
4,17% |
9,82% |
30,44% |
25,06% |
|||
|
I21.1 |
Akuter transmuraler Myokardinfarkt der Hinterwand |
4,95% |
11,34% |
32,37% |
25,78% |
|||
|
I21.2 |
Akuter transmuraler Myokardinfarkt an sonstigen Lokalisationen |
0,77% |
1,95% |
5,68% |
6,48% |
|||
|
I21.3 |
Akuter transmuraler Myokardinfarkt an nicht näher bezeichneter Lokalisation |
0,41% |
1,03% |
2,96% |
4,03% |
|||
|
I21.4 |
Akuter subendokardialer Myokardinfarkt |
5,14% |
18,64% |
32,55% |
51,10% |
|||
|
I21.9 |
Akuter Myokardinfarkt, nicht näher bezeichnet |
12,12% |
24,15% |
46,81% |
40,72% |
|||
|
I22.0 |
Rezidivierender Myokardinfarkt der Vorderwand |
0,12% |
0,29% |
1,43% |
4,10% |
|||
|
I22.1 |
Rezidivierender Myokardinfarkt der Hinterwand |
0,13% |
0,29% |
1,38% |
3,16% |
|||
|
I22.8 |
Rezidivierender Myokardinfarkt an sonstigen Lokalisationen |
0,08% |
0,21% |
1,03% |
2,21% |
|||
|
I22.9 |
Rezidivierender Myokardinfarkt an nicht näher bezeichneter Lokalisation |
0,21% |
0,53% |
1,78% |
4,10% |
|||
|
I24.0 |
Koronarthrombose ohne nachfolgenden Myokardinfarkt |
0,12% |
0,25% |
0,31% |
1,07% |
4,50% |
3,16% |
17,00% |
|
I24.1 |
Postmyokardinfarkt-Syndrom |
0,21% |
0,39% |
0,19% |
1,52% |
3,37% |
3,47% |
|
|
I24.8 |
Sonstige Formen der akuten ischämischen Herzkrankheit |
1,08% |
1,59% |
1,58% |
2,45% |
6,18% |
4,74% |
33,99% |
|
I24.9 |
Akute ischämische Herzkrankheit, nicht näher bezeichnet |
1,12% |
2,50% |
1,90% |
6,17% |
6,24% |
||
|
I25.0 |
Atherosklerotische Herz-Kreislauf-Krankheit, so beschrieben |
3,92% |
5,87% |
4,14% |
5,23% |
8,69% |
6,50% |
42,49% |
|
I25.1 |
Atherosklerotische Herzkrankheit |
2,57% |
3,52% |
3,62% |
3,71% |
8,73% |
5,44% |
33,99% |
|
I25.10 |
Atherosklerotische Herzkrankheit: Ohne hämodynamisch wirksame Stenosen |
4,42% |
5,12% |
4,62% |
4,88% |
8,58% |
5,46% |
59,49% |
|
I25.11 |
Atherosklerotische Herzkrankheit: Ein-Gefäßerkrankung |
10,41% |
19,36% |
21,41% |
39,36% |
31,07% |
37,29% |
84,99% |
|
I25.12 |
Atherosklerotische Herzkrankheit: Zwei-Gefäßerkrankung |
9,72% |
21,16% |
19,89% |
39,46% |
34,61% |
37,30% |
84,99% |
|
I25.13 |
Atherosklerotische Herzkrankheit: Drei-Gefäßerkrankung |
13,95% |
29,26% |
21,65% |
41,31% |
38,30% |
43,61% |
67,99% |
|
I25.14 |
Atherosklerotische Herzkrankheit: Stenose des linken Hauptstammes |
1,48% |
3,25% |
2,29% |
5,86% |
8,71% |
7,15% |
50,99% |
|
I25.15 |
Atherosklerotische Herzkrankheit: Mit stenosierten Bypass-Gefäßen |
0,84% |
2,56% |
1,60% |
3,59% |
6,76% |
6,14% |
17,00% |
|
I25.16 |
Atherosklerotische Herzkrankheit: Mit stenosierten Stents |
1,14% |
3,99% |
3,21% |
12,74% |
10,72% |
10,37% |
59,49% |
|
I25.19 |
Atherosklerotische Herzkrankheit: Nicht näher bezeichnet |
16,37% |
23,17% |
20,78% |
30,33% |
29,94% |
33,20% |
84,99% |
|
I25.2 |
Alter Myokardinfarkt |
2,13% |
3,05% |
1,53% |
4,65% |
5,62% |
5,76% |
17,00% |
|
I25.20 |
Alter Myokardinfarkt: 29 Tage bis unter 4 Monate zurückliegend |
1,82% |
6,15% |
0,83% |
19,21% |
5,62% |
18,84% |
25,50% |
|
I25.21 |
Alter Myokardinfarkt: 4 Monate bis unter 1 Jahr zurückliegend |
1,63% |
6,09% |
16,63% |
6,75% |
10,08% |
8,50% |
|
|
I25.22 |
Alter Myokardinfarkt: 1 Jahr und länger zurückliegend |
9,35% |
15,62% |
6,32% |
19,01% |
10,96% |
16,12% |
50,99% |
|
I25.29 |
Alter Myokardinfarkt: Nicht näher bezeichnet |
10,13% |
15,56% |
6,34% |
25,08% |
9,99% |
18,98% |
42,49% |
|
I25.3 |
Herz(-Wand)-Aneurysma |
0,78% |
1,46% |
0,63% |
2,67% |
5,62% |
3,59% |
8,50% |
|
I25.4 |
Koronararterien-Aneurysma |
0,09% |
0,22% |
0,26% |
1,23% |
4,50% |
3,47% |
|
|
I25.5 |
Ischämische Kardiomyopathie |
3,09% |
6,50% |
2,82% |
10,00% |
9,76% |
12,45% |
59,49% |
|
I25.6 |
Stumme Myokardischämie |
0,13% |
0,23% |
0,30% |
0,92% |
4,50% |
1,58% |
8,50% |
|
I25.8 |
Sonstige Formen der chronischen ischämischen Herzkrankheit |
2,95% |
4,39% |
3,44% |
5,42% |
8,11% |
5,48% |
59,49% |
|
I25.9 |
Chronische ischämische Herzkrankheit, nicht näher bezeichnet |
45,66% |
57,65% |
57,25% |
64,68% |
70,06% |
54,94% |
89,80% |
|
I48.0 |
Vorhofflattern |
0,23% |
0,35% |
1,01% |
2,81% |
1,58% |
||
|
I48.00 |
Vorhofflattern: Paroxysmal |
1,11% |
1,92% |
1,52% |
5,62% |
3,89% |
17,00% |
|
|
I48.01 |
Vorhofflattern: Chronisch |
0,31% |
0,52% |
0,92% |
3,37% |
2,53% |
8,50% |
|
|
I48.09 |
Vorhofflattern: Nicht näher bezeichnet |
0,64% |
0,99% |
0,98% |
3,93% |
3,16% |
25,50% |
|
|
I48.1 |
Vorhofflimmern |
1,48% |
2,08% |
1,19% |
5,06% |
2,53% |
59,49% |
|
|
I48.10 |
Vorhofflimmern: Paroxysmal |
9,36% |
15,07% |
8,28% |
12,27% |
12,21% |
93,48% |
|
|
I48.11 |
Vorhofflimmern: Chronisch |
7,60% |
11,42% |
3,87% |
9,26% |
7,20% |
76,49% |
|
|
I48.19 |
Vorhofflimmern: Nicht näher bezeichnet |
9,56% |
13,04% |
4,73% |
10,47% |
8,31% |
84,99% |
|
|
I63.0 |
Hirninfarkt durch Thrombose präzerebraler Arterien |
0,48% |
0,86% |
0,55% |
4,50% |
1,89% |
17,00% |
|
|
I63.1 |
Hirninfarkt durch Embolie präzerebraler Arterien |
0,34% |
0,60% |
0,92% |
3,93% |
1,89% |
17,00% |
|
|
I63.2 |
Hirninfarkt durch nicht näher bezeichneten Verschluss oder Stenose präzerebraler Arterien |
0,46% |
0,86% |
0,83% |
5,06% |
2,53% |
8,50% |
|
|
I63.3 |
Hirninfarkt durch Thrombose zerebraler Arterien |
2,10% |
2,78% |
0,92% |
5,62% |
2,84% |
33,99% |
|
|
I63.4 |
Hirninfarkt durch Embolie zerebraler Arterien |
2,10% |
3,07% |
1,17% |
6,18% |
3,16% |
42,49% |
|
|
I63.5 |
Hirninfarkt durch nicht näher bezeichneten Verschluss oder Stenose zerebraler Arterien |
3,73% |
5,04% |
1,44% |
5,62% |
3,79% |
59,49% |
|
|
I63.6 |
Hirninfarkt durch Thrombose der Hirnvenen, nichteitrig |
0,02% |
0,06% |
0,18% |
||||
|
I63.8 |
Sonstiger Hirninfarkt |
1,21% |
1,71% |
0,92% |
5,06% |
2,53% |
42,49% |
|
|
I63.9 |
Hirninfarkt, nicht näher bezeichnet |
7,47% |
10,56% |
1,99% |
7,64% |
4,69% |
42,49% |
|
|
I65.0 |
Verschluss und Stenose der A. vertebralis |
0,75% |
1,89% |
1,12% |
5,06% |
2,84% |
25,50% |
|
|
I65.1 |
Verschluss und Stenose der A. basilaris |
0,16% |
0,46% |
0,37% |
3,37% |
1,26% |
||
|
I65.2 |
Verschluss und Stenose der A. carotis |
9,73% |
20,06% |
6,45% |
12,03% |
8,20% |
84,99% |
|
|
I65.3 |
Verschluss und Stenose mehrerer und beidseitiger präzerebraler Arterien |
1,07% |
2,60% |
1,24% |
5,06% |
2,53% |
33,99% |
|
|
I65.8 |
Verschluss und Stenose sonstiger präzerebraler Arterien |
0,14% |
0,34% |
0,74% |
3,37% |
1,58% |
8,50% |
|
|
I65.9 |
Verschluss und Stenose einer nicht näher bezeichneten präzerebralen Arterie |
0,35% |
0,80% |
1,01% |
3,93% |
1,89% |
25,50% |
|
|
I66.0 |
Verschluss und Stenose der A. cerebri media |
0,24% |
0,58% |
0,64% |
3,93% |
1,58% |
25,50% |
|
|
I66.1 |
Verschluss und Stenose der A. cerebri anterior |
0,04% |
0,10% |
0,18% |
0,56% |
|||
|
I66.2 |
Verschluss und Stenose der A. cerebri posterior |
0,07% |
0,15% |
0,46% |
0,32% |
25,50% |
||
|
I66.3 |
Verschluss und Stenose der A. cerebelli |
0,10% |
0,20% |
0,74% |
2,81% |
2,21% |
8,50% |
|
|
I66.4 |
Verschluss und Stenose mehrerer und beidseitiger zerebraler Arterien |
0,08% |
0,22% |
0,64% |
2,81% |
1,26% |
||
|
I66.8 |
Verschluss und Stenose sonstiger zerebraler Arterien |
0,06% |
0,14% |
0,28% |
2,81% |
0,32% |
8,50% |
|
|
I66.9 |
Verschluss und Stenose einer nicht näher bezeichneten zerebralen Arterie |
0,23% |
0,43% |
0,83% |
2,81% |
1,58% |
8,50% |
|
|
I69.3 |
Folgen eines Hirninfarkts |
6,60% |
9,11% |
1,50% |
6,28% |
4,58% |
67,99% |
|
|
I70.2 |
Atherosklerose der Extremitätenarterien |
0,54% |
1,33% |
1,02% |
5,06% |
2,21% |
||
|
I70.20 |
Atherosklerose der Extremitätenarterien: Sonstige und nicht näher bezeichnet |
5,58% |
13,12% |
4,07% |
5,02% |
8,81% |
7,36% |
76,49% |
|
I70.21 |
Atherosklerose der Extremitätenarterien: Becken-Bein-Typ, mit belastungsinduziertem Ischämieschmerz |
4,88% |
14,82% |
3,75% |
5,23% |
11,82% |
6,40% |
59,49% |
|
I70.22 |
Atherosklerose der Extremitätenarterien: Becken-Bein-Typ, mit Ruheschmerzen |
1,51% |
4,61% |
1,00% |
1,65% |
6,18% |
3,64% |
25,50% |
|
I70.23 |
Atherosklerose der Extremitätenarterien: Becken-Bein-Typ, mit Ulzeration |
1,53% |
3,88% |
0,63% |
1,19% |
6,18% |
2,89% |
42,49% |
|
I70.24 |
Atherosklerose der Extremitätenarterien: Becken-Bein-Typ, mit Gangrän |
1,37% |
3,41% |
0,55% |
1,06% |
5,06% |
2,84% |
33,99% |
|
I70.25 |
Atherosklerose der Extremitätenarterien: Schulter-Arm-Typ, alle Stadien |
0,14% |
0,37% |
0,19% |
0,55% |
5,62% |
2,53% |
17,00% |
|
I73.9 |
Periphere Gefäßkrankheit, nicht näher bezeichnet |
13,96% |
31,95% |
9,33 % |
16,43% |
10,78% |
84,99% |
|
|
I79.2 |
Periphere Angiopathie bei anderenorts klassifizierten Krankheiten |
3,23% |
7,09% |
2,94% |
7,12% |
4,42% |
42,49% |
|
|
M30.3 |
Mukokutanes Lymphknotensyndrom (Kawasaki-Krankheit) |
0,03% |
0,03% |
0,10% |
0,32% |
|||
|
Z95.1 |
Vorhandensein eines aortokoronaren Bypasses |
9,97% |
14,49% |
9,52% |
9,62% |
13,79% |
12,56% |
|
|
Z95.5 |
Vorhandensein eines Implantats oder Transplantats nach koronarer Gefäßplastik |
12,01% |
27,76% |
24,84% |
50,68% |
46,67% |
44,32% |
|
|
Z95.88 |
Vorhandensein von sonstigen kardialen oder vaskulären Implantaten oder Transplantaten |
5,20% |
13,49% |
7,45% |
13,05% |
15,72% |
12,42% |
ILU: In-Label-Use gemäß Operationalisierung, OLU: Off-Label-Use gemäß Operationalisierung
Die Code-Bereiche I48.- (Vorhofflimmern und Vorhofflattern), I63.- (Hirninfarkt), I65.- (Verschluss und Stenose präzerebraler Arterien ohne resultierenden Hirninfarkt), I66.- (Verschluss und Stenose zerebraler Arterien ohne resultierenden Hirninfarkt) und I69.3 (Folgen eines Hirninfarkts) wurden für Prasugrel und Ticagrelor nicht als operationalisierend gewertet, waren aber in den Off-Label-Use-Gruppen häufiger als in den In-Label-Use-Gruppen (hier also als Komorbiditäten) kodiert worden, woraus sich größere Anteile des Off-Label-Use erklären ließen. Der Bereich I70.2- (Atherosklerose der Extremitätenarterien) wurde bei Clopidogrel in der Datenbankabfrage unscharf als endständig interpretiert (Tab. 4), was etwa 5% bis 10% als scheinbaren Off-Label-Use erklären könnte. Für Prasugrel und Ticagrelor war dieser zutreffend nicht als operationalisierend gewertete Code-Bereich in den Off-Label-Use-Gruppen häufiger als in den In-Label-Use-Gruppen (hier also als Komorbiditäten) kodiert worden und konnte nominal 10% bis über 80% als potenziell beabsichtigten Off-Label-Use erklären. Entsprechendes gilt (Tab. 4) für die unspezifischen Codes I739 (Periphere Gefäßkrankheit, nicht näher bezeichnet) und I79.2 (Periphere Angiopathie bei anderenorts klassifizierten Krankheiten).
Der In-Label-Use von Clopidogrel erwies sich als unvollständig operationalisiert, indem Z95.5 (Vorhandensein eines Implantats oder Transplantats nach koronarer Gefäßplastik) und Z95.88 (Vorhandensein von sonstigen kardialen oder vaskulären Implantaten oder Transplantaten) hätten einbezogen werden können. Damit wären mindestens 25% als scheinbarer Off-Label-Use erklärt. Entsprechendes gilt für Prasugrel, wo mindestens 47% als scheinbarer Off-Label-Use erklärt wären.
Formal war also möglich, dass alle vier Thrombozytenaggregationshemmer vollständig konform mit den zugelassenen Anwendungsgebieten eingesetzt wurden, soweit diese sich durch ICD-Codes operationalisieren lassen, und man die für beabsichtigten Off-Label-Use grundsätzlich geeigneten Codes als Ausdruck zufälliger Komorbiditäten interpretiert (und dabei die Häufungen in den Off-Label-Use-Gruppen ignoriert).
Wenn auch selten, so doch häufiger in den Off-Label-Use- als in den In-Label-Use-Gruppen, fanden sich Codes aus den Code-Bereichen I60.-, I67.- und I72.-, also bezüglich Aneurysmen der hirnversorgenden Arterien und Subarachnoidalblutungen (Tab. 5). Selbstverständlich kann nicht ausgeschlossen werden, dass sich im Beobachtungszeitraum zufällig solche Blutungen ereigneten (theoretisch könnten die Thrombozytenaggregationshemmer das Risiko erhöhen), was aber schwer mit der Häufung der Codes in den Off-Label-Use-Gruppen vereinbar wäre. Vielmehr ist bekannt, dass die Thrombozytenaggregationshemmer im Kontext interventionell-radiologischer Maßnahmen im Wege des Off-Label-Use eingesetzt werden, nicht aber in welchem Umfang. Die Codes I60.0 bis I60.6 sind disjunkt. Ignoriert man die Möglichkeit mehrerer gleichzeitig bestehender Aneurysmen, so waren als Schätzung (Datenschutzregelung) unter Clopidogrel etwa 2340, unter Prasugrel etwa 450 Versicherte betroffen (für Ticagrelor war eine Schätzung infolge der Datenschutzregelung nicht praktikabel). Der Code Z958.8 (Vorhandensein von sonstigen kardialen oder vaskulären Implantaten oder Transplantaten) ist zu unspezifisch, um eine eindeutige Zuordnung zu hirnversorgenden Arterien (Stents bei Aneurysmen oder Stenosen) zu erlauben.
Tab. 5. Häufigkeit von ICD-Codes aus dem Bereich der Subarachnoidalblutungen und Hirnarterienaneurysmen
|
ICD-Code |
ICD-Titel 2010/2011 |
Anteil an ASS |
Anteil an Clopidogrel ILU |
Anteil an Clopidogrel OLU |
Anteil an Prasugrel ILU |
Anteil an Prasugrel OLU |
Anteil an Ticagrelor ILU |
Anteil an Ticagrelor OLU |
|
I60.0 |
Subarachnoidalblutung, vom Karotissiphon oder der Karotisbifurkation ausgehend |
0,03% |
0,07% |
0,17% |
0,18% |
0,56% |
0,32% |
|
|
I60.1 |
Subarachnoidalblutung, von der A. cerebri media ausgehend |
0,04% |
0,05% |
0,17% |
0,28% |
0,32% |
||
|
I60.2 |
Subarachnoidalblutung, von der A. communicans anterior ausgehend |
0,04% |
0,06% |
0,21% |
0,18% |
2,25% |
0,32% |
8,50% |
|
I60.3 |
Subarachnoidalblutung, von der A. communicans posterior ausgehend |
0,03% |
0,05% |
0,14% |
0,28% |
1,69% |
||
|
I60.4 |
Subarachnoidalblutung, von der A. basilaris ausgehend |
0,03% |
0,06% |
0,14% |
0,09% |
2,25% |
||
|
I60.5 |
Subarachnoidalblutung, von der A. vertebralis ausgehend |
0,02% |
0,05% |
0,11% |
1,12% |
0,32% |
||
|
I60.6 |
Subarachnoidalblutung, von sonstigen intrakraniellen Arterien ausgehend |
0,03% |
0,05% |
0,16% |
0,18% |
0,56% |
8,50% |
|
|
I60.7 |
Subarachnoidalblutung, von nicht näher bezeichneter intrakranieller Arterie ausgehend |
0,05% |
0,07% |
0,20% |
0,18% |
0,56% |
0,95% |
8,50% |
|
I60.8 |
Sonstige Subarachnoidalblutung |
0,06% |
0,07% |
0,18% |
0,46% |
1,12% |
0,63% |
|
|
I60.9 |
Subarachnoidalblutung, nicht näher bezeichnet |
0,27% |
0,25% |
0,36% |
0,74% |
4,50% |
2,53% |
8,50% |
|
I67.0 |
Dissektion zerebraler Arterien |
0,08% |
0,11% |
0,20% |
0,37% |
1,12% |
0,63% |
|
|
I67.1 |
Zerebrales Aneurysma und zerebrale arteriovenöse Fistel |
0,04% |
0,06% |
0,21% |
0,18% |
3,93% |
8,50% |
|
|
I67.10 |
Zerebrales Aneurysma (erworben) |
0,23% |
0,30% |
0,62% |
0,74% |
6,18% |
1,26% |
50,99% |
|
I67.11 |
Zerebrale arteriovenöse Fistel (erworben) |
0,03% |
0,05% |
0,16% |
0,09% |
1,69% |
||
|
I72.0 |
Aneurysma und Dissektion der A. carotis |
0,15% |
0,22% |
0,32% |
1,01% |
5,06% |
0,63% |
50,99% |
|
1,13% |
1,49% |
3,35% |
4,97% |
32,60% |
7,89% |
144,48% |
ILU: In-Label-Use gemäß Operationalisierung; OLU: Off-Label-Use gemäß Operationalisierung
Zur Morbidität jenseits der zugelassenen Indikationen waren über 13000 ICD-Codes zu sichten. Tabelle 6 gibt einen Überblick. Die Anämien könnten in ursächlichem Zusammenhang mit den Thrombozytenaggregationshemmern stehen.
Tab. 6. Häufigkeiten (Auszug) von ICD-Codes zur allgemeinen Morbidität
|
ICD-Code |
ICD-Titel 2010/2011 |
Anteil an ASS |
Anteil an Clopidogrel ILU |
Anteil an Clopidogrel OLU |
Anteil an Prasugrel ILU |
Anteil an Prasugrel OLU |
Anteil an Ticagrelor ILU |
Anteil an Ticagrelor OLU |
|
D50.0 |
Eisenmangelanämie nach Blutverlust (chronisch) |
1,33% |
2,11% |
1,14% |
1,56% |
5,62% |
3,57% |
25,50% |
|
D50.8 |
Sonstige Eisenmangelanämien |
1,69% |
2,46% |
1,23% |
1,81% |
7,87% |
4,23% |
17,00% |
|
D50.9 |
Eisenmangelanämie, nicht näher bezeichnet |
4,36% |
5,33% |
3,50% |
3,45% |
6,99% |
5,19% |
42,49% |
|
D62 |
Akute Blutungsanämie |
7,02% |
10,66% |
5,19% |
6,94% |
9,05% |
9,71% |
59,49% |
|
D64.9 |
Anämie, nicht näher bezeichnet |
6,23% |
7,61% |
4,83% |
4,86% |
8,60% |
6,73% |
76,49% |
|
E11.90 |
Nicht primär insulinabhängiger Diabetes mellitus (Typ-2-Diabetes): Ohne Komplikationen: Nicht als entgleist bezeichnet |
34,70% |
38,57% |
28,86% |
30,51% |
37,87% |
33,18% |
93,48% |
|
E66.00 |
Adipositas durch übermäßige Kalorienzufuhr: Body-Mass-Index [BMI] von 30 bis unter 35 |
4,65% |
6,82% |
5,14% |
9,37% |
10,76% |
9,78% |
67,99% |
|
E66.01 |
Adipositas durch übermäßige Kalorienzufuhr: Body-Mass-Index [BMI] von 35 bis unter 40 |
2,27% |
2,96% |
2,14% |
3,79% |
6,60% |
4,95% |
67,99% |
|
E66.02 |
Adipositas durch übermäßige Kalorienzufuhr: Body-Mass-Index [BMI] von 40 und mehr |
1,34% |
1,49% |
1,14% |
2,02% |
5,62% |
3,47% |
25,50% |
|
E66.09 |
Adipositas durch übermäßige Kalorienzufuhr: Body-Mass-Index [BMI] nicht näher bezeichnet |
3,07% |
3,64% |
2,88% |
4,50% |
7,38% |
5,24% |
33,99% |
|
E66.99 |
Adipositas, nicht näher bezeichnet: Body-Mass-Index [BMI] nicht näher bezeichnet |
10,65% |
11,27% |
9,72% |
12,70% |
14,41% |
11,05% |
84,99% |
|
E78.0 |
Reine Hypercholesterinämie |
33,64% |
41,77% |
37,23% |
47,39% |
43,53% |
42,89% |
86,40% |
|
E78.2 |
Gemischte Hyperlipidämie |
17,18% |
28,37% |
21,20% |
38,03% |
35,79% |
36,43% |
67,99% |
|
E78.5 |
Hyperlipidämie, nicht näher bezeichnet |
31,41% |
41,73% |
33,65% |
48,28% |
44,46% |
43,55% |
77,34% |
|
E79.0 |
Hyperurikämie ohne Zeichen von entzündlicher Arthritis oder tophischer Gicht |
19,01% |
21,87% |
15,93% |
15,01% |
20,22% |
18,57% |
84,99% |
|
F17.1 |
Psychische und Verhaltensstörungen durch Tabak: Schädlicher Gebrauch |
10,16% |
16,37% |
10,09% |
28,14% |
16,28% |
20,63% |
101,98% |
|
F17.2 |
Psychische und Verhaltensstörungen durch Tabak: Abhängigkeitssyndrom |
3,09% |
5,27% |
3,07% |
9,57% |
7,91% |
8,46% |
50,99% |
|
G63.2 |
Diabetische Polyneuropathie |
7,30% |
9,91% |
3,96% |
4,87% |
9,76% |
6,93% |
59,49% |
|
I10.00 |
Benigne essenzielle Hypertonie: Ohne Angabe einer hypertensiven Krise |
45,68% |
60,44% |
47,79% |
64,95% |
65,15% |
66,71% |
122,10% |
|
I10.9 |
Essenzielle Hypertonie, nicht näher bezeichnet |
9,13% |
9,24% |
8,17% |
6,62% |
9,95% |
7,62% |
84,99% |
|
I10.90 |
Essenzielle Hypertonie, nicht näher bezeichnet: Ohne Angabe einer hypertensiven Krise |
73,88% |
77,12% |
71,30% |
70,45% |
76,02% |
69,62% |
121,25% |
|
I11.90 |
Hypertensive Herzkrankheit ohne (kongestive) Herzinsuffizienz: Ohne Angabe einer hypertensiven Krise |
11,08% |
14,40% |
12,53% |
13,64% |
18,08% |
16,70% |
76,49% |
|
I50.9 |
Herzinsuffizienz, nicht näher bezeichnet |
17,18% |
18,47% |
11,33% |
11,82% |
14,22% |
14,17% |
101,98% |
|
J44.99 |
Chronische obstruktive Lungenkrankheit, nicht näher bezeichnet: FEV1 nicht näher bezeichnet |
10,70% |
13,11% |
9,55% |
8,35% |
11,84% |
10,36% |
67,99% |
|
K21.0 |
Gastroösophageale Refluxkrankheit mit Ösophagitis |
11,83% |
14,05% |
13,60% |
12,06% |
15,44% |
12,94% |
84,99% |
|
M16.9 |
Koxarthrose, nicht näher bezeichnet |
10,95% |
10,81% |
9,26% |
6,37% |
10,36% |
8,56% |
84,99% |
|
M81.99 |
Osteoporose, nicht näher bezeichnet: Nicht näher bezeichnete Lokalisationen |
9,26% |
8,39% |
7,90% |
3,34% |
7,38% |
6,97% |
76,49% |
|
Z95.0 |
Vorhandensein eines implantierten Herzschrittmachers oder eines implantierten Kardiodefibrillators |
6,21% |
8,64% |
4,36% |
5,63% |
9,78% |
7,73% |
59,49% |
ILU: In-Label-Use gemäß Operationalisierung; OLU: Off-Label-Use gemäß Operationalisierung
Bei den psychischen Komorbiditäten fanden sich keine Häufungen, aber eine Bestätigung des generellen Trends zu unspezifischem Kodieren in Form der Dominanz des Code F32.9 (Depressive Episode, nicht näher bezeichnet; Tab. 7).
Tab. 7. Häufigkeiten psychischer Komorbidität (Auszug) unter Thrombozytenaggregationshemmern
|
ICD-Code |
ICD-Titel 2010/2011 |
Anteil an |
Anteil an Clopidogrel ILU |
Anteil an Clopidogrel OLU |
Anteil an Prasugrel ILU |
Anteil an Prasugrel OLU |
Anteil an Ticagrelor ILU |
Anteil an Ticagrelor OLU |
|
F32.0 |
Leichte depressive Episode |
1,97% |
2,23% |
1,74% |
2,14% |
6,75% |
3,79% |
42,49% |
|
F32.1 |
Mittelgradige depressive Episode |
4,37% |
4,56% |
3,67% |
4,37% |
6,86% |
5,23% |
59,49% |
|
F32.2 |
Schwere depressive Episode ohne psychotische Symptome |
2,17% |
2,18% |
1,88% |
2,30% |
6,18% |
4,10% |
50,99% |
|
F32.3 |
Schwere depressive Episode mit psychotischen Symptomen |
0,45% |
0,42% |
0,42% |
1,01% |
5,62% |
2,53% |
8,50% |
|
F32.8 |
Sonstige depressive Episoden |
2,64% |
2,70% |
2,30% |
2,23% |
6,18% |
3,49% |
25,50% |
|
F32.9 |
Depressive Episode, nicht näher bezeichnet |
14,79% |
14,83% |
13,11% |
11,95% |
13,19% |
12,30% |
93,48% |
|
F33.0 |
Rezidivierende depressive Störung, gegenwärtig leichte Episode |
0,58% |
0,62% |
0,57% |
0,94% |
3,93% |
2,84% |
33,99% |
|
F33.1 |
Rezidivierende depressive Störung, gegenwärtig mittelgradige Episode |
1,68% |
1,66% |
1,65% |
2,12% |
5,62% |
3,47% |
25,50% |
|
F33.2 |
Rezidivierende depressive Störung, gegenwärtig schwere Episode ohne psychotische Symptome |
1,24% |
1,23% |
1,23% |
1,59% |
5,62% |
3,47% |
17,00% |
|
F33.3 |
Rezidivierende depressive Störung, gegenwärtig schwere Episode mit psychotischen Symptomen |
0,27% |
0,23% |
0,30% |
0,92% |
2,25% |
2,53% |
8,50% |
|
F33.4 |
Rezidivierende depressive Störung, gegenwärtig remittiert |
0,25% |
0,25% |
0,27% |
0,92% |
3,37% |
2,53% |
|
|
F33.8 |
Sonstige rezidivierende depressive Störungen |
0,53% |
0,56% |
0,48% |
0,83% |
5,06% |
2,53% |
17,00% |
|
F33.9 |
Rezidivierende depressive Störung, nicht näher bezeichnet |
2,13% |
2,06% |
1,96% |
1,72% |
5,62% |
3,79% |
33,99% |
|
F34.1 |
Dysthymia |
1,58% |
1,63% |
1,56% |
1,97% |
5,06% |
3,79% |
33,99% |
|
F40.1 |
Soziale Phobien |
0,10% |
0,11% |
0,19% |
0,55% |
3,37% |
1,58% |
|
|
F41.0 |
Panikstörung (episodisch paroxysmale Angst) |
1,26% |
1,59% |
1,50% |
2,59% |
6,18% |
3,50% |
33,99% |
|
F41.1 |
Generalisierte Angststörung |
1,68% |
1,91% |
1,82% |
2,51% |
5,62% |
3,79% |
33,99% |
|
F41.9 |
Angststörung, nicht näher bezeichnet |
2,18% |
2,54% |
2,33% |
3,54% |
6,18% |
4,34% |
42,49% |
|
F43.2 |
Anpassungsstörungen |
2,64% |
2,98% |
2,53% |
4,43% |
7,38% |
4,75% |
59,49% |
ILU: In-Label-Use gemäß Operationalisierung; OLU: Off-Label-Use gemäß Operationalisierung
Seltene Krankheiten als mögliche Off-Label-Indikation für einen der Thrombozytenaggregationshemmer wurden nicht entdeckt.
Diskussion
In diesem Projekt werden erstmals sogenannte Routinedaten der Krankenkassen als Vollerfassung aller gesetzlich Krankenversicherten – anhand der Daten nach §§303a ff. SGBV – zur Frage des Off-Label-Use und für Zwecke der Pharmakovigilanz genutzt. Das Beispiel der hier dargestellten Thrombozytenaggregationshemmer belegt die grundsätzliche Praktikabilität dieses Forschungsansatzes, obwohl diese Routinedaten zu gänzlich anderen Zwecken übermittelt und eben nicht speziell erhoben werden, nämlich zu Abrechnungszwecken mit Sekundärnutzung für die Kalkulation des Risikostrukturausgleichs. Bei der Interpretation dieser Routinedaten müssen selbstverständlich die daraus resultierenden Schwächen der Daten berücksichtigt werden.
Den Leitlinien und Empfehlungen der Arbeitsgruppe Erhebung und Nutzung von Sekundärdaten (AGENS 2012) wurde – soweit anwendbar – gefolgt, insbesondere bezüglich des Datenschutzes. Interne oder externe Validierungen der Daten, hier also insbesondere der ATC- und ICD-Codes, waren nicht möglich und angesichts der Vollerfassung vermutlich auch nicht notwendig. Die Operationalisierung des In-Label-Use war konservativ zugunsten eines In-Label-Use, indem die auch nur einmalige Kodierung eines In-Label-Use operationalisierenden ICD-Codes – hier auch unspezifischer Codes – im zweijährigen Beobachtungszeitraum akzeptiert wurde als „Beleg“ für einen tatsächlichen In-Label-Use. Dieses „Vertrauen“ in die Kodierung wird auch unter anderen der Gesundheitsberichterstattung (GBE) des Bundes zugrunde gelegt [5], ganz abgesehen von der Nutzung der Daten für die Kalkulation des Risikostrukturausgleichs zwischen den GKVen. Dennoch liegt ohne Zweifel in der Datenqualität eine bedeutsame Limitation der Untersuchung. Dazu gehört auch, dass die Rekonstruktionen und die Identifikation der den Off-Label-Use mutmaßlich motivierenden Diagnosen letztlich nicht frei von subjektivem Ermessen sind.
Rekonstruktionen offenbarten die Grenzen der Möglichkeit, In-Label-Use bei den Thrombozytenaggregationshemmern a priori umfassend zu operationalisieren. Rekonstruktionen erlauben nur semiquantitative Schätzungen, auch infolge der hier anzuwendenden Datenschutzregelung. Nach Rekonstruktion belief sich der Off-Label-Use von Clopidogrel, Prasugrel und Ticagrelor auf nominal höchsten 1% bis 2%; bei ASS bestand wahrscheinlich aufgrund der breiteren Indikationsgebiete überhaupt kein Off-Label-Use. Dabei ist allerdings zu berücksichtigen, dass die Anwendungseinschränkungen und Kontraindikationen der jeweiligen Wirkstoffe nicht berücksichtigt werden konnten. Grundsätzlich werden Thrombozytenaggregationshemmer bei endovaskulären Interventionen nicht nur an den Koronararterien – hier im In-Label Use –, sondern auch an hirnversorgenden und peripheren Arterien – dann im Off-Label-Use – eingesetzt [2, 7]. Dies gilt derzeit nicht für die neu etablierte endovaskuläre Thrombektomie mittels Stent-Retriever an hirnversorgenden Arterien als Therapie des akuten ischämischen Hirninfarkts [6], weil hier der Stent nicht in der Arterie verbleibt. Hierzu fehlen bisher allerdings systematische Studien [7]. Seltene Erkrankungen als Motiv für einen Off-Label-Use von Thrombozytenaggregationshemmern konnten in dieser Stichprobe nicht identifiziert werden.
Die den Abrechnungsdaten zu entnehmende Last an Risikofaktoren (Adipositas, Hypertonie usw.) liegt zum Teil in der Größenordnung systematischer Studien, auch darüber und darunter, wobei säkulare Trends zu würdigen wären [3], für die für Deutschland Daten fehlen. Die in den Abrechnungsdaten kodierten weiteren Komorbiditäten – hier beispielsweise Eisenmangel- und Blutungsanämien – können nicht zwangsläufig kausal dem Wirkstoff – hier Thrombozytenaggregationshemmern – zugeschrieben werden. Es ist davon auszugehen, dass die Patienten im Beobachtungszeitraum mit weiteren Wirkstoffen behandelt wurden, die nicht erfasst wurden. Das wäre mittels spezifischer Datenbankabfragen nur teilweise möglich, da verschreibungsfreie Arzneimittel nicht erfasst sind, aber selbst dann bliebe es bei Assoziationen ohne zwingenden Kausalzusammenhang.
Indem die Daten originär Abrechnungszwecken gelten, muss mit unvollständiger Kodierung gerechnet werden. Folglich können die berichteten beispielsweise psychischen Komorbiditäten Unterschätzungen darstellen. Die hier gefundene „Zwei-Jahres-Prävalenz“ zumindest einer „nicht näher bezeichneten depressiven Episode (ICD-Code F32.9) – als Beispiel für einen generellen Trend zu unspezifischem Kodieren – lag in der in anderen Studien – bei großer Variabilität – gefundenen Größenordnung von ungefähr 15% [4].
Danksagung
Dem Bundesministerium für Gesundheit wird nachdrücklich für die finanzielle Unterstützung des Projekts gedankt. Herrn Prof. Dr. W. Schwerdtfeger, früherer Präsident des BfArM, wird herzlich für die Unterstützung bei der Initiierung dieses Projekts gedankt. Herrn Dr. Jochen Dreß und Herrn Dr Michael Schopen, Deutsches Institut für Medizinische Dokumentation und Information (DIMDI), gilt besonderer Dank für die Kooperation bei der Entwicklung der Datenbankabfrageskripte und deren Anwendung.
Interessenkonflikterklärung
JF hat in den letzten fünf Jahren Honorare für Beratertätigkeit von Amgen, Janssen, Lilly, Lundbeck, Nestlé, Novartis, Pfizer, Roche, St. Jude Medical, 3M, Sanvartis, Teva und dem Verband der privaten Krankenversicherung e.V. erhalten.
Die anderen Autoren geben an, keine Interessenkonflikte zu haben.
Literatur
1. Arbeitsgruppe Erhebung und Nutzung von Sekundärdaten (AGENS) der Deutschen Gesellschaft für Sozialmedizin und Prävention (DGSMP) und der Deutschen Gesellschaft für Epidemiologie (DGEpi) (2012) Gute Praxis Sekundärdatenanalyse (GPS) – Leitlinien und Empfehlungen. www.uni-ulm.de/fileadmin/website_uni_ulm/ethkom/Hinweise/Leitlinien_und_Empfehlungen_Gute_Praxis_Sekundäranalyse__GPS___2012_.pdf (letzter Zugriff am 14.12.2016).
2. Berlis A. Endovaskuläre Eingriffe in der interventionellen Neuroradiologie. Anaesthesist 2013;62:692–706.
3. Casagrande SS, Menke A, Cowie CC. Cardiovascular risk factors of adults age 20–49 years in the United States, 1971–2012: A series of cross-sectional studies. Plos One published online August 23, 2016; doi:10.1371/journal.pone.0161770.
4. Hare DL, Toukhsati SR, Johansson P, Jaarsma T. Depression and cardiovascular disease: a clinical review. Eur Heart J 2014;35: 1365–72.
5. Ohlmeier C, Frick J, Prütz F, Lampert T, et al. Nutzungsmöglichkeiten von Routinedaten der Gesetzlichen Krankenversicherung in der Gesundheitsberichterstattung des Bundes. Bundesgesundheitsbl 2014;57:464–72.
6. Widimsky P. Periprocedural antithrombotic medication in acute ischemic stroke treated by catheter-based thrombectomy. A review. Cor et Vasa 2015;57:e139–42.
7. Widimský P, Kočka V, Roháč F, Osmančík P. Periprocedural antithrombotic therapy during various types of percutaneous cardiovascular interventions. Eur Heart J Cardiovasc Pharmacother 2016;2:131–40.
Prof. Dr. med. Jürgen Fritze, Asternweg 65, 50259 Pulheim, E-Mail: juergen.fritze@dgn.de
Dr. med. Claudia Riedel, Angelika Escherich, Peggy Beinlich, Prof. Dr. Karl Broich, Priv.-Doz. Dr. Thomas Sudhop, Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), Kurt-Georg-Kiesinger-Allee 3, 53175 Bonn
Antiplatelet drugs: Spectra of prescribing and morbidities
In an ongoing project supported by the Federal Ministry of Health (BMG) off-label-use of pharmaceuticals with high prescription rates is investigated in a database comprising all citizens covered by public sick funds. The focus is on prevalences and indications as well as on the identification of off-label-use specifically addressing rare diseases in the context of the Action Plan of the National Action League for People with Rare Diseases (NAMSE). In the years 2010 through 2011 among antiplatelet drugs acetylsalicylic acid has completely been prescribed in conformity to the label. Clopidogrel, prasugrel and ticagrelor appear to have been prescribed off-label in up to 2% and 1%, respectively, in the context of endovascular interventions in peripheral and cerebral arteries. More than 99% had exclusively been treated as outpatients. Less than 0.03% of patients treated with clopidogrel, prasugrel and ticagrelor, respectively, have been younger than 18 years. Beyond the diagnoses putatively underlying in- and off-label-use, respectively, there were no prominent comorbidities – including psychiatric – except cardiovascular risk factors, although the anemias observed could be attributed to the antiplatelet drugs. Rare diseases potentially motivating off-label-use were not detected.
Key words: antiplatelet drugs, acetylsalicylic acid, ASS, clopidogrel, prasugrel, ticagrelor, off-label-use, National Action League for People with Rare Diseases, NAMSE
Psychopharmakotherapie 2017; 24(01)
