Marie Spies, Rupert Lanzenberger und Siegfried Kasper, Wien
Neurotransmittersysteme und depressive Symptomatik
Bereits seit Jahrzehnten wird das serotonerge System mit depressiver Symptomatik in Verbindung gebracht. Daneben sind auch Noradrenalin und Dopamin an der Pathophysiologie depressiver Symptomatik beteiligt.
Tryptophan-Depletionsstudien stellten eine Verbindung zwischen niedrigen Serotoninspiegeln und depressiver Symptomatik her. Im Rahmen dieser Studien nehmen die Probanden Aminosäuremischungen ein, die wenig Tryptophan, den Vorläufer von Serotonin, enthalten. Bei gesunden Kontrollprobanden [60], Personen mit erhöhtem Risiko für depressive Störungsbilder [5] und vor allem bei depressiven Patienten [12] können mit dieser Methode depressive Symptome ausgelöst werden. Außerdem zeigten Post-mortem-Autoradiographie-Untersuchungen [29, 38] sowie In-vivo-Bildgebungsstudien mittels Positronenemissionstomographie (PET) und Einzelphotonen-Emissionscomputertomographie (SPECT) [25] diverse molekulare Veränderungen im serotonergen System bei depressiven Patienten. Die Effektivität von selektiven Serotonin-Wiederaufnahmehemmern (SSRI), die bekanntermaßen durch die Blockade des Serotonintransporters zu einem Anstieg an extrazellulärem Serotonin führen [4], unterstreichen die Relevanz des Serotoninsystems in der Entstehung und Behandlung depressiver Störungsbilder.
Andere pharmakologische und klinische Hinweise legen jedoch die Relevanz weiterer Neurotransmittersysteme nahe. Durch SSRI erreichte antidepressive Effekte zeigen sich typischerweise erst nach einer Latenzzeit von mindestens zwei Wochen, sodass sekundäre Regulationsmechanismen, auch durch andere Neurotransmittersysteme, von Bedeutung sein dürften. Darüber hinaus weist die Depression ein komplexes klinisches Bild mit einem hohen Ausmaß an interindividueller Variabilität in Bezug auf klinische Merkmale wie Symptomatik, Therapieansprechen und Prognose auf.
Im komplexen multifaktoriellen Entstehungsmodell der Depression erklärt auch die variierende Beteiligung des dopaminergen und des noradrenergen Systems die klinische Variabilität dieser Erkrankung. So wird dem serotonergen System eine entscheidende Rolle bei Agitation und Unruhe sowie der Reduktion von Appetit und Libido zugeschrieben [23, 35]. Das noradrenerge System, welches im physiologischen Kontext eine essenzielle Rolle für die Vigilanz, Aufmerksamkeit, und Konzentration spielt [45], dürfte hingegen für die Entstehung der Antriebslosigkeit und der kognitiven Einschränkungen depressiver Patienten maßgeblich verantwortlich sein [23, 35]. Im Rahmen dieser primär noradrenerg bedingten Symptomatik kann auch ein Selbstfürsorgedefizit und ein sozialer Rückzug entstehen [22]. Dopamin dagegen ist der Hauptneurotransmitter des Belohnungssytems [20] und bei depressiven Patienten dürften Störungen im Dopaminsystem unter anderem Lust- und Freudlosigkeit begünstigen [58].
Die Relevanz von Noradrenalin und Dopamin für die Entstehung depressiver Symptomatik wird durch Studien unterstützt, in deren Rahmen Probanden Tyrosinhydroxylase-Hemmer einnahmen, wodurch die Synthese der Katecholamine reduziert wurde. Ein Vergleich zwischen den klinischen Effekten einer Serotonin- (Tryptophan-) und Katecholamin-Depletion unterstreicht die unterschiedliche Beteiligung der Neurotransmittersysteme bei der Entstehung einer depressiven Symptomatik. Eine Tryptophan-Depletion führte vermehrt zu einer gedrückten Stimmungslage, während die Katecholamin-Depletion zu vermehrter Antriebsminderung führte [19].
Einerseits stellt diese singuläre Zuschreibung gewisser Symptomgruppen zu einzelnen Neurotransmittern eine Vereinfachung dar, denn funktionelle Interaktionen zwischen den Neurotransmittersystemen sind anzunehmen. Andererseits entsteht durch die Aufschlüsselung depressiver Symptome anhand der Neurotransmitter ein wissenschaftlich hilfreiches Gerüst, um die Entstehung der Depression zu erforschen und therapeutische Ansätze zu entwickeln. Eine neurobiologisch fundierte antidepressive Therapie sollte die klinische Variabilität der Depression widerspiegeln und dabei individualisiert sowie auf Symptomschwerpunkte ausgerichtet sein.
Molekulares Profil von Milnacipran
Milnacipran (Abb. 1) wird als Serotonin-Noradrenalin-Wiederaufnahmehemmer (SNRI) klassifiziert.
Abb. 1. Milnacipran
Mittels PET konnte in Tiermodellen [50] sowie bei depressiven Patienten gezeigt werden, dass Milnacipran an den Noradrenalin- (NET) und den Serotonintransporter (SERT) bindet. Die Verteilung des SERT und NET im menschlichen Gehirn ist in Abbildung 2 dargestellt. Das Ausmaß der Bindung von Milnacipran an beiden Transportertypen zeigt ein dosisabhängiges Muster. Unter einer Therapie mit 100 mg/Tag Milnacipran, einer Dosis, die im klinischen Alltag häufig verordnet wird, waren jeweils etwa 40% der NET und SERT durch das Medikament besetzt [34]. SSRI binden selektiv nur an den SERT und besetzen diesen zu etwa 70 bis 80%. Allerdings konnte für SSRI bisher kein direkter Zusammenhang zwischen dem Ausmaß der Transporterbindung, Dosis und klinischer Effektivität erfasst werden [48], sodass von einer verringerten Bindung von Milnacipran an den SERT nicht direkt auf eine geringere antidepressive Potenz geschlossen werden kann.
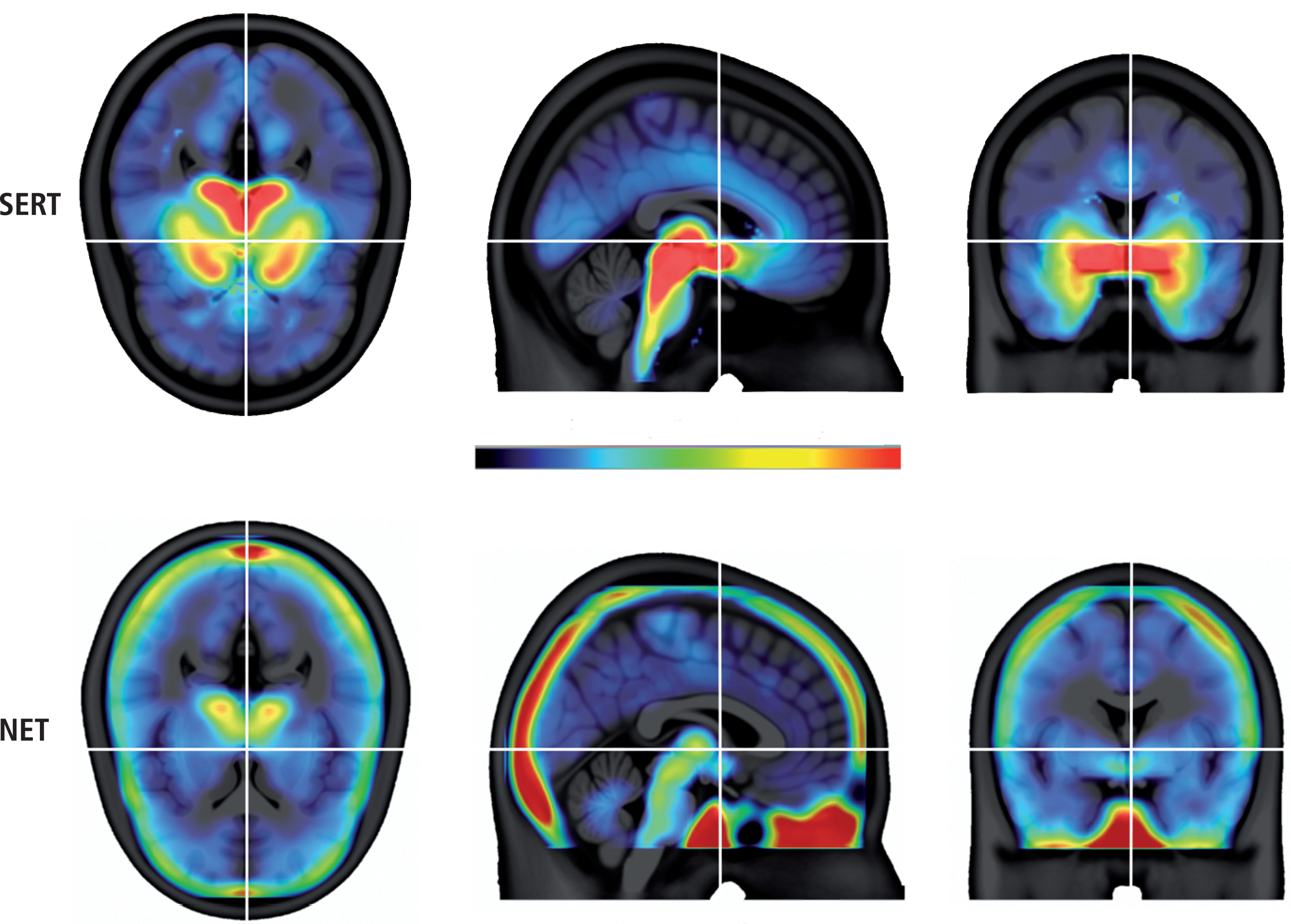
Abb. 2. Verteilung des Serotonin-Transporters und des Noradrenalin-Transporters im Gehirn quantifiziert mittels Positronenemissionstomographie Milnacipran bindet an den Serotonin-Transporter (SERT) und den Noradrenalin-Transporter (NET) und vermittelt somit seine antidepressiven Effekte. Die Positronenemissionstomographie (PET) erlaubt die Darstellung des SERT und des NET in vivo im menschlichen Gehirn. Bei der PET wird ein Radioligand, der ein Zielmolekül bindet und radioaktive Strahlung abgibt, verabreicht, um die Verteilung des Moleküls im Gehirn darzustellen. Der SERT (in dieser Abbildung gemessen mit dem Radioliganden [11C]DASB) wird im Mittelhirn, im Hirnstamm, in den Basalganglien, im Thalamus und in medialen temporalen Regionen hoch exprimiert. Im frontalen Kortex ist die Dichte des SERT mit Ausnahme des Zingulums niedrig. Der SERT ist in der grauen Substanz des Zerebellums kaum nachweisbar [44]. Die NET-Dichte (gemessen mit dem Radioliganden (S,S)-[18F]FMeNER-D2) ist im Thalamus und Mittelhirn hoch und in den Basalganglien niedrig. Die kortikale NET-Dichte kann mit den derzeit verfügbaren PET-Radioliganden nicht ausreichend dargestellt werden, das hohe Signal (rot) ist durch Knochenbindung des Radioliganden bedingt [57]. Der Farbbalken spiegelt die Dichte des SERT und des NET wider. In der Abbildung der Proteinverteilung von SERT und NET sind korrespondierende, auf strukturelle Magnetresonanzbilder überlagerte digitale Hirnschnitte in der axialen, sagittalen und koronaren Ebene durch weiße Kreuze gekennzeichnet.
In Untersuchungen an Thrombozyten konnte gezeigt werden, dass die Bindung von Milnacipran an den SERT und NET zu einem Anstieg der Serotonin- und Noradrenalin-Konzentrationen im Extrazellulärraum führt. Um zu überprüfen, in welchem Ausmaß klinisch relevante Dosierungen zu einem Serotonin- und Noradrenalin-Anstieg führen, wurde nach oraler Gabe von Milnacipran gesunden Probanden Blut entnommen und mit Blutplättchen, welche den SERT und den NET exprimieren, in vitro inkubiert. Hierbei zeigte sich, dass der Anstieg von Serotonin und Noradrenalin dosisabhängig ist [36]. Ein durch Milnacipran induzierter Anstieg von Serotonin und Noradrenalin im zerebralen Extrazellulärraum konnte auch durch Mikrodialysestudien in vivo dargestellt werden. In diesen Untersuchungen wurden bei Tieren mittels einer Sonde die Konzentrationen der Neurotransmitter im Gehirn nach Gabe von Milnacipran gemessen. Mittels Mikrodialyse wurde auch gezeigt, dass es zu einem äquipotenten Anstieg von Serotonin und Noradrenalin kommt [32], sodass Milnacipran in Bezug auf die Effekte auf das Noradrenalin- und Serotoninsystem als ausgewogenes Antidepressivum verstanden werden kann [8, 23].
Neben dem NET und dem SERT hat Milnacipran keine nennenswerte Affinität für weitere zerebrale Rezeptoren oder Transporter, insbesondere keine direkte Bindung an Transporter oder Rezeptoren des dopaminergen Systems [8]. Allerdings dürfte das dopaminerge System indirekt an der antidepressiven Wirkung von Milnacipran beteiligt sein [23]. Unter anderem scheint es durch Milnacipran zu einem präfrontalen Anstieg von Dopamin zu kommen [55]. Dies erklärt sich eventuell dadurch, dass der Noradrenalin-Transporter im präfrontalen Kortex, neben der Wiederaufnahme von Noradrenalin, auch die Wiederaufnahme von Dopamin reguliert [9].
Neurobiologische Befunde
Wie beschrieben, kommt es durch Milnacipran zu einem Anstieg der Serotonin- und Noradrenalin-Spiegel sowie auch indirekt zu einem Anstieg an Dopamin [55] im zerebralen Extrazellulärraum. In Bezug auf die serotonergen Wirkungen von Milnacipran werden, ähnlich wie bei SSRI, sekundäre Regulationsmechanismen, die verzögert auftreten und eine klinische Wirklatenz mit sich tragen, für die tatsächlichen antidepressiven Wirkungen verantwortlich gemacht. Hier dürfte, wie bei SSRI, eine Herunterregulation von inhibitorischen Autorezeptoren vom 5-HT1A-Subtyp und eine damit einhergehende Verstärkung der serotonergen Neurotransmission von peripheren Projektionsgebieten eine Rolle spielen. Studien, die eine Zunahme der klinischen Effektivität sowie eine Reduktion der Wirklatenz von Milnacipran nach Zugabe von Pindolol, einem 5-HT1A-Blocker [21], zeigten, untermauern diese Theorie.
Milnacipran scheint sich hinsichtlich der Effekte in den monoaminergen Projektionsgebieten von Venlafaxin und Duloxetin zu unterscheiden. Es wurde gezeigt, dass das Ausmaß des Anstiegs von Serotonin und Dopamin zwischen den Substanzen regional variiert [33]. Ähnlich wie bei SSRI [59] stellen Tierstudien einen möglichen antidepressiven Effekt über die Förderung der Neurogenese dar, die möglicherweise über die Aktivierung des BDNF-Systems (Brain-derived neurotrophic factor) vermittelt wird.
Pharmakokinetik
Als großer klinischer Vorteil erweist sich, dass Milnacipran ein äußerst geringes pharmakokinetisches Interaktionspotenzial mit anderen Pharmaka zeigt. Aufgrund der zunehmend steigenden Lebenserwartung, verbesserten therapeutischen Möglichkeiten in der Psychiatrie und auch in der somatischen Medizin sowie einer damit einhergehenden Polypharmazie ist dies eine hochrelevante Eigenschaft in Bezug auf die klinische Anwendbarkeit. Nachdem Guidelines zur antidepressiven Therapie bei fehlendem Therapieansprechen Add-on- beziehungsweise Augmentationsverfahren empfehlen, lässt sich Milnacipran optimal in antidepressive Therapieschemata eingliedern [3].
Nach oraler Einnahme zeigt Milnacipran eine hohe Bioverfügbarkeit von etwa 90% [40]. Es weist eine niedrige Plasmaproteinbindung auf und hat keine aktiven Metaboliten. Milnacipran wird zu etwa 50% unverändert über die Niere ausgeschieden, während ein kleiner Anteil (14%) über die Leber glukuronidiert und der Rest zu pharmakologisch inaktiven Metaboliten verstoffwechselt wird. Aufgrund des hohen Anteils der renalen Ausscheidung ist Milnacipran für Patienten mit Leberfunktionsstörungen gut geeignet, auch wenn gezeigt wurde, dass bei diesen die Bioverfügbarkeit erhöht und Plasmaspiegel des konjugierten Anteils etwas erniedrigt sein können. Der renal ausgeschiedene Anteil blieb unverändert. Diese pharmakokinetischen Veränderungen werden jedoch nicht als klinisch relevant angesehen und eine Dosisanpassung ist bei Patienten mit Leberfunktionsstörungen meist nicht notwendig [40, 41].
Im Gegensatz dazu ist eine Anpassung der Milnacipran-Dosis bei Patienten mit Nierenfunktionsstörungen indiziert. Allerdings korrelieren Schweregrad der Nierenfunktionsstörung und Ausmaß der Reduktion der renalen Elimination, sodass notwendige Dosisanpassungen einfach berechnet werden können [41].
Antidepressive Effektivität
Tierstudien
In präklinischen Studien wurde mittels Tiermodellen die Effektivität von Milnacipran untersucht. Mit dem „Forced-Swim Test“, einem Tiermodell für depressive Symptomatik, wurde die antidepressive Wirkung von Milnacipran untersucht [31, 42]. Außerdem konnte in einem Modell für konditionierte Angst die anxiolytische [31] und in einem Modell für neuropathische Schmerzen die analgetische Wirkung gezeigt werden [31]. Des Weiteren konnte in Ratten gezeigt werden, dass Milnacipran auch anti-impulsive Effekte aufweist [18, 53, 54].
Humanstudien
Ähnlich wie trizyklische Antidepressiva (TZA) weist Milnacipran eine kombiniert serotonerge und noradrenerge Wirkungsweise auf. Allerdings ergibt sich unter anderem aufgrund fehlender direkter anti-muskarinerger Wirkungen ein verträglicheres Nebenwirkungsprofil. In einer Zusammenfassung von sieben Studien, bei der das Ansprechen auf Milnacipran als eine mindestens 50%ige Reduktion der depressiven Symptomatik definiert wurde, wird eine Ansprechrate von 64% bei zweimal täglicher Gabe von 50 mg berichtet; für TZA wurde eine Ansprechrate von 67% beschrieben [24].
In den meisten Einzelstudien, die TZA und Milnacipran verglichen, wurde kein signifikanter Unterschied in der antidepressiven Wirksamkeit der Arzneistoffe gezeigt [2, 30, 49, 51, 56]. Teilweise wurde eine Überlegenheit von TZA demonstriert [27], wobei sich Milnacipran jedoch deutlich nebenwirkungsärmer und damit verträglicher zeigt. Zum Beispiel traten bei Patienten unter Behandlung mit Milnacipran signifikant weniger anticholinerge Nebenwirkungen auf als bei Patienten, die mit Amitriptylin [2] oder Clomipramin [27] behandelt wurden. Die geringere anticholinerge Wirkung ist besonders relevant in der Behandlung älterer Patienten, bei denen aufgrund somatischer Komorbiditäten, wie einem Glaukom, einer Prostatahyperplasie, oder einer Prädisposition für delirante Zustandsbilder, die Gefahr anticholinerger Komplikationen besteht. Des Weiteren wird diskutiert, ob die Wirkung mancher TZA, vor allem von Amitriptylin, in diesen Studien überschätzt wird. TZA weisen teils sedative Effekte auf und bessern somit eventuell rasch Schlaf-Symptome in Depressionsskalen [2] (Tab. 1).
Tab. 1. Studienauswahl: Milnacipran vs. trizyklische Antidepressiva
|
Studie |
Vergleich |
Ergebnis |
Kommentare |
|
Steen et al. 1997 [49] |
Milnacipran 200 mg (1 Wo. Aufdosierung, dann 9 Wo. fix, dann flexible Dosierung) vs. Clomipramin 150 mg (1 Wo. Aufdosierung, dann 9 Wo. fix, dann flexible Dosierung) |
− |
|
|
Leinonen et al. 1997 [27] |
Milnacipran 200 mg (1 Wo. Aufdosierung, dann 9 Wo. fix, dann flexible Dosierung) vs. Clomipramin 150 mg (1 Wo. Aufdosierung, dann 9 Wo. fix, dann flexible Dosierung) |
↓ |
Weniger Mundtrockenheit, mehr Schlafstörungen unter Milnacipran |
|
Tignol et al. 1998 [51] |
Milnacipran 100 mg vs. Imipramin 100 mg |
− |
Mehr anticholinerge Nebenwirkungen bei Imipramin |
|
Van Amerongen et al. 2002 [56] |
Milnacipran 100 mg vs. Imipramin 150 mg |
− |
Mehr anticholinerge Nebenwirkungen bei Imipramin |
|
Lopez-Ibor et al. 2004 [30] |
Milnacipran 100 mg vs. Imipramin 150 mg |
− |
Mehr anticholinerge Nebenwirkungen bei Imipramin Mehr Dysurie und Zittern bei Milnacipran |
−: kein Unterschied; ↓: schlechter
In weiteren Studien wurden die antidepressiven Effekte von Milnacipran mit jenen von SSRI verglichen. Während eine Studie die Überlegenheit von Milnacipran in Bezug auf allgemeines Therapieansprechen gegenüber Fluvoxamin zeigte [11], wiesen andere Untersuchungen keinen Unterschied auf [16]. Eine Studie zeigte sogar die Überlegenheit von Fluoxetin gegenüber Milnacipran in der Reduktion von Symptomen anhand von HAMD (Hamilton depression rating scale), MADRS (Montgomery-Åsberg depression rating scale) und CGI (Clinical global impression score) [1]. Allerdings vermuteten die Autoren, dass Milnacipran mit einer einmal täglichen Gabe von 100 mg möglicherweise unterdosiert war beziehungsweise dass, aufgrund der kurzen Plasmahalbwertszeit von etwa sieben Stunden, eine zweimal tägliche Gabe empfohlen werden sollte [1]. Eine Metaanalyse von sechs Studien mit insgesamt über 1000 Patienten zeigte keinen signifikanten Unterschied in der Wirksamkeit von Milnacipran und verschiedenen SSRI [37]. Dabei darf ein Dosiseffekt als mögliche Ursache der unterschiedlichen Studienresultate nicht außer Acht gelassen werden. Patienten die mit 150 mg statt 75 mg Milnacipran behandelt wurden, zeigten signifikant höhere Ansprech- (50% Symptomlinderung) und Remissionsraten (<7 Punkte HAMD) (Tab. 2).
Tab. 2. Studienauswahl: Milnacipran vs. selektive Serotonin-Wiederaufnahmehemmer
|
Studie |
Vergleich (Tagesdosen) |
Ergebnis (Milnacipran vs. Vergleich) |
Kommentare |
|
Ansseau et al. 1994 [1] |
Milnacipran 100 mg vs. Fluoxetin 20 mg |
↓ |
Mehr Schwindel bei Milnacipran |
|
Guelfi et al. 1998 [17] |
Milnacipran 100 mg oder 200 mg vs. Fluoxetin 20 mg |
− |
Mehr Tachykardie bei Milnacipran Mehr Gewichtsabnahme bei Fluoxetin |
|
Clerc et al. 2001 [11] |
Milnacipran 100 mg vs. Fluvoxamin 200 mg |
↑ |
Mehr Zittern und Müdigkeit bei Fluvoxamin |
|
Fukuchi et al. 2002 [16] |
Milnacipran initial 30–100 mg (Steigerung auf max. 150 mg) vs. Fluvoxamin 50–150 mg (Steigerung auf max. 250 mg) |
− (gesamte Patientengruppe) ↑ (Patienten mit schwerer Depression) |
Bei Patienten mit schwerer Depression Ansprechen auf Milnacipran häufiger als auf Fluvoxamin Besseres Ansprechen von Agitation und Schlafstörung auf Milnacipran Mehr gastrointestinale Nebenwirkungen bei Fluvoxamin Mehr Herzrasen oder urologische Probleme bei Milnacipran |
|
Sechter et al. 2004 [46] |
Milnacipran 100 mg vs. Paroxetin 20 mg |
− |
Vermehrte Antriebslosigkeit vor Therapiebeginn →besseres Ansprechen auf Milnacipran Weniger Absetzphänomene bei Milnacipran |
|
Lee et al. 2005 [26] |
Milnacipran 50 mg (Steigerung auf 100 mg nach 1 Wo.) vs. Fluoxetin 20 mg |
− |
Mehr Durchfall und Schlafstörungen bei Fluoxetin |
Auch Vergleiche zwischen Milnacipran und anderen SNRI zeigen eine ähnliche antidepressive Effektivität. Es konnten keine signifikanten Unterschiede in der Ansprechrate zwischen 100 mg Milnacipran und Venlafaxin gefunden werden, wobei Patienten täglich 75 bis 225 mg Venlafaxin einnahmen [10]. Des Weiteren berücksichtigen diese Studien nur begrenzt die Variabilität der Symptomatik und deren Schweregrad innerhalb von Patientengruppen. Es konnte gezeigt werden, dass Patienten mit einem höheren Symptomschweregrad, in diesem Fall mehr als 19 Punkte beim HAMD (Version mit 17 Fragen), häufiger auf Milnacipran ansprachen. Auch zeigte sich Milnacipran effektiver in der Behandlung von Agitation und Insomnie im Vergleich zu Fluvoxamin [16]. Andere Studien zeigten, dass es durch Milnacipran zu einer Besserung der Schlafstörungen von depressiven Patienten kam. Auf neurophysiologischer Ebene wurde gezeigt, dass eine zweimal tägliche Gabe von 50 mg Milnacipran zu einer Verlängerung der gesamten Schlafdauer, einer Verkürzung der Schlaflatenz und einer Zunahme der Schlafeffizienz führte [28].
Es wird diskutiert, dass besonders Patienten mit Symptomen, hinter denen eine noradrenerge Pathogenese vermutet wird, auch gut auf Milnacipran ansprechen. Zum Beispiel dürfte es bei Patienten, die vor Therapiebeginn unter ausgeprägter Antriebslosigkeit gelitten haben, besonders wirksam sein [46]. Des Weiteren wird die Besserung sozialer Dysfunktionen [7] und kognitiver Funktionsstörungen [39] betont.
Die klinische Bedeutung eines Antidepressivums ergibt sich nicht nur aus den initialen Ansprechraten, sondern auch anhand der Effektivität in Bezug auf eine Rückfallvermeidung. Es konnte gezeigt werden, dass Milnacipran hinsichtlich des Verhinderns einer neuerlichen depressiven Phase signifikant effektiver ist als Placebo. Unter Milnacipran zeigten 16,3% und unter Placebo 23,6% der Patienten ein Wiederauftreten einer depressiven Symptomatik, definiert als ≥18 HAMD-Punkte und die Notwendigkeit einer Therapieanpassung. Die Effektivität, mit der Milnacipran eine neuerliche depressive Phase verhindern konnte, nahm mit Dauer der Therapie ab [43] und war vergleichbar mit Rückfallraten, die unter SSRI berichtet wurden [14]. Im Vergleich zu Paroxetin dürfte Milnacipran mit einem geringeren Ausmaß an Absetzphänomenen vergesellschaftet sein [46].
Zusammenfassend lässt sich sagen, dass Milnacipran eine ähnliche Effektivität wie TZA und SSRI aufweist [37], auch in Bezug auf das Verhindern eines depressiven Rückfalls [43]. Allerdings zeigt Milnacipran, im Vergleich zu TZA, ein deutlich verträglicheres Nebenwirkungsprofil, beispielsweise eine verringerte anticholinerge Wirkung und ein geringeres Interaktionspotenzial. Milnacipran scheint besonders in der Behandlung solcher depressiver Symptome, die vermutlich auf eine noradrenerge Dysfunktion zurückzuführen sind, effektiv zu sein. Hier ist vor allem die Antriebslosigkeit [46] anzuführen.
Weitere Indikationen
Wie bei den anderen SNRI, insbesondere Duloxetin, wurde auch die analgetische Effektivität von Milnacipran ausführlich untersucht. Obwohl in einer Metaanalyse gezeigt wurde, dass Milnacipran im Allgemeinen keine Effekte auf neuropathische Schmerzen aufweist [13], konnte gezeigt werden, dass Milnacipran bei manchen spezifischen schmerztherapeutischen Indikationen eine Rolle spielen könnte. Zum Beispiel wurde die Effektivität von Milnacipran in der Schmerzbehandlung bei Patienten mit Fibromyalgie gezeigt [13] und stellt besonders für Patienten, die auch eine depressive Symptomatik aufweisen, eine therapeutische Option [6] dar. Die Daten zu Angsterkrankungen sind dagegen limitiert. Eine unkontrollierte Studie mit zehn Patienten mit generalisierter Angststörung zeigte eine etwa 70%ige Symptomverbesserung unter Milnacipran [52]. In Bezug auf die Panikstörung zeigte eine Metaanalyse von 14 Studien, dass derzeit nur eine unzureichende Evidenz für eine konkrete Aussage zur Effektivität von Milnacipran bei dieser Erkrankung zur Verfügung steht [47]. Milnacipran wurde auch bei Patienten mit Essstörungen untersucht. Unter anderem wurde anhand einer Gruppe von 16 Patienten beschrieben, dass eine Reduktion an Binge Eating erreicht werden konnte [15].
Zusammenfassung
Die moderne Psychopharmakologie sollte personalisierte und auf neurobiologischen Erkenntnissen basierte Therapieansätze im Sinne der Präzisionsmedizin anstreben. Inzwischen deutet eine Vielzahl von Studien, neben der Relevanz des serotonergen Systems, auf die Beteiligung anderer Neurotransmittersysteme bei der Entstehung von depressiver Symptomatik hin. Hier spielen vor allem Noradrenalin und Dopamin eine prominente Rolle. Dabei zeigen SNRI, die seit über 20 Jahren in der Psychopharmakotherapie angewendet werden, eine kombiniert serotonerg-noradrenerge Wirkungsweise. Aufgrund der klinisch relevanten pharmakokinetischen Eigenschaften, inklusive einer primär renalen Elimination und einem niedrigen Interaktionspotenzial mit anderen Psychopharmaka, stellt Milnacipran einen wichtigen Vertreter dieser Wirkstoffklasse dar.
Interessenkonflikterklärung
MS hat Honorare für Vorträge von Janssen und Forschungsbeihilfe von NARSAD (Young Investigator Grant) erhalten. Außerdem wurde sie durch Reisekostenzuschüsse von Janssen, Eli Lilly und AOP Orphan Pharmaceuticals sowie Workshop-Teilnahme von Eli Lilly unterstützt.
RL hat Reisekostenzuschüsse und Vortragshonorare von Roche Austria GmbH, Dr. Willmar Schwabe GmbH & Co. KG und Janssen-Cilag Pharma GmbH erhalten. Außerdem erhält er Drittmittelfinanzierung von Studienprojekten durch FWF, ÖNB, NARSAD und die Else Kröner-Fresenius-Stiftung.
SK hat innerhalb der letzten drei Jahre Honorare für die Beratung oder Teilnahme an Advisory Boards erhalten von: Angelini, AOP Orphan Pharmaceuticals AG, Eli Lilly, Janssen, KRKA-Pharma, Lundbeck, Neuraxpharm, Schwabe und Servier. Für Vorträge, Stellungnahmen oder Artikel hat SK in den letzten drei Jahren Honorare erhalten von: Angelini, AOP Orphan Pharmaceuticals AG, Eli Lilly, Janssen, KRKA-Pharma, Lundbeck, Neuraxpharm, Pierre Fabre, Schwabe und Servier. Forschungsbeihilfen erhielt er von Pfizer und Schwabe, sonstige Unterstützung in Form von Subventionen, Forschungsgeldern, Beratergebühren und Honoraren von Lundbeck und Schwabe.
Literatur
1. Ansseau M, Papart P, Troisfontaines B, Bartholome F, et al. Controlled comparison of milnacipran and fluoxetine in major depression. Psychopharmacology (Berl) 1994;114:131–7.
2. Ansseau M, von Frenckell R, Mertens C, de Wilde J, et al. Controlled comparison of two doses of milnacipran (F 2207) and amitriptyline in major depressive inpatients. Psychopharmacology (Berl) 1989;98:163–8.
3. Bauer M, Bschor T, Pfennig A, Whybrow PC, et al. World Federation of Societies of Biological Psychiatry (WFSBP) Guidelines for Biological Treatment of Unipolar Depressive Disorders in Primary Care. World J Biol Psychiatry 2007;8:67–104.
4. Bel N, Artigas F. Fluvoxamine preferentially increases extracellular 5-hydroxytryptamine in the raphe nuclei: an in vivo microdialysis study. Eur J Pharmacol 1992;229:101–3.
5. Benkelfat C, Ellenbogen MA, Dean P, Palmour RM, et al. Mood-lowering effect of tryptophan depletion. Enhanced susceptibility in young men at genetic risk for major affective disorders. Arch Gen Psychiatry 1994;51:687–97.
6. Bernstein CD, Albrecht KL, Marcus DA. Milnacipran for fibromyalgia: a useful addition to the treatment armamentarium. Expert Opin Pharmacother 2013;14:905–16.
7. Briley M, Moret C. Improvement of social adaptation in depression with serotonin and norepinephrine reuptake inhibitors. Neuropsychiatr Dis Treat 2010;6:647–55.
8. Briley M, Prost JF, Moret C. Preclinical pharmacology of milnacipran. Int Clin Psychopharmacol 1996;11(Suppl 4):9–14.
9. Bymaster FP, Katner JS, Nelson DL, Hemrick-Luecke SK, et al. Atomoxetine increases extracellular levels of norepinephrine and dopamine in prefrontal cortex of rat: a potential mechanism for efficacy in attention deficit/hyperactivity disorder. Neuropsychopharmacology 2002;27:699–711.
10. Chuang HY, Chang YH, Cheng LY, Wang YS, et al. Venlafaxine, paroxetine and milnacipran for major depressive disorder: a pragmatic 24-week study. Chin J Physiol 2014;57:265–70.
11. Clerc G. Antidepressant efficacy and tolerability of milnacipran, a dual serotonin and noradrenaline reuptake inhibitor: a comparison with fluvoxamine. Int Clin Psychopharmacol 2001;16:145–51.
12. Delgado PL, Price LH, Miller HL, Salomon RM, et al. Rapid serotonin depletion as a provocative challenge test for patients with major depression: relevance to antidepressant action and the neurobiology of depression. Psychopharmacol Bull 1991;27:321–30.
13. Derry S, Gill D, Phillips T, Moore RA. Milnacipran for neuropathic pain and fibromyalgia in adults. Cochrane Database Syst Rev 2012;(3):CD008244.
14. Doogan DP, Caillard V. Sertraline in the prevention of depression. Br J Psychiatry 1992;160:217–22.
15. El-Giamal N, de Zwaan M, Bailer U, Strnad A, et al. Milnacipran in the treatment of bulimia nervosa: a report of 16 cases. Eur Neuropsychopharmacol 2003;13:73–9.
16. Fukuchi T, Kanemoto K. Differential effects of milnacipran and fluvoxamine, especially in patients with severe depression and agitated depression: a case-control study. Int Clin Psychopharmacol 2002;17:53–8.
17. Guelfi JD, Ansseau M, Corruble E, Samuelian JC, et al. A double-blind comparison of the efficacy and safety of milnacipran and fluoxetine in depressed inpatients. Int Clin Psychopharmacol 1998;13:121–8.
18. Hiraide S, Ueno K, Yamaguchi T, Matsumoto M, et al. Behavioural effects of monoamine reuptake inhibitors on symptomatic domains in an animal model of attention-deficit/hyperactivity disorder. Pharmacol Biochem Behav 2013;105:89–97.
19. Homan P, Neumeister A, Nugent AC, Charney DS, et al. Serotonin versus catecholamine deficiency: behavioral and neural effects of experimental depletion in remitted depression. Transl Psychiatry 2015;5:e532.
20. Ikemoto S, Yang C, Tan A. Basal ganglia circuit loops, dopamine and motivation: A review and enquiry. Behav Brain Res 2015;290:17–31.
21. Isaac MT, Isaac MB, Gallo F, Tournoux A. Milnacipran and pindolol: a randomized trial of reduction of antidepressant latency. Hum Psychopharmacol 2003;18:595–601.
22. Kasper S, Meshkat D, Kutzelnigg A. Improvement of the noradrenergic symptom cluster following treatment with milnacipran. Neuropsychiatr Dis Treat 2011;7(Suppl 1):21–7.
23. Kasper S, Pail G. Milnacipran: a unique antidepressant? Neuropsychiatr Dis Treat 2010;6:23–31.
24. Kasper S, Pletan Y, Solles A, Tournoux A. Comparative studies with milnacipran and tricyclic antidepressants in the treatment of patients with major depression: a summary of clinical trial results. Int Clin Psychopharmacol 1996;11(Suppl 4):35–9.
25. Kasper S, Tauscher J, Willeit M, Stamenkovic M, et al. Receptor and transporter imaging studies in schizophrenia, depression, bulimia and Tourette‘s disorder – implications for psychopharmacology. World J Biol Psychiatry 2002;3:133–46.
26. Lee MS, Ham BJ, Kee BS, Kim JB, et al. Comparison of efficacy and safety of milnacipran and fluoxetine in Korean patients with major depression. Curr Med Res Opin 2005;21:1369–75.
27. Leinonen E, Lepola U, Koponen H, Mehtonen OP, et al. Long-term efficacy and safety of milnacipran compared to clomipramine in patients with major depression. Acta Psychiatr Scand 1997;96:497–504.
28. Lemoine P, Faivre T. Subjective and polysomnographic effects of milnacipran on sleep in depressed patients. Hum Psychopharmacol 2004;19:299–303.
29. Little KY, McLauglin DP, Ranc J, Gilmore J, et al. Serotonin transporter binding sites and mRNA levels in depressed persons committing suicide. Biol Psychiatry 1997;41:1156–64.
30. Lopez-Ibor JJ, Conesa A. A comparative study of milnacipran and imipramine in the treatment of major depressive disorder. Curr Med Res Opin 2004;20:855–60.
31. Mochizuki D, Tsujita R, Yamada S, Kawasaki K, et al. Neurochemical and behavioural characterization of milnacipran, a serotonin and noradrenaline reuptake inhibitor in rats. Psychopharmacology (Berl) 2002;162: 323–32.
32. Moret C, Briley M. Effects of milnacipran and pindolol on extracellular noradrenaline and serotonin levels in guinea pig hypothalamus. J Neurochem 1997;69:815–22.
33. Muneoka K, Shirayama Y, Takigawa M, Shioda S. Brain region-specific effects of short-term treatment with duloxetine, venlafaxine, milnacipran and sertraline on monoamine metabolism in rats. Neurochem Res 2009;34:542–55.
34. Nogami T, Takano H, Arakawa R, Ichimiya T, et al. Occupancy of serotonin and norepinephrine transporter by milnacipran in patients with major depressive disorder: a positron emission tomography study with [11C]DASB and (S,S)-[18F]FMeNER-D2. Int J Neuropsychopharmacol 2013;16:937–43.
35. Nutt DJ. Relationship of neurotransmitters to the symptoms of major depressive disorder. J Clin Psychiatry 2008;69(Suppl E1):4–7.
36. Palmier C, Puozzo C, Lenehan T, Briley M. Monoamine uptake inhibition by plasma from healthy volunteers after single oral doses of the antidepressant milnacipran. Eur J Clin Pharmacol 1989;37:235–8.
37. Papakostas GI, Fava M. A meta-analysis of clinical trials comparing milnacipran, a serotonin-norepinephrine reuptake inhibitor, with a selective serotonin reuptake inhibitor for the treatment of major depressive disorder. Eur Neuropsychopharmacol 2007;17:32–6.
38. Perry EK, Marshall EF, Blessed G, Tomlinson BE, et al. Decreased imipramine binding in the brains of patients with depressive illness. Br J Psychiatry 1983;142:188–92.
39. Puech A, Montgomery SA, Prost JF, Solles A, et al. Milnacipran, a new serotonin and noradrenaline reuptake inhibitor: an overview of its antidepressant activity and clinical tolerability. Int Clin Psychopharmacol 1997;12:99–108.
40. Puozzo C, Albin H, Vincon G, Deprez D, et al. Pharmacokinetics of milnacipran in liver impairment. Eur J Drug Metab Pharmacokinet 1998;23:273–9.
41. Puozzo C, Leonard BE. Pharmacokinetics of milnacipran in comparison with other antidepressants. Int Clin Psychopharmacol 1996;11(Suppl 4):15–27.
42. Reneric JP, Bouvard M, Stinus L. In the rat forced swimming test, chronic but not subacute administration of dual 5-HT/NA antidepressant treatments may produce greater effects than selective drugs. Behav Brain Res 2002;136:521–32.
43. Rouillon F, Warner B, Pezous N, Bisserbe JC. Milnacipran efficacy in the prevention of recurrent depression: a 12-month placebo-controlled study. Milnacipran recurrence prevention study group. Int Clin Psychopharmacol 2000;15:133–40.
44. Savli M, Bauer A, Mitterhauser M, Ding YS, et al. Normative database of the serotonergic system in healthy subjects using multi-tracer PET. Neuroimage 2012;63:447–59.
45. Schwarz LA, Luo L. Organization of the locus coeruleus-norepinephrine system. Curr Biol 2015;25:R1051–6.
46. Sechter D, Vandel P, Weiller E, Pezous N, et al. A comparative study of milnacipran and paroxetine in outpatients with major depression. J Affect Disord 2004;83:233–6.
47. Serretti A, Chiesa A, Calati R, Perna G, et al. Novel antidepressants and panic disorder: evidence beyond current guidelines. Neuropsychobiology 2011;63:1–7.
48. Spies M, Knudsen GM, Lanzenberger R, Kasper S. The serotonin transporter in psychiatric disorders: insights from PET imaging. Lancet Psychiatry 2015;2:743–55.
49. Steen A, Den Boer JA. A double-blind six months comparative study of milnacipran and clomipramine in major depressive disorder. Int Clin Psychopharmacol 1997;12:269–81.
50. Takano A, Halldin C, Farde L. SERT and NET occupancy by venlafaxine and milnacipran in nonhuman primates: a PET study. Psychopharmacology (Berl) 2013;226:147–53.
51. Tignol J, Pujol-Domenech J, Chartres JP, Leger JM, et al. Double-blind study of the efficacy and safety of milnacipran and imipramine in elderly patients with major depressive episode. Acta Psychiatr Scand 1998;97:157–65.
52. Tsukamoto T, Kondoh R, Ichikawa K. Efficacy and safety of milnacipran in the treatment of generalized anxiety disorder: an open study. Int J Psychiatry Clin Pract 2004;8:255–8.
53. Tsutsui-Kimura I, Ohmura Y, Izumi T, Yamaguchi T, et al. The effects of serotonin and/or noradrenaline reuptake inhibitors on impulsive-like action assessed by the three-choice serial reaction time task: a simple and valid model of impulsive action using rats. Behav Pharmacol 2009;20:474–83.
54. Tsutsui-Kimura I, Yoshida T, Ohmura Y, Izumi T, et al. Milnacipran remediates impulsive deficits in rats with lesions of the ventromedial prefrontal cortex. Int J Neuropsychopharmacol 2015;18(5):pyu083. Published online 2015 Jan 28, doi: 10.1093/ijnp/pyu083.
55. Umehara M, Ago Y, Fujita K, Hiramatsu N, et al. Effects of serotonin-norepinephrine reuptake inhibitors on locomotion and prefrontal monoamine release in spontaneously hypertensive rats. Eur J Pharmacol 2013;702:250–7.
56. Van Amerongen AP, Ferrey G, Tournoux A. A randomised, double-blind comparison of milnacipran and imipramine in the treatment of depression. J Affect Disord 2002;72:21–31.
57. Vanicek T, Spies M, Rami-Mark C, Savli M, et al. The norepinephrine transporter in attention-deficit/hyperactivity disorder investigated with positron emission tomography. JAMA Psychiatry 2014;71:1340–9.
58. Whitton AE, Treadway MT, Pizzagalli DA. Reward processing dysfunction in major depression, bipolar disorder and schizophrenia. Curr Opin Psychiatry 2015;28:7–12.
59. Yoshimura R, Mitoma M, Sugita A, Hori H, et al. Effects of paroxetine or milnacipran on serum brain-derived neurotrophic factor in depressed patients. Prog Neuropsychopharmacol Biol Psychiatry 2007;31:1034–7.
60. Young SN, Smith SE, Pihl RO, Ervin FR. Tryptophan depletion causes a rapid lowering of mood in normal males. Psychopharmacology (Berl) 1985;87:173–7.
O.Univ.-Prof.Dr.h.c.mult.Dr.med.Siegfried Kasper, Dr.Marie Spies, Assoc.Prof.Rupert Lanzenberger, MD, PD, Universitätsklinik für Psychiatrie und Psychotherapie, Medizinische Universität Wien, Währinger Gürtel 18–20, 1090 Wien, Österreich, E-Mail: sci-biolpsy@meduniwien.ac.at
−: kein Unterschied; ↓: schlechter; ↑: besser
Mechanisms of action, efficacy, and clinical application of milnacipran
Neuroscientific studies have revealed the relevance of changes to the neurotransmitter norepinephrine and associated molecules for the pathogenesis of depression. In addition, the monoamines serotonin and dopamine play a central role. Based on these findings, serotonin-norepinephrine reuptake inhibitors (SNRI) have been developed over the last decades in order to address and treat these aspects of depressive pathophysiology. Among available SNRI, milnacipran has shown great clinical efficacy, as studies have demonstrated that it is in general equally effective to selective serotonin reuptake inhibitors (SSRI), and tricyclic antidepressants (TCA). However, milnacipran exhibits numerous clinical benefits, including its lower risk of side effects, particularly anticholinergic side effects, in comparison to TCA. A study has also demonstrated that milnacipran may be particularly effective in patients with reduced energy and drive. Most important for its clinical relevance and applicability, however, is milnacipran’s pharmacokinetic profile. Milnacipran is primarily eliminated via the renal system and shows a low risk for interactions with other medications. These characteristics make milnacipran a clinically highly applicable antidepressant option, in particular when considering the high rates of multimorbidity and resulting polypharmacy in psychiatric patient groups.
Key words: milnacipran, antidepressive therapy, noradrenaline, SNRI
Psychopharmakotherapie 2016; 23(06)
