Sandra Thiel, Bochum/Düsseldorf, Ralf Gold und Kerstin Hellwig, Bochum
Fertilität und multiple Sklerose
Aus der klinischen Erfahrung scheint die Fertilität bei MS-Patienten nicht eingeschränkt zu sein [9]. Aber Frauen mit MS sind häufiger kinderlos und unterziehen sich häufiger reproduktionsmedizinischen Behandlungen als gesunde Frauen [34]. Bisher ist noch nicht geklärt, ob dies eine biologische Ursache, psychosoziale Faktoren oder eine Kombination widerspiegelt. Obwohl es zu den Auswirkungen immunmodulatorischer Therapien auf die Fertilität ebenfalls keine systematischen Untersuchungen gibt, scheinen auch diese aus dem klinischen Alltag heraus keinen größeren Einfluss auf die Fruchtbarkeit zu haben. Unter Interferon-beta-(IFN-β-)Therapie können Unregelmäßigkeiten oder Veränderungen der Menstruationsblutung auftreten [5], anscheinend jedoch ohne Einfluss auf die Ovulationsfähigkeit und somit auf die Fertilität. Im Gegensatz dazu tritt bei etwa 35% der Frauen älter als 35 Jahre unter Mitoxantron eine permanente Amenorrhö auf [52].
Unerfüllter Kinderwunsch und hormonelle Stimulationstherapien
Die Hinweise, dass reproduktionsmedizinische Behandlungen MS-Schübe auslösen können, mehren sich. Bei erfolgloser Stimulation zeigte sich ein Anstieg der Schubaktivität [11]. Ein generelles Abraten von dieser Behandlung sehen wir allerdings nicht als gerechtfertigt an. Die Ursache der Schuberhöhung bleibt spekulativ. Auf der einen Seite könnte der stetig schwankende Estrogenspiegel ein Grund sein, aber auch die direkten Effekte der verabreichten Hormone auf das Immunsystem. Auf der anderen Seite werden Faktoren wie Stress oder eine fehlende immunmodulatorische Begleittherapie diskutiert. Manche Autoren fanden, dass das Schubrisiko durch die Gabe von GnRH-Agonisten erhöht war, sodass eher GnRH-Antagonisten, sollte eine Downregulation notwendig sein, bevorzugt werden sollten. Wir raten Frauen in der Regel, ihre immunmodulatorische Therapie während der Stimulation beizubehalten.
Verlauf der multiplen Sklerose in der Schwangerschaft
Während die Schubrate in der Schwangerschaft kontinuierlich abnimmt (um bis zu 80% im letzten Drittel), kommt es in den ersten drei Monaten post partum zu einem signifikanten Schubanstieg. Dieser typische Verlauf konnte in vielen Studien reproduzierbar belegt werden, so auch in unserer Datenbank [28]. Tritt dennoch ein Schub in der Schwangerschaft auf (bei etwa 25% der Patienten), kann man vor allem bei einer schweren Symptomatik wie gewohnt hoch dosiert mit Glucocorticoiden behandeln. Bevorzugt eingesetzt werden sollte Prednisolon, das im Gegensatz zu Dexamethason nur zu etwa 10% plazentagängig ist. Da das Risiko der Bildung einer Lippen-Kiefer-Gaumenspalte nicht ausgeschlossen ist [44] und Steroide als „schwache Teratogene“ diskutiert werden, sollte man im ersten Trimenon, speziell zwischen der 8. und 11. Woche, mit einer Glucocorticoid-Therapie zurückhaltend sein. In der Regel wird nur ein Glucocorticoid-Puls in der Schwangerschaft notwendig werden, es kann jedoch insbesondere bei Mehrfachbehandlungen mit Steroiden zur intrauterinen Wachstumsretardierung, zur Frühgeburt sowie zur vorübergehenden Hypoglykämie, Hypotonie und Elektrolytstörungen beim Neugeborenen kommen [51]. Sollte in seltenen Fällen eine Glucocorticoid-Therapie bis zur Geburt notwendig sein, ist auf eine eventuelle Nebenniereninsuffizienz des Neugeborenen zu achten. Eine Alternative können Plasmaaustauschverfahren, insbesondere bei steroidresistenten Schüben, darstellen. Zusammenfassend können und sollten schwere Schübe während der Schwangerschaft mit einem Glucocorticoid behandelt werden, die Indikation für eine Schubtherapie sollte jedoch insbesondere im 1. Trimenon streng gestellt werden.
Gynäkologische Aspekte
Frauen mit MS müssen nicht mit einem vermehrten Auftreten von gynäkologischen Komplikationen in der Schwangerschaft rechnen. Weder die Abortrate noch das Auftreten von Fehlbildungen oder Frühgeburten ist durch die MS negativ beeinflusst [53]. Möglicherweise ist das Geburtsgewicht von Neugeborenen von Müttern mit MS reduziert (im Mittel um 150 bis 200 g) [13], was jedoch nicht in allen Studien nachgewiesen werden konnte. Eine erhöhte Rate an Schnittentbindungen ist beschrieben [34]. Der postpartale Schubanstieg ist allerdings unabhängig vom Entbindungsmodus; so korrelieren weder vaginale Spontangeburten noch Schnittentbindungen mit Schüben post partum. Die Art der Entbindung sollte somit in erster Linie von geburtshilflichen Erwägungen abhängig gemacht werden. Die Autoren der PRIMS-Studie und eine italienische Studie konnten zeigen, dass die Gabe einer Periduralanästhesie (PDA) nicht mit dem postpartalen Schubanstieg [54] oder Behinderung [45] korrelierte. Somit müssen Frauen, die an einer MS erkrankt sind, nicht auf eine PDA verzichten.
Immunmodulation und Kinderwunsch
Da die gängigen Substanzen in der Schwangerschaft kontraindiziert oder nur eingeschränkt zugelassen sind, wird eine Unterbrechung der Therapie vor geplanter Konzeption bzw. eine Beendigung spätestens mit Eintritt der Schwangerschaft empfohlen. Tritt eine Schwangerschaft unter den gängigen Immunmodulatoren auf, ist dies kein Grund für einen Schwangerschaftsabbruch, eine intensivierte Ultraschallvorsorge wird jedoch angeraten. Gerade bei einer Exposition mit potenziell teratogenen Substanzen wie Fingolimod [20] oder Teriflunomid [36] sollten diese Untersuchungen in speziellen von der Deutschen Gesellschaft für Ultraschall in der Medizin (DEGUM) zertifizierten Zentren durchgeführt werden. Eine immunmodulatorische Therapie ist in der Schwangerschaft aufgrund des günstigen natürlichen Verlaufs in den meisten Fällen nicht notwendig. Im Folgenden soll die Datenlage zu den einzelnen Wirkstoffen besprochen werden (Tab. 1).
Tab. 1. Übersicht über die derzeitige Datenlage der gängigen immunmodulatorischen und immunsuppressiven Therapien in Schwangerschaft und Stillzeit
|
Interferone |
Glatirameracetat |
Natalizumab |
Fingolimod |
Dimethylfumarat |
||||||
|
Erhöhtes Risiko |
Erhöhtes Risiko |
Erhöhtes Risiko |
Erhöhtes Risiko |
Erhöhtes Risiko |
||||||
|
Tierversuch |
Humane Daten |
Tierversuch |
Humane Daten |
Tierversuch |
Humane Daten |
Tierversuch |
Humane Daten |
Tierversuch |
Humane Daten |
|
|
Geringere Geburtsgröße |
Nein |
Fraglich |
– |
Nein |
Nein |
– |
Ja |
– |
Ja |
– |
|
Geringeres Geburtsgewicht |
Nein |
Fraglich |
– |
Nein |
Nein |
– |
Ja |
– |
Ja |
– |
|
Geringeres Gestationsalter |
– |
Fraglich |
– |
Nein |
– |
Nein |
– |
– |
– |
– |
|
Spontanabort |
Ja |
Nein |
– |
Nein |
Fraglich |
– |
Ja |
– |
Ja |
Unwahrscheinlich |
|
Fehlbildungen |
Nein |
Nein |
Nein |
Nein |
Nein |
Nein |
Ja |
Fraglich |
Nein |
Unwahrscheinlich |
|
Übergang Muttermilch |
– |
Unwahrscheinlich |
– |
Unwahrscheinlich |
Ja |
Ja |
Ja |
Wahrscheinlich |
Ja |
Wahrscheinlich |
|
Empfehlung Schwangerschaft |
Die Therapie kann mit Eintritt der Schwangerschaft beendet werden. Ein Fortführen der Medikation in der Schwangerschaft bei aktiver Erkrankung kann erwogen werden. |
Die Therapie kann mit Eintritt der Schwangerschaft beendet werden. |
Die Therapie kann bis zum Eintritt der Schwangerschaft unter strenger Risiko-Nutzen-Abwägung fortgeführt werden. Natalizumab kann bei aggressiven MS-Verläufen auch in der Schwangerschaft verordnet werden. |
Die Therapie sollte zwei Monate vor einer geplanten Schwangerschaft beendet werden. |
Die Therapie sollte mit dem Versuch schwanger zu werden oder spätestens mit Eintritt der Schwangerschaft abgesetzt werden. |
|||||
|
Empfehlungen Stillzeit |
Es liegen derzeit keine ausreichenden Erfahrungen vor. Die Wirkstoffaufnahme durch den Säugling scheint aufgrund des großen Molekulargewichts und der geringen oralen Bioverfügbarkeit unwahrscheinlich. |
Es liegen derzeit keine ausreichenden Erfahrungen vor. Die pharmakokinetischen Daten lassen ein Stillen unter Therapie möglich erscheinen. |
Natalizumab geht in die Muttermilch über, daher sollte unter Natalizumab nicht gestillt werden. |
Fingolimod geht im Tierversuch in die Muttermilch über. Humane Daten liegen derzeit nicht vor. Daher sollte unter Fingolimod nicht gestillt werden. |
Dimethylfumarat geht im Tierversuch in die Muttermilch über. Humane Daten liegen derzeit nicht vor. Daher sollte unter Dimethylfumarat nicht gestillt werden. |
|||||
|
Zitationen |
3, 18, 19, 30, 38, 55 |
33, 38, 41 |
12, 17, 26, 48 |
20, 21, 35 |
25, 37 |
|||||
Tab. 1. Übersicht über die derzeitige Datenlage der gängigen immunmodulatorischen und immunsuppressiven Therapien in Schwangerschaft und Stillzeit (Fortsetzung)
|
Teriflunomid |
Alemtuzumab |
Mitoxantron |
Azathioprin |
Rituximab |
||||||
|
Erhöhtes Risiko |
Erhöhtes Risiko |
Erhöhtes Risiko |
Erhöhtes Risiko |
Erhöhtes Risiko |
||||||
|
Tierversuch |
Humane Daten |
Tierversuch |
Humane Daten |
Tierversuch |
Humane Daten |
Tierversuch |
Humane Daten |
Tierversuch |
Humane Daten |
|
|
Geringere Geburtsgröße |
– |
– |
– |
Unwahrscheinlich* |
Ja |
– |
– |
– |
– |
– |
|
Geringeres Geburtsgewicht |
– |
– |
– |
Unwahrscheinlich* |
Ja |
– |
– |
– |
– |
– |
|
Geringeres Gestationsalter |
– |
– |
– |
Unwahrscheinlich* |
Ja |
– |
– |
Fraglich |
– |
– |
|
Spontanabort |
– |
– |
Ja |
Unwahrscheinlich* |
– |
– |
Ja |
– |
– |
– |
|
Fehlbildungen |
Ja |
– |
Nein |
Unwahrscheinlich* |
Nein |
Ja |
Ja |
Fraglich |
Nein |
Unwahrscheinlich |
|
Übergang Muttermilch |
Ja |
Wahrscheinlich |
Ja |
Wahrscheinlich |
Ja |
Ja |
Ja |
Ja |
Ja |
Wahrscheinlich |
|
Empfehlung Schwangerschaft |
Bei akutem Kinderwunsch muss Teriflunomid beschleunigt eliminiert werden, bis die Plasmaspiegel von Teriflunomid unter 0,02 mg/l liegen; ebenso bei akzidentiell eingetretener Schwangerschaft. |
Vor jeder Infusion muss ein Schwangerschaftstest durchgeführt werden. Die Therapie sollte vier Monate vor einer geplanten Schwangerschaft abgesetzt werden. |
Vor jeder Infusion muss ein Schwangerschaftstest durchgeführt werden. Die Therapie sollte sechs Monate vor einer geplanten Schwangerschaft von beiden Geschlechtern abgesetzt werden. Tritt eine Schwangerschaft unter Mitoxantron auf, ist eine embryotoxische Beratungsstelle aufzusuchen. |
Die Therapie kann bis zum Eintritt der Schwangerschaft beibehalten werden. Azathioprin kann nach intensiver Nutzen-Risiko-Abwägung auch in der Schwangerschaft angewendet werden, eine intensivierte Ultraschallvorsorge und eine sorgfältige hämatologische Überwachung ist angeraten. |
Die Therapie sollte zwölf Monate vor einer geplanten Schwangerschaft abgesetzt werden. |
|||||
|
Empfehlungen Stillzeit |
Teriflunomid geht im Tierversuch in die Muttermilch über. Humane Daten liegen derzeit nicht vor. Daher sollte unter Teriflunomid nicht gestillt werden. |
Alemtuzumab geht im Tierversuch in die Muttermilch über. Humane Daten liegen derzeit nicht vor. Daher sollte unter Alemtuzumab nicht gestillt werden. |
Mitoxantron geht in die Muttermilch über, daher sollte unter Mitoxantron nicht gestillt werden. |
Azathioprin geht in die Muttermilch über, daher sollte unter Azathioprin nicht gestillt werden. |
Rituximab geht im Tierversuch in die Muttermilch über. Humane Daten liegen derzeit nicht vor. Daher sollte unter Rituximab nicht gestillt werden. |
|||||
|
Zitationen |
8, 10, 22, 36 |
1, 6, 23 |
4, 16, 24, 32, 52 |
2, 7, 14, 15, 40, 50 |
39, 42, 49 |
|||||
* Bei Konzeption >4 Monate post infusionem – Datenlage nicht ausreichend
Interferon beta
In Tierversuchen wurde bei der Gabe von sehr hohen Dosen Interferon beta (IFN-β) ein anovulatorischer und abortiver Effekt beobachtet [18]. In den meisten humanen Studien wurde kein erhöhtes Risiko für das Auftreten von Spontanaborten nach IFN-β-Exposition in der Schwangerschaft gefunden. Einige Arbeitsgruppen konnten jedoch ein geringeres Geburtsgewicht [55], eine geringere Geburtslänge [19] und auch ein vermehrtes Auftreten von Frühgeburten [3] nach IFN-β-Exposition beobachten. 2012 veröffentlichten Lu et al. die Ergebnisse eines systematischen Reviews [38] zu 761 IFN-β-exponierten Schwangerschaften. Die Autoren kommen zu dem Schluss, dass die Exposition mit IFN-β kein nennenswertes teratogenes oder abortives Risiko für den Embryo darstellt. Allerdings zeigten sich ein vermindertes mittleres Geburtsgewicht, eine verminderte mittlere Geburtsgröße sowie eine erhöhte Frühgeburtlichkeit nach IFN-β-Exposition. Auch unsere eigenen Daten aus 78 Schwangerschaften [30] und jüngste Auswertungen von mehr als 200 bisher unveröffentlichten IFN-β-exponierten Schwangerschaften geben keinen Hinweis auf ein teratogenes, abortives oder Wachstums-restriktives Risiko. In Deutschland ist es gängige Praxis, die Therapie mit Eintritt der Schwangerschaft zu beenden. Ein Fortführen der Medikation in der Schwangerschaft bei aktiver Erkrankung kann erwogen werden.
Glatirameracetat
Bisher veröffentlichte Studien konnten keinen Zusammenhang zwischen einem negativen Schwangerschaftsausgang und einer Exposition mit Glatirameracetat (GLAT) in der Schwangerschaft herstellen [38]. Die Firma Teva veröffentlichte kürzlich 7343 GLAT-exponierte Schwangerschaften, ohne Auffälligkeiten in den 5042 Schwangerschaften mit bekanntem Ausgang [41]. Wir selbst konnten kürzlich die zweitgrößte Kohorte mit 151 GLAT-exponierten Schwangerschaften auswerten und mit 95 nicht exponierten Schwangerschaften MS-erkrankter Frauen vergleichen [33]. Dabei zeigte sich, dass eine GLAT-Exposition im 1. Trimenon weder einen Einfluss auf Spontanaborte, Frühgeburten oder das Auftreten von Fehlbildungen hat noch das Geburtsgewicht beeinflusst. Für die Praxis gilt, dass die Therapie bis zur Bestätigung der Schwangerschaft beibehalten werden kann und bei Vorliegen eines positiven Schwangerschaftstests beendet werden sollte.
Natalizumab
Aus dem firmeneigenen Schwangerschaftsregister wurden bisher Daten zu 362 Natalizumab-exponierten Schwangerschaften veröffentlicht [12]. Die Rate großer und kleiner Fehlbildungen ist mit 8,5% in dieser Kohorte erhöht, jedoch ohne erkennbares Fehlbildungsmuster. Wir fanden in 101 Natalizumab-exponierten Schwangerschaften aus dem deutschsprachigen Multiple Sklerose und Kinderwunschregister (DMSKW) kein teratogenes Risiko (Fehlbildungsrate 3,9%) [17] und auch eine italienische Gruppe konnte in 28 exponierten Schwangerschaften kein erhöhtes Risiko nachweisen [48]. Ein Grund für die unterschiedlichen Fehlbildungsraten könnten uneinheitliche Definitionen für Fehlbildungen sein. Da ein Plazentaübergang im 1. Trimenon für Natalizumab unwahrscheinlich ist, erscheint eine normale Fehlbildungsrate plausibel. Verglichen mit gesunden Frauen ergab sich jedoch ein erhöhtes Risiko für Spontanaborte und ein signifikant niedrigeres Geburtsgewicht [17]. Diese Unterschiede bestanden jedoch nicht im Vergleich zu einer Kontrollgruppe MS-erkrankter Schwangerer ohne Natalizumab-Exposition. Somit ist zum jetzigen Zeitpunkt noch nicht geklärt, ob sich durch die Gabe von Natalizumab Auswirkungen auf das Geburtsgewicht und die Fehlgeburtenrate ergeben. Zehn von 13 Neugeborenen, deren Mütter aufgrund einer hochaktiven MS im 3. Trimenon mit Natalizumab behandelt wurden, wiesen hämatologische Veränderungen auf (Anämie und/oder Thrombozytopenie), welche innerhalb der ersten vier Monate post partum reversibel waren [26]. Wir konnten außerdem Natalizumab im Serum von fünf Neugeborenen, deren Mütter im 3. Trimenon behandelt wurden, bei der Geburt nachweisen, bedingt durch den ansteigenden aktiven Transport humaner IgGs im Verlauf der Schwangerschaft (Abb. 1) [26]. Bei Kinderwunsch kann die Therapie bis zum Eintritt der Schwangerschaft unter Risiko-Nutzen-Abwägung fortgeführt werden. Setzt man Natalizumab vor der Schwangerschaft ab, scheint es zu einer erhöhten Schubrate in der Schwangerschaft zu kommen. Natalizumab kann bei aggressiven MS-Verläufen mit Gefahr eines Rebounds nach Rücksprache mit einem MS-Zentrum auch in der Schwangerschaft verordnet werden. Die Infusionsintervalle sollten dann auf sechs Wochen gestreckt und die Therapie vor der 30. Woche beendet werden. Die Entbindung in einer Klinik mit angeschlossener Pädiatrie ist empfohlen. Die Kontrolle von großem Blutbild, Leberwerten, Bilirubin und Haptoglobin beim Neugeborenen muss post partum erfolgen.
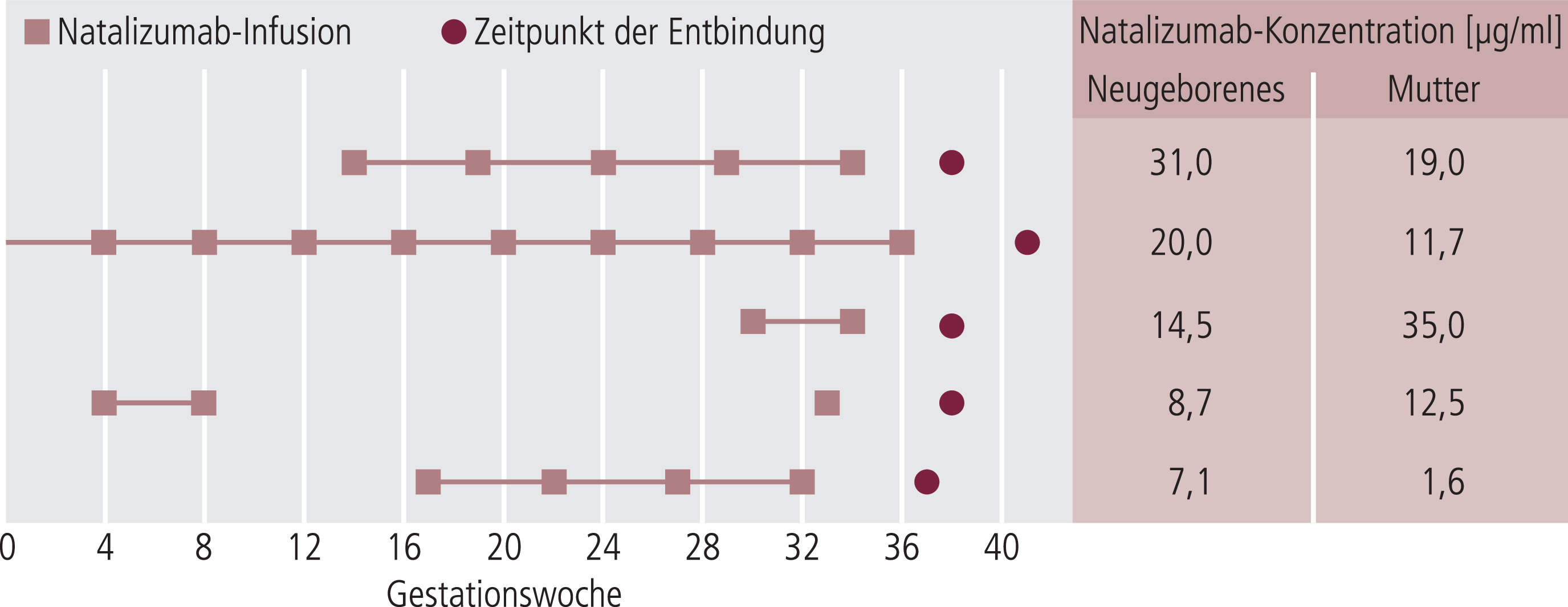
Abb. 1. Natalizumab-Konzentration [μg/ml] in Neugeborenen und Müttern nach der Geburt abhängig von der Anzahl an Natalizumab-Infusionen während der Schwangerschaft und der Zeitspanne zwischen der letzten Infusion und der Geburt [26]
Fingolimod
Fingolimod erwies sich in einem von zwei Tierversuchen als teratogen [20]. In den Zulassungsstudien wurden 66 Schwangerschaften unter Fingolimod beobachtet. 26 Kinder (40%) wurden gesund geboren, ein Kind mit einer kongenitalen posteromedialen Verkrümmung der Tibia und eines mit Akranie. Neun Schwangerschaften (14%) endeten in einem Spontanabort, 24 Schwangerschaften (36%) wurden elektiv terminiert, eine davon aufgrund einer zuvor diagnostizierten Fallot’schen Tetralogie. Insgesamt wurden drei Fehlbildungen (5%) in dieser Kohorte beschrieben. Vier Schwangerschaften waren zum Zeitpunkt der Auswertung noch intakt und bei einer Schwangerschaft konnte der Ausgang nicht beobachtet werden [35]. Kürzlich wurden weitere 879 Schwangerschaften mit Fingolimod-Exposition präsentiert [21]. In 94 Schwangerschaften mit bekanntem Ausgang wurde nur eine einzige Fehlbildung beobachtet (1,2%). Eine abschließende Beurteilung über ein mögliches teratogenes Risiko beim Menschen ist noch nicht möglich, allerdings zeigen diese Daten, dass die meisten Neugeborenen auch nach Fingolimod-Exposition gesund geboren werden. Wegen seiner langen Halbwertszeit von bis zu neun Tagen gilt die Empfehlung, Fingolimod zwei Monate vor einer geplanten Schwangerschaft abzusetzen. Tritt dennoch eine Schwangerschaft unter Fingolimod auf, ist eine intensivierte Ultraschalluntersuchung angeraten.
Dimethylfumarat (DMF)
Tierversuche geben keinen Hinweis auf teratogene Risiken nach Dimethylfumarat-Exposition. Ein verringertes Geburtsgewicht und Fehlbildungen traten nur bei sehr hohen Dosierungen auf, die auch für das Muttertier toxisch waren [25]. Beim Menschen zeigt die erste Auswertung von 60 Schwangerschaften, die innerhalb der MS-Zulassungsstudien und unter Fumaderm® eingetreten sind, folgende Ergebnisse [37]: 29 Kinder (49%) wurden gesund geboren, fünf Schwangerschaften (8%) endeten in Spontanaborten und 13 Schwangerschaften wurden elektiv terminiert. Aus Postmarketing-Daten konnten weitere 401 Dimethylfumarat-exponierte Schwangerschaften ausgewertet werden [37]. 72 Kinder wurden gesund geboren und drei (3%) mit einer Fehlbildung. Des Weiteren traten 38 Spontanaborte (9%), sieben ektope Schwangerschaften und elf elektive Schwangerschaftsabbrüche auf. 252 Schwangerschaften waren zum Zeitpunkt der Auswertung noch intakt und bei 14 konnte kein Ausgang beobachtet werden. Insgesamt gibt es noch nicht genügend Daten, um zu beurteilen, ob die Exposition in der Schwangerschaft sicher ist. Allerdings ist DMF, aufgrund der sehr kurzen Halbwertszeit und der fehlenden Gewebeakkumulation, sehr gut steuerbar. DMF sollte mit dem Versuch, schwanger zu werden, oder spätestens bei Feststellen einer Schwangerschaft abgesetzt werden.
Teriflunomid
In Tierversuchen zeigte Teriflunomid in Dosierungen im humantherapeutischen Bereich embryotoxische und teratogene Eigenschaften [22]. Klinische Erfahrungen beschränken sich auf wenige Schwangerschaften in den Zulassungsstudien: Von 70 Schwangerschaften unter Teriflunomid wurden 26 gesunde Kinder geboren, 29 Schwangerschaften vorzeitig elektiv beendet, 13 Spontanaborte (18,6%) traten auf, eine Schwangerschaft war noch nicht beendet und ein Schwangerschaftsausgang konnte nicht beobachtet werden. Es traten weder Fehlbildungen auf noch konnten Auffälligkeiten bezüglich des Geburtsgewichts oder des Gestationsalters bei Geburt beobachtet werden [36]. Teriflunomid ist der aktive Metabolit von Leflunomid (Arava®), das zur Behandlung der rheumatoiden Arthritis eingesetzt wird. Auch für Leflunomid liegen derzeit nur begrenzt Erfahrungen zur Anwendung bei Schwangeren vor. In zwei kleinen retrospektiven Studien mit 64 und 45 unbeabsichtigten Schwangerschaften unter Leflunomid zeigte sich keine signifikante Erhöhung der Gesamtrate von bedeutenden strukturellen Schäden [10, 8]. Frauen im gebärfähigen Alter müssen während einer Therapie mit Teriflunomid eine zuverlässige Verhütungsmethode anwenden. Patientinnen, die eine Schwangerschaft planen, ist zu empfehlen, Teriflunomid abzusetzen und ein Verfahren zur beschleunigten Elimination mit Colestyramin oder alternativ Aktivkohlepulver durchzuführen, bis die Plasmaspiegel von Teriflunomid unter 0,02 mg/l liegen. Teriflunomid hat eine sehr lange Halbwertszeit von 19 Tagen [22]. Wenn kein Verfahren zur beschleunigten Elimination angewendet wird, ist zu erwarten, dass es durchschnittlich acht Monate dauert, bis Spiegel von unter 0,02 mg/l erreicht werden. Im Einzelfall kann dies auch bis zu zwei Jahre dauern. Daher sollten die Plasmaspiegel von Teriflunomid gemessen werden, bevor eine Frau versucht, schwanger zu werden. Wenn festgestellt wurde, dass eine Plasmakonzentration von unter 0,02 mg/l erreicht wurde, muss die Plasmakonzentration nach einem Zeitraum von mindestens 14 Tagen erneut gemessen werden. Wenn die Plasmakonzentrationen bei beiden Messungen unter 0,02 mg/l liegen, ist kein Risiko für den Fetus zu erwarten [31]. Bei akzidentiell eingetretener Schwangerschaft sollte Teriflunomid ebenfalls beschleunigt eliminiert werden.
Alemtuzumab
Tierversuche mit Alemtuzumab geben keinen Hinweis auf Teratogenität, es wurde jedoch Reproduktionstoxizität beobachtet [23]. In klinischen Studien sind bisher 193 Schwangerschaften aufgetreten. Fast alle Schwangerschaften traten mehr als vier Monate nach der letzten Alemtuzumab-Infusion auf, nur acht Schwangerschaften innerhalb von vier Monaten post infusionem. Der Ausgang der meisten Schwangerschaften ist bekannt; 16 sind noch nicht beendet und zehn Schwangere haben die Studie vorzeitig verlassen (lost to follow-up). Von den 167 Schwangerschaften mit bekanntem Ausgang wurden 110 Kinder (65,9%) gesund geboren, 37 Schwangerschaften (22,2%) endeten in einem Spontanabort, 19 (11,4%) wurden elektiv terminiert und eine Totgeburt (0,6%) wurde beobachtet [1]. Eine zuverlässige Kontrazeption während und vier Monate nach der Behandlungsphase wird laut Fachinformation empfohlen [23]. Sollte im Behandlungszyklus oder kurz danach eine Schwangerschaft auftreten, erscheint eine höhergradige Reproduktionstoxizität unwahrscheinlich, da Antikörper im 1. Trimenon nicht in nennenswertem Umfang über die Plazentaschranke transportiert werden. Aufgrund einer Halbwertszeit von wenigen Tagen ist ein Übertritt im 2. Trimenon nicht zu erwarten. Alemtuzumab ist nach etwa 30 Tagen nicht mehr im Serum nachweisbar. Problematisch können autoimmune Schilddrüsenerkrankungen sein, die durch die Behandlung entstehen können. Hypothyreote Stoffwechsellagen können die Fertilität beeinträchtigen, Autoantikörper auch zum Fetus übergehen und Symptome verursachen [6]. Dies ist bei Kinderwunsch auch nach einer Behandlung mit Alemtuzumab zu bedenken und zu überprüfen.
Mitoxantron
Bei Mitoxantron handelt es sich um ein unspezifisches Immunsuppressivum mit genotoxischem Potenzial. In Tierversuchen erwies sich Mitoxantron als nicht teratogen, wobei die verabreichten Dosen bei 0,01% bis 0,03% der empfohlenen Dosis beim Menschen lagen. Es konnte selbst bei diesen geringen Dosen eine Wachstumsretardierung der Jungtiere und ein erhöhtes Risiko für Frühgeburten beobachtete werden [52]. Bislang gibt es nur zwei Fallberichte von Mitoxantron-exponierten Schwangerschaften bei MS-Patienten. Es wurden ein leicht wachstumsretardierter, aber gesunder Säugling und ein Säugling mit Pierre-Robin-Sequenz geboren [16, 32]. Ansonsten gibt es nur wenige Fallberichte onkologischer Patienten, die polychemotherapeutisch behandelt wurden mit unterschiedlichem Outcome der Schwangerschaft – von intrauterinem Fruchttod bis hin zu gesunden Kindern [4, 24]. Es wird daher MS-Patienten beider Geschlechter empfohlen, die Therapie mindestens sechs Monate vor einer geplanten Schwangerschaft abzusetzen. Vor jeder Mitoxantron-Gabe muss ein Schwangerschaftstest durchgeführt werden.
Azathioprin
In Tierversuchen erwies sich Azathioprin als teratogen und embryoletal [40]. Der plazentare Übergang im Menschen ist zwar gering, es konnte jedoch ein aktiver Metabolit des Azathioprin in den Erythrozyten dreier Mutter-Kind-Paare nachgewiesen werden, die durch die gesamte Schwangerschaft mit Azathioprin behandelt wurden [15]. Studien und Fallserien mit mehr als 2000 Schwangerschaften zeigen kein erhöhtes Risiko für Fehlbildungen nach Azathioprin-Exposition [50, 7], ein erhöhtes Risiko für Frühgeburten wird jedoch diskutiert [2]. Außerdem wurde von Leukozytopenien und/oder Thrombozytopenien in einigen Neugeborenen berichtet, deren Mütter in der Schwangerschaft Azathioprin erhalten hatten [14]. Bei einer stabil eingestellten neuroimmunologischen Erkrankung kann Azathioprin bis zum Eintritt der Schwangerschaft beibehalten werden. Sollte durch das Absetzen eine Exazerbation der Grunderkrankung zu befürchten sein, kann Azathioprin nach intensiver Nutzen-Risiko-Abwägung auch in der Schwangerschaft angewendet werden. Tritt eine Schwangerschaft unter Azathioprin auf, ist eine intensivierte Ultraschallvorsorge mit Organscreening und bei Exposition in der Schwangerschaft eine sorgfältige hämatologische Überwachung angeraten. Bei Leukopenie der Mutter muss gegebenenfalls die Dosis reduziert werden.
Rituximab
In Tierversuchen zeigte sich keine Auswirkung von Rituximab auf die fetale Entwicklung, allerdings konnte ein Rückgang der B-Zellen in den Feten festgestellt werden [49]. Dieser B-Zell-Verlust wurde auch bei Neugeborenen beschrieben, deren Mütter im 2. und 3. Trimenon mit Rituximab behandelt wurden [39]. Diese Kinder waren ansonsten gesund und die B-Zell-Depletion war nach drei bis sechs Monaten nicht mehr nachweisbar. Die Berichte zur Ersttrimester-Exposition mit Rituximab beschreiben bisher keine Fehlbildungen [42]. Laut Fachinformation sollten Frauen im gebärfähigen Alter während und 12 Monate nach einer Behandlung mit Rituximab kontrazeptive Methoden anwenden.
Stillen und multiple Sklerose
Wir konnten kürzlich zeigen, dass ausschließlich stillende Frauen mit MS in den ersten sechs Monaten signifikant weniger Schübe erleiden; wobei einige Frauen mit Einführung der Beikost erneut Schübe bekommen. Innerhalb des ersten Jahres hatten nahezu gleich viele Frauen, die ausschließlich gestillt hatten, Schübe verglichen mit Frauen, die nicht oder teilgestillt hatten [31]. Erfreulicherweise zeigte auch eine Metaanalyse, dass stillende Frauen weniger Schübe haben als Frauen, die nicht stillen (Abb. 2) [43]. Auch wenn nicht alle Studien einen positiven Stilleffekt nachweisen konnten [46], unterstützt die vorhandene Datenlage Frauen, die stillen möchten. Die Gabe von Glucocorticoiden zur Schubbehandlung in der Stillzeit ist möglich. Die einmalige Gabe hoher Dosen bis zu 1 g (z.B. Methylprednisolon) erfordert keine Einschränkung des Stillens. Bei wiederholter Gabe solch hoher Dosen sollte, wenn es sich einrichten lässt, 3 bis 4 Stunden mit dem Stillen gewartet werden [51].
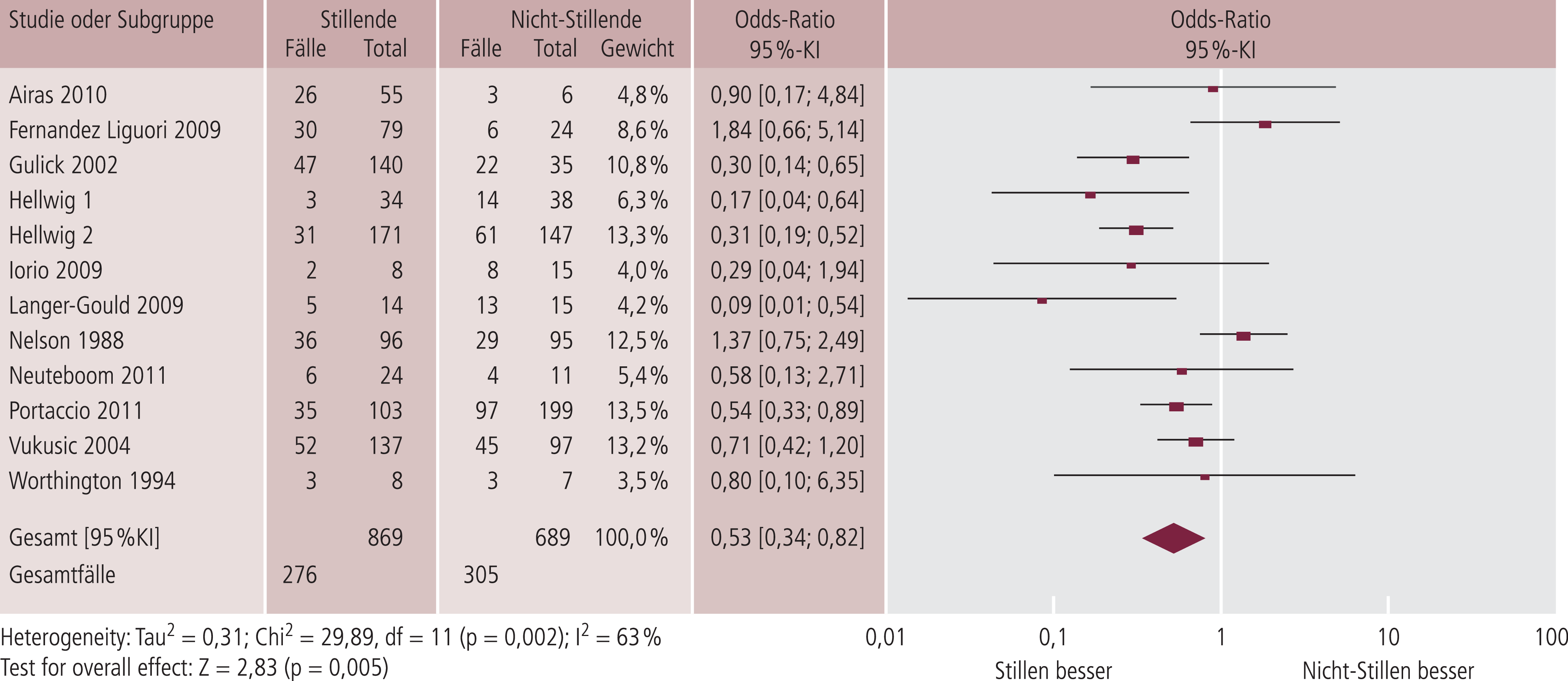
Abb. 2. Vergleich zwischen stillenden und nicht stillenden MS-Patientinnen in Bezug auf postpartale Schübe [mod. nach 43]
Stillen und Immunmodulation
Die gängigen Immunmodulatoren wie IFN-β oder GLAT sind in der Stillzeit nicht zugelassen, wenngleich es sich um große Moleküle mit geringer oraler Bioverfügbarkeit handelt, was einen Übertritt zum Säugling sehr unwahrscheinlich macht. Selbst hohe Dosen eines Interferons waren nicht in nennenswertem Umfang in der Milch nachzuweisen [27]. Unsere Erfahrungen beschränken sich auf wenige Mutter-Kind-Paare, die unter diesen Therapien gestillt haben mit normaler Kindsentwicklung. Natalizumab, Fingolimod und Mitoxantron sind in der Milch nachweisbar, daher ist das Stillen unter Therapie kontraindiziert. Zu anderen oralen Substanzen liegen keine Daten vor, aber die kleine Molekülgröße macht einen Übertritt in die Milch wahrscheinlich, daher sollte unter diesen Therapien nicht gestillt werden. Ob die Gabe von intravenösen Immunglobulinen direkt nach der Geburt einen Mehrwert hat, ist bisher noch ungeklärt. Wenn Frauen stillen möchten, gilt diese Behandlung für das Kind als unbedenklich. Verzichten Frauen auf das Stillen, ist es gängige Praxis, sofort mit einer immunmodulatorischen Therapie anzufangen. Der Beginn der MS-Therapie in den ersten drei Monaten zeigt einen Trend zur reduzierten Schubrate im ersten Jahr post partum [47]. Frauen mit hoher Krankheitsaktivität vor oder in der Schwangerschaft (typischerweise mit Natalizumab behandelte Frauen), sollten die Therapie nach Ausschluss von Infektzeichen zügig nach Geburt (innerhalb der ersten beiden Wochen) wieder aufnehmen. Dies gilt möglicherweise auch für Fingolimod, wobei es hierzu zu wenige Daten oder Erfahrung gibt.
Vaterschaft und multiple Sklerose
Die Gefahr, dass reproduktive Toxizität durch die Samenflüssigkeit verursacht wird, ist insgesamt als sehr gering einzuschätzen. Bei Vätern mit MS scheint weder die Erkrankung selbst noch Exposition mit immunmodulatorischen Arzneistoffen einen negativen Einfluss auf den Ausgang der Schwangerschaft zu haben [29]. Allgemein gilt: Männer, die eine Familie gründen wollen, müssen ihre immunmodulatorische Therapie vor der Zeugung nicht absetzen. Bei einer Therapie mit Mitoxantron wird allerdings aufgrund der Genotoxizität eine Therapiepause von sechs Monaten vor geplanter Zeugung empfohlen.
Danksagung
Wir danken allen Betroffenen für die freiwillige Teilnahme, ebenso allen Kollegen und MS-Schwestern, die unser Register unterstützen. Die Deutsche Gesellschaft für Multiple Sklerose (DMSG) weist regelmäßig auf Ergebnisse bzw. Projekte des Registers hin und unterstützt damit unsere Arbeit. Die Registerarbeit ist nur durch die freundliche Unterstützung der Firmen Bayer Healthcare, Biogen, Genzyme, Merck Serono, Novartis- und Teva Pharma möglich. Vielen Dank!
Interessenkonflikterklärung
ST: keine
KH: Unterstützung von der Deutschen Forschungsgemeinschaft – DFG; Referentenhonorar von Biogen Idec, Teva, Sanofi Aventis, Novartis, Bayer Healthcare und Merck Serono
RG: Vergütungen für Beratungsleistungen von Biogen und Teva sowie Referentenhonorar und Forschungszuschüsse von Biogen Idec Germany, Teva, Sanofi Aventis, Novartis, Bayer Healthcare und Merck Serono
Das Deutsche Multiple Sklerose und Kinderwunschregister wird unterstützt von Biogen-Idec Germany, Bayer Healthcare, Teva Pharma, Sanofi Aventis, Merck Serono, Novartis Pharma und Genzyme
Literatur
1. Achiron A, Chambers C, Fox EJ, et al. Pregnancy outcomes in patients with active RRMS who received alemtuzumab in the clinical development program. 31st Congress of the European Committee for Treatment and Research in Multiple Sclerosis (ECTRIMS), October 7−10, 2015: (P1122).
2. Akbari M, Shah S, Velayos FS, et al. Systematic review and meta-analysis on the effects of thiopurines on birth outcomes from female and male patients with inflammatory bowel disease. Inflamm Bowel Dis 2013;19:15–22.
3. Amato MP, Portaccio E, Ghezzi A, et al. Pregnancy and fetal outcomes after interferon-beta exposure in multiple sclerosis. Neurology 2010;75:1794–802.
4. Azuno Y, Kaku K, Fujita N, et al. Mitoxantrone and etoposide in breast milk. Am J Hematol 1995;48:131–2.
5. Bayer. Fachinformation Betaferon® 250 Mikrogramm/ml. August 2014.
6. Carp HJA, Selmi C, Shoenfeld Y. The autoimmune bases of infertility and pregnancy loss. J Autoimmun 2012;38:J266–74.
7. Casanova MJ, Chaparro M, Domenech E, et al. Safety of thiopurines and anti-TNF-alpha drugs during pregnancy in patients with inflammatory bowel disease. Am J Gastroenterol 2013;108:433–40.
8. Cassina M, Johnson DL, Robinson LK, et al. Pregnancy outcome in women exposed to leflunomide before or during pregnancy. Arthritis Rheum 2012;64:2085–94.
9. Cavalla P, Rovei V, Masera S, et al. Fertility in patients with multiple sclerosis: current knowledge and future perspectives. Neurol Sci 2006;27:231–9.
10. Chambers CD, Johnson DL, Robinson LK, et al. Birth outcomes in women who have taken leflunomide during pregnancy. Arthritis Rheum 2010;62:1494–503.
11. Correale J, Farez MF, Ysrraelit MC. Increase in multiple sclerosis activity after assisted reproduction technology. Ann Neurol 2012;72:682–94.
12. Cristiano L, Bozic C, Friend S, Bloomgren G. Evaluation of pregnancy outcomes from the TYSABRI® (Natalizumab) pregnancy exposure registry. Neurology 2013;80(Meeting Abstracts 1):P02.127.
13. Dahl J, Myhr KM, Daltveit AK, et al. Pregnancy, delivery and birth outcome in different stages of maternal multiple sclerosis. J Neurol 2008;255:623–7.
14. Davison JM, Dellagrammatikas H, Parkin JM. Maternal azathioprine therapy and depressed haemopoiesis in the babies of renal allograft patients. Br J Obstet Gynaecol 1985;92:233–9.
15. de Boer NKH, Jarbandhan SVA, de Graaf P, et al. Azathioprine use during pregnancy: unexpected intrauterine exposure to metabolites. Am J Gastroenterol 2006;101: 1390–2.
16. De Santis M, Straface G, Cavaliere AF, et al. The first case of mitoxantrone exposure in early pregnancy. Neurotoxicology 2007;28:696–7.
17. Ebrahimi N, Herbstritt S, Gold R, et al. Pregnancy and fetal outcomes following natalizumab exposure in pregnancy. A prospective, controlled observational study. Mult Scler 2015;21:198–205.
18. EMA. Avonex: EPAR – Product Information.
19. Fragoso YD, Boggild M, Macias-Islas MA, et al. The effects of long-term exposure to disease-modifying drugs during pregnancy in multiple sclerosis. Clin Neurol Neurosurg 2013;115:154–9.
20. Geissbuhler Y, Butzkueven H, Hernandez-Diaz S. Pregnancy outcomes from fingolimod clinical trials and post-marketing experience and the need for a multinational Gilenya (fingolimod) Pregnancy Exposure Registry in Multiple Sclerosis. ECTRIMS, Lyon, France, 2012:Abstract 751.
21. Geissbühler Y, Koren G, Wang H, et al. Pregnancy outcomes after exposure to fingolimod and in the general population. 31st Congress of the European Committee for Treatment and Research in Multiple Sclerosis, 2015: P611.
22. Genzyme. Fachinformation Aubagio®. Juni 2015.
23. Genzyme. Fachinformation Lemtrada® 12 mg Konzentrat zur Herstellung einer Infusionslösung, Dezember 2013.
24. Giacalone PL, Laffargue F, Benos P. Chemotherapy for breast carcinoma during pregnancy: A French national survey. Cancer 1999;86:2266–72.
25. Gold R, Phillips J, Havrdova E, et al. BG-12 (dimethyl fumarate) and pregnancy: preclinical and clinical data from the clinical development program. 65th Annual Meeting of the American Academy of Neurology 16–23 March, 2013; (P02129).
26. Haghikia A, Langer-Gould A, Rellensmann G, et al. Natalizumab use during the third trimester of pregnancy. JAMA Neurol 2014;71:891–5.
27. Hale TW, Siddiqui AA, Baker TE. Transfer of interferon beta-1a into human breastmilk. Breastfeed Med 2012;7:123–5.
28. Hellwig K, Brune N, Haghikia A, et al. Reproductive counselling, treatment and course of pregnancy in 73 German MS patients. Acta Neurol Scand 2008;118:24–8.
29. Hellwig K, Haghikia A, Gold R. Parenthood and immunomodulation in patients with multiple sclerosis. J Neurol 2010;257:580–3.
30. Hellwig K, Haghikia A, Rockhoff M, et al. Multiple sclerosis and pregnancy: experience from a nationwide database in Germany. Ther Adv Neurol Disord 2012;5:247–53.
31. Hellwig K, Rockhoff M, Herbstritt S, et al. Exclusive breastfeeding and the effect on postpartum multiple sclerosis relapses. JAMA Neurol 2015;72:1132–8.
32. Hellwig K, Schimrigk S, Chan A, et al. A newborn with Pierre Robin sequence after preconceptional mitoxantrone exposure of a female with multiple sclerosis. J Neurol Sci 2011;307:164–5.
33. Herbstritt S, Langer-Gould A, Rockhoff M, et al. Glatiramer acetate during early pregnancy – a prospective cohort study. Mult Scler January 11, 2016; doi:10.1177/1352458515623366.
34. Jalkanen A, Alanen A, Airas L. Pregnancy outcome in women with multiple sclerosis: results from a prospective nationwide study in Finland. Mult Scler 2010;16:950–5.
35. Karlsson G, Francis G, Koren G, et al. Pregnancy outcomes in the clinical development program of fingolimod in multiple sclerosis. Neurology 2014;82:674–80.
36. Kieseier B, Benamor M. Pregnancy outcomes from the Teriflunomide Clinical Development Program. Pactrims 2013:P79.
37. Li J, Fox R, Phillips J, et al. Delayed-release dimethyl fumarate and pregnancy: preclinical studies and pregnancy outcomes from clinical trials and pPost-marketing experience. 31st Congress of the European Committee for Treatment and Research in Multiple Sclerosis, 2015: (P608).
38. Lu E, Wang BW, Guimond C, et al. Disease-modifying drugs for multiple sclerosis in pregnancy: a systematic review. Neurology 2012;79:1130–5.
39. Mandal PK, Dolai TK, Bagchi B, et al. B-cell suppression in newborn following treatment of pregnant diffuse large B-cell lymphoma patient with rituximab containing regimen. Indian J Pediatr 2014;81:1092–4.
40. Mibe. Fachinformation Azaimun® 50 mg Tabletten, 2014.
41. Neudorfer O, Sandberg-Wollheim M, Coyle PK, et al. The Branded Glatiramer Acetate Pregnancy Database. 31st Congress of the European Committee for Treatment and Research in Multiple Sclerosis, Barcelona, Spain, October 7–10, 2015:P1507.
42. Ojeda-Uribe M, Afif N, Dahan E, et al. Exposure to abatacept or rituximab in the first trimester of pregnancy in three women with autoimmune diseases. Clin Rheumatol 2013;32:695–700.
43. Pakpoor J, Disanto G, Lacey MV, et al. Breastfeeding and multiple sclerosis relapses: a meta-analysis. J Neurol 2012;259:2246–8.
44. Park-Wyllie L, Mazzotta P, Pastuszak A, et al. Birth defects after maternal exposure to corticosteroids: prospective cohort study and meta-analysis of epidemiological studies. Teratology 2000;62:385–92.
45. Pasto L, Portaccio E, Ghezzi A, et al. Epidural analgesia and cesarean delivery in multiple sclerosis post-partum relapses: the Italian cohort study. BMC Neurol 2012;12:165.
46. Portaccio E, Ghezzi A, Hakiki B, et al. Breastfeeding is not related to postpartum relapses in multiple sclerosis. Neurology 2011;77:145–50.
47. Portaccio E, Ghezzi A, Hakiki B, et al. Postpartum relapses increase the risk of disability progression in multiple sclerosis: the role of disease modifying drugs. J Neurol Neurosurg Psychiatry 2014;85:845–50.
48. Portaccio E. Pregnancy outcomes and disease activity after exposure to natalizumab in patients with multiple sclerosis. ECTRIMS Online Library Portaccio E; 64544. Oct 11, 2014.
49. Roche. Fachinformation MabThera® i.v.
50. Saavedra MA, Sanchez A, Morales S, et al. Azathioprine during pregnancy in systemic lupus erythematosus patients is not associated with poor fetal outcome. Clin Rheumatol 2015;34:1211–6.
51. Schaefer C, Spielmann H, Vetter K, et al. Arzneimittel in Schwangerschaft und Stillzeit. 8., vollständig überarbeitete Auflage. München: Elsevier GmbH, Urban & Fischer Verlag, 2012.
52. TEVA. Fachinformation Mitoxantron TEVA® 2 mg/ml Injektionslösung. May 2014.
53. van der Kop ML, Pearce MS, Dahlgren L, et al. Neonatal and delivery outcomes in women with multiple sclerosis. Ann Neurol 2011;70:41–50.
54. Vukusic S, Hutchinson M, Hours M, et al. Pregnancy and multiple sclerosis (the PRIMS study): clinical predictors of post-partum relapse. Brain 2004;127(Pt 6):1353–60.
55. Weber-Schoendorfer C, Schaefer C. Multiple sclerosis, immunomodulators, and pregnancy outcome: a prospective observational study. Mult Scler 2009;15:1037–42.
Sandra Thiel, Neurologische Klinik, Ruhr Universität Bochum, St. Josef- und St. Elisabeth-Hospital gGmbH, Gudrunstraße 56, 44791 Bochum und Institut für Klinische Pharmazie und Pharmakotherapie, Heinrich-Heine-Universität Düsseldorf, Universitätsstraße 1, 40225 Düsseldorf, E-Mail: Sandra.Herbstritt@uni-duesseldorf.de
Prof. Dr. Ralf Gold, Priv.-Doz. Dr. Kerstin Hellwig, Neurologische Klinik, Ruhr Universität Bochum, St. Josef- und St. Elisabeth-Hospital gGmbH, Gudrunstraße 56, 44791 Bochum
Family planning and multiple sclerosis
Multiple sclerosis (MS) mostly affects young women of reproductive age. Patients and treating physicians are frequently confronted with questions concerning family planning, pregnancy, delivery, and when to stop disease modifying therapies prior to conceiving due to unknown safety of immunomodulatory drug exposure in early pregnancy.
This article aims to answer most of these practically relevant aspects. We will refer to the existing literature, to recently available safety data from the 31st Congress of the European Committee for Treatment and Research in Multiple Sclerosis (ECTRIMS) in October 2015, to our experiences from the German Multiple Sclerosis and Pregnancy Registry and to the guidelines of Network Multiple Sclerosis (Kompetenznetz Multiple Sklerose KKNMS).
Key words: Multiple sclerosis, pregnancy, disease modifying therapies
Psychopharmakotherapie 2016; 23(03)
