Karl Broich, Christine Greiner, Norbert Paeschke und Martin Huber, Bonn
Viele Frauen mit psychiatrischen Erkrankungen haben unabhängig von ihrer Erkrankung einen Kinderwunsch, und neuauftretende oder sich verschlechternde psychische Störungen während einer Schwangerschaft sind nicht selten. Der behandelnde Arzt sieht sich in diesen Situationen besonderen Herausforderungen gegenüber, da der Einsatz jeglicher Medikation während der Schwangerschaft nicht nur in der Öffentlichkeit, sondern auch unter Fachleuten umstritten ist; die Erfahrungen mit Thalidomid haben sich hier tief ins Bewusstsein gegraben. Trotzdem bedarf es hier einer sorgfältigen Abwägung zwischen den möglichen Risiken einer medikamentösen Therapie, beispielsweise mit Antidepressiva, und den potenziellen Risiken einer zum Beispiel unzureichend behandelten Depression und deren Auswirkungen auf Mutter und Kind [12, 36, 42]. So gelten Fehl- und Frühgeburten, angeborene Fehlbildungen, kardiale Fehlbildungen, neonatale Anpassungsstörungen, persistierende pulmonale Hypertension und längerfristige neurokognitive Entwicklungsstörungen oder Erkrankungen des Autismus-Spektrums als mögliche Folgen einer Therapie mit Antidepressiva während der Schwangerschaft, die Datenlage ist dazu aber sehr widersprüchlich. Auf der anderen Seite ist die Schwangerschaft durch eine unbehandelte schwere depressive Symptomatik ebenfalls gefährdet: Vorsorgetermine werden nicht wahrgenommen, Appetitmangel führt zu Ernährungsstörungen, erhöhter Substanzgebrauch von Nicotin und Alkohol ist beschrieben, und suizidale Verhaltensweisen können auftreten mit teilweise langfristigen Auswirkungen auf das Wohlergehen von Mutter und Kind selbst, aber auch hinsichtlich des persönlichen Umfelds. So wird eine bestehende Depression auch als Risikofaktor für das Auftreten von Präeklampsie, Frühgeburten und langfristigen Entwicklungsstörungen des Neugeborenen diskutiert [32, 33, 48]. In vielen Fällen ist daher im Interesse der Sicherheit der Mutter und des Kindes beziehungsweise im Hinblick auf eine Sicherstellung der Versorgung des Neugeborenen nach der Geburt eine ganzheitliche Behandlung durch erfahrene Zentren erforderlich [11, 12].
Im klinischen Alltag bestehen für die aktuelle Fragestellung in der Regel vier verschiedene Szenarien [mod. nach 26]:
- Frauen in Remission unter antidepressiver Medikation mit Kinderwunsch
- Frauen in Remission unter antidepressiver Medikation, die schwanger werden
- Schwangere Frauen, die erstmalig eine depressive Erkrankung entwickeln
- Schwangere Frauen mit einem Wiederauftreten/Rückfall der depressiven Erkrankung
Dabei wird in der Literatur und von erfahrenen Zentren immer wieder darauf hingewiesen, dass bei der Diskussion und Abwägung der Optionen die Risiken der Nichtbehandlung einer depressiven Episode während der Schwangerschaft unterschätzt und die Risiken einer medikamentösen Therapie überschätzt werden, und zwar von Betroffenen wie von Therapeuten [42]. In einem aktuellen multinationalen Survey bestätigten Petersen et al., dass Frauen vor allem auch gegenüber Antidepressiva größere Vorbehalte haben und Risiken für das Kind sehen [46]. Vor dem Hintergrund dieser möglichen Konstellationen sollten alle Frauen im gebärfähigen Alter mit schweren psychischen Störungen Zugang zu entsprechenden Beratungsmöglichkeiten haben; hierbei ist insbesondere das individuelle Risiko eines Rückfalls oder eines Wiederauftretens der Erkrankung zu berücksichtigen [12, 32]. Ein abruptes Absetzen einer bestehenden und wirksamen antidepressiven Therapie bei Eintritt einer Schwangerschaft ist nicht nötig und sollte aufgrund des damit verbundenen Rückfallrisikos vermieden werden. In jedem einzelnen Fall muss aber schlussendlich eine individuelle Abwägung gegenüber den möglichen Risiken für das ungeborene Kind durch die Anwendung des Arzneimittels erfolgen [26, 50].
Antidepressiva in der Schwangerschaft – regulatorische Aspekte
Antidepressiva sind eine sehr heterogene Gruppe von Arzneimitteln, die bei depressiven Syndromen einen stimmungsaufhellenden und antriebsverbessernden Therapieeffekt aufweisen. Die frühere Einteilung bezog sich vorwiegend auf die chemische Struktur (trizyklisch, tetrazyklisch, chemisch neuartig), während die neueren Antidepressiva vorwiegend nach ihrem primären Angriffspunkt in zentralnervösen Neurotransmittersystemen eingeteilt werden. Im Folgenden wurde die Einteilung nach Roter Liste mit den entsprechenden Texten in Fach- und Gebrauchsinformation berücksichtigt:
- Monoaminoxidase-Hemmer (synonym: MAO-Hemmer)
- Selektive Serotonin-Wiederaufnahmehemmer (SSRI)
- Selektive Serotonin-/Noradrenalin-Wiederaufnahmehemmer (SNRI)
- Noradrenerge und spezifisch serotonerge Antidepressiva (NaSSA)
- Trizyklische Antidepressiva
- Tetrazyklische Antidepressiva
- Andere
In Deutschland existiert derzeit kein einziges Antidepressivum, welches explizit für die Anwendung während der Schwangerschaft zugelassen ist. Lediglich der Originator von Fluoxetin erkennt im Abschnitt 4.6 der Fachinformation an, dass eine Gabe in der Schwangerschaft möglich ist. Zwei der zugelassenen antidepressiven Wirkstoffe sind in der Schwangerschaft kontraindiziert (Trimipramin und Johanniskraut [nur beim Originator]). In vielen Fällen ist vor Einsatz des entsprechenden Antidepressivums eine individuelle Abwägung von erwartetem Nutzen und potenziellen Risiken notwendig.
Für die vorliegende Arbeit wurde jeweils der Abschnitt 4.6 Fertilität, Schwangerschaft und Stillzeit der Fachinformation für die in Deutschland verkehrsfähig zugelassenen Antidepressiva (basierend auf der jeweiligen Originatorzulassung, soweit verfügbar) hinsichtlich der Aussagen zu einer Anwendung in der Schwangerschaft ausgewertet:
- Trimipramin (Stangyl®): Eine Schwangerschaft stellt eine absolute Kontraindikation dar. Auch ist die Anwendung von Johanniskraut (Jarsin®) in der Schwangerschaft kontraindiziert, allerdings ist diese absolute Kontraindikation für das Originalpräparat (nicht bei Generikapräparaten) eher historisch zu verstehen.
- Tianeptin (Tianeurax®), Bupropion (Zyban®): sollte in der Schwangerschaft nicht angewendet werden.
- Agomelatin (Valdoxan®): Eine Anwendung in der Schwangerschaft sollte vermieden werden.
- Tranylcypromin (Jatrosom®): soll im ersten Trimenon nicht angewendet werden (im zweiten und dritten Trimenon nur bei zwingender Indikation).
Für die anderen, oben nicht einzeln aufgeführten Antidepressiva ist die Anwendung in der Schwangerschaft gemäß Fachinformation nicht explizit ausgeschlossen. Der Abschnitt 4.6 enthält hier Empfehlungen wie beispielsweise:
- „Bei der Anwendung in der Schwangerschaft ist Vorsicht geboten.“
- „Sollte in der Schwangerschaft nicht angewendet werden, es sei denn bei eindeutiger Notwendigkeit und nach sorgfältiger Nutzen-Risiko-Abwägung.“
- „Sollte in der Schwangerschaft nur bei zwingender Indikation angewendet werden.“
- „Darf nur bei zwingender Notwendigkeit und nach strenger Nutzen-Risiko-Abwägung angewandt werden.“
- „Einnahme während der Schwangerschaft wird nicht empfohlen, es sei denn, der klinische Zustand der Patientin lässt einen Nutzen der Behandlung erwarten, der das potenzielle Risiko übertrifft.“
- „Darf bei schwangeren Frauen nur angewendet werden, wenn der zu erwartende Nutzen die möglichen Risiken überwiegt“
- „Darf während der Schwangerschaft nur eingenommen werden, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus rechtfertigt.“
- „Darf während der Schwangerschaft nicht angewendet werden, es sei denn, dass eine Behandlung aufgrund des klinischen Zustands der Frau erforderlich ist.“
- „Sollte während der Schwangerschaft, insbesondere im ersten sowie im letzten Trimenon nicht angewendet werden, es sei denn, dies ist dringend erforderlich.“
- „Ist die Anwendung während der Schwangerschaft zu vermeiden und nur dann in Betracht zu ziehen, wenn der erwartete Nutzen das potenzielle Risiko für den Föten rechtfertigt.“
Im Abschnitt 4.6 der Fachinformation werden also die für die jeweilige Substanz verfügbaren Daten aus Humanstudien sowie tierexperimentellen Untersuchungen wiedergegeben. Vielfach ist die Datenlage jedoch begrenzt und es liegen nur limitierte Erfahrungen mit der Anwendung des Arzneimittels bei Schwangeren vor. Dies bedingt, dass von den Zulassungsinhabern – auch vor dem Hintergrund haftungsrechtlicher Aspekte – nur eingeschränkte Empfehlungen zum Einsatz in der Schwangerschaft gemacht werden. Die Angaben in den Fachinformationen spiegeln die generelle Schwierigkeit beziehungsweise das Dilemma der Thematik wider: Aus ethischen Gründen existieren für die meisten Arzneimittel und so auch Antidepressiva keine kontrollierten randomisierten Studien im Hinblick auf die Anwendung bei Schwangeren, im Gegenteil, in der Regel gelten eine potenzielle Schwangerschaft und nicht ausreichende Kontrazeption als Ausschlusskriterium für die allermeisten klinischen Prüfungen. Zwar empfiehlt vor diesem Hintergrund das Council for International Organizations of Medical Sciences (CIOMS) im Rahmen seiner International Ethical Guidelines for Biomedical Research Involving Human Subjects in Guideline 17 schon länger, dass auch schwangere Frauen prinzipiell für biomedizinische Forschung infrage kommen sollen – solange diese für die spezifischen Gesundheitsbedürfnisse einer Schwangeren und ihres Fetus beziehungsweise für schwangere Frauen insgesamt Relevanz hat [9]; der Bedarf randomisierter klinischer Studien zur Wirksamkeit und Sicherheit von Antidepressiva bei Schwangeren wurde jüngst auch noch einmal wiederholt [43]. Aus regulatorischer Sicht wäre eine verbesserte Datenlage sicher wünschenswert, eine Änderung der Praxis in klinischen Prüfungen mit schwangeren Patientinnen ist hier aber nicht zu erwarten. Diesbezügliche Erkenntnisse stützen sich daher im Wesentlichen auf einzelne Fallberichte, Fallserien oder Kohortenstudien, die jedoch alle bezüglich ihrer Aussagekraft mit Einschränkungen behaftet sind [6, 14, 27, 56]. Aus diesem Grund fördert das BfArM – gemeinsam mit dem Land Berlin – das Pharmakovigilanz- und Beratungszentrum für Embryonaltoxikologie Embryotox (www.embryotox.de), das zum Institut für Klinische Pharmakologie und Toxikologie der Charité – Universitätsmedizin Berlin gehört. Das Zentrum arbeitet unabhängig von der pharmazeutischen Industrie und initiierte verschiedene internationale Kooperations- und Forschungsprojekte. Es zählt inzwischen zu den führenden Referenzzentren mit internationalem Ruf für Arzneimittelsicherheit in der Schwangerschaft [53, 54]. Fast ein Fünftel aller Anfragen an das Zentrum entfällt auf die Therapie mit Psychopharmaka, was diese nicht nur zu der am häufigsten angefragten Arzneimittelgruppe gemacht hat, sondern auch deren besondere Bedeutung in der Schwangerschaft unterstreicht. Für die Gruppe der Antidepressiva überblickt das Zentrum viele tausend Schwangerschaften und gibt daher auch konkrete Empfehlungen zu deren Einsatz [50, 52].
Untersuchungen zur Anwendungshäufigkeit
Episoden einer Depression vor, während und nach einer Schwangerschaft sind nicht selten. So wurden Raten einer Depression zwischen 7,4 und 11% für das erste Trimenon beschrieben, im zweiten Trimenon lagen die Raten zwischen 8,9 und 12,8% und im letzten Trimenon zwischen 8,5 und 12% [48]. Die Prävalenz über die gesamte Schwangerschaft betrug in einer Studie 18,4% gegenüber nur 7 bis 9% in der Gesamtbevölkerung [17]. Wenn Frauen in Remission wegen einer geplanten Schwangerschaft ihre Medikation absetzten, erlitten in einer Studie 68% von ihnen einen Rückfall, ganz überwiegend schon in den ersten Monaten der Schwangerschaft [7]. Roca et al. berichteten, dass 57% der Frauen mit ungeplanten Schwangerschaften nach Absetzen schon im ersten Trimenon wieder mit Antidepressiva beginnen mussten [49]. Auf Antidepressiva kann daher im klinischen Alltag auch in der Schwangerschaft nicht verzichtet werden. Ganz im Vordergrund stehen dabei heute die SSRI (in Europa vorwiegend Citalopram/Escitalopram, in den USA vorwiegend Sertralin), die bis zu 80% der Verordnungen ausmachen.
Auswertungen an größeren Populationen zur Anwendungshäufigkeit von Antidepressiva liegen aus Europa (am Beispiel Großbritannien) sowie den USA vor. Eine Studie basierend auf Daten aus Großbritannien (Clinical Practice Research Datalink [CPRD]’s Mother-Baby Link; 421645 Schwangerschaften wurden erfasst) für den Zeitraum 1989 bis 2010 konnte eine Abnahme der Verschreibungen von Antidepressiva nach dem Beginn der Schwangerschaft zeigen [38]. Dabei betrug die Prävalenz von Antidepressiva-Verordnungen vor der Schwangerschaft 4,7%, um dann auf 2,8% im ersten Trimenon und auf 1,3% im zweiten und dritten Trimenon abzufallen, nach der Entbindung aber wieder auf 5,5% deutlich anzusteigen. Dieser U-förmige Trend bezüglich der Verordnungshäufigkeit zeigte sich für SSRI, Trizyklika und andere Antidepressiva; die relative Verteilung ist in Abbildung 1 dargestellt.
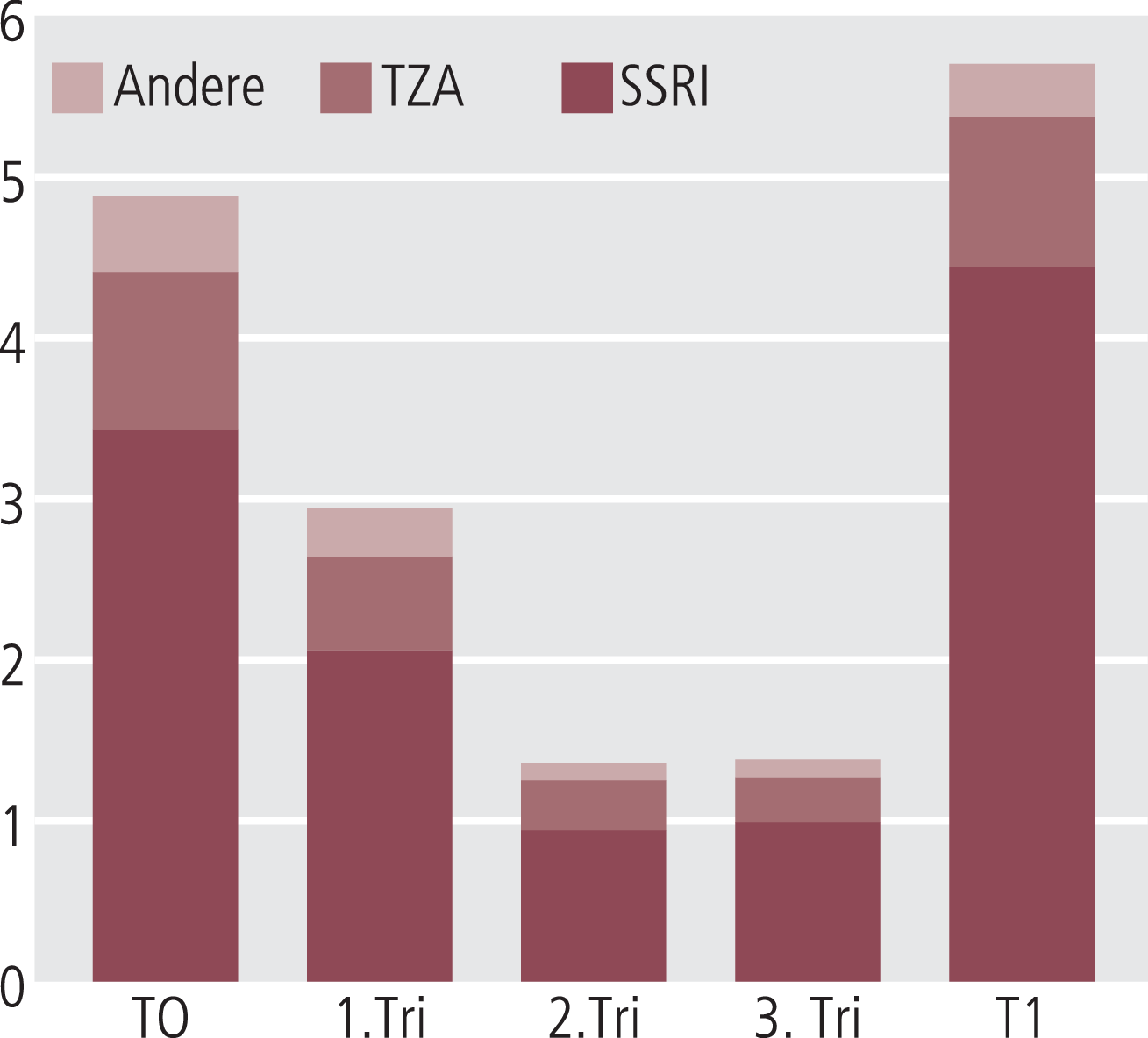
Abb. 1. Daten zum Antidepressiva-Einsatz während der Schwangerschaft in Großbritannien im Zeitraum von 1989 bis 2010. T0 umfasst die 3 Monate vor der Schwangerschaft, 1. Tri bis 3. Tri die jeweiligen Trimester während der Schwangerschaft und T1 die ersten 3 Monate nach der Entbindung [mod. nach 38]
Von den Frauen mit Antidepressiva-Verordnungen in den drei Monaten vor der Schwangerschaft beendeten 79,6% die Behandlung, weitere 5,1% vereinfachten die Medikation vorwiegend im Sinne einer Dosisreduktion im dritten Trimenon. Nur 9,1% der Frauen führten ihre Therapie unverändert über die Schwangerschaft fort, 4% der Frauen stiegen auf andere Antidepressiva um, bei 2% musste die Behandlung intensiviert werden. 0,4% der Nichtanwenderinnen in den drei Monaten vor der Schwangerschaft begannen erstmals mit Antidepressiva im dritten Trimenon [38].
Auch eine weitere Studie aus Großbritannien – durchgeführt mit der Datenbank THIN (The Health Improvement Network; 114999 Schwangerschaften wurden erfasst) unter Berücksichtigung des Zeitraumes 1992 bis 2006 – ergab, dass Antidepressiva in einem hohen Prozentsatz in der Schwangerschaft abgesetzt werden, über 90% der Frauen hatten im dritten Trimenon ihre antidepressive Therapie beendet [45]. Für die skandinavischen Länder wurde eine niedrigere Verordnungsrate von Antidepressiva beschrieben, die bei 1 bis 2% lag und in der Tendenz im Gegensatz zu anderen Studien auch eher fortgeführt wurde [34].
Ähnliche Zahlen liegen aus den USA vor, die Verordnungszahlen liegen im Trend aber höher [2, 43]. Huybrechts et al. werteten eine große Kohorte schwangerer Frauen anhand von Medicaid-Daten aus 47 Staaten aus den Jahren 2000 bis 2007 aus und erfassten dabei mehr als 1,1 Millionen Schwangerschaften. Insgesamt nahmen 8,1% der Frauen zu irgendeinem Zeitpunkt ihrer Schwangerschaft Antidepressiva ein. Von den 5,3% Frauen, die vor Beginn der Schwangerschaft Antidepressiva genommen hatten, führten aber nur noch 17% der Frauen diese nach 180 Tagen fort. In einer weiteren Medicaid-Auswertung wurde beschrieben, dass Schwangere im ersten Trimenon in 10% Antidepressiva verordnet worden waren, 72% davon waren SSRI [8], aber auch hier führten nur 25% der schwangeren Frauen die medikamentöse Behandlung fort.
Aktuelle Empfehlungen zu Antidepressiva in der Schwangerschaft
Auch wenn wir den Fokus auf die regulatorischen Aspekte legen und diese Übersicht nicht als klinischen Leitfaden für die Behandlung von schwangeren Frauen mit Depression verstanden wissen wollen, so sollen doch der Vollständigkeit halber aktuelle Übersichten und Leitlinien kurz dargestellt werden. Dabei beschränken wir uns auf aktuelle Publikationen und Metaanalysen aus jüngerer Zeit.
Auch wenn an der Wirksamkeit von Antidepressiva wegen des Mangels an kontrollierten klinischen Prüfungen aus methodischen Gründen Zweifel angemeldet werden [47, 55, 57], so sprechen die Daten aus vielen Observationsstudien in ihrer Gesamtheit doch für eine Wirksamkeit der Antidepressiva auch bei schwangeren Frauen, und für Trizyklika und vor allem SSRI liegen umfangreiche Erfahrungen vor [18, 20, 43, 48, 50]. In den aktuellen Leitlinien der Fachgesellschaften zur Behandlung der unipolaren Depression [12]und bipolarer Störungen [10] wird die Thematik aufgenommen und es finden sich Empfehlungen zur medikamentösen Behandlung während der Schwangerschaft, die vom Evidenzgrad als klinische Konsenspunkte (KKP, entspricht Expertenkonsens) markiert sind. Zur unipolaren Depression werden dort folgende Empfehlungen gegeben [11]:
- Bei einer geplanten Schwangerschaft und vorbestehender rezidivierender Depression ist eine sorgfältige Nutzen-Risiko-Abwägung vorzunehmen. Bei hohem individuellem Rezidivrisiko ist – in Abwägung der Auswirkung einer erneuten Erkrankung – eine niedrig dosierte Monotherapie auch während der Schwangerschaft sinnvoll. Eine ungeplante Schwangerschaft wird üblicherweise in der siebten, achten oder noch späteren Schwangerschaftswoche festgestellt, nachdem die wesentlichen Schritte in der embryonalen Entwicklung bereits abgeschlossen sind. Durch das Absetzen wird der Einfluss der Medikation auf die Organentwicklung nicht mehr verhindert, aber mit hoher Wahrscheinlichkeit eine Destabilisierung des psychischen Zustands ausgelöst, sodass ebenfalls eine niedrig dosierte Monotherapie fortgeführt werden kann.
- Die Auswahl des Medikaments vor einer geplanten Schwangerschaft oder während der Schwangerschaft richtet sich vor allem danach, inwieweit die Substanz teratogen und daher für das Kind nachteilig sein könnte. Für Trizyklika wurden bisher keine Zusammenhänge zwischen einer pränatalen Gabe und Geburtsdefekten beim Kind gefunden, vereinzelt jedoch kurzzeitig nach der Geburt bestehende Verhaltenssymptome wie Unruhe und Hypererregbarkeit. Beim Einsatz von tri- und tetrazyklischen Substanzen ist jedoch deren anticholinerge und hypotensive Nebenwirkung relevant. Auch für SSRI werden im Allgemeinen keine teratogenen Wirkungen gefunden.
- Allerdings zeigen zwei Studien nach einer Gabe von Paroxetin im ersten Trimester der Schwangerschaft einerseits überzufällig häufig kardiovaskuläre bzw. rechtsventrikuläre Defekte. Demgegenüber fand eine weitere Studie diese Zusammenhänge bei Gabe von Paroxetin nicht. In einer Metaanalyse wird Paroxetin, das im ersten Trimester eingenommen wird, ebenfalls mit kardialen Missbildungen in Verbindung gebracht, während dies in einer anderen Metaanalyse nicht gezeigt werden konnte.
- Die Gabe von SSRI im dritten Trimester scheint zudem mit einem dreifach erhöhten Risiko für neonatale Verhaltenssyndrome wie Atemnot, Irritabilität und Problemen bei der Nahrungsaufnahme verbunden zu sein, wobei diese im Allgemeinen mäßig ausgeprägt und selbstlimitierend sind und vor allem mit Paroxetin assoziiert scheinen.
- Auf beschränkter Studienbasis gibt es für Mirtazapin, Bupropion und Venlafaxin keine Hinweise auf teratogene Wirkung, während Duloxetin bislang kaum untersucht ist.
- Die Geburt bei antidepressiv medizierten Frauen sollte möglichst in einer Geburtsklinik mit angeschlossener Neonatologie stattfinden, sodass beim Auftreten von Absetzeffekten und Nebenwirkungen der Medikation beim Kind jederzeit eine intensive Überwachung möglich ist.
Nach einer grundsätzlichen Diskussion des Für und Wider einer medikamentösen Behandlung werden für die Behandlung der bipolaren Depression die folgenden Konsensempfehlungen gegeben [10]:
- SSRI sollten zu einer Akutbehandlung einer bipolaren Depression bei Schwangeren und Stillenden erwogen werden. In der Literatur wird ein teratogenes Risiko für die beiden Substanzen Paroxetin und Fluoxetin diskutiert. Deshalb sollen diese beiden Substanzen in der Schwangerschaft nicht neu verordnet werden. Ist eine Einstellung schon vor Eintreten der Schwangerschaft erfolgt, kann die Umstellung auf ein anderes SSRI erwogen werden. Für die Substanzen Sertralin und Citalopram liegt die beste Datenlage in Schwangerschaft und Stillzeit vor, sodass der Einsatz dieser Substanzen am ehesten in der Akutbehandlung empfohlen werden kann.
- SNRI können zu einer Akutbehandlung einer bipolaren Depression bei Schwangeren und Stillenden erwogen werden. Eine spezifische Teratogenität von SNRI ist nicht bekannt. Jedoch ist einschränkend zu bedenken, dass die Datenlage für diese Substanzen sehr gering ist. Das erhöhte Switch-Risiko ist zu bedenken.
- Trizyklische Antidepressiva können zu einer Akutbehandlung einer bipolaren Depression bei Schwangeren und Stillenden erwogen werden. Eine spezifische Teratogenität trizyklischer AD ist nicht bekannt. Bei der Verordnung sollen unerwünschte Wirkungen für die Mutter bedacht werden. Die Möglichkeit der Verabreichung nebenwirkungsärmerer Substanzen, wie beispielsweise SSRI sollte erwogen werden. Das erhöhte Switch-Risiko ist zu bedenken.
- Bupropion kann zu einer Akutbehandlung einer bipolaren Depression bei Schwangeren und Stillenden erwogen werden. Eine spezifische Teratogenität von Bupropion ist nicht bekannt. Jedoch ist einschränkend zu bedenken, dass die Datenlage für diese Substanz gering ist.
Die Aktualisierung der internationalen Guideline der World Federation of Societies of Biological Psychiatry (WFSBP) zur Behandlung der unipolaren Depressionen kommt im Kapitel Schwangerschaft und Stillzeit zu ähnlichen Empfehlungen zu Antidepressiva während der Schwangerschaft [4]:
- Aufgrund der vorliegenden Erfahrungen werden Citalopram und Sertralin empfohlen, für SNRI wird die Datenlage als limitiert und MAO-Hemmer als kontraindiziert angesehen.
- Falls möglich und klinisch gerechtfertigt, sollte die Einleitung einer Behandlung wegen des höchsten Missbildungsrisikos im ersten Trimenon auf das zweite oder dritte Trimenon verschoben werden. Falls eine Behandlung im ersten Trimenon klinisch notwendig ist, muss diese einer klaren Nutzen-Risiko-Analyse folgen, dafür sollten aber auch psychotherapeutische Ansätze und eine Elektrokonvulsionstherapie als Alternative in Betracht gezogen werden.
Basierend auf einer Spezialambulanz für schwangere Frauen und den vielen Daten des Embryotox-Beratungszentrums fassen Rohde und Schäfer [50] ihre Erfahrungen so zusammen, dass die Behandlung von Patientinnen mit unipolarer Depression in der Vorgeschichte mit Antidepressiva eher unproblematisch ist, wenn einige wichtige Grundprinzipien berücksichtigt werden (siehe Kasten).
Empfehlungen nach Rohde und Schäfer unter Berücksichtigung der Daten von Embryotox [50, 52], www.embryotox.de
- Mittel der Wahl bei pharmakologisch therapiebedürftiger Depression in der Schwangerschaft: SSRI (Citalopram, Sertralin), Trizyklika (Amitriptylin, Nortriptylin)
- Nicht empfohlen sind: Moclobemid, Tranylcypromin
- Antidepressiva der 2. Wahl in der Schwangerschaft sind: Mirtazapin, Venlafaxin, Duloxetin
- Empfehlung des Beibehalts einer stabilen antidepressiven Therapie bei bereits erfolgter Einstellung bei fast allen Antidepressiva mit folgenden Ausnahmen: Fluoxetin und Paroxetin (Beibehalt nur bei schwieriger Einstellung)
- Bei allen bis zur Geburt eingenommenen Antidepressiva muss mit einem neonatalen Adaptationssyndrom gerechnet werden, das bei den SSRI auch als serotonerge Überstimulation interpretiert wird. Hierzu gehört eventuell der seltene pulmonale Hochdruck des Neugeborenen.
- Auch wenn die neonatalen Adaptationsstörungen üblicherweise auf wenige Tage begrenzt sind und selbstlimitierend verlaufen, sollte in den ersten Tagen nach der Geburt die Beobachtung gewährleistet sein, am besten durch Entbindung in einem Perinatalzentrum.
- Soweit klinisch vertretbar, kann mit der Schwangeren eine Reduktion oder auch das vorübergehende Absetzen des Antidepressivums vor der Entbindung vereinbart werden; das erforderliche Zeitintervall richtet sich dabei nach der Halbwertszeit des Antidepressivums.
Sie betonen, dass „eine unter Therapie stabile Patientin, die eine antidepressive Therapie tatsächlich braucht, selbst wenn ihr Antidepressivum nicht zu den hier empfohlenen gehört, während der Schwangerschaft die Therapie unverändert fortsetzen soll, um keine für Mutter und Kind bedrohlichen Krisen zu provozieren. Dies gilt insbesondere dann, wenn sich eine medikamentöse Einstellung als schwierig erwiesen hat („never change a winning team“).
Wie an den Empfehlungen ablesbar, ist neben der Wirksamkeit der Antidepressiva für die individuelle Therapieentscheidung auch das Profil potenzieller Nebenwirkungen von entscheidender Bedeutung. Hierbei sollen im Folgenden noch einmal die aktuellen Diskussionsstände zu möglichen teratogenen, perinatalen und postnatalen Entwicklungsstörungen dargelegt werden.
Spontane Aborte und Frühgeburten
In einer systematischen Übersicht von 735 Publikationen und einer Metaanalyse über 23 Studien ergab sich kein statistisch signifikant erhöhtes Risiko für spontane Aborte [51]. Eine große Kohortenstudie aus Dänemark bei schwangeren Frauen und Einnahme von SSRI zeigte ein Hazard-Ratio (HR) von 1,27 (95%-Konfidenzintervall [KI]: 1,22–1,33) gegenüber unbehandelten Schwangeren. Allerdings war dieses in der gleichen Größenordnung wie das Hazard-Ratio (1,24; 95%-KI: 1,18–1,30) bei Schwangeren, die ihre SSRI bis zu einem Jahr vorher abgesetzt hatten [1]. Eine weitere Kohortenstudie aus Dänemark zeigte eine Rate von Spontanaborten von 12% für Patientinnen mit Antidepressiva gegenüber unbehandelten Schwangeren (HR 1,14; 95%-KI: 1,10–1,18), allerdings verlor sich der Effekt gegenüber unbehandelten depressiven Patientinnen [35]. Beide Gruppen gehen davon aus, dass das erhöhte Risiko nicht auf die Antidepressiva zurückgeht, sondern eher mit depressiven Verhaltensweisen beziehungsweise der Erkrankung selbst zusammenhängt. In dieser Studie wurde allerdings ein möglicherweise erhöhtes Risiko für Aborte unter Therapie mit SNRI bei Patientinnen berichtet, bei denen die Diagnose der Depression in einem Behandlungsregister gestellt worden war, nicht aber unter SSRI oder Trizyklika (Abb. 2). Da aber nicht alle möglichen Kofaktoren erhoben werden konnten, sind diese Daten vorläufig und müssen in weiteren Studien überprüft werden.
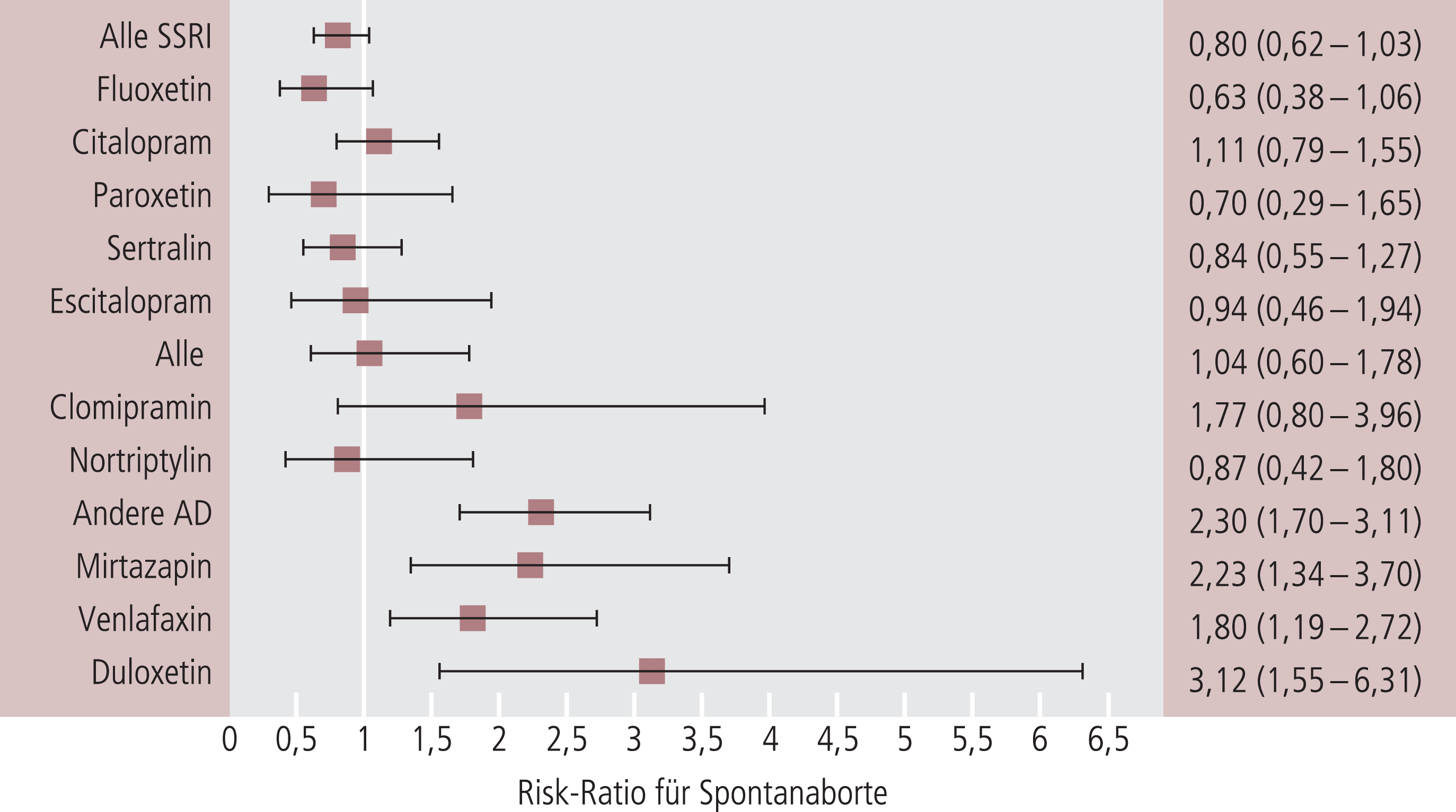
Abb. 2. Nichtadjustierte Risk-Ratios für spontane Aborte nach Exposition mit verschiedenen Antidepressiva bei Frauen mit nachgewiesener Depression [mod. nach 35]. AD: Antidepressiva; SSRI: selektive Serotonin-Wiederaufnahmehemmer
Kongenitale Malformationen/ Kardiale Malformationen
Das Risiko für relevante kongenitale Malformationen liegt für Neugeborene in der Normalbevölkerung zwischen 1 und 3%. Demgegenüber wurden in früheren Studien bei Neugeborenen für Paroxetin und Fluoxetin leicht erhöhte Raten für kardiale Malformationen berichtet, was zur Aufnahme der folgenden Textpassagen in den Abschnitt 4.6 der Fachinformation für diese beiden Substanzen führte: „Einige epidemiologische Studien deuten auf ein erhöhtes Risiko für angeborene Fehlbildungen, insbesondere kardiovaskulärer Art (z.B. Ventrikelseptumdefekte und Vorhofseptumdefekte), im Zusammenhang mit der Anwendung von … im ersten Schwangerschaftsdrittel hin. Der zugrunde liegende Mechanismus ist unbekannt. Die Daten legen nahe, dass das Risiko für einen kardiovaskulären Defekt beim Neugeborenen nach …-Exposition der Mutter geringer als 2/100 ist im Vergleich zu einer zu erwartenden Häufigkeit von solchen Defekten von ungefähr 1/100 in der Gesamtpopulation.“
Aktuelle systematische Übersichten, Metaanalysen und Kohortenstudien zeigen, dass unter Behandlung mit Antidepressiva die Ergebnisse zwar nicht ganz einheitlich sind und einzelne Studien auch ein leicht erhöhtes Risiko (bei Paroxetin und Fluoxetin) für kardiale Malformationen erbrachten, dass dieses aber nicht als wirklich klinisch relevant angesehen wird und auch auf nicht ausreichend erfassten Kofaktoren beruhen könnte [3, 19, 22, 31]. Eine aktuelle und methodisch sehr gute Kohortenstudie aus den skandinavischen Ländern, in der zwischen 1996 und 2010 36772 Neugeborene erfasst wurden, deren Mütter während der Schwangerschaft SSRI oder Venlafaxin erhalten hatten, zeigte ebenfalls keine erhöhte Rate an Malformationen und schätzt des teratogene Risiko dieser Antidepressiva daher zusammenfassend eher gering ein [16].
Neonatales Anpassungssyndrom
Das neonatale Adaptationssyndrom zeigt sich klinisch mit den möglichen Symptomen erhöhter Muskeltonus, Tremor, Atemstörungen mit Zyanose, Hyperreflexie, Unruhe und Schlafstörungen sowie Trinkstörungen bei bis zu 30% der Neugeborenen, wenn die Mütter auch in den letzten Wochen vor der Entbindung Antidepressiva eingenommen haben, vorwiegend nach SSRI und SNRI. In einer aktuellen Metaanalyse berichteten Grigoriadis et al. [21], dass das Risiko für Neugeborene bei Exposition mit Antidepressiva um das Fünffache erhöht war (HR: 5,07; 95%-KI: 3,25–7,90). Allerdings sind die Symptome in der Regel mild und bilden sich innerhalb von zwei Wochen nach der Entbindung spontan zurück. Die Ursache des Syndroms ist nicht sicher geklärt, diskutiert wird eine serotonerge Überstimulation oder aber auch eine Entzugsproblematik. Die folgenden Texte sind daher in der Fachinformation von SSRI und SNRI aufgenommen: „Folgende Symptome können beim Neugeborenen auftreten, wenn die Mutter in späteren Stadien der Schwangerschaft mit SSRIs/SNRIs behandelt wurde: Atemnot, Zyanose, Apnoe, Krampfanfälle, Instabilität der Körpertemperatur, Schwierigkeiten beim Füttern, Erbrechen, Hypoglykämie, Hypertonie, Hypotonie, Hyperreflexie, Tremor, Überspanntheit, Reizbarkeit, Lethargie, anhaltendes Weinen, Somnolenz und Schlafstörungen. Diese Symptome könnten sowohl auf serotonerge Wirkungen als auch auf Entzugssymptome zurückzuführen sein. In den meisten Fällen setzen die Komplikationen unmittelbar oder bald (<24 Stunden) nach der Geburt ein.“ Eine aktuelle Studie fand keinen Zusammenhang zwischen dem Ausmaß der Plazenta-Passage von Antidepressiva und dem Auftreten eines postnatalen Adaptationssyndroms [15].
Persistierende pulmonale Hypertension des Neugeborenen
Eine weitere Nebenwirkung, die auch zu regulatorischen Maßnahmen geführt hat, ist die in seltenen Fällen auftretende persistierende pulmonale Hypertension (PPH). Sie tritt bei 0,19% der Neugeborenen auf und wird mit einer Therapie mit Antidepressiva in späteren Stadien der Schwangerschaft in Zusammenhang gebracht. Allerdings sind auch hier die Befunde widersprüchlich und weitere Risikofaktoren wie kongenitale Malformationen, mütterliches Übergewicht oder Sektio-Entbindung wurden assoziiert [23, 41]. Eine Kohortenstudie aus Skandinavien zeigte ein 2-fach erhöhtes Risiko nach Therapie mit verschiedenen SSRI (HR: 2,1; 95%-KI: 1,5–3,0) und die Autoren gehen von einem Klasseneffekt aus. Da aber auch die Mortalität des Syndroms zwischen 10 und 20% liegt, reagierten Zulassungsbehörden im Jahr 2006 und beauflagten die folgenden Texte für die Fachinformation von SSRI und SNRI, hier am Beispiel Venlafaxin: „Daten aus epidemiologischen Studien deuten darauf hin, dass die Anwendung von selektiven Serotonin-Wiederaufnahme-Inhibitoren (SSRI) in der Schwangerschaft, insbesondere im späten Stadium einer Schwangerschaft, das Risiko für das Auftreten einer primären pulmonalen Hypertonie bei Neugeborenen (PPHN, auch persistierende pulmonale Hypertonie genannt) erhöhen kann. Obwohl es keine Studien gibt, die einen Zusammenhang zwischen der Behandlung mit SNRI und dem Auftreten von PPHN untersucht haben, kann dieses potenzielle Risiko für Venlafaxin nicht ausgeschlossen werden, wenn man den zugehörigen Wirkungsmechanismus (Inhibition der Wiederaufnahme von Serotonin) berücksichtigt.“
Huybrechts et al. berichteten nun jüngst Ergebnisse einer sehr großen Kohortenstudie mit Medicaid-Daten (128950 Patientinnen mit Antidepressiva in Spätstadien der Schwangerschaft aus den Jahren 2000 bis 2010) aus 46 US-Bundesstaaten. Auch hier fand sich ein leicht erhöhtes Risiko für das Auftreten einer PPH, aber niedriger als in früheren Studien (HR für SSRI: 1,28; 95%-KI 1,01–1,64) [30]. Dazu passen die regulatorischen Aussagen der FDA, dass wegen des geringen Risikos einer PPH unter Antidepressiva die Therapie mit SSRI oder SNRI auch in späteren Stadien der Schwangerschaft nicht abgesetzt werden soll, wenn sie klinisch erforderlich ist.
Neurokognitive Entwicklungsstörungen
Aussagen hierzu sind sehr widersprüchlich, einige Berichte weisen zwar auf kindliche Entwicklungsverzögerungen sowohl nach der Geburt wie auch in den ersten Lebensjahren hin, wenn Antidepressiva in der Schwangerschaft eingenommen wurden. Allerdings wurde dies auch für Kinder unbehandelter depressiver Patientinnen berichtet [13, 24, 28]. So berichteten Pedersen et al., dass in ihrer Studie die unbehandelte Depression der Mütter mit emotionalen und Verhaltensauffälligkeiten bei 4- bis 5-jährigen Kindern assoziiert war, nicht etwa die Behandlung mit Antidepressiva in der Schwangerschaft [43a]. Nulman et al. fanden keine Unterschiede in der neurokognitiven Entwicklung von 3- bis 7-jährigen Kindern mit oder ohne Exposition von Antidepressiva in der Schwangerschaft [39]. Diese Autoren konnten auch in einer Geschwisterstudie (45 Geschwisterpaare) zeigen, dass Antidepressiva während der Schwangerschaft keinen negativen Effekt auf deren neurokognitive Entwicklung hatten [40].
Autismus-Spektrum-Erkrankungen
Es wurden in einigen Studien Hinweise auf einen Zusammenhang zwischen Exposition von Antidepressiva in der Schwangerschaft und Autismus-Spektrum-Erkrankungen berichtet [13, 25]. Hier werden die Befunde aber von anderen Autoren wegen methodischer Mängel noch als sehr vorläufig eingeschätzt, sodass hier keinerlei definitive Aussagen möglich und weitere Studien nötig sind [43, 44].
Das Spontanmeldesystem zur Erfassung von Nebenwirkungen durch Antidepressiva
Ergänzende Erkenntnisse zu den Effekten der Anwendung von Antidepressiva während der Schwangerschaft lassen sich auch im Rahmen der sogenannten Spontanberichterstattung von Nebenwirkungen gewinnen. Der Begriff Nebenwirkung wird im Arzneimittelgesetz (AMG) in § 4 Abs. 13 wie folgt definiert: „Nebenwirkungen sind bei Arzneimitteln, die zur Anwendung bei Menschen bestimmt sind, schädliche und unbeabsichtigte Reaktionen auf das Arzneimittel. Schwerwiegende Nebenwirkungen sind Nebenwirkungen, die tödlich oder lebensbedrohend sind, eine stationäre Behandlung oder Verlängerung einer stationären Behandlung erforderlich machen, zu bleibender oder schwerwiegender Behinderung, Invalidität, kongenitalen Anomalien oder Geburtsfehlern führen.“
Kongenitale Anomalien sowie Geburtsfehler werden dementsprechend aufgrund ihrer besonderen Bedeutung immer als schwerwiegend klassifiziert und spielen gerade auch bei Psychopharmaka in der Schwangerschaft eine große Rolle, wie zuvor beschrieben.
Bei Spontanmeldungen zu Nebenwirkungen (Synonym: unerwünschten Arzneimittelwirkungen – UAW) handelt es sich um Berichte, die nicht aus systematischen Untersuchungen (beispielsweise klinischen Studien) stammen, sondern – wie der Name besagt – spontan berichtet werden und die in klinischen Prüfungen erhobenen Sicherheitsdaten ergänzen; in Deutschland erfolgt dies vor allem durch Angehörige der Heilberufe (insbesondere Ärzte und Apotheker) und die Industrie, mittlerweile können Patienten aber auch selbst Nebenwirkungen an das BfArM berichten. Nebenwirkungen von Arzneimitteln werden im Regelfall bereits im Rahmen der klinischen Prüfung vor der Zulassung erfasst und ausgewertet. Die Bedingungen in klinischen Studien spiegeln aber teilweise nur begrenzt den klinischen Alltag nach der Zulassung eines Arzneimittels wider; bestimmte Patientengruppen (z.B. schwangere Frauen) sind nicht oder nur sehr eingeschränkt repräsentiert. Selten und sehr selten auftretende Nebenwirkungen können häufig aufgrund der begrenzten Zahl eingeschlossener Patienten nicht erfasst werden. Berichte zu Nebenwirkungen aus der Spontanerfassung stellen daher einen wichtigen zusätzlichen Beitrag zur Signalerfassung und Bewertung der Sicherheit von Arzneimitteln dar [29], daher werben wir auch immer wieder für ein aktiveres Meldeverhalten, beispielsweise auf unserer Website (www.bfarm.de/DE/Arzneimittel/Pharmakovigilanz/RisikenMelden/uaw/_node.html). Für die vorliegende Übersicht wurde eine Recherche in der Datenbank des BfArM zu Nebenwirkungsberichten aus Deutschland im Zusammenhang mit der Anwendung von Antidepressiva durchgeführt. Der Fokus lag auf Nebenwirkungen aus den beiden Systemorganklassen Schwangerschaft, Wochenbett und perinatale Erkrankungen sowie kongenitale, familiäre und genetische Erkrankungen. Die Abfrage berücksichtigte alle derzeit in Deutschland verkehrsfähig zugelassenen Antidepressiva. Die Ausgabe der Ergebnisse erfolgte wirkstoffbezogen. Zu beachten ist, dass ein Fallbericht auch mehrere Nebenwirkungen enthalten kann. Die Ergebnisse der Recherche sind in Tabelle 1 dargestellt.
Tab. 1. Anzahl der Fallberichte zu Nebenwirkungen aus Deutschland, geordnet nach betroffenen Wirkstoffen (Stand: 02.09.2015)
|
Wirkstoff |
SOC A1 |
SOC B2 |
Verordnungen 2013* DDD [Mio.] |
||
|
Agomelatin |
16 |
7 |
24,8 |
||
|
Amitriptylin (N06AA09) |
48 |
51 |
21 |
23 |
90,8 |
|
Amitriptylinoxid (N06AA25) |
3 |
2 |
7,1 |
||
|
Atomoxetin |
2 |
10 |
2,0 |
||
|
Bupropion |
10 |
6 |
18,7 |
||
|
Citalopram |
160 |
74 |
329,5 |
||
|
Clomipramin |
26 |
14 |
7,6 |
||
|
Doxepin |
28 |
8 |
47,5 |
||
|
Duloxetin |
37 |
14 |
53,7 |
||
|
Escitalopram |
88 |
40 |
44,2 |
||
|
Fluoxetin |
56 |
30 |
55,9 |
||
|
Fluvoxamin |
4 |
4 |
1,3 |
||
|
Imipramin |
2 |
0 |
2,2 |
||
|
Johanniskraut |
17 |
3 |
32,1 |
||
|
Maprotilin |
1 |
3 |
2,7 |
||
|
Mianserin |
0 |
0 |
0,83 |
||
|
Mirtazapin |
45 |
22 |
165,0 |
||
|
Moclobemid |
5 |
3 |
1,7 |
||
|
Nortriptylin |
3 |
4 |
2,7 |
||
|
Opipramol |
37 |
22 |
79,8 |
||
|
Paroxetin |
90 |
41 |
45,9 |
||
|
Reboxetin |
9 |
3 |
k. A. |
||
|
Sertralin |
97 |
50 |
94,9 |
||
|
Tianeptin |
1 |
0 |
1,3 |
||
|
Tranylcypromin |
2 |
1 |
3,1 |
||
|
Trazodon |
5 |
2 |
2,7 |
||
|
Trimipramin |
16 |
7 |
30,4 |
||
|
Tryptophan |
0 |
0 |
k. A. |
||
|
Venlafaxin |
211 |
93 |
160,3 |
||
|
Vortioxetin |
0 |
0 |
k.A. |
||
1Schwangerschaft, Wochenbett und perinatale Erkrankungen; 2Kongenitale, familiäre und genetische Erkrankungen; *Quelle: Schwabe/Paffrath (Hrsg.). Arzneiverordnungs-Report 2014 [37]; SOC (System Organ Class): Systemorganklasse; DDD: definierte Tagesdosen; k.A.: keine Angabe
Bei der Interpretation der dargestellten Daten ist zu berücksichtigen, dass basierend auf der Spontanberichterstattung nur sehr eingeschränkt Aussagen zur Häufigkeit von Nebenwirkungen gemacht werden können; auch definitive Aussagen zu einem kausalen Zusammenhang zwischen dem angewendeten Arzneimittel und der aufgetretenen Nebenwirkung sind nur selten möglich [29].
Im vorliegenden Fall liegen für Citalopram, Escitalopram, Paroxetin, Sertralin und Venlafaxin die meisten Fallberichte zu Nebenwirkungen aus den beiden untersuchten Systemorganklassen vor. Die genannten Wirkstoffe gehören jedoch auch zu den am häufigsten verordneten Antidepressiva und die Zahlen spiegeln somit letztendlich auch die Verordnungshäufigkeit in Deutschland wider [37]. Die Art der gemeldeten Nebenwirkungen umfasste für die einzelnen Wirkstoffe zwar ein breites Spektrum, bewegte sich aber im Rahmen der Ereignisse, die in aktuellen Übersichten, Leitlinien und Fachinformationen dargelegt sind. Trotz aller damit verbundenen Einschränkungen können Nebenwirkungsberichte aus der Spontanerfassung neue Erkenntnisse zur Sicherheit von Arzneimitteln liefern und werden von uns gerade im Hinblick auf spezielle Populationen wie Schwangere sorgfältig ausgewertet.
Zusammenfassung und Ausblick
Die Therapie mit Antidepressiva in der Schwangerschaft stellt eine komplexe Herausforderung im klinischen Alltag dar und bedarf einer sorgfältigen Abwägung von möglichen Risiken für Mutter und Kind. Sowohl eine unbehandelte Depression wie auch eine Behandlung mit Antidepressiva können negative Auswirkungen haben, allerdings scheint sich basierend auf den Erfahrungen in spezialisierten Zentren, den Ergebnissen aus vielen, teilweise auch sehr großen Observationsstudien und den Datensammlungen in internationalen embryotoxikologischen Zentren eine individuelle Therapie mit den schwangeren Frauen gut durchführen zu lassen; entsprechend umfangreiche Therapieleitlinien stehen mittlerweile zur Verfügung. Bestimmte Nebenwirkungen und Risiken müssen berücksichtigt werden, sind unter dem Strich aber doch eher selten und auch aus regulatorischer Sicht in den Fachinformationen für die jeweiligen Antidepressiva abgebildet. Dieser Themenkomplex unterstreicht aber auch das regulatorische Dilemma, bei oft unklarer Datenlage schon risikominimierende Maßnahmen anzuordnen, die sich auch direkt auf Verordnungszahlen auswirken können. So führten die Warnhinweise zu den möglichen Nebenwirkungen einer Therapie mit Antidepressiva in der Schwangerschaft durch europäische und amerikanische Behörden zu einem Rückgang der Verschreibungen von Antidepressiva mit dem Risiko einer Nichtbehandlung behandlungsbedürftiger Patientinnen (Abb. 3).
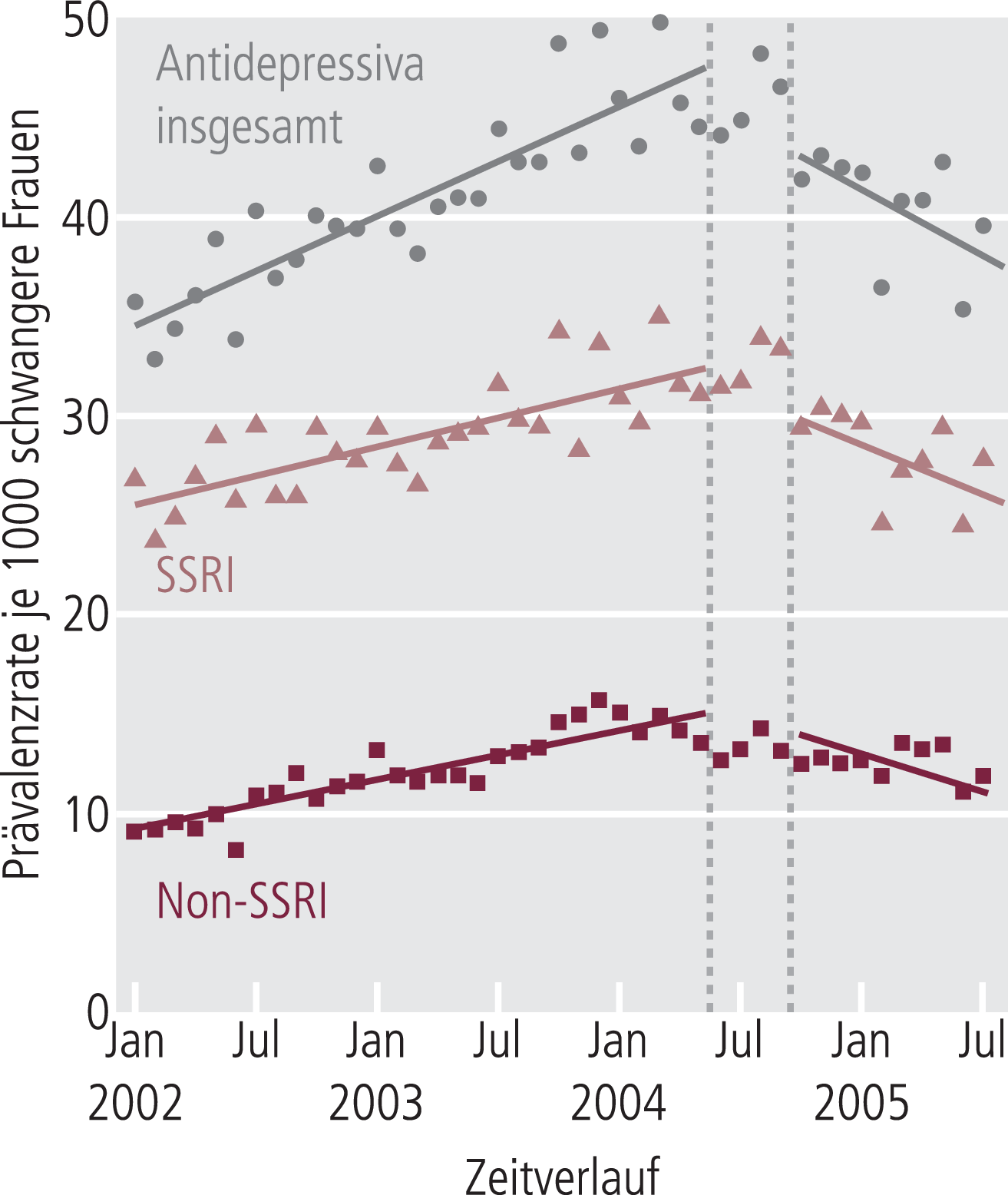
Abb. 3. Änderungen in der Prävalenz von Antidepressiva-Verordnungen nach Warnungen von FDA und Health Canada Mitte 2005 wegen möglicher perinataler Komplikationen wegen Einnahme von Antidepressiva während der Schwangerschaft [mod. nach 5]
Die aufgeführten Empfehlungen erscheinen aus regulatorischer Sicht sinnvoll, allerdings wird dann im klinischen Alltag eventuell auch stärker reagiert, als es für die betroffenen Patienten sinnvoll erscheint. Wir begrüßen daher die Empfehlung zu methodisch besser angelegten Studien für solche Fragestellungen [55], aus regulatorischer Sicht müssen wir in Zukunft aber auch stärker überprüfen, wie unsere risikominimierenden Maßnahmen umgesetzt werden und welche Konsequenzen sie nach sich ziehen.
Danksagung
Die Autoren danken Barbara Koch (Bonn) für die Durchführung der Recherchen.
Interessenkonflikterklärung
MH: Vortragshonorare von Forum Institut für Management und Temas.
NP: Vortragshonorare von Forum Institut für Management und DGRA.
Für KB und CG bestehen keine Interessenkonflikte.
Literatur
1. Andersen JT, Andersen NL, Horwitz H, Poulsen HE, et al. Exposure to selective serotonin reuptake inhibitors in early pregnancy and the risk of miscarriage. Obstet Gynecol 2014;124:655–61.
2. Andrade SE, Raebel MA, Brown J, Lane K, et al. Use of antidepressant medications during pregnancy: a multisite study. Am J Obstet Gynecol 2008;198:194.e1–5.
3. Ban L, Gibson JE, West J, Fiaschi L, et al. Maternal depression, antidepressant prescriptions, and congenital anomaly risk in offspring: a population-based cohort study. BJOG 2014;121:1471–81.
4. Bauer M, Pfennig A, Severus E, Whybrow PC, et al. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for biological treatment of unipolar depressive disorders, part 1: update 2013 on the acute and continuation treatment of unipolar depressive disorders. World J Biol Psychiatry 2013;14:334–85.
5. Bobo WV, Epstein RA Jr., Hayes RM, Shelton RC, et al. The effect of regulatory advisories on maternal antidepressant prescribing, 1995–2007: an interrupted time series study of 228,876 pregnancies. Arch Womens Ment Health 2014;17:17–26.
6. Byatt N, Deligiannidis KM, Freeman MP. Antidepressant use in pregnancy: a critical review focused on risks and controversies. Acta Psychiatr Scand 2013;127:94–114.
7. Cohen LS, Altshuler LL, Harlow BL, Nonacs R, et al. Relapse of major depression during pregnancy in women who maintain or discontinue antidepressant treatment. JAMA 2006; 295:499–507.
8. Cooper WO, Willy ME, Pont SJ, Ray WA. Increasing use of antidepressants in pregnancy. Am J Obstet Gynecol 2007;196:544.e1–5.
9. Council for International Organizations of Medical Sciences (CIOMS). International Ethical Guidelines for Biomedical Research Involving Human Subjects Geneva, 2002.
10. Deutsche Gesellschaft für Psychiatrie und Psychotherapie, Psychosomatik und Nervenheilkunde. S3-Leitlinie zur Diagnostik und Therapie Bipolarer Störungen (Langfassung). www.awmf.org/leitlinien/detail/ll/038-019.html, 2012. (Zugriff 15.10.15).
11. Deutsche Gesellschaft für Psychiatrie und Psychotherapie, Psychosomatik und Nervenheilkunde. S3-Leitlinie/Nationale Versorgungsleitlinie: Unipolare Depression (Langfassung). www.leitlinien.de/mdb/downloads/nvl/depression/depression-1aufl-vers5-lang.pdf, 2015 (Zugriff 15.10.15).
12. Dorsch V, Meurers A, Rohde A. Verantwortung für Psychopharmaka in der Schwangerschaft. Der Neurologe & Psychiater 2014; 15:48–56.
13. El Marroun H, White T, Verhulst FC, Tiemeier H. Maternal use of antidepressant or anxiolytic medication during pregnancy and childhood neurodevelopmental outcomes: a systematic review. Eur Child Adolesc Psychiatry 2014;23:973–92.
14. Epstein RA, Moore KM, Bobo WV. Treatment of nonpsychotic major depression during pregnancy: patient safety and challenges. Drug Health Patient Saf 2014;6:109–29.
15. Ewing G, Tatarchuk Y, Appleby D, Schwartz N, et al. Placental transfer of antidepressant medications: implications for postnatal adaptation syndrome. Clin Pharmacokinet 2015; 54:359–70.
16. Furu K, Kieler H, Haglund B, Engeland A, et al. Selective serotonin reuptake inhibitors and venlafaxine in early pregnancy and risk of birth defects: population based cohort study and sibling design. BMJ 2015;350:h1798.
17. Gavin NI, Gaynes BN, Lohr KN, Meltzer-Brody S, et al. Perinatal depression: a systematic review of prevalence and incidence. Obstet Gynecol 2005;106:1071–83.
18. Gentile S. Drug treatment for mood disorders in pregnancy. Curr Opin Psychiatry 2011;24: 34–40.
19. Gentile S. Early pregnancy exposure to selective serotonin reuptake inhibitors, risks of major structural malformations, and hypothesized teratogenic mechanisms. Expert Opin Drug Metab Toxicol 2015;11:1585–97.
20. Grigoriadis S, Mamisashvili L, Ross LE. Achieving the balance: treating depressed pregnant women with antidepressants. J Clin Psychiatry 2013;74:375–6.
21. Grigoriadis S, VonderPorten EH, Mamisashvili L, Eady A, et al. The effect of prenatal antidepressant exposure on neonatal adaptation: a systematic review and meta-analysis. J Clin Psychiatry 2013;74:e309–20.
22. Grigoriadis S, VonderPorten EH, Mamisashvili L, Roerecke M, et al. Antidepressant exposure during pregnancy and congenital malformations: is there an association? A systematic review and meta-analysis of the best evidence. J Clin Psychiatry 2013;74:e293–308.
23. Grigoriadis S, Vonderporten EH, Mamisashvili L, Tomlinson G, et al. Prenatal exposure to antidepressants and persistent pulmonary hypertension of the newborn: systematic review and meta-analysis. BMJ 2014; 348:f6932.
24. Hanley GE, Oberlander TF. Neurodevelopmental outcomes following prenatal exposure to serotonin reuptake inhibitor antidepressants: a “social teratogen” or moderator of developmental risk? Birth Defects Res A Clin Mol Teratol 2012;94:651–9.
25. Harrington RA, Lee LC, Crum RM, Zimmerman AW, et al. Prenatal SSRI use and offspring with autism spectrum disorder or developmental delay. Pediatrics 2014;133: e1241–8.
26. Hasan A, Falkai P, Wobrock T, Lieberman J, et al. World Federation of Societies of Biological Psychiatry (WFSBP) Guidelines for Biological Treatment of Schizophrenia. Part 3: Update 2015 Management of special circumstances: Depression, suicidality, substance use disorders and pregnancy and lactation. World J Biol Psychiatry 2015;16:142–70.
27. Hayes RM, Wu P, Shelton RC, Cooper WO, et al. Maternal antidepressant use and adverse outcomes: a cohort study of 228,876 pregnancies. Am J Obstet Gynecol 2012;207:49.e1–9.
28. Hermansen TK, Melinder A. Prenatal SSRI exposure: Effects on later child development. Child Neuropsychol 2015;21:543–69.
29. Huber M, Blumberg A, Chatterjee S, Haenisch B, et al. [Drug safety: challenge in an aging society]. Nervenarzt 2014;85:1352–62.
30. Huybrechts KF, Bateman BT, Palmsten K, Desai RJ, et al. Antidepressant use late in pregnancy and risk of persistent pulmonary hypertension of the newborn. JAMA 2015;313:2142–51.
31. Huybrechts KF, Hernandez-Diaz S, Avorn J. Antidepressant use in pregnancy and the risk of cardiac defects. N Engl J Med 2014;371:1168–9.
32. Jones I, Chandra PS, Dazzan P, Howard LM. Bipolar disorder, affective psychosis, and schizophrenia in pregnancy and the post-partum period. Lancet 2014;384:1789–99.
33. Jones I, McDonald L. Living with uncertainty: antidepressants and pregnancy. Br J Psychiatry 2014;205:103–4.
34. Kieler H, Artama M, Engeland A, Ericsson O, et al. Selective serotonin reuptake inhibitors during pregnancy and risk of persistent pulmonary hypertension in the newborn: population based cohort study from the five Nordic countries. BMJ 2012;344:d8012.
35. Kjaersgaard MI, Parner ET, Vestergaard M, Sorensen MJ, et al. Prenatal antidepressant exposure and risk of spontaneous abortion – a population-based study. PLoS One 2013;8:e72095.
36. Kruger S. Psychopharmacological treatment of mood and anxiety disorders during pregnancy. Handb Exp Pharmacol 2012;(214): 279–305.
37. Lohse M, Müller-Oerlinghausen B. Psychopharmaka. In: Schwabe U, Paffrath D (Hrsg.). Arzneiverordnungs-Report 2014. Berlin: Springer, 2014:921–65.
38. Margulis AV, Kang EM, Hammad TA. Patterns of prescription of antidepressants and antipsychotics across and within pregnancies in a population-based UK cohort. Matern Child Health J 2014;18:1742–52.
39. Nulman I, Koren G, Rovet J, Barrera M, et al. Neurodevelopment of children following prenatal exposure to venlafaxine, selective serotonin reuptake inhibitors, or untreated maternal depression. Am J Psychiatry 2012;169:1165–74.
40. Nulman I, Koren G, Rovet J, Barrera M, et al. Neurodevelopment of children prenatally exposed to selective reuptake inhibitor antidepressants: Toronto sibling study. J Clin Psychiatry 2015;76:e842–7.
41. Occhiogrosso M, Omran SS, Altemus M. Persistent pulmonary hypertension of the newborn and selective serotonin reuptake inhibitors: lessons from clinical and translational studies. Am J Psychiatry 2012;169: 134–40.
42. Osborne LM, Payne J. Antidepressants, pregnancy, and stigma: how we are failing mothers and babies. J Nerv Ment Dis 2015; 203:164–6.
43. Pearlstein T. Depression during pregnancy. Best Pract Res Clin Obstet Gynaecol 2015;29:754–64.
43a.Pedersen LH, Henriksen TB, Bech BH, Licht RW, et al. Prenatal antidepressant exposure and behavioral problems in early childhood – a cohort study. Acta Psychiatr Scand 2013;127:126–35.
44. Petersen I, Evans S, Nazareth I. Prenatal exposure to selective serotonin reuptake inhibitors and autistic symptoms in young children: another red herring? Br J Psychiatry 2014;205:105–6.
45. Petersen I, Gilbert RE, Evans SJ, Man SL, et al. Pregnancy as a major determinant for discontinuation of antidepressants: an analysis of data from The Health Improvement Network. J Clin Psychiatry 2011;72:979–85.
46. Petersen I, McCrea RL, Lupattelli A, Nordeng H. Women’s perception of risks of adverse fetal pregnancy outcomes: a large-scale multinational survey. BMJ Open 2015;5: e007390.
47. Ray S, Stowe ZN. The use of antidepressant medication in pregnancy. Best Pract Res Clin Obstet Gynaecol 2014;28:71–83.
48. Robinson GE. Controversies about the use of antidepressants in pregnancy. J Nerv Ment Dis 2015;203:159–63.
49. Roca A, Imaz ML, Torres A, Plaza A, et al. Unplanned pregnancy and discontinuation of SSRIs in pregnant women with previously treated affective disorder. J Affect Disord 2013;150:807–13.
50. Rohde A, Dorsch V, Schaefer C. Psychopharmakotherapie in Schwangerschaft und Stillzeit: Behandlungsprinzipien – Leitlinien – Peripartales Management. 4. Aufl. Stuttgart: Thieme Verlag, 2015.
51. Ross LE, Grigoriadis S, Mamisashvili L, Vonderporten EH, et al. Selected pregnancy and delivery outcomes after exposure to antidepressant medication: a systematic review and meta-analysis. JAMA Psychiatry 2013;70:436–43.
52. Schaefer C. Antidepressive Behandlung. In: Schaefer C, Spielmann H, Vetter K, Weber-Schöndorfer C (Hrsg.). Arzneimittel in Schwangerschaft und Stillzeit. 8. Aufl. München: Elsevier, 2012:267–84.
53. Schaefer C, Spielmann H, Vetter K, Weber-Schöndorfer C (Hrsg.). Arzneimittel in Schwangerschaft und Stillzeit. 8. Aufl. München: Elsevier, 2012.
54. Schaefer C. Arzneimittelprojekt Embryotox: Sicherheit für Mutter und Kind. Dtsch Arztebl 2013;110:A-1048.
55. Swanson SA, Hernandez-Diaz S, Palmsten K, Mogun H, et al. Methodological considerations in assessing the effectiveness of antidepressant medication continuation during pregnancy using administrative data. Pharmacoepidemiol Drug Saf 2015;24:934–42.
56. Yonkers KA, Blackwell KA, Glover J, Forray A. Antidepressant use in pregnant and postpartum women. Annu Rev Clin Psychol 2014;10:369–92.
57. Yonkers KA, Gotman N, Smith MV, Forray A, et al. Does antidepressant use attenuate the risk of a major depressive episode in pregnancy? Epidemiology 2011;22:848–54.
Prof. Dr. Karl Broich, Dr.Christine Greiner, Dr.Norbert Paeschke, Dr. Martin Huber, Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), Kurt-Georg-Kiesinger-Allee 3, 53175 Bonn, E-Mail: leitung@bfarm.de
Use of antidepressants during pregnancy
Episodes of depression are not rare in women before, during, or after pregnancy and treatment with antidepressants must be considered. The possible harm posed by the untreated depressive illness must be balanced against the possible risks of using medications like antidepressants. Clinical experience in these situations shows, that the potential risks of antidepressants to a fetus are consistently overestimated whereas the possible harm of insufficient treatment of depression is underestimated. So there is common experience that antidepressants are reduced or stopped during pregnancy with the risk of deterioration or acute exacerbation of depressive episodes despite evidence from many thousand pregnancies and use of antidepressants. However, currently no antidepressant is authorized for use in pregnant women due to missing evidence from classical randomized clinical trials. Therefore decisions about use of antidepressants in pregnant women must be balanced on a careful and personalized risk-benefit analysis.
This review does not intend to be a clinical guidance for the treatment with antidepressants during pregnancy. The aim is rather to present a short overview of the topic with a focus on regulatory aspects. Possible consequences of regulatory warnings or other risk-minimizing measures will be discussed.
Key words: Antidepressants, benefit-risk, pregnancy, adverse drug reactions
Psychopharmakotherapie 2015; 22(06)
