Uwe Schlegel, Bochum, und Agnieszka Korfel, Berlin
Primäre ZNS-Lymphome (PZNSL) sind ganz überwiegend diffuse großzellige B-Zelllymphome [8], die bei Erstdiagnosestellung auf das Gehirn, das Rückenmark, die Meningen und die Augen (vitreoretinales Lymphom) beschränkt sind [26]. Die Tumoren sind selten und machen etwa 2 bis 3% aller primären intrakraniellen Neubildungen aus [6]. Ihre Prognose ist überwiegend schlecht [1, 18, 26, 27]. Unbehandelt sterben Patienten innerhalb weniger Wochen bis Monate. Durch eine auf Hochdosis-Methotrexat (HDMTX) basierte Chemotherapie hat sich die Prognose dieser Tumoren jedoch in den letzten 25 Jahren deutlich gebessert; bei Patienten unter 65 Jahren kann durch eine solche Chemotherapie oft eine mehrjährige Kontrolle der Erkrankung und wahrscheinlich in einigen Fällen auch eine Heilung erzielt werden [21, 23, 24, 34]. Klinische Symptome sind oft unspezifisch und umfassen ein organisches Psychosyndrom, neurologische fokale Symptome, seltener Anfälle und noch seltener Hirnnervenausfälle oder andere Symptome [26]. Das Magnetresonanztomogramm (MRT) ist die überlegene apparative diagnostische Maßnahme, die sehr häufig einen unilokulären oder multilokulären, intensiv und homogen Kontrastmittel-aufnehmenden Tumor zeigt, der in mehr als 90% der Fälle Anschluss an das Ventrikelsystem hat [29] (Abb. 1).
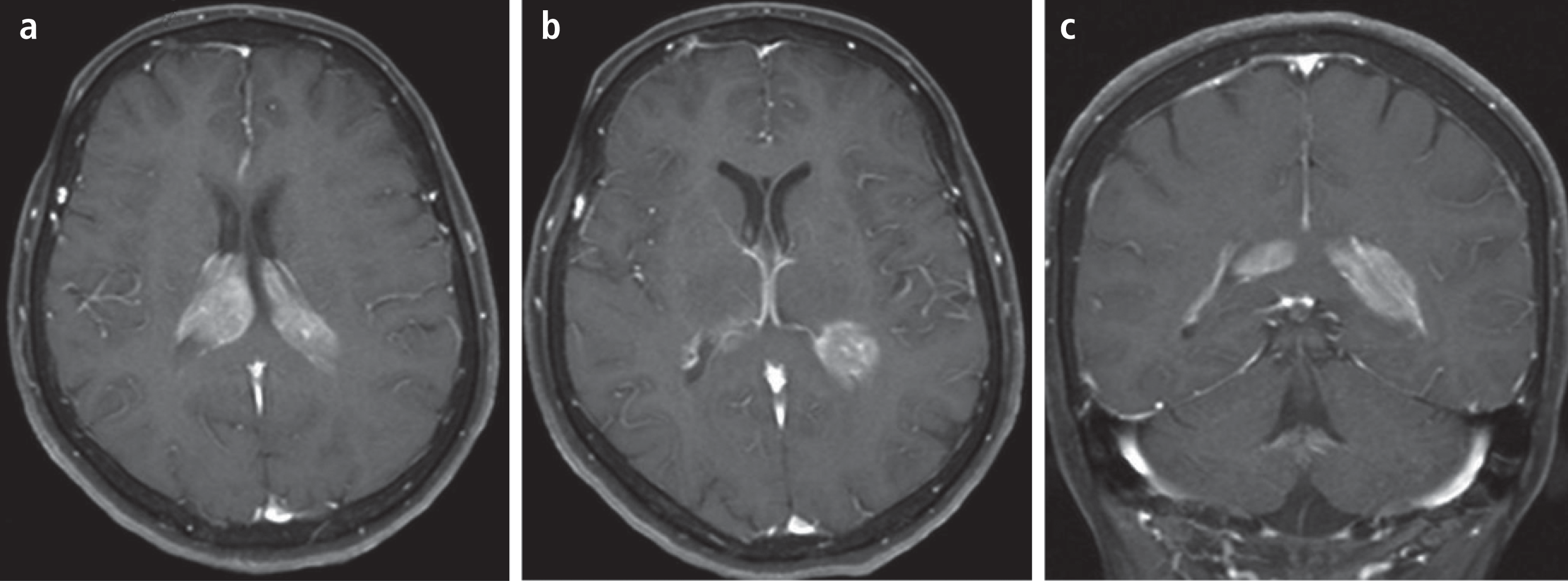
Abb. 1. MRT einer 68-jährigen Patientin mit histologisch gesichertem PZNSL Die Sequenzen in T1-Wichtung nach Kontrastmittelgabe zeigen den intensiv und homogen Kontrastmittel-aufnehmenden multilokulären Tumor in typischer periventrikulärer Lokalisation axial (a, b) und koronar (c).
Obwohl die Tumoren sehr häufig Anschluss an das Ventrikelsystem und damit an die Meningen und das Liquorkompartiment haben, sind Tumorzellen im Liquor cerebrospinalis nur bei weniger als 20% der PZNSL-Patienten nachweisbar; diese Sensitivität wird auch durch zusätzliche diagnostische Maßnahmen wie die PCR zur Detektion monoklonaler B-Zellen nur unwesentlich erhöht [28].
Eine früher postulierte Regel, dass diese Tumoren nicht operativ angegangen werden sollten, wurde durch eine Untersuchung infrage gestellt [44]: Nach den Ergebnissen einer ungeplanten Post-hoc-Analyse am Patientenkollektiv einer großen prospektiven Therapiestudie ist es wohl gerechtfertigt, singuläre Läsionen, die operativ gut erreichbar sind, zu resezieren.
Mit Ausnahme der sehr seltenen Fälle, in denen ein zytopathologischer Nachweis von Tumorzellen im Nervenwasser oder im Glaskörper des Auges gelingt, ist eine histopathologische Diagnose erforderlich [26]. Ist bei multilokulären Prozessen und/oder bei einer operativ schwer zugänglichen Läsion eine Biopsie erforderlich, sollte diese mithilfe der Stereotaxie durchgeführt werden und dann idealerweise, bevor Glucocorticoide gegeben werden, da Glucocorticoide lymphotoxisch sind und damit die Diagnosestellung behindern können [26, 37]. Da eine grundsätzlich wirksame Strahlentherapie bei diesen Tumoren, insbesondere in Kombination mit einer HDMTX-Therapie zu fatalen neurotoxischen Therapiefolgen führen kann [7, 9, 33], wird in der Primärtherapie dieser Tumoren zunehmend auf die Strahlentherapie verzichtet. Dieses Vorgehen wird durch die bisher einzige publizierte randomisierte Phase-III-Studie bei PZNSL nahegelegt, in der kein Überlebensvorteil für die nachbestrahlten Patienten gefunden wurde [43]. Wenngleich in Teilen der USA und Europas noch eine Strahlentherapie in der Primärbehandlung eingesetzt wird, ist diese Therapie in Deutschland (und z.B. auch in Frankreich) verlassen worden: Es besteht hier Konsensus unter Experten aller Fachrichtungen darüber, dass die Primärtherapie des PZNSL nach histopathologischer Diagnosesicherung (Biopsie oder Resektion) eine rein medikamentöse Therapie ist (www.awmf.org/leitlinien/detail/ll/030-059.html). Im Folgenden soll daher diese medikamentöse Therapie der PZNSL dargestellt werden.
Prinzipien der Chemotherapie
Zur Therapie der PZNSL im Allgemeinen und zur Chemotherapie dieser Tumoren gibt es sehr wenig evidenzbasierte Befunde (www.awmf.org/leitlinien/detail/ll/030-059.html). Es besteht jedoch Konsens darüber, dass eine HDMTX-Therapie mit >3 Gramm pro m2 Körperoberfläche (g/m2 KOF) pro Infusion, über mehrere Zyklen intravenös gegeben, die Grundlage jeder wirksamen Therapie ist [26]. Diese Therapie führt bei mehr als der Hälfte der Patienten zu einer zumindest vorübergehenden Tumorremission; langhaltende Tumorremissionen lassen sich mit einer HDMTX-Monotherapie jedoch in aller Regel nicht erreichen [2, 16]. Es besteht daher ein weitgehender wissenschaftlicher Konsens darüber, dass sich einer HDMTX-basierten Initialtherapie des PZNSL (mit dem Ziel, eine Remission zu erreichen) wenn möglich eine konsolidierende intensivierte Therapie anschließen sollte. Diese intensivierte Chemotherapie kann – besonders bei jungen Patienten, die aggressive Therapien tolerieren, – eine potenziell myeloablative Hochdosistherapie mit anschließender autologer Stammzelltransplantation (HD+ASCT) sein oder eine intensivierte konventionelle Chemotherapie. Darüber hinaus werden bereits in der Initialtherapie zusätzlich zu HDMTX häufig weitere Substanzen wie das Zytostatikum Ifosfamid (Holoxan®) und/oder der Anti-CD20-Antikörper Rituximab (MabThera®) eingesetzt. Eine zusätzliche intraventrikuläre Chemotherapie mit Zytostatika und Glucocorticoiden wurde und wird an einzelnen Zentren zur Therapieintensivierung eingesetzt, hat jedoch keine breite Anwendung gefunden [17]. Im Folgenden sollen zunächst die häufig eingesetzten Substanzen eingeführt und dann gebräuchliche Chemotherapie-Protokolle dargestellt werden.
Hochdosis-Methotrexat (HDMTX)
MTX ist ein Folsäureantagonist; daher kann eine HDMTX-Therapie nur unter gleichzeitiger Gabe von Folinsäure zum Schutz vor unerwünschter Toxizität gegeben werden. Bei PZNSL wurden nach therapeutischem Ansprechen als effektiv zu beurteilende Dosierungen zwischen 1 g/m2 KOF und 8 g/m2 KOF appliziert [26, 27]. Die optimale Dosis ist nicht etabliert; es werden jedoch in der Regel Dosierungen zwischen 3 und 8 g/m2 KOF eingesetzt [26]. In diesem Dosierungsbereich ist eine ausreichende Penetration der Substanz in das Liquorkompartiment, in das Hirnparenchym und in den dort liegenden Tumor wahrscheinlich. Untersuchungen deuten darauf hin, dass eine über drei bis vier Stunden verabreichte Infusion einen hohen Wirkspiegel erreicht und eine ausreichende zytotoxische Konzentration über Tage sicherstellt [5, 13]. MTX wird über die Niere ausgeschieden und kristallisiert bei saurem oder normalem pH-Wert des Urins im Nierentubulus aus, sodass diese Therapie nur unter einer Hyperhydratation (6 bis 8 l Flüssigkeit/Tag) und unter Urinalkalisierung mittels Hydrogencarbonat-Infusionen durchgeführt werden kann. Auch bei älteren und alten Patienten ist grundsätzlich eine solche Therapie durchführbar [22, 32, 39]. Voraussetzung hierfür ist jedoch die Beachtung der Nierenfunktion und eine Dosisanpassung von MTX an eine reduzierte glomeruläre Filtrationsrate (GFR) [22]. Unterhalb einer GFR von 50 ml/min ist eine HDMTX-Therapie in der beschriebenen Weise nicht durchführbar.
Cytosinarabinosid (AraC)
AraC ist ebenfalls ein Antimetabolit, der in mehreren Kombinationschemotherapien beim PZNSL in hohen Dosierungen von 2 bis 3 g/m2 KOF (HDAraC) pro Infusion eingesetzt wird [21, 34] mit bis zu acht Infusionen in einem Zyklus [41]. In einer kleinen prospektiven randomisierten Phase-II-Studie konnte gezeigt werden, dass HDAraC, zusätzlich zu einer HDMTX-Monotherapie gegeben (allerdings in beiden Therapiearmen gefolgt von einer Ganzhirnbestrahlung), sowohl die Ansprechrate als auch das progressionsfreie Überleben (nicht jedoch das Gesamtüberleben) verlängerte [11]. Kritisch muss jedoch zu dieser Studie angemerkt werden, dass im Standardarm die Monotherapie von HDMTX unterdosiert war. Hinzu kommt, dass die Kombination mit einer sehr hohen Rate an schweren Leuko- und Thrombopenien deutlich toxischer war. Basierend auf diesen Ergebnissen wurde von den Studienautoren postuliert, dass HDMTX/HDAraC als Standardtherapie bei PZNSL zu betrachten ist. Von den Verfassern des vorliegenden Artikels werden diese Ergebnisse kritischer gesehen.
Ifosfamid
Ifosfamid (Ifo) ist ein Alkylans und wurde innerhalb der großen G-PZNSL-SG1-Studie [43] nachträglich gemäß eines Amendments zur Induktionstherapie mit HDMTX hinzugegeben, wodurch im Rahmen dieser Studie die Ansprechrate signifikant erhöht wurde. Ob Ifosfamid, zusätzlich zu HDMTX gegeben, auch die Gesamtüberlebenszeit verlängert, konnte die Studie nicht beantworten. Ifosfamid wurde auch in anderen Kombinationschemotherapien gegen das PZNSL eingesetzt [34], da es eine sehr wirksame Substanz bei malignen Lymphomen ist. Es besitzt ein spezifisches Nebenwirkungsprofil und kann in seltenen Fällen zu einer akuten zentralen Neurotoxizität mit Lethargie, Somnolenz bis hin zum Koma und auch epileptischen Anfällen führen [42]. Ob diese durch spezifische prophylaktische Maßnahmen, wie durch die hochdosierte Gabe von Thiamin, verhindert werden können, ist offen. In einer Dosis von 800 mg/m² KOF an vier aufeinander folgenden Tagen innerhalb des Bonner Protokolls [23, 34] verursachte Ifosfamid keine zentralen neurotoxischen Therapiefolgen.
Andere Chemotherapeutika
Zu den bei PZNSL in der Primärtherapie eingesetzten Substanzen zählen zahlreiche weitere, die bei systemischen Lymphomen effektiv sind, beispielsweise Procarbazin, Lomustin (CCNU), Vincaalkaloide, Etoposid sowie auch das sich durch sehr gute ZNS-Gängigkeit auszeichnende Temozolomid und weitere. Insbesondere Etoposid – als Bestandteil einer intensivierten Chemotherapie zur Konsolidierung des Therapieerfolgs im Rahmen der amerikanischen CALGB-50202-Studie – verdient Erwähnung, da die Kombination von hochdosiertem Etoposid und HDAraC in dieser Therapiestudie zwar zu einer erheblichen Myelotoxizität (WHO-Grad-3- und -4-Toxizität von über 80%) führte, aber mit überraschend langen Gesamtüberlebenszeiten verbunden war [41].
In der Rezidivtherapie wirksame Therapien – gemessen am Tumoransprechen – sind Temozolomid allein oder in Kombination mit Rituximab, Topotecan, die Kombination aus Procarbazin, CCNU und Vincristin (PCV) [10, 12, 15, 38] und nach vorherigem langem Ansprechen auf eine Primärtherapie mit HDMTX ein HDMTX-„Re-Challenge“ [35].
Hochdosis-Chemotherapie mit autologer Stammzelltransplantation (HDASCT)
Das Prinzip der potenziellen myeloablativen Hochdosis-Chemotherapie besteht bei PZNSL darin, Lymphom-wirksame Substanzen in sehr hohen Dosen zu verabreichen, um möglichst hohe ZNS-Konzentrationen zu erreichen, was allerdings das blutbildende Knochenmark wesentlich schädigt. Um diese Therapieform durchführen zu können, ist eine vorherige Blutstammzellmobilisation und anschließende Stammzell-„Ernte“ erforderlich, sodass diese autologen Stammzellen nach Durchführung der Hochdosistherapie appliziert werden und das Knochenmark wieder aufbauen können. Im Freiburger Protokoll zu PZNSL wird nach einer HDMTX-basierten Initialtherapie unter einer Induktionstherapie mit HDAraC plus niedrig dosiertem Thiotepa (TT) unter Gabe von Granulozyten-Kolonie-stimulierendem Faktor (G-CSF) zur Stammzellmobilisation durchgeführt, gefolgt von einer hochdosierten Gabe von Carmustin (BCNU) und TT mit anschließender Stammzelltransplantation. In einer ersten Therapiestudie wurden alle 30 Patienten obligat nach Durchführung der Hochdosistherapie mit Stammzelltransplantation ganzhirnbestrahlt, was erwartungsgemäß bei einem Teil der Patienten zu toxischen Enzephalopathien führte [21, 24]. In einem weiterentwickelten Konzept wurde die medikamentöse Therapie intensiviert, durch den Anti-CD20-Antikörper Rituximab angereichert und eine Ganzhirnbestrahlung nur noch bei einem inkompletten Ansprechen des Tumors auf die Chemotherapie durchgeführt [20].
Intraventrikuläre Chemotherapie
PZNSL-Zellen zeigen einen ausgeprägten Tropismus zu den Meningen, wobei Ventrikel und Ventrikelwände ein Kompartiment bilden, das zumindest theoretisch für Tumorzellen ein Sanktuarium darstellt, in dem sie von einer systemisch applizierten Chemotherapie schlecht oder schlechter erreicht werden. Daher wurde in das sogenannte Bonner Protokoll eine intraventrikuläre Therapie eingeschlossen, die über ein subgaleales Reservoir (Ommaya-Reservoir oder Rickham-Reservoir) eine tägliche Gabe von niedrig dosiertem MTX plus Prednisolon und danach gefolgt von AraC vorsah. Dieses Protokoll war das erste Therapieprotokoll bei PZNSL, das a priori auf eine Ganzhirnbestrahlung in der Erstlinientherapie verzichtete. Die 2003 [34] und 2010 [23] publizierten Ergebnisse zeigten für mehr als die Hälfte der unter 65-jährigen Patienten eine Tumorkontrolle im Median von über zehn Jahren und damit für einen erheblichen Teil dieser Patienten eine kurative Therapiesituation.
Aufgrund einer hohen Reservoir-Infektionsrate [34], und bei Fehlen anderer Studien zur Untermauerung der Wirksamkeit einer zusätzlichen intraventrikulären Therapie, hat sich dieses Protokoll nicht durchgesetzt [17]. Am Zentrum eines der Autoren (U.S.) wird dieses Protokoll in modifizierter Form eingesetzt (Abb. 2), wobei die Implantation eines Ommaya-Reservoirs bei Patienten mit Ansprechen auf drei Zyklen einer Therapie mit HDMTX, Ifosfamid und Rituximab (X3) erst vor dem 4. Zyklus erfolgt, was die Reservoir-Infektionsrate auf unter 5% reduziert hat.
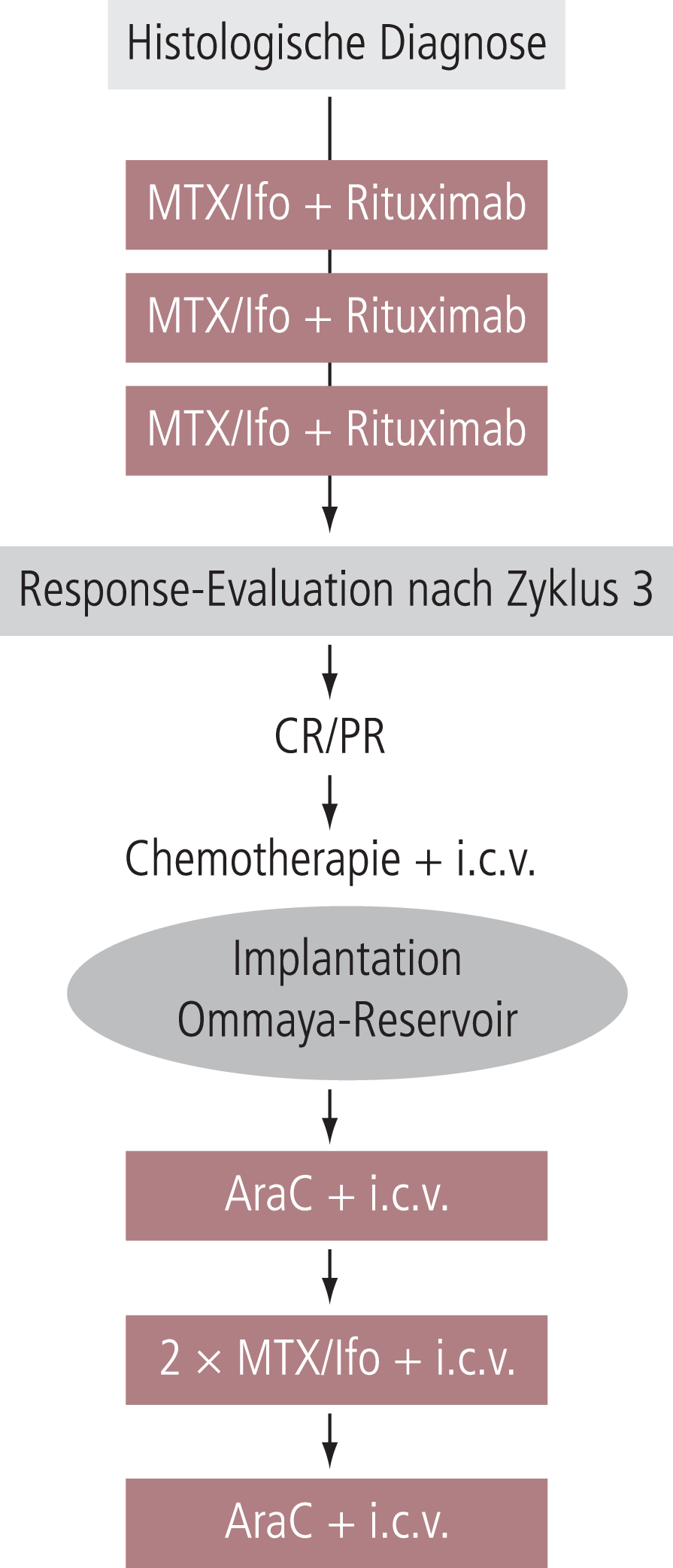
Abb. 2. Das dargestellte Bochumer Protokoll ist eine Fortentwicklung des Bonner Protokolls [23, 34] Es besteht aus einer Initialtherapie von drei Zyklen einer Chemo-Immuntherapie mit R/MTX/Ifo (X3): – Rituximab 500 mg/m2 KOF an Tag 0 – MTX 4 g/m2 KOF über 4 Stunden an Tag 1 – Ifosfamid 800 mg/m2 KOF/Tag an Tagen 2 bis 5 Diese Therapie wird alle 14 Tage durchgeführt. Dann wird bei Ansprechen (CR =komplette Remission, PR =partielle Remission) ein Ommaya-Reservoir implantiert. Daran schließt sich eine intensivierte Therapie an: – AraC 3 g/m2 KOF über 3 Stunden an den Tagen 1 und 2 (Zyklus 4 und 7) – MTX 4 g/m2 KOF über 4 Stunden an Tag 1 + Ifosfamid 800 mg/m2 KOF/Tag an den Tagen 2 bis 5 (Zyklus 5 und 6) + jeweils eine intraventrikuläre (i.c.v.) Therapie an den Tagen 3 bis 6 mit – MTX 3 mg + Prednisolon 2,5 mg pro Tag an den Tagen 3, 4, 5 – AraC 30 mg an Tag 6 Dem Zyklus 4 folgt eine zweiwöchige Pause, den anderen Zyklen jeweils eine einwöchige Pause. AraC: Cytosinarabinosid; Ifo: Ifosfamid; KOF: Körperoberfläche; MTX: Methotrexat; R: Rituximab
Anti-CD20-Antikörper
Der Anti-CD20-Antikörper Rituximab ist seit mehreren Jahren ein fester Bestandteil in der Therapie von systemischen Non-Hodgkin-Lymphomen der B-Zellreihe. Retrospektive Analysen bei PZNSL legen nahe, dass Patienten unter Zugabe von Rituximab zu einer HDMTX-basierten Initialtherapie zum einen bessere Ansprechraten als unter HDMTX allein zeigen [4] und zum anderen deutliche längere progressionsfreie und Gesamt-Überlebenszeiten aufweisen [14]. Derzeit werden Therapiestudien durchgeführt, in denen prospektiv randomisiert Therapiearme unter Einschluss von Rituximab mit solchen ohne Rituximab verglichen werden. Zum jetzigen Zeitpunkt darf davon ausgegangen werden, dass Rituximab mit hoher Wahrscheinlichkeit die Therapieeffizienz bei PZNSL erhöht.
Neue Substanzen
Die Passage von Rituximab in das Liquorkompartiment ist allerdings gering [40] und damit wohl auch sein Übertritt in Hirn- und Tumorgewebe, welches nur bei Therapiebeginn und großer Tumormasse eine gestörte Blut-/Tumorschranke aufweisen dürfte. Geringe Konzentration in Hirn und Tumor schränken wahrscheinlich die Effektivität von Rituximab ein. Ob dies auch für neuere Anti-CD20-Antikörper gilt, wie für GA101 (Obinutuzumab) [31], das ohne Komplementaktivierung auskommt und daher im ZNS möglicherweise effektiver ist, muss in der Zukunft überprüft werden.
Insbesondere in der Rezidivsituation, die eine sehr ungünstige Prognose bedeutet und für die es keine etablierte Therapie gibt, werden neuere Substanzen evaluiert [36]. In der kurz vor dem Abschluss stehenden prospektiven deutschen Studie wurde der mTOR-Inhibitor Temsirolimus bei 37 Patienten (medianes Alter 69 Jahre; 23 bis 83) mit refraktärem/rezidiviertem PZNSL, die nicht für eine HDASCT geeignet waren oder diese bereits bekommen hatten und danach rezidiviert sind, evaluiert. Die Gesamtansprechrate betrug bei diesen umfangreich vorbehandelten Patienten immerhin 58% bei allerdings relativ hoher Toxizität, insbesondere hinsichtlich des Auftretens von Infektionen [25]. Ein Beispiel für einen erfolgreichen Therapieverlauf zeigt Abbildung 3.
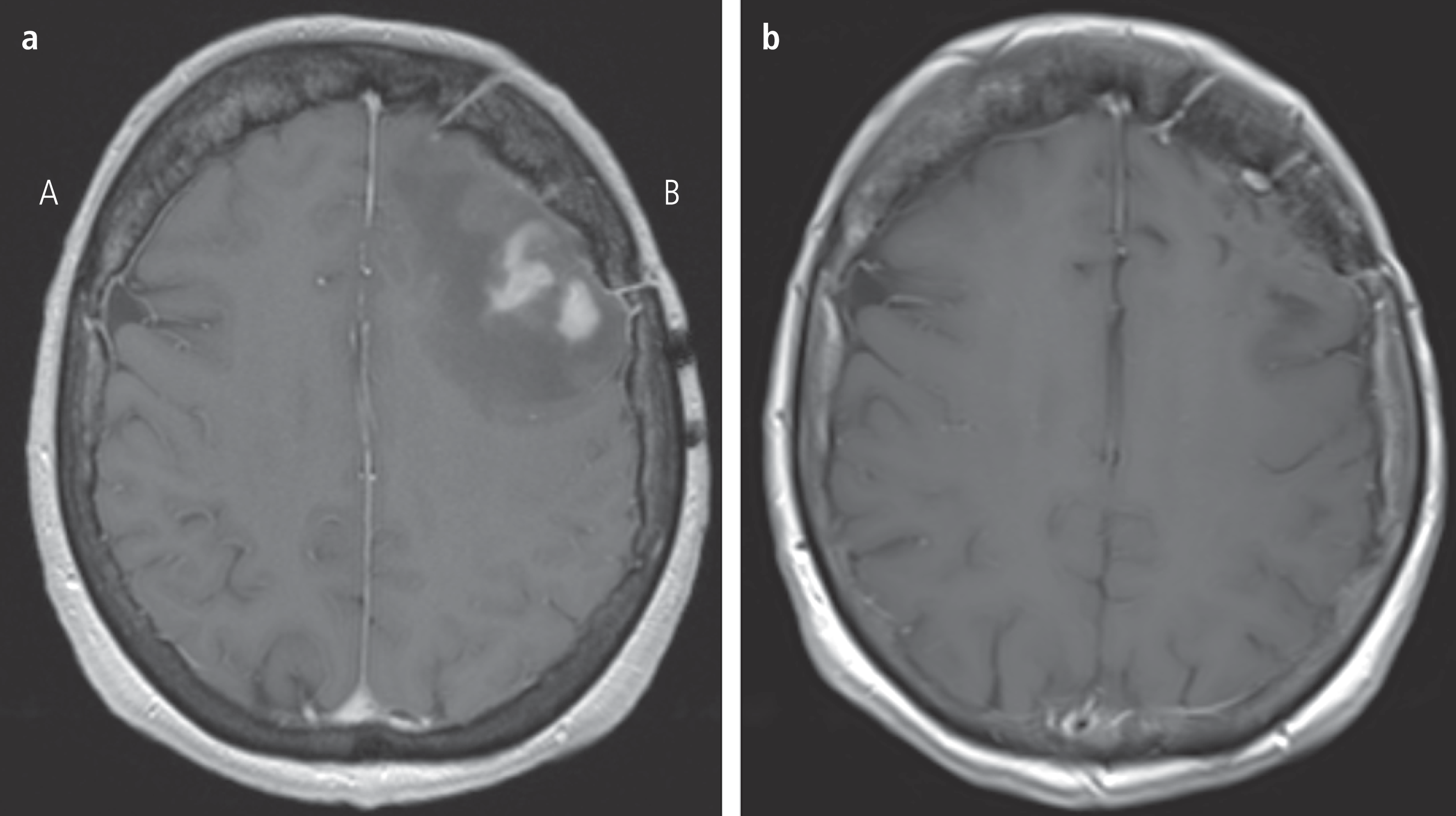
Abb. 3. MRT einer 72-jährigen Patientin mit Rezidiv eines PZNSL nach initialer Remission auf eine HDMTX-basierte Chemotherapie. Die Sequenzen in T1-Wichtung nach Kontrastmittelgabe zeigen den links frontalen Rezidivtumor vor (a) und nach Ansprechen auf vier Zyklen einer Therapie mit Temsirolimus 75 mg i.v. einmal pro Woche (b). HDMTX: Hochdosis-Methotrexat; PZNSL: Primäres ZNS-Lymphom
Lenalidomid ist ein für die Therapie des multiplen Myeloms zugelassener Immunmodulator; in einer retrospektiven Auswertung von sechs Patienten mit rezidiviertem PZNSL zeigten zwei von sechs eine komplette Remission, die bei einem Patienten 24 Monate anhielt [19]. Die Substanz wird in aktuell laufenden Studien evaluiert. Das ebenfalls für das multiple Myelom zugelassene Pomalidomid, das in einem Mausmodell eine gute Blut-Hirn-Schranken-Penetration aufwies und gegen Lymphomzellen im ZNS effektiv war [30], wird ebenfalls in einer laufenden klinischen Studie überprüft. Da die meisten PZNSL nach dem aktuellen Kenntnisstand zum „aktivierten B-Zell-Typ“(ABC)-Subtyp des diffusen großzelligen B-Zell-Lymphoms gehören, müssten sie eine dauerhafte Aktivierung des B-Zell-Rezeptors aufweisen, was ein Angriffspunkt für selektive Inhibitoren wie Ibrutinib wäre. Eine Studie mit der Kombination von Ibrutinib mit einer „klassischen“ Chemotherapie als Erstlinientherapie wird aktuell in den USA durchgeführt. Auch andere Signalwege, zum Beispiel der PI3K-mTOR-Signalweg, stellen beim PZNSL ein potenzielles Therapietarget dar. Entsprechende Studien befinden sich in Planung. Aussichtsreich erscheint außerdem der Ansatz am Tumor-„Microenvironment“, das möglicherweise eine wichtige Rolle in der Pathogenese des PZNSL spielt. Offensichtlich schaffen sich PZNSL innerhalb des ZNS selbst eine ihr Wachstum begünstigende Umgebung, die sich durch eine Immuntoleranz auszeichnet. Das „Programmed death protein 1“ (PD1; CD279) und sein Ligand PD-L1 (B7H1, CD274) könnten dabei eine pathogenetische Rolle spielen: Beide waren immunohistochemisch beim PZNSL nachweisbar [3]. Der therapeutische Einsatz entsprechender Inhibitoren ist interessant, eine entsprechende Studie befindet sich in Planung.
Fazit für die medikamentöse Therapie der PZNSL
- Basis jeder effektiven (Poly-)Chemotherapie bei PZNSL ist Hochdosis-Methotrexat (HDMTX).
- Die zusätzliche Gabe von weiteren Zytostatika, vor allem von Cytosinarabinosid und Ifosfamid verbessert die Ansprechrate und das progressionsfreie Überleben. Ob damit auch das Gesamtüberleben verlängert wird, wurde bisher in randomisierten Studien nicht gezeigt.
- Analog gilt dies für die zusätzliche Gabe des Anti-CD20-Antikörpers Rituximab, wobei vergleichende Studien zu dessen Wirksamkeitsnachweis laufen.
- Angesichts der ungünstigen Prognose mit HDMTX allein sollte daher Patienten, die eine intensivierte Chemotherapie tolerieren, eine über die HDMTX-Monotherapie hinaus intensivierte Chemotherapie angeboten werden, beispielsweise in Form einer nicht kreuzresistenten konventionell dosierten Chemotherapie oder in Form einer Hochdosis-Chemotherapie mit autologer Stammzelltransplantation.
- Die Identifikation von pathogenetisch bedeutsamen Signalwegen erlaubt wahrscheinlich die Identifizierung neuer therapeutischer Targets und findet bereits ihren Weg in die aktuelle Planung von Therapiestudien.
Interessenskonflikterklärung
US erhielt Honorare von Essex Pharma, Novartis, Mundipharma, sigma tau, medac, GSK, Roche, Orthobiotech und Optune für Berater- und Vortragstätigkeiten. US erhält Förderungen von der Deutschen Forschungsgemeinschaft (SCHL 268/4–1) und von der Deutschen Krebshilfe (110586).
AK erhielt Honorare von Mundipharma und Riemser für Berater- und Vortragstätigkeiten.
Literatur
1. Abrey LE, Batchelor TT, Ferreri AJ, et al.; International Primary CNS Lymphoma Collaborative Group. Report of an international workshop to standardize baseline evaluation and response criteria for primary CNS lymphoma. J Clin Oncol 2005;23:5034–43.
2. Batchelor T, Carson K, O’Neill A, et al. Treatment of primary CNS lymphoma with methotrexate and deferred radiotherapy: a report of NABTT 96–07. J Clin Oncol 2003;21:1044–9.
3. Berghoff AS, Ricken G, Widhalm G, et al. PD1 (CD279) and PD-L1 (CD274, B7H1) expression in primary central nervous system lymphomas (PCNSL). Clin Neuropathol 2014;33:42–9.
4. Birnbaum T, Stadler EA, von Baumgarten L, et al. Rituximab significantly improves complete response rate in patients with primary CNS lymphoma. J Neurooncol 2012;109:285–91.
5. Borsi JD, Moe PJ. A comparative study on the pharmacokinetics of methotrexate in a dose range of 0.5 g to 33.6 g/m2 in children with acute lymphoblastic leukemia. Cancer 1987;60:5–13.
6. CBTRUS. Primary brain and central nervous system tumors diagnosed in the United States 2007–2011. Neuro Oncol 2012;16(Suppl 4).
7. Correa DD, Shi W, Abrey LE, et al. Cognitive functions in primary CNS lymphoma after single or combined modality regimens. Neuro Oncol 2012;14:101–8.
8. Deckert M, Engert A, Brück W, et al. Modern concepts in the biology, diagnosis, differential diagnosis and treatment of primary central nervous system lymphoma. Leukemia 2011;25:1797–807.
9. Doolittle ND, Korfel A, Lubow M, et al. Long-term cognitive function, neuroimaging and quality of life in primary CNS lymphoma. Neurology 2013;81:84–92.
10. Enting RH, Demopoulos A, De Angelis LM, Abrey LE. Salvage therapy for primary CNS lymphoma with a combination of rituximab and temozolomide. Neurology 2004;63:901–3.
11. Ferreri AJ, Reni M, Foppoli M, et al. High-dose cytarabine plus high-dose methotrexate versus high-dose methotrexate alone in patients with primary CNS lymphoma: a randomised phase 2 trial. Lancet 2009;374:1512–20.
12. Fischer L, Thiel E, Klasen HA, et al. Prospective trial on topotecan salvage therapy in primary CNS lymphoma. Ann Oncol 2006;17:1141–5.
13. Glantz MJ, Cole BF, Recht L, et al. High-dose intravenous methotrexate for patients with nonleukemic leptomeningeal cancer: is intrathecal chemotherapy necessary? J Clin Oncol 1998;16:1561–7.
14. Gregory G, Arumugaswamy A, Leung T, et al. Rituximab is associated with improved survival for aggressive B cell CNS lymphoma. Neuro Oncol 2013;15:1068–73.
15. Herrlinger U, Brugger W, Bamberger M, et al. PCV salvage chemotherapy for recurrent primary CNS lymphoma. Neurology 2000;54:1707–8.
16. Herrlinger U, Küker W, Uhl M, et al. NOA-03 trial of high-dose methotrexate in primary central nervous system lymphoma: final report. Ann Neurol 2005;57:843–7.
17. Herrlinger U, Glantz M, Schlegel U, et al. Should intra-cerebrospinal fluid prophylaxis be part of initial therapy for patients with non-Hodgkin lymphoma: what we know, and how we can find out more. Semin Oncol 2009;36:25–34.
18. Hoang-Xuan K, Bessell E, Bromberg J, et al. Diagnosis and treatment of primary CNS lymphoma in immunocompetent patients: guidelines from the European Association for Neuro-Oncology. Lancet Oncol 2015;16:e322–32.
19. Houillier C, Choquet S, Touitou V, et al. Lenalidomide monotherapy as salvage treatment for recurrent primary CNS. Neurology 2014;84:325–6.
20. Illerhaus G, Fritsch K, Egerer G, et al. Sequential high dose immuno-chemotherapy followed by autologous peripheral blood stem cell transplantation for patients with untreated primary central nervous system lymphoma – a multicentre study by the Collaborative PCNSL Study Group Freiburg. ASH Meeting 8.–11.12.2012, Atlanta, Abstract 302.
21. Illerhaus G, Marks R, Ihorst G, et al. High dose chemotherapy with autologous stem-cell transplantation and hyperfractionated radiotherapy as first-line treatment of primary CNS lymphoma. J Clin Oncol 2006;24:3865–70.
22. Jahnke K, Korfel A, Martus P, et al. High-dose methotrexate toxicity in elderly patients with primary central nervous system lymphoma. Ann Oncol 2005;16:445–9.
23. Juergens A, Pels H, Rogowski S, et al. Long-term survival with favorable cognitive outcome after chemotherapy in primary central nervous system lymphoma. Ann Neurol 2010;67:182–9.
24. Kasenda B, Schorb E, Fritsch K, et al. Prognosis after high-dose chemotherapy followed by autologous stem-cell transplantation as first-line treatment in primary CNS lymphoma – a long-term follow-up study. Ann Oncol 2012;23:2670–5.
25. Kiewe P, Martus P, Thiel E, et al. Phase II trial of temsirolimus for relapsed/refractory primary central nervous system lymphoma (PCNSL). Oncol Res Treat 2014;37(Suppl 5):268.
26. Korfel A, Schlegel U. Diagnosis and treatment of primary CNS lymphoma. Nat Rev Neurol 2013;9:317–27.
27. Korfel A, Schlegel U. Primary ZNS lymphoma – progress in the diagnostics and therapy. Nervenarzt 2015;86:710–5.
28. Korfel A, Weller M, Martus P, et al. Prognostic impact of meningeal dissemination in primary CNS lymphoma (PCNL): Experience from the G-PCNSL-SG1 trial. Ann Oncol 2012;23:2374–80.
29. Küker W, Nägele T, Thiel E, et al. Primary central nervous system lymphomas (PCNSL): MRI response criteria revised. Neurology 2005;65:1129–31.
30. Li Z, Qiu Y, Personett D, et al. Pomalidomide shows significant therapeutic activity against CNS lymphoma with a major impact on the tumor microenvironment in murine models. PLoS One 2013;8:e71754.
31. Mössner E, Brünker P, Moser S, et al. Increasing the efficacy of CD20 antibody therapy through the engineering of a new type II anti-CD20 antibody with enhanced direct and immune effector cell-mediated B-cell cytotoxicity. Blood 2010;115:4393–402.
32. Ney DE, Reiner AS, Panageas KS, et al. Characteristics and outcomes of elderly patients with primary central nervous system lymphoma: the Memorial Sloan-Kettering Cancer Center experience. Cancer 2010;116:4605–12.
33. Omuro AM, Ben-Porat LS, Panageas KS, et al. Delayed neurotoxicity in primary central nervous system lymphoma. Arch Neurol 2005;62:1595–600.
34. Pels H, Schmidt-Wolf IG, Glasmacher A, et al. Primary central nervous system lymphoma: results of a pilot and phase II study of systemic and intraventricular chemotherapy with deferred radiotherapy. J Clin Oncol 2003;21:4489–95.
35. Plotkin SR, Betensky RA, Hochberg FH, et al. Treatment of relapsed central nervous system lymphoma with highdose methotrexate. Clin Cancer Res 2004;10:5643–6.
36. Ponzoni M, Issa S, Batchelor TT, et al. Beyond high-dose methotrexate and brain radiotherapy: novel targets and agents for primary CNS lymphoma. Ann Oncol 2014;25:316–22.
37. Porter AB, Giannini C, Kaufmann T, et al. Primary central nervous system lymphoma can be histologically diagnosed after previous corticosteroid use: a pilot study to determine whether corticosteroids prevent the diagnosis of primary central nervous system lymphoma. Ann Neurol 2008;63:662–7.
38. Reni M, Zaja F, Mason W, et al. Temozolomide as salvage treatment in primary brain lymphomas. Br J Cancer 2007;96:864–7.
39. Roth P, Martus P, Kiewe P, et al. Outcome of elderly patients with primary CNS lymphoma in the G-PCNSL-SG-1 trial. Neurology 2012;79:890–6.
40. Rubenstein JL, Combs D, Rosenberg J, et al. Rituximab therapy for CNS lymphomas: targeting the leptomeningeal compartment. Blood 2003;101:466–8.
41. Rubenstein J, His E, Johnson J, et al. Intensive chemotherapy and immunotherapy in patients with newly diagnosed primary CNS lymphoma: CALGB 50202 (Alliance 50202). J Clin Oncol 2013;31:3061–8.
42. Szabatura AH, Cirrone F, Harris C, et al. An assessment of risk factors associated with ifosfamide-induced encephalopathy in a large academic cancer center. J Oncol Pharm Pract 2015;21:188–93.
43. Thiel E, Korfel A, Martus P, et al. High-dose methotrexate with or without whole brain radiotherapy for primary CNS lymphoma (G-PCNSL-SG-1): a phase 3, randomised, non-inferiority trial. Lancet Oncol 2010;11:1036–47.
44. Weller M, Martus P, Roth P, et al.; German PCNSL Study Group. Surgery for primary CNS lymphoma? Challenging a paradigm. Neuro Oncol 2012;14:1481–4.
Prof. Dr. med. Uwe Schlegel, Neurologische Universitätsklinik, Knappschaftskrankenhaus, Klinikum der Ruhruniversität, In der Schornau 23–25, 44892 Bochum, E-Mail: uwe.schlegel@kk-bochum.de
Priv.-Doz. Dr. med. Agnieszka Korfel, Klinik für Hämatologie, Onkologie und Tumorimmunologie, Charité Universitätsmedizin Berlin, Hindenburgdamm 30, 12200 Berlin
Drug therapy of primary CNS lymphoma
The most efficient therapy of primary CNS lymphoma is medical treatment, based on cytostatic drugs. Backbone of every effective pharmacotherapy is high-dose methotrexate (MTX) intravenously. Additional drugs like cytosine-arabinoside or ifosfamide improve response, as do probably antibodies to the CD20 surface antigen. A theoretical rationale exists for novel substances as mTOR inhibitors, immunomodulating agents, selective inhibitors of B-cell receptors and drugs that influence the tumor microenvironment.
Key words: Primary CNS lymphoma, methotrexate, anti-CD20-antibodies, novel substances
Psychopharmakotherapie 2015; 22(05)
