Holger Petri, Bad Wildungen*
H1-Antihistaminika finden in der symptomatischen Behandlung allergischer Reaktionen Verwendung.
Antihistaminika der 1. Generation
Die Substanzen der 1. Generation blockieren nicht nur periphere, sondern auch zentrale H1-Rezeptoren. Ausgeprägte sedierende und anticholinerge Eigenschaften erklären die im Vergleich zu den H1-Antihistaminika der zweiten Generation schlechtere Verträglichkeit. Aufgrund der geringeren Lipophilie wirken diese nahezu selektiv an peripheren H1-Rezeptoren [12]. Gemäß PRISCUS-Liste gelten die Antihistaminika der ersten Generation als potenziell inadäquat bei älteren Patienten [13]. Zur Linderung der allergischen Rhinitis und der Urtikaria sind die Substanzen der zweiten Generation Mittel der Wahl. Wegen ihrer parenteralen Verfügbarkeit haben die älteren Antihistaminika Clemastin und Dimetinden noch Bedeutung in der Prophylaxe und Therapie anaphylaktischer Reaktionen [11]. Zudem werden Clemastin und Hydroxyzin in der Therapie des Upper Airway Cough Syndroms (UACS) empfohlen [3].
Antihistaminika der 2. Generation
Terfenadin
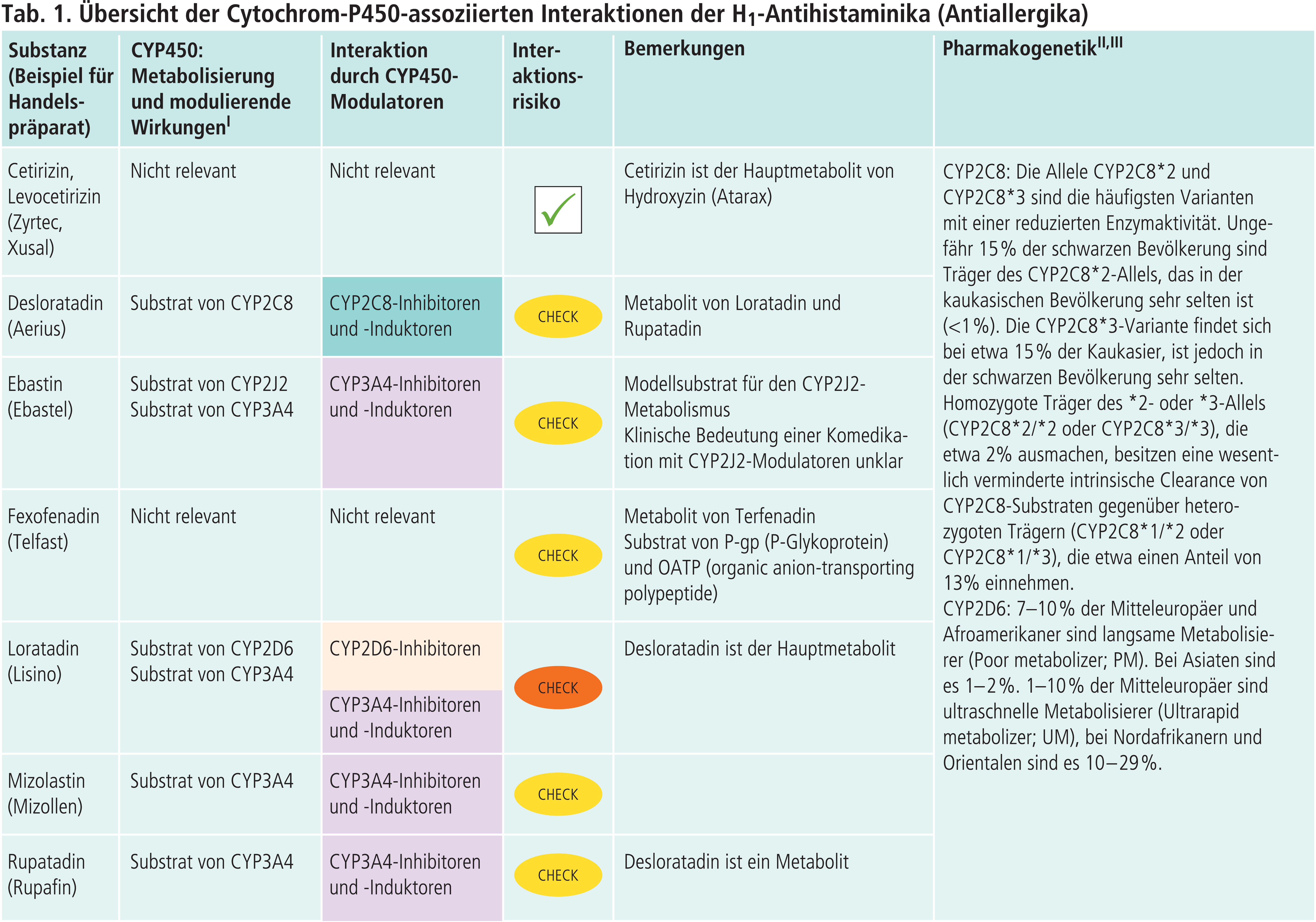
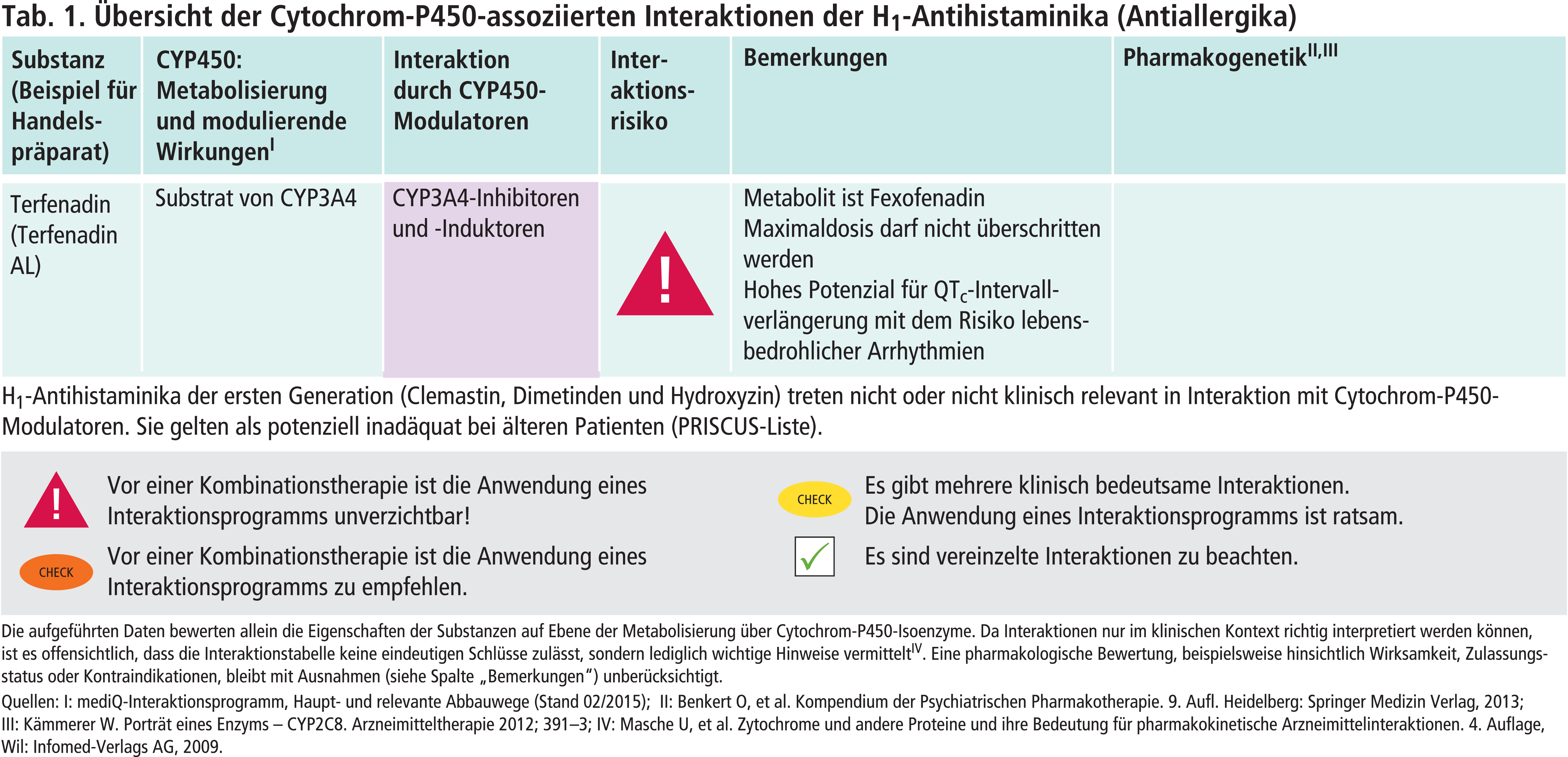
Als früher Vertreter der zweiten Generation ist Terfenadin wegen seines hohen Risikos für kardiale Arrhythmien, insbesondere Torsades de Pointes (TdP), nur noch eingeschränkt verordnungsfähig [7]. Aus demselben Grund sind Astemizol-haltige Arzneimittel weltweit außer Handel. Terfenadin wird über CYP3A4 zu Fexofenadin abgebaut. Kontraindiziert ist Terfenadin bei gleichzeitiger Behandlung mit CYP3A4-Inhibitoren. Hierunter fallen auch Antimykotika und Makrolid-Antibiotika, die topisch angewendet werden [7].
Fexofenadin
Andere Substanzen der zweiten Generation wie Fexofenadin haben eine große therapeutische Breite und in der zugelassenen Dosierung ein geringes bis gar kein QTc-verlängerndes Potenzial [9]. Fexofenadin ist Substrat des Effluxtransporters P-Glykoprotein (P-gp) und des Aufnahmetransporters OATP (organic anion-transporting polypeptide) [2].
Substrate von intestinalem P-gp werden aus den Enterozyten zurück in das Darmlumen gepumpt. Intestinale OATP-Transporter fördern die Resorption, hepatische OATP-Transporter die Aufnahme in die Leberzelle. Klinisch folgt hieraus, dass Induktoren von intestinalem P-gp (z.B. Carbamazepin) die AUC(Area under the curve)-Werte von Fexofenadin senken, während Inhibitoren (z.B. Itraconazol, Verapamil) diese erhöhen [1]. Rifampicin induziert P-gp und hemmt hepatische OATP. In Summe überwiegt bei Komedikation mit Fexofenadin der hemmende Effekt auf die OATP-Transporter, sodass es zu einem Plasmaspiegelanstieg des Antihistaminikums kommt [2]. Die Bioverfügbarkeit sinkt bei Hemmung der intestinalen OATP-Transporter. Eine Wirkungsabschwächung ist daher möglich bei gleichzeitigem Konsum von Fruchsäften wie Apfel-, Grapefruit- und Orangensaft, deren Inhaltsstoffe intestinale OATP-Transporter blockieren [4].
Gemäß Leitlinie ist die empfohlene Therapie der chronischen Urtikaria die symptomatische Behandlung mit einem nichtsedierenden H1-Antihistaminikum [10]. Wenn die Standarddosierung nicht ausreichend wirksam ist, sollte die Dosis bis auf das Vierfache erhöht werden [10]. Vor diesem Hintergrund sollte für jeden einzelnen Wirkstoff geprüft werden, ob eine Komedikation mit CYP-Inhibitoren zu einer klinisch signifikanten Plasmaspiegelsteigerung mit reduziertem Verträglichkeitsprofil führen kann. Beispielsweise erhöht die Verabreichung des starken CYP3A4-Hemmers Ketoconazol die systemische Exposition des CYP3A4-Substrats Rupatadin um das 10-Fache [6]. Loratadin, das primär über CYP3A4 und nachgeordnet über CYP2D6 verstoffwechselt wird, zeigt als trizyklische Substanz bei Überdosierung anticholinerge Nebenwirkungen [5, 8]. Besondere Vorsicht gilt bei Patienten mit Risikofaktoren für eine TdP-Arrhythmie wie Alter >65 Jahre, weibliches Geschlecht, myokardiale Hypertrophie, kongenitales QT-Syndrom, Bradykardien und Elektrolytstörungen [14] sowie bei Komedikation mit proarrhythmogen Arzneimitteln wie Clarithromycin, die selbst CYP3A4 inhibierend wirken (Abb. 1).
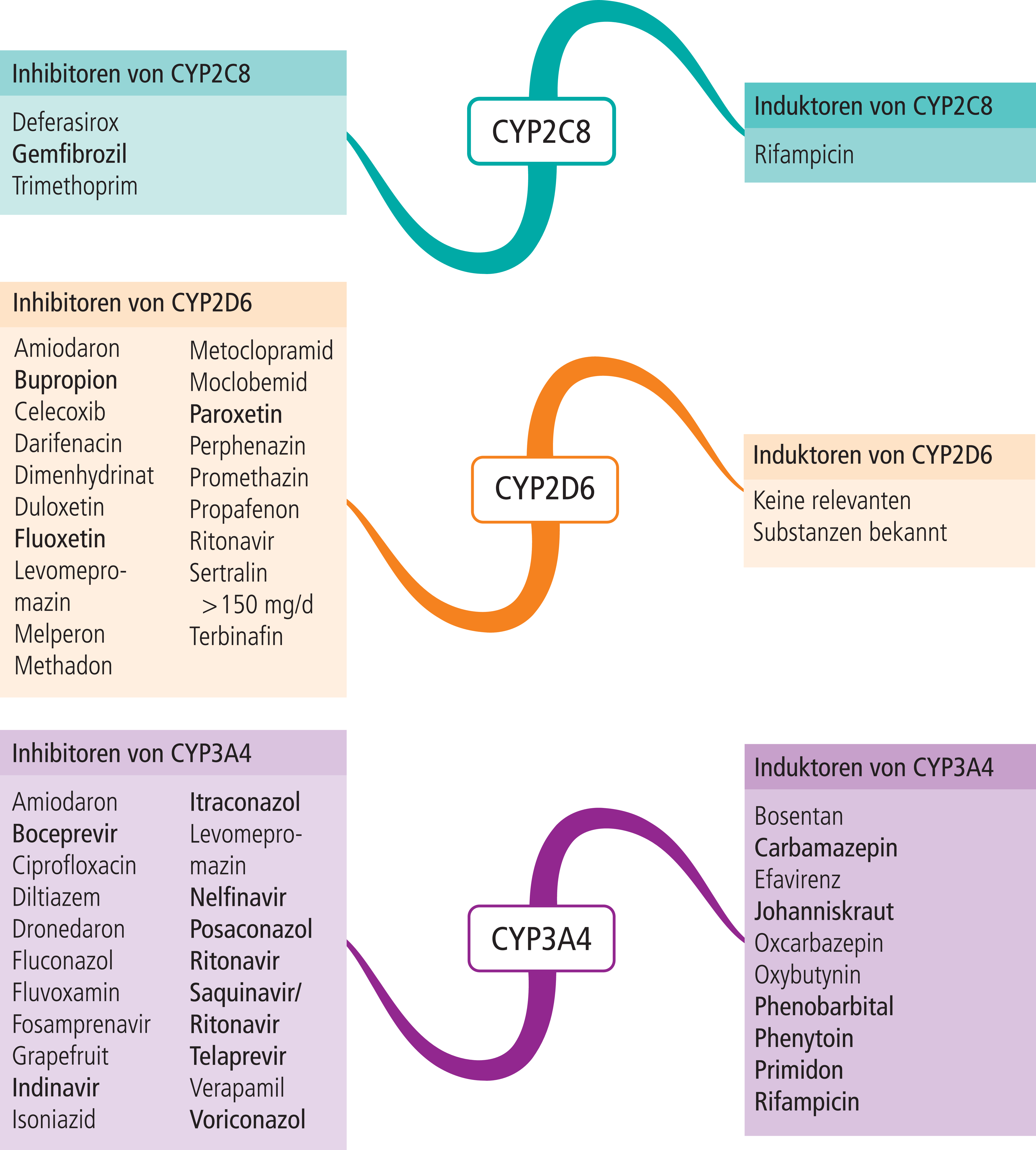
Abb. 1. Auswahl von modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf Cytochrom P450 2C8, 2D6 und 3A4 (Stand: 02/2015) [Quelle: mediQ-Interaktionsprogramm]
Vom pharmakokinetischen Interaktionsprofil sind H1-Antihistaminika der zweiten Generation mit einem inerten Verhalten zu den Cytochrom-P450-Enzymen für die Dosiseskalationstherapie der chronischen Urtikaria zu bevorzugen.
Literatur
1. Akamine Y, et al. Carbamazepine differentially affects the pharmacokinetics of fexofenadine enantionmers. Br J Clin Pharmacol 2011;73:478–81.
2. Akamine Y, et al. Effect of multiple-dose rifampicin 450 mg on the pharmacokinetics of fexofenadine enationmers in Japanese volunteers. J Clin Pharm Ther 2015;40:98–103.
3. DEGAM-Leitlinie Nr. 11: Husten. Stand Februar 2014. www.awmf.org/uploads/tx_szleitlinien/053-013l_S3_Husten_2014-02.pdf (Zugriff am 10.02.2015).
4. Dresser GK, et al. Fruit juices inhibit organic anion transporting polypeptide-mediated drug uptake to decrease the oral availability of fexofenadine. Clin Pharmacol Ther 2002;71:11–20.
5. Fachinformation Loratadin-ratiopharm®. Stand: April 2014.
6. Fachinformation Rupafin®. Stand: Januar 2012.
7. Fachinformation Terfenadin AL 60. Stand: Mai 2012.
8. Ghosal A, et al. Metabolism of loratadine and further characertization of its in vitro metabolites. Drug Metab Lett. 2009;3:162–70.
9. www.mediq.ch/about/interaktionswissen/antihistaminika-und-torsade-de-pointes/ (Zugriff am 10.02.2015).
10. Leitlinie Klassifikation und Diagnostik der Urtikaria – deutschsprachige Version der internationalen S3-Leitlinie (wird zurzeit überprüft). www.awmf.org/uploads/tx_szleitlinien/013-028l_S3_Urtikaria_Klassifikation_Diagnostik_Therapie_2011-abgelaufen.pdf (Zugriff am 10.02.2015).
11. Leitlinie zu Akuttherapie und Management der Anaphylaxie. AWMF-Leitlinien-Register-Nummer 061–025, Fertigstellung 1. Dezember 2013. www.awmf.org/uploads/tx_szleitlinien/061-025l_S2k_Akuttherapie_anaphylaktischer_Reaktionen_2013-12.pdf (Zugriff am 10.02.2015).
12. Mutschler E, et al. Mutschler Arzneimittelwirkungen: 10. Aufl. Stuttgart: Wissenschaftliche Verlagsgesellschaft Stuttgart 2013.
13. PRISCUS-Liste potenziell inadäquater Medikation für ältere Menschen. http://priscus.net/download/PRISCUS-Liste_PRISCUS-TP3_2011.pdf (Zugriff am 10.02.2015).
14. Wenzel-Seifert K, et al. Unerwünschte kardiovaskuläre Wirkungen von Psychopharmaka. Pathophysiologie und Risikominimierung. Psychopharmakotherapie 2013;20:148–57.
*Nachdruck aus Krankenhauspharmazie 2015;36:143–6.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2015; 22(02)
