Bruno Pfuhlmann und Stefan Unterecker, Würzburg
Polypharmazie als Realität in der alltäglichen medizinischen Versorgung
Auch wenn es bis heute keine allgemein anerkannte Definition für Polypharmazie gibt und es strittig ist, ob nun ab einer gleichzeitigen Gabe von mehr als 3, 4 oder 5 Medikamenten von Polypharmazie gesprochen werden soll, muss diese unabhängig von definitorischen Einzelheiten länder- und diagnosenübergreifend als unbestreitbare klinische Realität angesehen werden [5, 9, 13, 24, 35]. Dies gilt sowohl für die Psychopharmakotherapie [24] als auch für allgemeine medikamentöse Therapien [4] und ist speziell beim weiblichen Geschlecht [16] und bei älteren und multimorbiden Patienten [6, 11] bedeutsam. So wurden beispielsweise in einem unselektierten Kollektiv überwiegend hospitalisierter depressiver Patienten im Mittel gleichzeitig 3,9 Psychopharmaka verabreicht [33], während bei älteren Patienten über 65 Jahre insgesamt durchschnittlich fünf Pharmaka gleichzeitig angewendet werden [14] mit weiter steigender Tendenz bei zunehmendem Alter [10]. Hinzu kommt die vielfach betriebene, in ihren Einzelheiten und im Ausmaß jedoch wenig bekannte und auch kaum zuverlässig erfassbare Selbstmedikation (v.a. mit Phytopharmaka). In Bezug auf die Psychopharmakotherapie ist eine begriffliche Unterscheidung zu treffen zwischen einer Kombinationsbehandlung im Sinne einer gleichzeitigen Verordnung von zwei oder mehr Pharmaka derselben Kategorie und der Augmentation im Sinne einer gleichzeitigen Verordnung eines Pharmakons mit einem oder mehreren Pharmaka einer anderen Kategorie.
Gründe für eine Polypharmazie können in einem unzureichenden Erfolg einer Monotherapie liegen, wie bei nicht wenigen Patienten zu beobachten ist, aber auch in einer psychiatrischen oder somatischen Komorbidität, die gerade bei multimorbiden Patienten oft eine Anwendung von mehreren verschiedenen Medikamenten unumgänglich macht, um alle vorliegenden Erkrankungen adäquat behandeln zu können. Die Behandlung oder Verbesserung von unerwünschten Effekten eines unverzichtbaren Medikaments kann ebenfalls einen Grund für eine Polypharmazie darstellen.
Mit einer Polypharmazie ist aber unweigerlich eine Reihe von Problembereichen verbunden, die damit beginnen, dass es zur Effektivität bestimmter Kombinations- oder Augmentationsstrategien nur in seltenen Fällen tatsächlich evidenzbasierte Daten gibt [1, 25, 26], was deren Sinn jedoch nicht prinzipiell infrage stellt. Oftmals sind allerdings polypharmazeutische Strategien klinisch überhaupt nicht hinreichend begründet, was die Probleme umso mehr in den Vordergrund rückt. So ist generell mit steigender Anzahl gleichzeitig einzunehmender Medikamente eine sinkende Adhärenz anzunehmen und ebenso ein steigendes Risiko von Medikationsfehlern [12]. Als Hauptproblem müssen jedoch problematische Arzneimittelinteraktionen angesehen werden. Etwa 7% der Arzneimittelkombinationen werden als gefährlich eingeschätzt, das heißt, etwa jeder 15. Patient mit einer Kombinationstherapie ist davon betroffen [31].
Arzneimittelinteraktionen: allgemeine Grundlagen
Unter einer Arzneimittelinteraktion wird definitionsgemäß die Beeinflussung von Wirksamkeit oder Verträglichkeit eines Medikaments durch ein anderes, gleichzeitig verabreichtes Medikament verstanden. Legt man die Wechselwirkung jeweils zweier Substanzen miteinander zugrunde, so lässt sich die Anzahl möglicher Interaktionspaare (i) aus der Anzahl (n) der gleichzeitig verabreichten Medikamente nach folgender Formel berechnen:
i =(n2 – n)/2
Mit der Anzahl gleichzeitig verabreichter Medikamente steigt also die Anzahl der möglichen Interaktionen. Zudem kann der Metabolismus einer Substanz im Sinne einer zunehmenden Hemmung der Metabolisierung bei steigender Anzahl von Komedikamenten beeinflusst werden, wie am Beispiel von Venlafaxin gezeigt werden konnte [33].
Bei Arzneimittelwechselwirkungen müssen hinsichtlich der zugrundeliegenden Mechanismen pharmakodynamische von pharmakokinetischen Interaktionen unterschieden werden. Pharmakodynamische Interaktionen entstehen, wenn die kombinierten Substanzen an der gleichen Wirkstruktur oder an funktionell verbundenen Strukturen oder Systemen angreifen. Hier wäre etwa die Summierung anticholinerger Effekte bei Gabe mehrerer anticholinerg wirkender Substanzen einzuordnen, die zu schwerwiegenden Nebenwirkungen wie beispielsweise Harnverhalt oder deliranten Syndromen führen kann. Pharmakodynamische Interaktionen stellen die in der Praxis häufigsten Interaktionen dar und bilden im Idealfall auch das Wirkprinzip einer synergistischen Wirkungsverstärkung. Bei Substanzen mit antagonistischer Wirkungsweise kann durch eine derartige Interaktion aber auch eine Wirkungsabschwächung resultieren.
Pharmakokinetische Interaktionen liegen vor, wenn ein Medikament Absorption, Verteilung in den Kompartimenten, Metabolismus oder/und Exkretion eines anderen Medikaments beeinflusst und dadurch dessen Konzentration im Blut beziehungsweise am Wirkort verändert. Solche Interaktionen sind in vielen Fällen glücklicherweise unproblematisch, können in einigen Fällen durchaus nützlich sein, jedoch in einem signifikanten Prozentsatz auch gefährlich bis hin zu lebensbedrohlicher Toxizität. Bei den pharmakokinetischen Arzneimittelinteraktionen sind verschiedene zugrundeliegende Mechanismen denkbar. Die Verdrängung eines Medikaments aus der Plasmaproteinbindung nach Zugabe eines anderen hat dabei in der Psychopharmakotherapie kaum klinische Relevanz [7]. Ob dagegen die Beeinflussung der Absorption eines Arzneistoffs durch Induktion oder Inhibition von Transporterstrukturen wie P-gp durch ein anderes Medikament klinisch Bedeutung hat, ist bislang nicht geklärt [19]. Die Beeinflussung der renalen Exkretion ist ein eher seltener Interaktionsmechanismus, der aber Bedeutung erlangen kann bei Arzneistoffen, die ohne vorherige hepatische Metabolisierung direkt renal eliminiert werden, beispielsweise bei Lithiumsalzen. Als zugrundeliegender Mechanismus der großen Mehrzahl der klinisch-praktisch relevanten pharmakokinetischen Interaktionen ist die Beeinflussung der hepatischen Metabolisierung eines Arzneistoffs durch eine andere Substanz im Wege einer Induktion oder Inhibition von Cytochrom-P450-(CYP450-)Isoenzymen anzusehen [22].
Die klinischen Auswirkungen von pharmakokinetischen Interaktionen können ebenfalls in verschiedene Richtungen gehen. Führt die Interaktion zu einem Anstieg der Arzneistoffkonzentration, kann ein erhöhtes Nebenwirkungsrisiko bei üblicherweise gut verträglichen Dosierungen, gegebenenfalls aber auch ein früher Wirkungseintritt bereits bei niedrigen Dosierungen resultieren. Führt die Interaktion zu einem Abfall der Arzneistoffkonzentration, sind Non-Response oder Wirkungsverlust bei üblicherweise effektiven Dosierungen, gegebenenfalls aber auch Ausbleiben von Nebenwirkungen trotz ungewöhnlich hoher Dosierungen die klinischen Effekte.
Für die Prädiktion des Auftretens von Arzneimittelwechselwirkungen gibt es komplexe mathematische Modelle [2, 23], durch die jedoch die klinische Relevanz einer bestimmten Interaktion nicht beurteilt werden kann. Für die klinische Relevanz einer pharmakokinetischen Interaktion spielt es eine Rolle, ob Arzneistoffe mit geringer therapeutischer Breite betroffen sind, inwieweit eine Konzentrationsabhängigkeit des Effekts (Wirkung, Auftreten von Nebenwirkungen) besteht und ob die Beeinflussung eines Stoffwechselwegs durch alternative Metabolisierungswege ausgeglichen werden kann oder nicht.
Beitrag des TDM zur Verbesserung einer Pharmakotherapie bei Polypharmazie
Therapeutisches Drug-Monitoring (TDM) ermöglicht die Kontrolle des Einflusses pharmakokinetischer Parameter in der Arzneimitteltherapie und ist damit das wichtigste Hilfsmittel zur Identifikation und zum klinischen Management pharmakokinetischer Interaktionen. Es umfasst die Messung der Konzentration eines Arzneistoffs im Plasma oder Serum und die Interpretation des gemessenen Spiegels unter Berücksichtigung des empfohlenen therapeutischen Bereiches, der verabreichten Dosis, eventuell gegebener Komedikation, der beobachteten klinischen Wirkung und eventuell aufgetretener Nebenwirkungen, um daraus Empfehlungen für die weitere Arzneimitteltherapie (z.B. Dosisänderungen, Umstellung der Medikation, Änderungen der Komedikation) ableiten zu können [18].
Hierdurch ergeben sich verschiedene Ansatzpunkte, über die TDM zur Verbesserung einer Pharmakotherapie bei Polypharmazie beitragen kann: vorher nicht absehbare Interaktionen können identifiziert werden, bekannte Interaktionen bei klinisch notwendiger Kombination von Medikamenten mit potenziell problematischem Interaktionspotenzial können überwacht werden und bekannte therapeutisch nutzbare Interaktionen können entsprechend sicher gesteuert werden.
In folgenden klinischen Situationen können unvorhergesehene und potenziell problematische Interaktionen vorliegen, die mittels TDM identifizierbar sind:
- Wirkungsverlust eines Medikaments nach Zugabe einer Komedikation, die als Induktor eines relevanten CYP450-Isoenzyms fungiert → Abfall des Blutspiegels
- Auftreten von Nebenwirkungen nach Zugabe einer Komedikation, die als Inhibitor eines relevanten CYP450-Isoenzyms fungiert → Anstieg des Blutspiegels
- Wirkungsverlust eines Medikaments nach Absetzen einer Komedikation, die als Inhibitor eines relevanten CYP450-Isoenzyms fungiert → Abfall des Blutspiegels
- Auftreten von Nebenwirkungen nach Absetzen einer Komedikation, die als Induktor eines relevanten CYP450-Isoenzyms fungiert → Anstieg des Blutspiegels
Ein Fallbeispiel aus der klinischen Praxis soll dies illustrieren (s. Kasten).
Fallbeispiel
Auftreten schwerer UAW bei Kombination von Amitriptylin und Valproinsäure [34]
- 73-jähriger Patient mit rezidivierender depressiver Störung, zuletzt schwere depressive Episode mit Therapieresistenz auf Mirtazapin und Venlafaxin, auch unter Augmentation mit Lithium und Quetiapin keine ausreichende Besserung. Daher Aufdosierung von Amitriptylin auf 150 mg/Tag; beginnende antidepressive Response, leichter Tremor. Hinzugabe von Valproinsäure als Stimmungsstabilisator, Aufdosierung bis 1200 mg.
- Daraufhin erhebliche Verstärkung des Tremors, zunehmende Schwierigkeiten bei der Selbstversorgung (Nahrungs- und Flüssigkeitszufuhr, Ankleiden), Auftreten von Rigor, Ataxie, Dysarthrie, Somnolenz, Desorientiertheit, Verwirrtheit, Agitiertheit.
- Unter dem Verdacht eines anticholinergen Delirs Pausieren von Amitriptylin und Absetzen von Valproinsäure. Anschließend allmähliche Befundbesserung.
- Eine Klärung der Ursache der UAW konnte durch TDM erfolgen: Die Hinzugabe von Valproinsäure hatte zu einem erheblichen Spiegelanstieg des Trizyklikums geführt (Abb. 1).
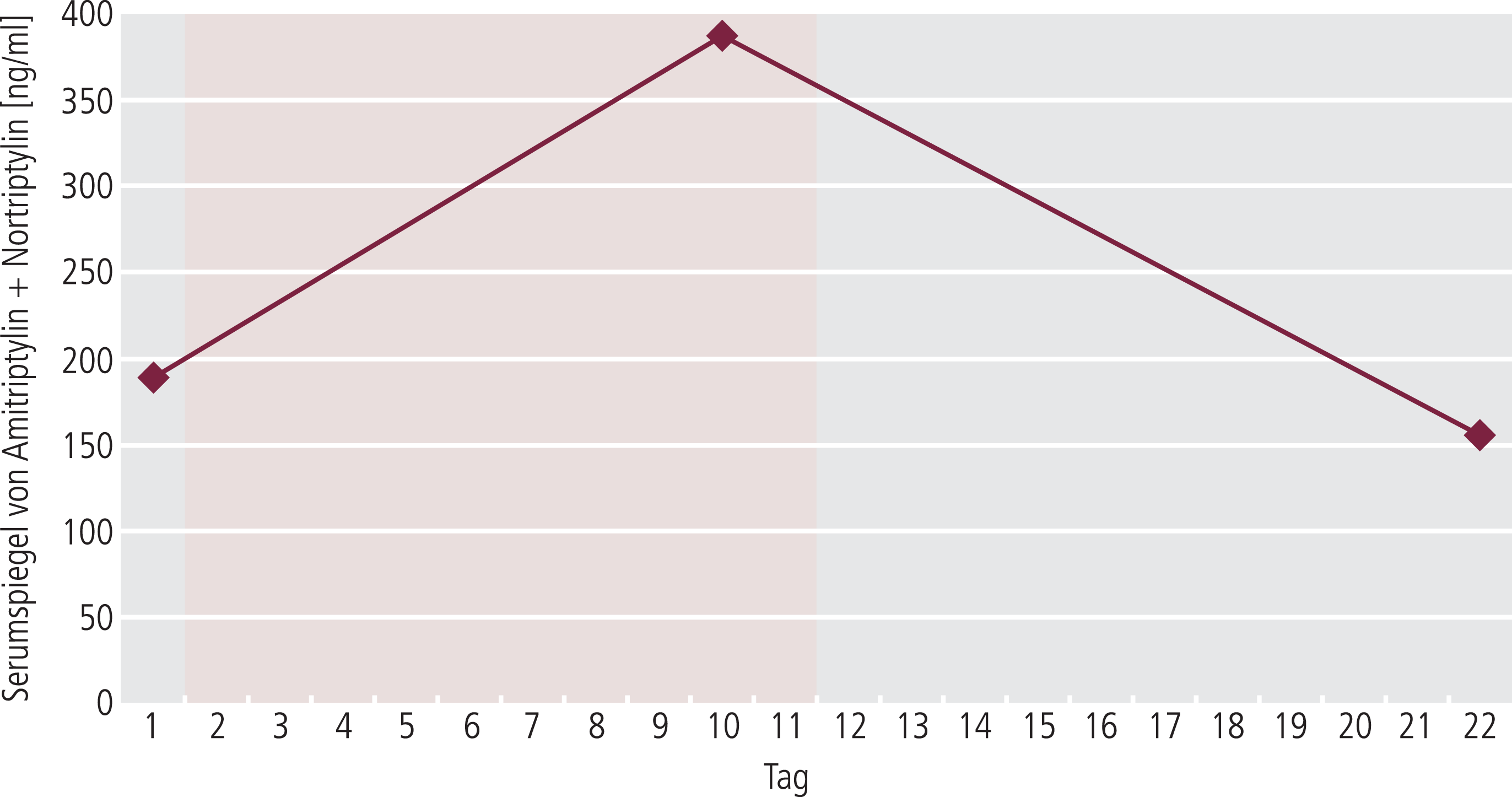
Abb. 1. Serumspiegel von Amitriptylin + Nortriptylin [empfohlener therapeutischer Bereich 80–200 ng/ml] unter 150 mg/Tag Amitriptylin (Saroten®) vor (Tag 1), während (Tag 10) und nach (Tag 22) Valproinsäure-Komedikation; farbig unterlegt: Zeitraum der Valproinsäure-Komedikation
TDM ermöglicht ferner rechtzeitige und individuelle Dosisanpassungen bei klinisch notwendiger Kombination von Medikamenten mit bekanntem Interaktionspotenzial und kann dadurch das Risiko für schwerwiegende Folgen einer Interaktion, beispielsweise gravierende Nebenwirkungen oder Toxizität, minimieren.
Interaktionen können aber auch therapeutisch nutzbar sein und mittels TDM sicher gesteuert werden. So kann durch Hinzugabe eines Inhibitors eines relevanten CYP-Isoenzyms der Serumspiegel eines Arzneistoffs so angehoben werden, dass mit niedrigen Dosierungen bereits therapeutisch wirksame Spiegel erreicht werden, wodurch im Idealfall der therapeutische Effekt bei verbesserter Verträglichkeit gesteigert werden kann. Ein Beispiel hierfür ist die Gabe des selektiven Serotonin-Wiederaufnahmehemmers (SSRI) Fluvoxamin, eines CYP1A2-Inhibitors, bei einer Behandlung mit Clozapin oder Olanzapin, die in der Literatur als in bestimmten Fällen nützlich beschrieben wird [17, 30]. Zur sicheren Steuerung einer solchen kontrollierten Interaktion ist TDM als obligat anzusehen, und die als Inhibitor hinzugegebene Substanz muss sich sinnvoll in das medikamentöse Behandlungskonzept einfügen lassen. Unter diesem Gesichtspunkt wäre etwa eine gezielte Hinzugabe von Ciprofloxacin als Inhibitor des Metabolismus von Clozapin nicht sinnvoll!
Psychopharmaka-Kombinationen mit potenziell kritischem Interaktionspotenzial finden sich im klinischen Alltag nicht selten (Tab. 1) und sollten dann immer mittels TDM kontrolliert werden.
Tab. 1. Im Alltag häufig vorkommende Psychopharmaka-Kombinationen/Augmentationen, die aufgrund ihres Interaktionspotenzials durch TDM überwacht werden sollten
|
Kombination von trizyklischen Antidepressiva (TZA) mit Fluoxetin oder Paroxetin → Spiegelanstieg vieler TZA durch CYP2D6-Inhibition |
|
Kombination von TZA oder Venlafaxin mit Bupropion → Spiegelanstieg bei vielen TZA und bei Venlafaxin durch CYP2D6-Inhibition |
|
Kombination von TZA mit Valproinsäure → Spiegelanstieg bei vielen TZA, Mechanismen nur teilweise klar, wahrscheinlich auch über Inhibition bei CYP450-Isoenzymen |
|
Kombination von Valproinsäure und Lamotrigin → Spiegelanstieg von Lamotrigin durch Inhibition von UGT1A4 (Phase-II-Metabolisierung) |
|
Kombination von Clozapin mit Fluvoxamin → Spiegelanstieg von Clozapin durch CYP1A2-Inhibition |
|
Kombination von Antipsychotika oder Antidepressiva mit Carbamazepin → Spiegelabfall vieler Antipsychotika und Antidepressiva durch CYP1A2- und CYP3A4-Induktion |
CYP: Cytochrom-P450-Isoenzym; UGT1A4: Uridinglucuronyltransferase-Isoenzym 1A4
Besondere Risikokonstellationen stellen Interaktionen bei Arzneistoffen mit geringer therapeutischer Breite und hoher Toxizität dar, aber auch Arzneistoffkombinationen mit sowohl pharmakokinetischem als auch pharmakodynamischem Interaktionspotenzial. Wird beispielsweise das Antibiotikum Ciprofloxacin bei einem Patienten, der Clozapin erhält, hinzugegeben, ist eine pharmakokinetische Interaktion infolge einer CYP1A2-Hemmung durch Ciprofloxacin zu erwarten, durch die der Clozapin-Spiegel im Blut erhöht und bis in toxische Bereiche verschoben werden kann [3, 27]. Gleichzeitig können beide Arzneistoffe pharmakodynamisch interagieren durch einen additiven Effekt einerseits im Hinblick auf eine Senkung der Krampfschwelle mit erhöhter Gefahr von Krampfanfällen [15, 29] und andererseits im Hinblick auf kardiale Reizleitungsstörungen mit der Gefahr maligner Tachyarrhythmien [8, 20]. Diese Kombination sollte demnach wenn möglich vermieden und allenfalls bei dringlicher Indikation unter TDM-gesteuerter Dosisanpassung des Clozapins angewendet werden.
Ein weiteres Beispiel ist die Gabe des Antidepressivums Fluvoxamin bei einem Patienten, der das orale Antikoagulans Phenprocoumon erhält. Hier wird auf Grund einer CYP2C9- und CYP3A4-Hemmung [32] durch Fluvoxamin der Phenprocoumon-Spiegel erhöht und gleichzeitig pharmakodynamisch über verschiedene Mechanismen additiv eine verstärkte Blutungsneigung bewirkt, sodass in der Kombination der pharmakokinetischen und -dynamischen Interaktion eine erhöhte Gefahr insbesondere gastrointestinaler Blutungen entsteht [28]. Eine derartige Kombination ist somit problematisch, da üblicherweise immer auch andere wirksame Antidepressiva zur Verfügung stehen werden, die weder pharmakokinetisch noch pharmakodynamisch mit Phenprocoumon interagieren. Allerdings scheint nach einer neueren großen Fall-Kontroll-Studie kein erhöhtes Blutungsrisiko durch eine Kombination zwischen SSRI und Phenprocoumon zu bestehen [21], sodass das Gefahrenpotenzial hier relativiert werden muss.
Fazit: Was kann TDM bei Polypharmazie zur Verbesserung der Therapie beitragen?
Die Bedeutung von TDM bei polypharmazeutischer Behandlung beruht darauf, dass sich hierdurch pharmakokinetische Interaktionen erfassen und kontrollieren lassen. Damit ist eine Verbesserung der Therapiesteuerung und Erhöhung der Therapiesicherheit bei klinisch notwendiger Kombination von Substanzen mit bekanntem Interaktionspotenzial möglich, aber auch eine Klärung der Ursache sowohl bei unerwartetem Nichtansprechen oder Wirkungsverlust einer Medikation als auch bei Auftreten von unerwarteten oder unerwartet stark ausgeprägten Nebenwirkungen im Zuge einer Medikamentenkombination oder -augmentation mit zuvor unklarem Interaktionspotenzial. Insbesondere in der Behandlung von potenziellen Risikopatienten (z.B. ältere Patienten, Kinder) ist ein solcher Gewinn an Sicherheit von hohem Wert.
Noch weiter gesteigert wird der Nutzen und Informationswert von TDM, wenn bei der Interpretation der gemessenen Arzneistoffspiegel internetbasierte und kontinuierlich aktualisierte Datenbanken zum Stand des Wissens über Arzneimittelinteraktionen wie beispielsweise Psiac (www.psiac.de) oder mediQ (www.mediq.ch) herangezogen werden, was die bestmögliche Abschätzung der potenziellen Risiken, aber auch des möglichen Nutzens einer polypharmazeutischen Behandlung erlaubt.
Interessenkonflikterklärung
Die Autoren haben sonstige Unterstützung (z.B. Ausrüstung, Personal, Unterstützung bei der Ausrichtung einer Veranstaltung) für sich oder die von ihnen vertretene Einrichung erhalten von AstraZeneca, Janssen-Cilag, Lilly und Otsuka (BP) bzw. Lilly, Pfizer und Servier (SU).
Literatur
1. Antai-Otong D. The art of prescribing. Monotherapy antidepressant: a thing of the past? Implications for the treatment of major depressive disorder. Perspect Psychiatr Care 2007; 43:142–5.
2. Bertz RJ, Granneman GR. Use of in vitro and in vivo data to estimate the likelihood of metabolic pharmacokinetic interactions. Clin Pharmacokinet 1997;32:210–58.
3. Brouwers EE, Söhne M, Kuipers S, van Gorp EC, et al. Ciprofloxacin strongly inhibits clozapine metabolism: two case reports. Clin Drug Investig 2009;29:59–63.
4. Cascorbi I. Arzneimittelinteraktionen. Prinzipien, Beispiele und klinische Folgen. Dtsch Ärztebl 2012;109:546–56.
5. Chakos MH, Glick ID, Miller AL, Hamner MB, et al. Baseline use of concomitant psychotropic medications to treat schizophrenia in the CATIE trial. Psychiatr Serv 2006;57:1094–101.
6. Chermá MD, Löfgren UB, Almkvist G, Hallert C, et al. Assessment of the prescription of antidepressant drugs in elderly nursing home patients: a clinical and laboratory follow-up investigation. J Clin Psychopharmacol 2008;28:424–31.
7. DeVane CL. Clinical significance of drug binding, protein binding and binding displacement drug interactions. Psychopharmacol Bull 2002;36:5–21.
8. Dhillon R, Bastiampillai T, Tee K, Vanlint A. Clozapine and associated QTc prolongation. Aust N Z J Psychiatry 2011;45:1098–9.
9. Elmstahl S, Linder H. Polypharmacy and inappropriate drug use among older people – a systematic review. Healthy Aging & Clinical Care in the Elderly 2013;5:1–8.
10. Fialova D, Topinkova E, Gambassi G, Finne-Soveri H, et al. Potentially inappropriate medication use among elderly home care patients in Europe. JAMA 2005;293:1348–58.
11. Field TS, Gurwitz JH, Harrold LR, Rothschild J, et al. Risk factors for adverse drug events among older adults in the ambulatory setting. J Am Geriatr Soc 2004;52:1349–54.
12. Field TS, Mazor KM, Briesacher B, Debellis KR, et al. Adverse drug events resulting from patient errors in older adults. J Am Geriatr Soc 2007;55:271–6.
13. Frye MA, Ketter TA, Leverich GS, Huggins T, et al. The increasing use of polypharmacotherapy for refractory mood disorders: 22 years of study. J Clin Psychiatry 2000;61:9–15.
14. Gallagher PF, Barry PJ, Ryan C, Hartigan I, et al. Inappropriate prescribing in an acutely ill population of elderly patients as determined by Beers’ Criteria. Age Ageing 2008;37:96–101.
15. Haller E, Binder RL. Clozapine and seizures. Am J Psychiatry 1990;147:1069–71.
16. Hausner H, Wittmann M, Hajak G, Haen E. Polypharmazie als geschlechtsspezifisches Phänomen in der Psychiatrie. Psychopharmakotherapie 2008;15:21–3.
17. Hiemke C, Peled A, Jabarin M, Hadjez J, et al. Fluvoxamine augmentation of olanzapine in chronic schizophrenia. Pharmacokinetic interactions and clinical response. J Clin Psychopharmacol 2002;22:502–6.
18. Hiemke C, Baumann P, Bergemann N, Conca A, et al. AGNP consensus guidelines for therapeutic drug monitoring in psychiatry: update 2011. Pharmacopsychiatry 2011;44:195–235.
19. Hiemke C, Baumann P. Pharmakokinetik, Pharmakogenetik und therapeutisches Drug-Monitoring. In: Holsboer F, Gründer G, Benkert O (Hrsg.). Handbuch der Psychopharmakotherapie. Heidelberg: Springer, 2008: 376–97.
20. Ibrahim M, Omar B. Ciprofloxacin-induced torsade de pointes. Am J Emerg Med 2012; 252:5–9.
21. Jobski K, Behr S, Garbe E. Drug interactions with phenprocoumon and the risk of serious haemorrhage: a nested case-control study in a large population-based German database. Eur J Clin Pharmacol 2011;67:941–51.
22. Leucuta SE, Vlase R. Pharmacokinetics and metabolism drug interactions. Curr Clin Pharmacol 2006;1:5–20.
23. Li L, Yu M, Chin R, Lucksiri A, et al. Drug-drug interaction prediction: a Bayesian meta-analysis approach. Stat Med 2007;26: 3700–21.
24. Messer T, Schmauß M (Hrsg.). Polypharmazie in der Behandlung psychischer Erkrankungen. Wien: Springer, 2006.
25. Messer T, Tiltscher C, Schmauß M. Kombinationen von Psychopharmaka. In: Riederer P, Laux G (Hrsg.). Grundlagen der Neuropsychopharmakologie. Ein Therapiehandbuch. Wien, New York: Springer, 2010: 425–49.
26. Post RM, Ketter TA, Pazzaglia PJ, Denicoff K, et al. Rational polypharmacy in the bipolar affective disorders. Epilepsy Res Suppl 1996;11:153–80.
27. Raaska K, Neuvonen PJ. Ciprofloxacin increases serum clozapine and N-desmethylclozapine: a study in patients with schizophrenia. Eur J Clin Pharmacol 2000;56:585–9.
28. Schalekamp T, Klungel OH, Souverein PC, de Boer A. Increased bleeding risk with concurrent use of selective serotonin reuptake inhibitors and coumarins. Arch Intern Med 2008;168:180–5.
29. Slavich IL, Gleffe RF, Haas EJ. Grand mal epileptic seizures during ciprofloxacin therapy. JAMA 1989;261:558–9.
30. Szegedi A, Wiesner J, Hiemke C. Improved efficacy and fewer side effects under clozapine treatment after addition of fluvoxamine. J Clin Psychopharmacol 1995;15:141–3.
31. Thomsen LA, Winterstein AG, Sondergaard B, Haugbolle LS, et al. Systematic review of the incidence and characteristics of preventable adverse drug events in ambulatory care. Ann Pharmacother 2007;41:1411–26.
32. Ufer M. Comparative pharmacokinetics of vitamin K antagonists: warfarin, phenprocoumon and acenocoumarol. Clin Pharmacokinet 2005;44:1227–46.
33. Unterecker S, Hiemke C, Greiner C, Haen E, et al. The effect of age, sex, smoking and co-medication on serum levels of venlafaxine and o-desmethylvenlafaxine under naturalistic conditions. Pharmacopsychiatry 2012;45:229–35.
34. Unterecker S, Burger R, Hohage A, Deckert J, et al. Interaction of valproic acid and amitriptyline – Analysis of therapeutic drug monitoring data under naturalistic conditions. J Clin Psychopharmacol 2013 (accepted for publication).
35. Zarate CA Jr, Quiroz JA. Combination treatment in bipolar disorder: a review of controlled trials. Bipolar Disord 2003;5:217–25.
Prof. Dr.med. Bruno Pfuhlmann, Dr. med. Stefan Unterecker, Klinik und Poliklinik für Psychiatrie, Psychosomatik und Psychotherapie, Universitätsklinikum Würzburg, Füchsleinstraße 15, 97080 Würzburg, E-Mail: Pfuhlmann_B@klinik.uni-wuerzburg.de
Polypharmacy in psychopharmacotherapy: Can therapeutic drug monitoring contribute to an improved treatment?
Polypharmacy is widely used in somatic as well as psychiatric pharmacotherapy and is often indispensable due to multimorbidity or insufficient response to treatment with a single drug. However, with an increasing number of simultaneously applied drugs the probability of pharmacodynamic or pharmacokinetic drug-drug interactions is increasing. Such interactions may result in therapeutically useful additive effects as well as in an elevated risk of adverse effects up to intoxication.
Examples of drug combinations from everyday clinical practice demonstrate, how therapeutic drug monitoring (TDM) can help to identify and control pharmacokinetic interactions. In particular, the problematic consequences of a drug-drug interaction like lack of response or occurrence of serious adverse effects could be resolved by TDM. TDM therefore represents the most important tool for the management of such interactions and should be regularly applied to optimize safety and efficacy of polypharmaceutic treatment.
Key words: Polypharmacy, psychopharmacotherapy, therapeutic drug monitoring, interactions
Psychopharmakotherapie 2013; 20(04)
