Pierre Baumann, Prilly-Lausanne, und Olivier Trégouët, La Chaux-de-Fonds
Absorption, Distribution (Verteilung), Metabolismus und Eliminierung (ADME) bestimmen das Schicksal eines Medikaments im Organismus. Restriktive chirurgische Eingriffe im Magen-Darm-Bereich üben deshalb einen Einfluss auf die Absorption und den Metabolismus eines enteral verabreichten Medikaments aus. Solche Eingriffe werden vorgenommen bei Patienten mit Magenkrebs und bei Patienten, die in suizidaler Absicht giftige, den Verdauungstrakt zerstörende Substanzen eingenommen haben. Als bariatrische Eingriffe bezeichnet, werden sie heute zunehmend bei stark übergewichtigen Patienten ausgeführt. Die vor zehn Jahren geschätzte Anzahl von weltweit 1,7 Milliarden an Übergewicht leidenden Menschen dürfte sich inzwischen noch erhöht haben [6]. Bariatrische Chirurgie ist weltweit ein relativ häufiger Eingriff; so waren es beispielsweise 350000 Operationen im Jahre 2008. Sie hat zum Ziel, durch eine chirurgische Restriktion im Bereich des Magen-Darm-Trakts eine Verminderung der Nahrungsaufnahme in den Organismus und somit eine Gewichtsreduktion beim Patienten zu bewirken [4, 24, 25]. Die am häufigsten angewandten Techniken sind Roux-en-Y-Bypass, Anlegen eines Magenbands und zu einem geringeren Prozentsatz Magenschlauchbildung [20, 24, 32]. Ein Kurzdarmsyndrom entsteht unter anderem als Folge einer operativen Entfernung von 50 bis 70% des Dünndarms [36]. Bariatrische Chirurgie ist nach Metaanalysen effizient [4]. Dennoch fehlt es an Langzeituntersuchungen (>5 Jahre) über die Mortalität und Komorbidität im Zusammenhang mit Übergewicht [24], obwohl inzwischen schon bei Hunderttausenden von Patienten eine bariatrische Operation vollzogen wurde.
Patienten mit Schizophrenie oder Depression neigen zu Übergewicht; der Prozentsatz von Übergewichtigen bei Patienten mit einer mentalen Störung ist höher als bei psychisch Gesunden [1]. Eine amerikanische Prävalenzstudie zeigt beispielsweise, dass 29% der Männer und 60% der Frauen mit schwerer und persistierender psychiatrischer Erkrankung an Übergewicht leiden. Bei Männern und Frauen einer Kontrollgruppe aus der NHANES-III-Studie (Third National Health and Nutrition Examination Survey) betrugen die Prävalenzen 17,7% respektive 28,5%. In einer deutschen Studie zeigte sich, dass ungefähr die Hälfte der Patienten, bei denen eine bariatrische Operation wegen Übergewicht geplant war, an psychiatrischen Störungen leidet, wobei Essstörungen und affektive Störungen einen hohen Prozentsatz ausmachen [22], – aber auch Angststörungen sind häufig [29].
Viele Patienten werden deshalb vor und nach solchen Eingriffen mit Psychopharmaka behandelt. Überraschenderweise wurden aber bisher kaum Studien zur Pharmakokinetik von psychotropen Pharmaka bei solchen Patienten veröffentlicht.
Eine kurze Literaturübersicht wird hier eingeleitet von der Beschreibung eines Falls, der sich im Zusammenhang mit der Behandlung eines depressiven Patienten mit Antidepressiva nach einer Gastrektomie infolge eines Magenkarzinoms ereignete. Der Verlauf des Wirkstoffplasmaspiegels wurde mittels therapeutischem Drug-Monitoring (TDM) dokumentiert.
Fallbeschreibung
Bei dem männlichen, 77-jährigen Patienten wurde 2010 durch Zufall ein Adenokarzinom im Magen entdeckt. Zunächst wurde er zwischen Juni und August 2010 dreimal mit Chemotherapie nach Schema ECF (Epirubicin, Cisplatin, Fluorouracil) behandelt, aber dann im September 2010 einer totalen Gastrektomie unterzogen. Die Zeit zwischen dem 8. Juli und dem 12. August 2011 verbrachte der Patient wegen einer schweren Unterernährung als Folge einer Malabsorption nach Gastrektomie zunächst in der internistischen Abteilung einer somatischen Klinik und dann in einer somatischen Rehabilitationsklinik. Der bei einer Größe von 167 cm nur noch 47 kg (BMI: 16,9) schwere Patient wurde mittels einer nasogastrischen Sonde enteral ernährt. Im Verlauf der somatischen Hospitalisierung wurde bei ihm eine mittelgradige bis schwere depressive Episode mit somatischem Syndrom (F32.11) diagnostiziert, mit nach DSM-IV-TR-Kriterien melancholischen Zügen. Anamnestisch ist zu erwähnen, dass der Patient bereits 1970 an einer Depression gelitten hatte, die aber nicht medikamentös behandelt wurde, sowie in der Zwischenzeit und aktuell an einem gastroduodenalen Ulkus, an einer rechten femoral axonalen Mononeuropathie sowie an Osteoporose mit Wirbelkörperkompression. Der Patient hatte bereits mit 60 Jahren das Rauchen eingestellt.
Ein Thorax-Abdomen-Pelvis-CT-Scan erbrachte am 8. Juli keinen Hinweis für ein Rezidiv des Tumors (Remission). Im Laufe der Hospitalisierung wurde der Patient von Morphin (MST®) entwöhnt, das ihm wegen Rückenschmerzen (L5S1) verschrieben worden war. Im Weiteren wurde er je nach Bedarf mit Paracetamol behandelt.
Zur Behandlung der depressiven Episode wurde zunächst eine Therapie mit 20 mg/Tag Citalopram (in Tablettenform) begonnen. Wegen schwerer Nebenwirkungen (Übelkeit, Erbrechen, Durchfall, Anorexie) wurde das Medikament bald abgesetzt und nach 12 Tagen durch eine abendliche Gabe von 30 mg/Tag Mirtazapin (Remeron®, in Tablettenform) ersetzt.
Zwei Wochen später (Mitte August) wurde der Patient entlassen und weiter ambulant behandelt. Zum Zeitpunkt der Entlassung betrug das Gewicht des Patienten 50,5 kg, weshalb die enterale Ernährung (500 ml/24 h) schrittweise durch eine zunehmende orale Ernährung ersetzt wurde. Es wurde eine langsame Verbesserung der depressiven Symptomatik festgestellt, ebenso eine Gewichts- und Appetitzunahme. Zwar verbesserte sich die Schlafdauer, aber nicht die Schlafqualität. Besonders am Morgen litt der Patient noch an ausgeprägten Stimmungsschwankungen, an einer refraktären Asthenie, Irritabilität, Dysphorie und Anhedonie. Die Mirtazapin-Dosis wurde deshalb am 21. Oktober von 30 mg/Tag auf 45 mg/Tag (eine Tablette abends nach der Mahlzeit) erhöht. Am 11. November wurde eine deutliche Verbesserung der Depression festgestellt: Zunahme der Libido, von Appetit, Abnahme von Asthenie, – das Gewicht normalisierte sich bei 58 kg (BMI: 20,8). Der Patient berichtete über wenig störende Nebenwirkungen, die der Mirtazapin-Behandlung zugeschrieben wurden: abendliche Palpitationen, Probleme der Orthostase beim Aufstehen, Glieder- und Brustschmerzen (Mammae).
Am 26. Januar 2012 wurde eine vollständige Remission der depressiven Episode festgestellt, bei abgeschwächten Nebenwirkungen, die am 8. März völlig abgeklungen waren. Zu diesem Zeitpunkt wurde die Zugabe von ergänzenden Nährstoffen unterbrochen, nachdem das Körpergewicht über mehrere Monate bei 59 kg stabilisiert war. Nachdem auch keine intestinalen Störungen mehr vorlagen, wurde die Schmerzbehandlung (Niveau 1) mit Paracetamol, aber nicht die antidepressive Therapie mit Mirtazapin (45 mg/Tag, abends) abgesetzt. Wegen Osteoporose wurde im Januar 2012 eine einmalige intravenöse Behandlung mit Zoledronsäure vorgenommen.
Regelmäßig wurden Plasmaspiegel von Mirtazapin gemessen, jeweils strikt zum gleichen Zeitpunkt, nämlich nüchtern morgens um 8 Uhr. Auch die Medikamenteneinnahme fand regelmäßig, nämlich stets nach der Abendmahlzeit um 21 bis 22 Uhr statt. Die Plasmakonzentrationen von Mirtazapin betrugen im Zeitraum vom 20. September 2011 bis 9. November 2011 zwischen 26 und 27 ng/ml. Nach der Dosiserhöhung von 30 mg/Tag auf 45 mg/Tag stiegen sie auf 34 bis 41 ng/ml (3 Messungen zwischen dem 09.11.2011 und dem 12.06.2012; therapeutischer Bereich: 30–80 ng/ml) [13].
Für den dosiskorrigierten Bereich ergeben sich folgende Werte: 26 ng/ml nach Einnahme von 30 mg/Tag entsprechen 0,87 ng/(ml·mg); 34 ng/ml nach Einnahme von 45 mg/Tag entsprechen 0,76 ng/(ml·mg); die Literaturwerte liegen bei 0,37 bis 0,85 ng/(ml·mg) [13, 34].
Die Messergebnisse weisen darauf hin, dass bei dem Patienten die Mirtazapin-Plasmaspiegel im Bereich derer lagen, die auch bei unversehrten behandelten Patienten oder Versuchspersonen gemessen werden. Mit der niedrigeren Dosis von 30 mg/Tag wurde der therapeutische Bereich jedoch nicht erreicht, sondern erst bei der höheren Dosis (45 mg/Tag).
Der behandelnde Arzt sieht sich in einer solchen Situation mit der Frage konfrontiert, wieweit eine Gastrektomie die Absorption des Antidepressivums beeinflusst und ob eine eventuell verminderte Absorption die Aussichten auf einen Therapieerfolg beeinträchtigt. Therapeutisches Drug-Monitoring erwies sich hier als wertvolles Werkzeug. Zwar wurde keine vollständige Pharmakokinetik von Mirtazapin bei diesem Patienten gemessen, aber die gemessenen Gleichgewichtskonzentrationen unterschieden sich nicht von denen von Patienten, welche keine Gastrektomie erfahren hatten. Somit wäre dies ein erster Hinweis dafür, dass ein solcher Eingriff keine Wirkung auf die Absorption von Mirtazapin hat.
Pharmakokinetik psychotroper Pharmaka nach restriktiver gastrointestinaler Chirurgie
Restriktive gastrointestinale Eingriffe
Restriktive gastrointestinale Eingriffe unterscheiden sich je nach angewandter Technik, indem Teile des Magens, der gesamte Magen und unterschiedliche Teile des Darmtrakts chirurgisch entfernt respektive umgangen werden. Dies hat unterschiedliche Konsequenzen für die Aufnahme (Absorption) von enteral verabreichten Medikamenten, verbunden mit einem Risiko von Malabsorption. Bei jedem Patienten müssen deshalb die möglichen Auswirkungen individuell eingeschätzt werden, beispielsweise nach Gastrektomie infolge Magenkrebses oder Vergiftung durch magenzerstörerische Substanzen, oder nach einer bariatrischen Operation.
Bei bariatrischer Intervention werden vor allem zwei Techniken verwendet, die zu Malabsorption führen können [7, 20]:
- Roux-en-Y-gastrischer Bypass: Nach beträchtlicher Reduktion des Magens und Durchtrennung des Dünndarms wird der entstehende kleine Vormagen mit dem Dünndarm verbunden, sodass eine Umgehung des Duodenums und von 50 bis 70 cm des Jejunums resultiert.
- Biliopankreatische Diversion mit duodenalem Switch: Der Magen wird schlauchförmig reduziert und mit dem Ileum verbunden, was zu einer 60%igen Umgehung des Dünndarms führt.
Es gibt Hinweise, dass nach bariatrischer Chirurgie der Bedarf an Medikamenten sinkt. Betroffen sind wenig überraschend solche Medikamente, die in einem eher direkten Zusammenhang mit Übergewicht verschrieben werden, wie Medikamente gegen Diabetes mellitus Typ 2 oder kardiovaskuläre Erkrankungen [9, 18]. Hingegen wird zumindest im ersten Jahr nach der Intervention keine Veränderung in Bezug auf die Verschreibungshäufigkeit von Antidepressiva festgestellt [18].
Bei übergewichtigen, an Diabetes mellitus Typ 2 leidenden Patienten wird zudem vermutet, dass nicht nur die Gewichtsreduktion, sondern auch eine Veränderung im hormonalen Haushalt für eine Verbesserung der klinischen Befindlichkeit und in häufigen Fällen zu einer Remission des Diabetes führt. Die Spiegel von Appetit anregendem Ghrelin werden reduziert, Sättigung signalisierende Stoffe wie GLP-1 und Peptid YY nehmen zu [9].
Diese Interventionen haben eine eher positive Auswirkung auf den psychosozialen Status (Lebensqualität) der operierten Patienten, aber Studienergebnisse über Auswirkungen auf psychiatrische Komorbiditäten wie Depression und Suizidalität sind widersprüchlich [35].
Allgemeine pharmakokinetische Konsequenzen (Tab. 1; Abb. 1)
Die gastrointestinale Aufnahme von Wirkstoffen hängt von mehreren Faktoren ab [30]: vom pH des Milieus, der Oberfläche des betroffenen Organs, der Peristaltik, der Permeabilität, der Durchblutung, der Anwesenheit von Nahrung und von Xenobiotika. Sie hängt auch ab von den Eigenschaften des Medikaments: galenische Zubereitung des Wirkstoffs, Löslichkeit in Wasser respektive im hydrophoben Milieu, seiner Eigenschaften als Säure oder Base, seiner Polarität, der Größe des Moleküls. Durch eine Verkleinerung des Magens wird die Produktion von Magensäure verringert, was sich auf den pH des Darms auswirkt. Die Aufnahme von Wirkstoffen und die Permeabilität vom Darm in das Blut hängt bei operierten Patienten von der Länge des noch vorhandenen Dünndarms ab, zumal die Oberfläche pro Längeneinheit vom Duodenum zum Rektum abnimmt [30].
Tab. 1. Faktoren, die Einfluss auf die Aufnahme (Absorption) von psychotropen Wirkstoffen ausüben [6, 7, 19]
|
Pharmazeutische Phase |
|
Galenische Form des Medikaments |
|
Auflösungseigenschaften der galenischen Form (Desintegration, Auflösungsgeschwindigkeit) |
|
Säure-Basen-Eigenschaften des Arzneistoffs (pKa) |
|
Wasser- bzw. Fettlöslichkeit |
|
Gastrointestinale Situation |
|
Art des restriktiven Eingriffs |
|
Entleerungsgeschwindigkeit des verbleibenden Magens |
|
Länge des Magen-Darm-Trakts |
|
Für die Absorption zur Verfügung stehende Oberfläche des Magen-Darm-Trakts |
|
pH des Darms nach Gastrektomie |
|
Motilität des Darms |
|
Transitzeit für das Medikament |
|
Verteilung im Magen-Darm-Trakt von Cytochrom P450 und p-Glykoprotein |
|
Anwesenheit von Gallensalzen |
|
Pharmakokinetik des Arzneistoffs |
|
Absorptionsstelle und Aufnahmegeschwindigkeit (tmax) im Magen-Darm-Trakt |
|
Substrateigenschaften gegenüber Cytochrom P450, konjugierenden Enzymen, p-Glykoprotein, … |
|
Einfluss von Nahrung |
|
Pharmakogenetischer Status |
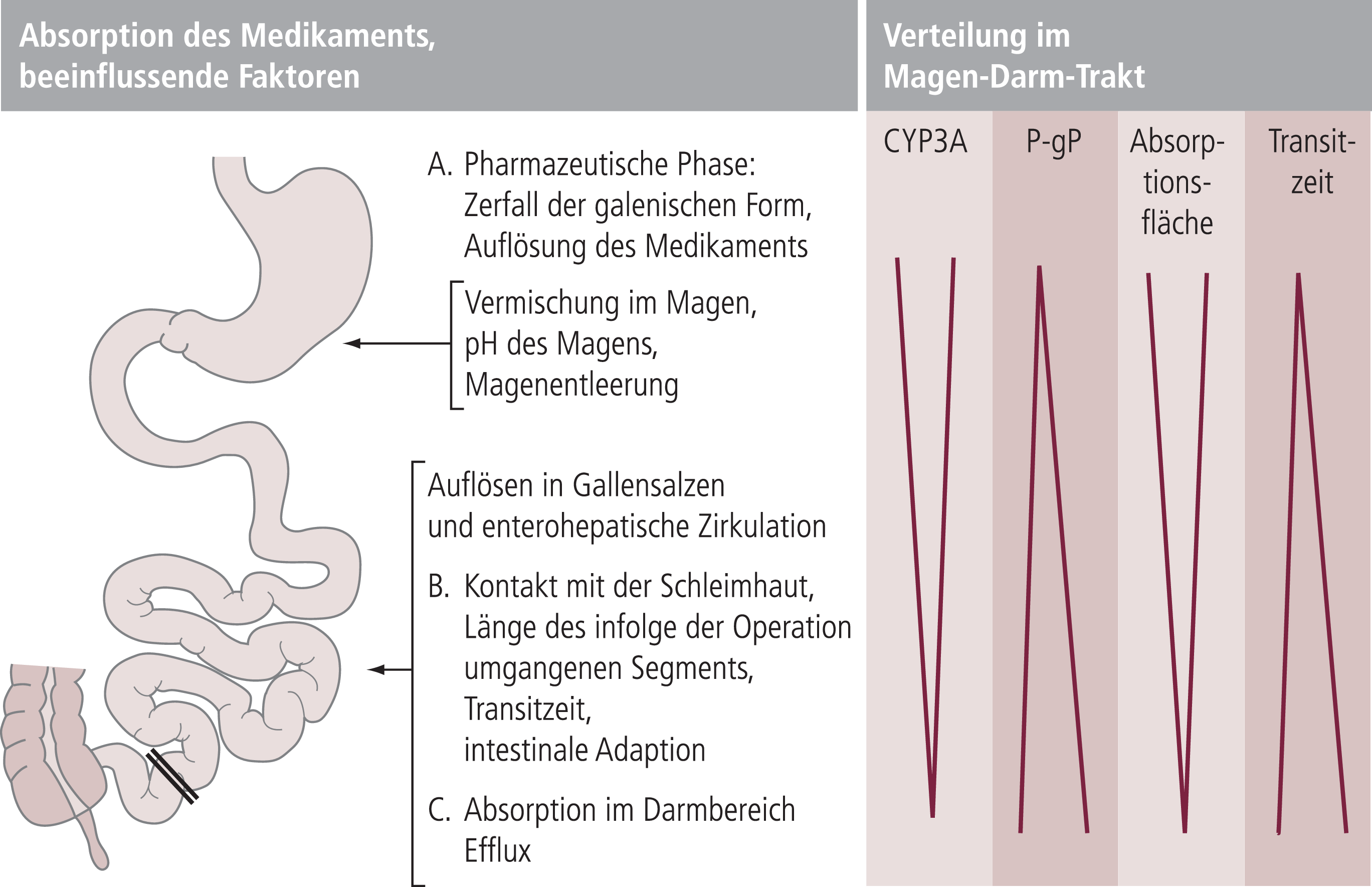
Abb. 1. Überblick über die regionale Verteilung von Faktoren im Magen-Darm-Trakt, welche die Absorption von Medikamenten beeinflussen [nach 23]. CYP3A: Cytochrom P450-3A; P-gP: P-Glykoprotein
Man würde annehmen, dass mit der Kenntnis des Verteilungskoeffizienten zwischen wässrigem und hydrophobem Milieu (log P) sowie des Ionisierungsgrads des Moleküls das Maß seiner Aufnahme in den Blutkreislauf vorhersagbar ist. Dies ist nicht der Fall. Tatsächlich muss in Betracht gezogen werden, dass die Oberfläche des Darms, die für die Aufnahme von Molekülen zur Verfügung steht, diejenige des Magens weit übersteigt. Deshalb werden selbst ionisierte Moleküle allgemein im Darm besser, d.h. in größerem Umfang aufgenommen als im Magen [2].
Obwohl der proximale Teil des Dünndarms eine größere Oberfläche als der distale aufweist, ist die Transitperiode in Letzterem länger, weshalb in diesem Abschnitt die Aufnahme von Arzneistoffen größer ist. Zusätzlich kompliziert wird die Voraussagbarkeit der Aufnahmekapazität dadurch, dass sich nach chirurgischen Interventionen Adaptionsphänomene entwickeln (Hypertrophie der Schleimhaut), wodurch sich die Aufnahme von Arzneistoffen kompensatorisch erhöht [23].
Im Magen- und Darmbereich befinden sich Transportmoleküle und Enzyme, die durch eine Transporthemmung oder durch präsystemischen enzymatischen Abbau die Aufnahme von Substraten in den Blutkreislauf beeinträchtigen. Transportproteine wie P-Glykoprotein (MDR1), Enzyme vom Typ Cytochrom P450 (insbesondere CYP3A4) und glucurokonjugierende Enzyme sind hier von Bedeutung [19, 32]. Das für den Abbau von zahlreichen Arzneistoffen wichtige CYP3A weist im Duodenum die höchste mRNS-Expression auf [33]. Andererseits nimmt die MDR-mRNS vom Duodenum zum Kolon hin signifikant zu [33]. Die Konzentration von P-Glykoprotein verdoppelt sich vom proximalen zum distalen Darm und anscheinend auch seine Aktivität [21]. Für Arzneistoffe, die Substrat von sowohl CYP3A als auch P-Glykoprotein sind, gilt also vermutlich, dass ihre systemische Aufnahme im oberen Darmteil von CYP3A und für die Anteile, die hier nicht metabolisiert wurden, im distalen Teil durch P-Glykoprotein beeinträchtigt wird.
Es stellt sich auch die Frage, ob und wieweit sich übergewichtige Patienten von normalgewichtigen Patienten bezüglich der Pharmakokinetik nach einer restriktiven gastrointestinalen Intervention unterscheiden. Die Analyse von Jain et al. (2011) [14] zeigt klar, dass ein Mangel an Studien zur Pharmakokinetik von Arzneistoffen bei stark übergewichtigen, nicht bariatrisch operierten Patienten besteht. Häufig ist bei übergewichtigen im Vergleich zu normalgewichtigen Patienten das Verteilungsvolumen von Arzneistoffen größer, ebenso die Clearance; dies gilt aber eben nicht für alle Arzneistoffe [12, 17]. So ist beispielsweise das Verhältnis der durch das Gesamtkörpergewicht normalisierten Verteilungsvolumina bei übergewichtigen Patienten im Vergleich zu nicht-übergewichtigen Personen >1 für Diazepam, Sulfentanil, Verapamil und Trazodon, aber <1 für Digoxin, Ciclosporin, Atracurium und Methylprednisolon, und ca. 1 für Lorazepam, obwohl alle Arzneistoffe ähnlich lipophil sind (mit log P, als Maß für ihre Lipidlöslichkeit, >0) [14]. Obwohl Coffein vergleichsweise hydrophil und Lorazepam lipophil ist, ist für beide Verbindungen der Wert gleich (=1), d.h. es gibt keine Unterschiede in den Verteilungsvolumina zwischen Übergewichtigen und nicht Übergewichtigen. Auffallenderweise haben mehrere lipophile Arzneistoffe (mit log P >1) bei übergewichtigen Patienten kleinere Verteilungsvolumina als bei normalgewichtigen Personen, deshalb müssen noch andere Faktoren für die Verteilung der Verbindungen eine entscheidende Rolle spielen, beispielsweise die Eiweißbindung im Blut. Es hat sich auch gezeigt, dass für manche Verbindungen bei starkem Übergewicht keine proportionale Zunahme des Verteilungsvolumens mehr stattfinden kann, also eine Sättigung eintritt oder keine ebenmäßige Verteilung mehr stattfindet [14].
Erkenntnisse für einzelne Vertreter einer Medikamentenklasse gestatten demnach keine Übertragung auf andere Wirkstoffe innerhalb der gleichen Klasse. Es wird deshalb gefordert, dass zur Zulassung von Medikamenten entsprechende Daten nicht nur bei Patienten mit Leber- oder Niereninsuffizienz, sondern auch bei stark übergewichtigen Patienten und erhoben werden, und dann in den Fachinformationen entsprechende Behandlungsempfehlungen aufgeführt werden sollten.
Noch magerer ist die Datenlage zur Pharmakokinetik bei bariatrisch operierten Patienten. Ein der Pharmakokinetik bei „besonderen Populationen“ gewidmeter Artikel [26] erwähnt die Situation dieser Patienten interessanterweise gar nicht. Und selbst mehrere Übersichtsartikel, die sich spezifisch mit diesem Thema befassen [7, 20, 23, 32, 36], belegen nur, dass eigentlich wenige Studien zu diesem Thema veröffentlicht wurden. Immerhin, bei übergewichtigen Patienten, die nach einer bariatrischen Operation bedeutend an Gewicht verloren haben, muss häufig, aber nicht immer mit einer Erniedrigung des Verteilungsvolumens eines Arzneistoffs gerechnet werden [14, 26]. Es gibt keine Studien, die dazu konkrete Daten liefern.
Pharmakokinetische Studien über psychotrope Pharmaka
Bei psychotropen Pharmaka vom Typ Antidepressiva oder Antipsychotika handelt es sich meist um basische Verbindungen, die bevorzugt im Darm und weniger im Magen aufgenommen werden. Diese zuvor erwähnten Übersichtsarbeiten [7, 20, 24, 32, 36] beziehen alle Medikamente ein, im Folgenden werden aber nur die Ergebnisse von Studien über psychotrope Pharmaka zusammengefasst.
Antidepressiva
Der erste Schritt des Absorptionsprozesses ist die Auflösung des pharmazeutischen Produkts im jeweiligen Milieu, wie es im gastrointestinalen Bereich vorkommt. Eine Arbeitsgruppe [31] hat dies anhand eines Modells untersucht, indem die Löslichkeit von psychotropen Pharmaka unter präoperativen Bedingungen und dann unter solchen nach Roux-en-Y-Interventionen bestimmt wurde. Die Löslichkeit der meisten Arzneistoffe war unter postoperativen Bedingungen signifikant geringer (Amitriptylin, Fluoxetin, Paroxetin, Sertralin, Clozapin, Olanzapin, Quetiapin, Risperidon, Ziprasidon, Lithiumcarbonat). Unverändert war sie für Citalopram, Venlafaxin, Trazodon, Haloperidol und für die meisten Tranquilizer; für Bupropion war sie sogar größer.
Trizyklische Antidepressiva. Zwei Falluntersuchungen bei depressiven Patienten mit Kurzdarmsyndrom zeigten keine Auffälligkeiten der Plasmaspiegel von Amitriptylin [27] und Nortriptylin [3] während einer Behandlung mit dem einen respektive dem anderen Medikament. Bei der mit Amitriptylin behandelten Patientin wies der proximale Dünndarm noch eine Länge von 45 cm auf, bei der mit Nortriptylin behandelten Patientin war der Dünndarm noch 150 bis 180 cm lang. Die Amitriptylin-Tabletten wurden vor der Verabreichung zu Pulver verarbeitet; zur Verabreichungsart von Nortriptylin liegen keine diesbezüglichen Angaben vor.
Eine 55-jährige Patientin mit rekurrenter Depression verübte einen Suizidversuch mit Natronlauge [5]. Nach einer Ösogastrektomie und cephalischer Pankreatoduodenektomie traten metabolische Probleme auf, die die Gabe von Nahrungszusätzen und eine medikamentöse Behandlung mit subkutanem Insulin und Pankreasenzymen bedingten. Im Gegensatz zu früheren Episoden sprachen nun neue depressive Episoden nicht mehr auf Antidepressiva an. Wegen Anästhesie-Kontraindikationen wurde auf eine EKT-Behandlung verzichtet, eine intravenöse Therapie mit Antidepressiva wurde von der Patientin zurückgewiesen. Eine orale abendliche Behandlung mit 2,5 Clomipramin-Tabletten à 75 mg brachte innerhalb vier Wochen nicht den gewünschten therapeutischen Erfolg. Die etwa drei Stunden vor der nächsten Dosis gemessenen Clomipramin-Spiegel waren unterhalb der Nachweisgrenze (<50 ng/ml). Erst die orale Behandlung mit einer Amitriptylin-Lösung (40 mg/ml) führte bereits nach zwei Wochen zu einer wesentlichen klinischen Besserung, wobei nach einer Anfangsdosis von 75 mg abends die Dosis wöchentlich um 25 mg/Tag angehoben wurde. Bei einer Dosis von 200 mg/Tag betrug der Plasmaspiegel von Amitriptylin 158 ng/ml und derjenige des Metaboliten Nortriptylin 65 ng/ml. Von Interesse ist noch, dass der Talspiegel von Amitriptylin drei Tage nach Behandlungsbeginn bereits 65 ng/ml erreichte; zwei Stunden nach der 75-mg-Abenddosis wurden hier bereits 145 ng/ml gemessen.
Serotonerge Wirkstoffe. Die Pharmakokinetik einer 100-mg-Einzeldosis von Sertralin wurde bei fünf Patienten etwa ein Jahr nach einer bariatrischen Roux-en-Y-Bypass-Operation gemessen; als Kontrollen dienten fünf Personen mit vergleichbarem demographischem und pharmakogenetischem (CYP2C19, CYP2D6; ausgeschlossen waren ultraschnelle und langsame Metabolisierer) Status [28]. Es wurden ganze, also nicht vorher zerkleinerte Tabletten verabreicht (JL Roerig, persönliche Mitteilung). Bedenkt man, dass die Halbwertszeit von Sertralin etwa einen Tag beträgt [7], ist es bedauerlich, dass die AUC (Area under the curve) von Sertralin im Blut nur über zehn Stunden gemessen wurde, aber sie war unter diesen Bedingungen bei den Patienten etwa 60% signifikant geringer als bei den Kontrollen, ebenso die maximale Sertralin-Konzentration (ca. 61% geringer).
Eine wichtige, kürzlich veröffentlichte Arbeit untersuchte die Pharmakokinetik von serotonergen Antidepressiva (Venlafaxin, Duloxetin, Citalopram, Escitalopram, Sertralin) bei zwölf übergewichtigen Patienten, die sich einer Roux-en-Y-Bypass-Operation unterzogen und an einer affektiven Störung litten [10]. Ein Jahr nach der Operation hatten die Patienten durchschnittlich die Hälfte ihres Übergewichts verloren (excessive weight loss [EWL] ca. 50%). Die Pharmakokinetik der Antidepressiva wurde über acht Stunden nach ihrer Einnahme gemessen, und zwar kurz vor der Intervention sowie 1, 6 und 12 Monate danach. Leider sind keine Angaben über die galenische Form und die Dosis erhältlich. Einen Monat nach der Operation fiel bei acht Patienten die AUC der Arzneistoffe im Blut auf einen Mittelwert von 54% (Bereich 36–80%) des präoperativen Niveaus. Bei sechs Patienten normalisierte sich die AUC im 6. Monat auf das präoperative Niveau. Bei anderen Patienten verlief die Kinetik unterschiedlich. Wegen der geringen Anzahl von Patienten, die mit einem bestimmten Medikament behandelt wurden, wird hier nicht auf Details eingegangen. Auffällig war, dass der klinische Zustand mehrerer Patienten sich perioperativ verschlechterte, um sich dann mehrheitlich bis zum 6. Monat wieder zu verbessern. Die schon erwähnten Adaptationsphänomene könnten dazu beigetragen haben.
Antipsychotika
Bariatrische Chirurgie kann auch bei übergewichtigen schizophrenen Patienten sinnvoll und erfolgreich sein [11]. Fünf schizophrene Patienten wurden zu einem nichtpsychotischen Zeitpunkt einem restriktiven gastrischen Eingriff wegen Übergewicht unterzogen [16]. Eine parenterale antipsychotische Therapie wurde innerhalb von 24 bis 48 Stunden wieder problemlos eingeführt. Bei einem sechsten Patienten wurde die medikamentöse Behandlung vor dem Eingriff zu früh unterbrochen. Er erlitt einen psychotischen Rückfall, weshalb die Autoren empfehlen, die Medikation bis 24 Stunden vor der Operation aufrecht zu erhalten. Es wurde nicht über eventuelle Plasmaspiegel der nicht spezifizierten Antipsychotika berichtet.
Bei einer 51-jährigen schizophrenen, mit 20 mg/Tag Haloperidol erfolgreich behandelten Patientin, die sich wegen Übergewicht einer gastrischen Bypass-Operation (Erhalten einer kleinen proximalen Magentasche, Umgehen von distalem Magen und Duodenum) unterzog, wurde die Haloperidol-Behandlung zwei Wochen vor dem Eingriff unterbrochen. Drei Tage nach der Operation wurde in der Klinik wegen erneuter psychotischer Symptomatik die Behandlung mit 20 mg/Tag Haloperidol wieder eingeführt. Nach der Entlassung erhöhte die Familie die Dosis selbstständig auf 40 mg/Tag. Dennoch war eine Hospitalisierung notwendig. Später, unter Gleichgewichtsbedingungen, wurde bei 20 mg/Tag Haloperidol dessen Pharmakokinetik gemessen – der Talspiegel lag bei 14 ng/ml, was im Vergleich mit der Literatur als normal interpretiert wurde [8]. Nicht geklärt ist in diesem Fall die Frage, ob die Patientin perioperativ eine höhere Dosis aus pharmakokinetischen Gründen gebraucht hätte und sich die Kinetik mittelfristig kompensatorisch wieder normalisierte.
Olanzapin und Quetiapin werden wegen ihrer Säurelöslichkeit vermutlich hauptsächlich im Magen (und Duodenum) absorbiert, weshalb ihre Aufnahme ins Blut je nach Form des chirurgischen Eingriffs gefährdet sein kann [20]. Entsprechende Studien wurden aber leider nicht veröffentlicht.
Zusammenfassung und Schlussfolgerungen
Restriktive chirurgische Eingriffe im Magen-Darm-Trakt sind häufig, auch bei Patienten, die mit psychotropen Medikamenten behandelt werden. Studien über die Pharmakokinetik von Antidepressiva und Antipsychotika sind jedoch in diesem Zusammenhang sehr selten. Glücklicherweise scheinen bisher – der geringen Zahl von Veröffentlichungen nach zu schließen – kaum schwere Zwischenfälle im Rahmen einer Psychopharmakotherapie bei solchen Eingriffen vorgekommen zu sein. Dennoch können für eine optimale, sichere Behandlung mit Psychopharmaka die in Tabelle 2 dargestellten vorläufigen Empfehlungen nützlich sein.
Tab. 2. Empfehlungen zur Psychopharmakotherapie nach restriktiven gastrointestinalen Eingriffen [erweitert nach 32]
|
1. Bei bestehender psychotroper Prämedikation: verifizieren, ob deren Weiterführung aus Sicherheitsgründen auch noch nach dem Eingriff gerechtfertigt ist |
|
2. Wenn möglich, Eingriff erst nach optimaler Response auf die medikamentöse Vorbehandlung vornehmen |
|
3. Perioperativ möglichst kurze Unterbrechung der medikamentösen Behandlung, um Risiko für Rückfälle oder Absetzsymptome niedrig zu halten |
|
4. Therapeutisches Drug-Monitoring vor und nach dem Eingriff. Zumindest nach 6 und 12 Monaten wiederholen (Adaptationsmechanismen) |
|
5. Falls postoperativ eine Änderung in der Psychopharmakotherapie notwendig wird, ist zu berücksichtigen:
|
Insbesondere sind Plasmaspiegelbestimmungen des Psychopharmakons vor und nach dem Eingriff empfehlenswert. Basiswerte können hilfreich sein, um nach der Operation gemessene Spiegel zu interpretieren und um gegebenenfalls die Dosis anzupassen. Nach der bestehenden Literatur scheint allgemein das Risiko für eine Intoxikation nicht bedeutend zu sein, aber sie zeigt, dass die pharmakokinetischen Folgen einer restriktiven gastrointestinalen Intervention interindividuell stark unterschiedlich sein können. Veränderungen können sich zudem als Folge von Adaptationsvorgängen noch Monate nach der Operation manifestieren. TDM erweist sich demnach als nützliches Instrument zur Optimierung der Pharmakotherapie, doch sind auf jeden Fall mehr pharmakokinetische Studien bei stark übergewichtigen und operierten Patienten erforderlich.
Literatur
1. Allison DB, Newcomer JW, Dunn AL, et al. Obesity among those with mental disorders: a National Institute of Mental Health meeting report. Am J Prev Med 2009;36:341–50.
2. Benet LZ, Kroetz DL, Sheiner LB. Pharmacokinetics the dynamics of drug absorption, distribution, and elimination. In: Hardman JG, Limbird LE (eds.). Goodman & Gilman’s The pharmacological basis of therapeutics. New York: McGraw-Hill Companies; 1996:3–27.
3. Broyles JE, Brown RO, Self TH, et al. Nortriptyline absorption in short bowel syndrome. JPEN 1990;14:326–7.
4. Buchwald H, Avidor Y, Braunwald E, et al. Bariatric surgery: a systematic review and meta-analysis. JAMA 2004;292:1724–37.
5. Couturier PL, Zahr N, Goldwirt L, et al. Therapeutic drug monitoring of clomipramine and amitriptyline in a depressed patient with upper digestive tract resection. Ther Drug Monit 2011;33:467–8.
6. Deitel M. Overweight and obesity worldwide now estimated to involve 1.7 billion people. Obes Surg 2003;13:329–30.
7. Edwards A, Ensom MH. Pharmacokinetic effects of bariatric surgery. Ann Pharmacother 2012;46:130–6.
8. Fuller AK, Tingle D, DeVane CL, et al. Haloperidol pharmacokinetics following gastric bypass surgery. J Clin Psychopharmacol 1986;6:376–8.
9. Goldfine AB, Shoelson SE, Aguirre V. Expansion and contraction: treating diabetes with bariatric surgery. Nat Med 2009;15:616–7.
10. Hamad GG, Helsel JC, Perel JM, et al. The effect of gastric bypass on the pharmacokinetics of serotonin reuptake inhibitors. Am J Psychiatry 2012;169:256–63.
11. Hamoui N, Kingsbury S, Anthone GJ, et al. Surgical treatment of morbid obesity in schizophrenic patients. Obes Surg 2004;14:349–52.
12. Hanley MJ, Abernethy DR, Greenblatt DJ. Effect of obesity on the pharmacokinetics of drugs in humans. Clin Pharmacokinet 2010;49:71–87.
13. Hiemke C, Baumann P, Bergemann N, et al. AGNP consensus guidelines for therapeutic drug monitoring in psychiatry: Update 2011. Pharmacopsychiatry 2011;44:195–235
14. Jain R, Chung SM, Jain L, et al. Implications of obesity for drug therapy: limitations and challenges. Clin Pharmacol Ther 2011;90: 77–89.
15. Laux G, König W, Baumann P. Infusionstherapie bei Depressionen – Leitfaden für Klinik und Praxis. Stuttgart: Hippokrates Verlag, 1997.
16. Lawlor BA, Rand CS. Schizophrenia and gastric surgery for obesity. Am J Psychiatry 1986;143:1321.
17. Mahmood I. Prediction of clearance and volume of distribution in the obese from normal weight subjects: an allometric approach. Clin Pharmacokinet 2012;51:527–42.
18. Malone M, Alger-Mayer SA. Medication use patterns after gastric bypass surgery for weight management. Ann Pharmacother 2005;39:637–42.
19. Marzolini C, Paus E, Buclin T, et al. Polymorphisms in human MDR1 (P-glycoprotein): recent advances and clinical relevance. Clin Pharmacol Ther 2004;75:13–33.
20. Miller AD, Smith KM. Medication and nutrient administration considerations after bariatric surgery. Am J Health Syst Pharm 2006;63:1852–7.
21. Mouly S, Paine MF. P-glycoprotein increases from proximal to distal regions of human small intestine. Pharm Res 2003;20:1595–9.
22. Mühlhans B, Horbach T, de Zwaan M. Psychiatric disorders in bariatric surgery candidates: a review of the literature and results of a German prebariatric surgery sample. Gen Hosp Psychiatry 2009;31:414–21.
23. Padwal R, Brocks D, Sharma AM. A systematic review of drug absorption following bariatric surgery and its theoretical implications. Obes Rev 2010;11:41–50.
24. Padwal R, Klarenbach S, Wiebe N, et al. Bariatric surgery: a systematic review of the clinical and economic evidence. J Gen Intern Med 2011;26:1183–94.
25. Padwal R, Klarenbach S, Wiebe N, et al. Bariatric surgery: a systematic review and network meta-analysis of randomized trials. Obes Rev 2011;12:602–21.
26. Poggesi I, Benedetti MS, Whomsley R, et al. Pharmacokinetics in special populations. Drug Metab Rev 2009;41:422–54.
27. Robbins B, Reiss RA. Amitriptyline absorption in a patient with short bowel syndrome. Am J Gastroenterol 1999;94:2302–4.
28. Roerig JL, Steffen K, Zimmerman C, et al. Preliminary comparison of sertraline levels in postbariatric surgery patients versus matched non-surgical cohort. Surg Obes Relat Dis 2012; 8:62–6.
29. Rosik CH. Psychiatric symptoms among prospective bariatric surgery patients: rates of prevalence and their relation to social desirability, pursuit of surgery, and follow-up attendance. Obes Surg 2005;15:677–83.
30. Rowland M, Tozer TN. Clinical Pharmacokinetics and Pharmacodynamics. Concepts and Applications. Philadelphia: Wolters Kluwer, Lippincott, Williams & Wilkins, 2011.
31. Seaman JS, Bowers SP, Dixon P, et al. Dissolution of common psychiatric medications in a Roux-en-Y gastric bypass model. Psychosomatics 2005;46:250–3.
32. Smith A, Henriksen B, Cohen A. Pharmacokinetic considerations in Roux-en-Y gastric bypass patients. Am J Health Syst Pharm 2011;68:2241–7.
33. Thörn M, Finnstrom N, Lundgren S, et al. Cytochromes P450 and MDR1 mRNA expression along the human gastrointestinal tract. Br J Clin Pharmacol 2005;60:54–60.
34. Timmer CJ, Sitsen JMA, Delbressine LP. Clinical pharmacokinetics of mirtazapine. Clin Pharmacokinet 2000;38:461–74.
35. Wadden TA, Sarwer DB, Fabricatore AN, et al. Psychosocial and behavioral status of patients undergoing bariatric surgery: what to expect before and after surgery. Med Clin North Am 2007;91:451–69, xi–xii.
36. Ward N. The impact of intestinal failure on oral drug absorption: a review. J Gastrointest Surg 2010;14:1045–51.
Prof. Dr. Pierre Baumann, Département de psychiatrie (DP-CHUV), Site de Cery, 1008 Prilly-Lausanne, Schweiz, E-Mail: pierre.baumann@chuv.ch
Dr. Olivier Trégouët, Centre neuchâtelois de psychiatrie (CNP), Rue Sophie-Mairet 29, 2300 La Chaux-de-Fonds, Schweiz
Psychopharmacotherapy after restrictive gastrointestinal surgery
Bariatric surgery in morbidly obese patients, restrictive gastrointestinal resection in patients, who suffer from gastric cancer or who, for suicidal purposes, ingested toxic substances has an influence on the absorption process of drugs in the gastrointestinal tract. A 77-year-old patient with gastric cancer is described, who was submitted to total gastrectomy. While he was hospitalised in a somatic hospital because of severe undernutrition due to malabsorption, a depressive episode accompanied by a somatic syndrome (F32.11) was diagnosed. Only a treatment with 45 mg/day mirtazapine resulted in a clearcut clinical response. Although the antidepressant was administered as whole tablets, plasma concentrations of mirtazapine were within those observed in patients not submitted to surgery. A review of the literature about the pharmacokinetics of antidepressants and antipsychotics in patients submitted to surgery in the gastrointestinal tract is presented. Treatment recommendations are proposed which should help to minimise risks for pharmacotherapy and optimise treatment response in these patients. In particular, therapeutic drug-monitoring is recommended before and after surgery, as adaptation processes may modify the fate of the drug in the organism.
Key words: Gastrectomy, antidepressants, antipsychotics, pharmacokinetics, therapeutic drug-monitoring, mirtazapine
Psychopharmakotherapie 2013; 20(01)
