Imke Hoell und Ursula Havemann-Reinecke, Göttingen
In Deutschland konsumieren zurzeit etwa 200000 Menschen (grober Schätzwert) illegale Drogen, vorzugsweise Heroin [31], wobei die Dunkelziffer hoch sein dürfte. Die Betreuung schwangerer opioidabhängiger Frauen ist für alle Beteiligten eine enorme Herausforderung: sie erfordert ein außergewöhnlich hohes Maß an Verantwortung und eine intensive interdisziplinäre Zusammenarbeit von Suchttherapeuten in (Drogen-)Beratungsstellen, Angestellten in Schwangerschaftsberatungsstellen, Gynäkologen, Psychiatern, Allgemeinmedizinern, Psychologen und selbstverständlich auch Pharmazeuten.
In Teil I dieses Artikels werden die Folgen eines Missbrauchs, schädlichen Gebrauchs (Abusus) oder einer Abhängigkeit sowie die Toxizitäten von Opiaten und anderen Suchtstoffen in der Schwangerschaft skizziert und akute medizinische Behandlungsstrategien anhand aktueller wissenschaftlicher Erkenntnisse diskutiert. Eine erste Darstellung wurde bereits 2011 publiziert [56]. In Teil II des Beitrags werden die psychiatrischen und somatischen Komorbiditäten und deren Therapie anhand der aktuellen Studienlage und den Empfehlungen der Food and Drug Administration (FDA) dargestellt.
Patienten
Unter Opioidabhängigen versteht man
- Patienten, die von klassischen Opiaten, also Substanzen vom Morphintyp wie Codein oder Heroin (Diacetylmorphin, Abb. 1a), abhängig sind, sowie
- Patienten, die abhängig sind von Substanzen wie Tramadol, Tilidin, Fentanyl, Oxycodon oder Piritramid, deren chemische Struktur vom Morphintyp abweicht (Abb. 1b) und die dennoch eine hohe Affinität zu μ-Opioidrezeptoren aufweisen.
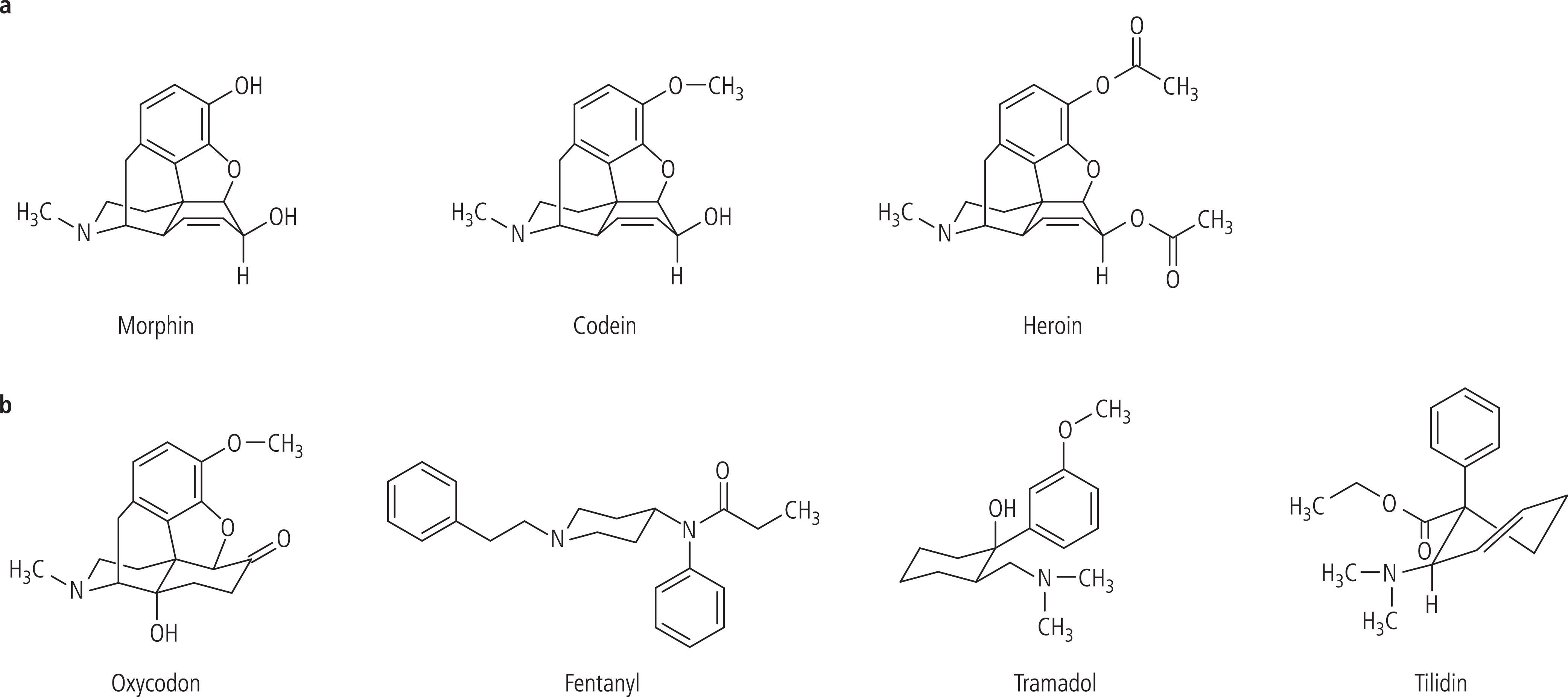
Abb. 1. Opioide vom Morphintyp (Opiate, a) und Opioide, deren chemische Struktur vom Morphintyp abweicht (b)
Im letzteren Fall handelt es sich meist um Patienten, die von Arzneimitteln abhängig sind, die von einem Arzt verschrieben und von den Patienten legal erworben wurden („legale Patienten“). Dabei sind die Abhängigkeiten von Tramadol (z.B. Tramal®) und Tilidin (z.B. Valoron®) bei dieser Patientengruppe aktuell am häufigsten [46, klinische Beobachtung und persönliche Angabe U. Havemann-Reinecke 2011]. In einer Stichprobe von 140 Tramadol-abhängigen Patienten, die sich in der Göttinger Psychiatrischen Universitätsklinik zur Entzugsbehandlung befanden, gehörten bezüglich der Diagnose „Tramadol-Abhängigkeit als Erstdiagnose“ 88% den „legalen Patienten“ an, während nur 12% der Patienten Tramadol illegal erworben hatten („illegale Patienten“) [persönliche Angabe U. Havemann-Reinecke, 2011]. Bei der Gruppe der Patienten mit „legaler“ Opioidabhängigkeit handelt es sich meist um Patienten mittleren und höheren Alters, bei denen nur noch wenige oder keine Schwangerschaften mehr zu erwarten sind. Dennoch waren in dieser Stichprobe von 123 „legal“ Tramadol-Abhängigen auch jüngere Patienten im Alter von 20 bis 30 Jahren (11%) sowie von 30 bis 40 Jahren (21%) [persönliche Angabe U. Havemann-Reinecke, 2011]. Bei der gemessenen Geschlechtsverteilung von 50% männlichen und 50% weiblichen Patienten könnte es in der Gruppe der „legal“ Abhängigen also durchaus schwangere Patientinnen geben, die entsprechend behandelt werden müssen. Berichte über die Behandlung „legal“ opioidabhängiger Patientinnen sind den Verfassern nicht bekannt. Möglicherweise werden diese Frauen aufgrund der endokrinen Wirkungen der Opioide seltener schwanger als Frauen, die nicht von Opioiden abhängig sind. Ein anderer, wahrscheinlicherer Grund kann sein, dass die „legale“ Opioidabhängigkeit weniger äußerlich sichtbar ist als die Heroinabhängigkeit und dass Tramadol und Tilidin (wie einige andere Opioide) mit den üblichen immunologischen Untersuchungsmethoden nicht qualitativ nachgewiesen werden können, sondern nur gaschromatographisch/massenspektrographisch oder mit speziellen Urin-Sticks. Die „legale“ Opioidabhängigkeit wird daher möglicherweise eher unterdiagnostiziert.
Bei den opioidabhängigen Schwangeren handelt es sich folglich meist um „illegale“ Patientinnen, die hauptsächlich von Opiaten (vor allem Heroin) und häufig zusätzlich von Tabak (Nicotin), Alkohol, Benzodiazepinen, Cocain, Cannabis und Psychostimulanzien abhängig sind oder entsprechenden Missbrauch betreiben.
Die Schwangerschaften opiat- bzw. opioidabhängiger oder polytoxikomaner Patientinnen sind als Hochrisikoschwangerschaften einzuordnen. Bei einem multiplen Substanzmissbrauch oder einer Polytoxikomanie (Glossar) der Schwangeren ist es kaum möglich, die Vielfalt der toxischen Schädigungen bei Mutter und Kind differenziert auf einen der Suchtstoffe zurückzuführen, insbesondere dann, wenn ein begleitender Konsum von Alkohol und Zigaretten vorliegt. Aus unserer Sicht ist eine differenzierte Betrachtung der toxischen Wirkungen und Behandlungsstrategien hinsichtlich der einzelnen Suchtstoffe dennoch sinnvoll, um bei den betroffenen Schwangeren für eine möglichst klare Informationsvermittlung zu sorgen, eine individuelle Behandlungsmotivation zu wecken und therapeutische Konsequenzen aufzuzeigen.
Glossar
Opiate: Stoffe, deren chemische Struktur dem Morphin ähnelt und die an Opioidrezeptoren als Agonist wirken
Opioide: Stoffe mit unterschiedlicher chemischer Struktur, die an Opioidrezeptoren als Agonist wirken
Polytoxikomanie: Konsum von drei oder mehr Suchtstoffen innerhalb der letzten sechs Monate
Missbrauch, Abusus oder Abhängigkeit
Für die Therapie ist es wichtig zu wissen, ob im vorliegenden Fall einer schwangeren Patientin ein Missbrauch und/oder ein Abusus oder ein Abhängigkeitssyndrom der verschiedenen Substanzklassen vorliegt.
Als Missbrauch bezeichnet man den Konsum von süchtig machenden Substanzen unabhängig oder abweichend von einer medizinischen Verordnung. Bei Patienten, die Missbrauch betreiben, können (noch) keine Zeichen von Abusus oder Abhängigkeit diagnostiziert werden.
Unter Abusus (schädlicher Gebrauch) versteht man nach der internationalen Klassifikation der Krankheiten (International Classification of Diseases 2010, ICD-10) ein Konsummuster von Suchtstoffen, das bereits zu einer Gesundheitsschädigung seelischer oder körperlicher Art des Betroffenen geführt hat, bei dem jedoch noch keine Anzeichen für ein Abhängigkeitssyndrom vorliegen.
Unter einer Abhängigkeit versteht die Weltgesundheitsorganisation (WHO) einen „seelischen, eventuell auch körperlichen Zustand, der dadurch charakterisiert ist, dass ein dringliches oder unbezwingbares Bedürfnis besteht, sich die entsprechende Substanz fortgesetzt oder periodisch zuzuführen“. Bei einer Abhängigkeit nach ICD-10 kommt es im Rahmen des Konsums schließlich zu
- zunehmendem Kontrollverlust bezüglich der Einnahme der Substanz,
- einer Toleranzentwicklung,
- während Abstinenzphasen zu körperlichen Entzugssymptomen,
- zu einer fortschreitenden Vernachlässigung anderer Verpflichtungen und Interessen und/oder
- zu einer vom Konsumenten bewusst in Kauf genommenen körperlichen oder seelischen Schädigung.
Zur Diagnosestellung eines Abhängigkeitssyndroms müssen mindestens drei dieser Kriterien erfüllt sein.
Begleiterkrankungen und psychosoziale Begleitumstände
Opioidabhängige Patienten leiden neben ihrer Opioidabhängigkeitserkrankung nicht selten an zusätzlichem Abusus oder Missbrauch von anderen süchtig machenden Substanzen. Laut einer eigenen multizentrischen Studie litten 51% der opioidsubstituierten Patienten, darunter signifikant mehr weibliche Patienten, gleichzeitig unter einer Achse-I-Störung wie einer affektiven Störung, einer Erkrankung aus dem schizophrenen Formenkreis oder einer Angststörung [122]. Dabei war unter den Patienten mit psychischer Komorbidität ein höherer Gebrauch von Benzodiazepinen, Alkohol und Cannabis festzustellen als bei Patienten, die keine weiteren psychischen Erkrankungen hatten. Der Heroinbeikonsum war dagegen bei Patienten mit und ohne Achse-I-Störung vergleichbar [122].
Die opioidabhängigen Patientinnen sind im Rahmen ihrer Grunderkrankung maßgeblich auf die Beschaffung von Drogen eingeengt und wenden dem Bereich der Schwangerschaftsverhütung daher weniger Bedeutung zu. Den Betroffenen fehlen häufig auch die finanziellen Mittel zur regelmäßigen Einnahme von Kontrazeptiva. Teilweise betreiben diese Frauen auch Prostitution für den Lebensunterhalt und die Beschaffung von Drogen. Aus diesen Gründen wird ein beachtlicher Anteil opioidabhängiger, polytoxikomaner Frauen ungewollt schwanger und häufig wird diese Schwangerschaft ärztlich erst spät diagnostiziert.
Für viele opioidabhängige/polytoxikomane Frauen stellt eine Schwangerschaft zunächst eine massive psychosoziale Belastungssituation dar, die verdrängt wird. Für diese Frauen ist die Vorstellung, zukünftig für ein Kind sorgen zu müssen, vor dem Hintergrund ihrer Lebenssituation, ihres Lebensstils und häufig bestehender psychiatrischer und somatischer Begleiterkrankungen eine extreme Herausforderung. Vielfach handelt es sich bei den Vätern der Kinder ebenfalls um suchtkranke psychiatrische Patienten. Auf der anderen Seite hängen die schwangeren opioidabhängigen Mütter an ihrer Schwangerschaft und den Kindern und erleben ein „Nichtgelingen“ als schweres Versagen. Eine Schwangerschaft kann und wird von den Frauen aber auch als Chance für einen Neuanfang gesehen. In dieser Phase der Schwangerschaft ist es wichtig, den Müttern die unbedingte Notwendigkeit der Therapie der Opioidabhängigkeit mittels einer Substitutionstherapie sowie eines Entzugs von Cannabis, Alkohol, Psychostimulanzien, Cocain, Sedativa oder Tabak und einer zukünftigen Abstinenz klarzumachen. Eine enge interdisziplinäre und kooperative Zusammenarbeit verschiedener Berufsgruppen wie Allgemeinmedizinern, Gynäkologen, Psychologen, Pädiatern, Psychiatern, Pharmazeuten und Sozialtherapeuten zur Entlastung der Mutter und Planung einer Zukunftsperspektive ist daher während und nach der Schwangerschaft der Betroffenen von großer Bedeutung.
Suchtspezifische Screening-Methoden und Drug-Monitoring bei opioidabhängigen und polytoxikomanen Schwangeren
Über den spezifischen Substanzmissbrauch polytoxikomaner Patienten kann mittels Urindiagnostik bereits eine valide Aussage und Beurteilung des Verlaufs erfolgen. Dabei können sowohl Opioide wie Morphin, Codein, Heroin, Hydrocodon und Hydromorphon als auch Alkohol, Amphetamine, Benzodiazepine, Cocain und Cannabinoide semiquantitativ (insbesondere über immunologische Screening-Verfahren) bestimmt werden. Für den Nachweis einiger dieser Substanzen werden von verschiedenen Herstellern auch Urinsticks angeboten. So gibt es Kombitests, mit denen verschiedene Suchtstoffe oder deren Metaboliten zusammen orientierend gemessen werden können, beispielsweise Opiate (aber nicht Opioide!), Methadon (durch Nachweis des Metaboliten 2-Ethyliden-1,5-dimethyl-3,3-diphenylpyrrolidin [EDDP]), Amphetamine wie Ecstasy (3,4-Methylendioxy-N-methylamphetamin, MDMA), Cannabinoide und Benzodiazepine auf Diazepam-Basis. Einzelsticks gibt es beispielsweise zum gesonderten Nachweis von Buprenorphin oder Tramadol.
Wenn der Verdacht besteht, dass die betroffene Person andere Suchtstoffe konsumiert hat, die mit den standardmäßig eingesetzten immunologischen Methoden und Urin-Sticks zunächst nicht erfasst werden, kann der Urin der Betroffenen mittels Gaschromatographie und angeschlossener Massenspektometrie (GC-MS-Verfahren) auf sämtliche andere Substanzen bzw. deren Metaboliten untersucht werden, etwa „Spice“ (ein synthetisches Cannabinoid), „Speed“ (ein Amphetamin), „Liquid Ecstasy“ (Gamma-Hydroxy-Buttersäure), Lormetazepam oder die Opioide Buprenorphin, Tramadol, Tilidin, Fentanyl, Piritramid und Oxycodon.
Der Einsatz von Urin-Sticks zum Drogennachweis ist im Rahmen von Notfallversorgungen bei akut intoxikierten Patienten eine notwendige Untersuchung, um spezifische, von der konsumierten Droge abhängige medizinische Komplikationen frühzeitig zu erkennen oder pharmakologische Interaktionen im Falle einer medikamentösen Anbehandlung zu vermeiden.
Im nicht notfallmäßigen Setting sollte der Einsatz von Urin-Sticks zum Nachweis eines Drogenkonsums dagegen mit den Betroffenen im Vorfeld besprochen werden. Wenn dies nicht geschieht, könnte sich im Falle eines positiven Testergebnisses die Wahrnehmung des Betroffenen, „ausgetrickst“ worden zu sein, negativ auf eine eventuelle Therapiemotivation auswirken. Eine Entzugsbehandlung beziehungsweise eine langfristige Drogentherapie wird ohne ausreichende Therapie- und Änderungsmotivation beim Betroffenen in den allermeisten Fällen nicht erfolgreich sein oder gar nicht zustande kommen. Im Falle eines vermuteten/nachgewiesenen Drogenkonsums sollte daher grundsätzlich an behandelnde Ärzte und wohnortnahe Beratungsstellen verwiesen werden. Dies gilt insbesondere auch dann, wenn Eltern oder andere Angehörige bei Jugendlichen einen Drogenkonsum vermuten und in der Apotheke nach Schnelltests fragen, um diesen nachzuweisen.
Die Serumspiegel der zur Substitution eingesetzten Opioide können quantitativ bestimmt und therapeutischen Bereichen zugeordnet werden (Tab. 1) [12, 54]. Im Falle von Buprenorphin gibt es aktuell nur Daten, dass 4 mg Buprenorphin bei einem opioidabhängigen Patienten 0,7 bis 1,6 ng/ml entspricht. Gesicherte therapeutische Spiegel für Substitutionstherapie existieren für Buprenorphin im Gegensatz zu Methadon noch nicht.
Tab. 1. Therapeutische Bereiche verschiedener Opioide im Rahmen einer Substitutionstherapie [12, 54]
|
Wirkstoff |
Fertigarzneimittel (Beispiel) |
Serumspiegel [ng/ml] |
|
D/L-Methadon |
Methaddict® |
400–600 |
|
Levomethadon |
L-Polamidon® |
250–400 |
|
Buprenorphin* |
Subutex® |
0,7–1,6 |
*Eine Dosis von 4 mg Buprenorphin täglich entspricht einem Serumspiegel von 0,7–1,6 ng/ml.
Alkohol
Ein Konsum von Alkohol kann auf verschiedene Arten direkt nachgewiesen werden:
- in der Atemluft als Ethanol,
- im Urin als Ethanol unmittelbar bis 24 Stunden nach Aufnahme oder als Ethylglucuronid (ETG) bis zu zwei oder drei Tage nach dem letzten Konsum,
- im Blut als Ethanol.
Ein chronischer Alkoholkonsum kann außerdem indirekt über Veränderungen im Blutbild festgestellt werden, so weisen alkoholkranke Patienten meist eine Erhöhung des Leberenzyms Gamma-Glutamyltransferase (Gamma-GT) und eine Veränderung der roten Blutkörperchen auf, die sich im Volumen der Erythrozyten (mean corpuscular volume, MCV) sowie im Hämoglobingehalt der Erythrozyten (mean corpuscular hemoglobin, MCH) widerspiegelt. Verhältnismäßig spezifische Langzeitverlaufsparameter sind der CDT-Wert (Carbohydrate deficient transferrin), der im Serum erst nach mindestens einwöchiger Aufnahme von 60 g reinem Ethanol pro Tag erhöht ist und sich bei vollständiger Abstinenz nach zwei bis vier Wochen wieder normalisiert, sowie der HAA-Wert (hemoglobin-associated acetaldehyde), der bereits nach regelmäßigem moderatem Alkoholkonsum erhöht sein kann und sich bei Abstinenz im Verlauf eines Monats wieder normalisiert.
Es konnte gezeigt werden, dass einige dieser Parameter mit der Ausprägung des fetalen Alkoholsyndroms (siehe Abschnitt Alkohol, Toxizität) korrelieren [106], dennoch sind einzelne Werte für die Diagnosestellung einer Alkoholerkrankung alleine nicht wegweisend; vielmehr sollten sie gemeinsam erhoben und unter Berücksichtigung der klinischen Symptome beurteilt werden. Insbesondere bei Schwangeren muss der Verlauf des CDT-Werts mit Vorsicht betrachtet werden: Ein Anstieg des CDT-Werts ist bei Schwangeren nicht unbedingt auf einen vermehrten Alkoholkonsum innerhalb der vorausgegangenen Wochen zurückzuführen, denn der Wert korreliert infolge der Zunahme von Transferrin während der Schwangerschaft auch positiv mit der Anzahl der Schwangerschaftswochen [115]. Darüber hinaus ist zu bedenken, dass ein pathologischer CDT-Wert (>2,5%) bei einer nichtschwangeren Person ein regelmäßiges Trinken von mehr als 60 g Alkohol pro Tag voraussetzt und dass diese Menge an Alkohol bereits weit über dem Grenzwert für einen riskanten Konsum für die Entwicklung somatischer toxischer Folgen liegt. Zusammenfassend können MCV, Gamma-GT und Urinkontrollen auf Ethanol und Ethylglucuronid während der Schwangerschaft als die Laborparameter bezeichnet werden, die für die Diagnosestellung einer Alkoholabhängigkeit am besten geeignet sind; der CDT-Wert sollte dagegen bei Schwangeren als Prozentsatz des Gesamttransferrins angegeben werden [106].
Sicherheit von Arzneimitteln während der Schwangerschaft
Als Orientierungshilfe zur Einschätzung potenzieller oder bestehender Risiken für das ungeborene Kind durch eine medikamentöse Behandlung schwangerer Patientinnen bietet sich die international anerkannte Einteilung der FDA an (Tab. 2). Bei dieser Einteilung werden fünf Gruppen unterschieden. Die Zuordnung der Wirkstoffe zu einer der Gruppen wird regelmäßig aktualisiert. Die FDA führt selbst zwar keine Schwangerschaftsstudien durch, sie führt aber ein Register für alle unerwünschten Ereignisse durch Pharmaka in der Schwangerschaft.
Tab. 2. Pregnancy Categories der Food and Drug Administration zur Einschätzung der Sicherheit von Arzneimitteln in der Schwangerschaft
|
Kategorie |
Beschreibung |
|
A |
In adäquaten und kontrollierten Studien konnte kein fetales Risiko während des ersten bis dritten Trimenons festgestellt werden |
|
B |
In tierexperimentellen Studien konnte kein fetales Risiko festgestellt werden, jedoch existieren bisher keine adäquaten oder kontrollierten Studien für eine Anwendung bei schwangeren Frauen. |
|
C |
In tierexperimentellen Studien konnte ein nachteiliger Effekt auf die fetale Entwicklung festgestellt werden, entsprechende adäquate oder kontrollierte Studien beim Menschen existieren bisher noch nicht. Es sollte in Erwägung gezogen werden, ob der potenzielle Nutzen eines Einsatzes des Medikaments bei schwangeren Frauen dennoch das Risiko einer nachteiligen Auswirkung auf die fetale Entwicklung überwiegt. |
|
D |
Auf dem Hintergrund klinischer Erfahrungen oder klinischer humaner Studien existieren klare Hinweise für ein fetales Risiko beim Menschen. Es wird aber darauf hingewiesen, dass der potenzielle Nutzen eines Einsatzes des Medikaments bei schwangeren Frauen dennoch das Risiko einer nachteiligen Auswirkung auf die fetale Entwicklung überwiegen könnte. |
|
X |
In humanen sowie tierexperimentellen Studien konnten fetale Entwicklungsstörungen nachgewiesen werden und/oder es existieren klare Hinweise für fetale Risiken auf dem Hintergrund bisheriger klinischer Erfahrungen. Dabei überwiegen die fetalen Risiken, die eine Einnahme des Medikaments während der Schwangerschaft beinhaltet, zweifellos jeglichen potenziellen Nutzen. |
Im weiteren Textverlauf ist die Zuordnung der Pharmaka zur entsprechenden FDA-Kategorie in Klammern angegeben, dargestellt ist der Stand vom 3. Juni 2011.
In Deutschland erfolgt die Überwachung von Arzneimitteln nach Markteinführung, gerade auch unter dem Aspekt der Sicherheit in der Schwangerschaft und postpartaler Folgen, durch unterschiedliche Organisationen (z.B. Arzneimittelkommission der deutschen Ärzteschaft) sowie durch Behörden, wie durch das Bundesinstitut für Arzneimittel- und Medizinprodukte (BfArM) auf nationaler Ebene und die European Medicines Agency (EMA) auf europäischer Ebene.
Opioidabhängigkeit in der Schwangerschaft
Wirkung und Toxizität von Heroin
Heroin bindet als Agonist an μ-Opioidrezeptoren im zentralen Nervensystem – vorrangig in Thalamus, Basalganglien und mesolimbischem Striatum (dem Belohnungssystem) – und bewirkt so eine Gi-Protein-Aktivierung und nachfolgend eine Hemmung der cAMP-Synthese. Hierdurch kommt es schließlich zu einer Disinhibition und damit zu einer Aktivierung dopaminerger Neurone sowie zu vielfältigen Wirkungen auf andere Nervenzellen [37, 50]. Klinisch zeigt sich eine Verengung der Pupillen (Miosis, „pin pupils“) sowie eine atemdepressive, analgetische, euphorisierende und abhängigkeitsfördernde Wirkung.
Kinder von heroinkonsumierenden Frauen sind signifikant kleiner und haben ein geringeres Geburtsgewicht als Kinder gesunder Mütter [74]. Auch wurden bei opiatabhängigen Schwangeren mehr Komplikationen während der Schwangerschaft und Fehlgeburten beobachtet als bei anderen Schwangeren, jedoch existiert bisher kein Hinweis auf eine signifikant erhöhte Anzahl von kongenitalen Fehlbildungen. Naeye et al. fanden heraus, dass ein Opiatkonsum während der Schwangerschaft eine fetale Entwicklungsverzögerung verursachen kann und dass die Häufigkeit einer intrauterinen fetalen Abstoßung signifikant höher ist als bei Frauen ohne Opiatkonsum [81]. Im Zusammenhang mit einem Heroinkonsum besteht weiterhin ein erhebliches Risiko für genitale Infektionen, Aborte und vorzeitige Plazentaablösungen; die perinatale Säuglingssterblichkeit und die Häufigkeit von Komplikationen durch virale Infektionen (z.B. HIV, Hepatitis C), die im Zweifelsfall einen geplanten Kaiserschnitt notwendig machen, sind erhöht [48, 66].
Ausgelöst durch die kurze Halbwertszeit von Heroin kommt es als weitere Komplikation bei opiatabhängigen Schwangeren intermittierend zu Entzugssymptomen und vorzeitiger Wehentätigkeit, die im schlimmsten Fall zur Früh- oder Fehlgeburt führen kann.
Bei regelmäßiger Einnahme von Opioiden während der Schwangerschaft treten beim Neugeborenen postnatal Entzugssymptome auf, die unter anderem zur Atemdepression und zerebralen Krampfanfällen führen können. Die Kinder opioidabhängiger Mütter müssen daher in einem entsprechenden spezialisierten Zentrum stationär beobachtet werden, gegebenenfalls ist eine Entzugsbehandlung notwendig.
Im Spätverlauf zeigen die Kinder opiatabhängiger Frauen schließlich gehäuft Verhaltensstörungen im Sinne einer Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung [48, 89].
Die werdende Mutter muss über eventuell zu erwartende perinatale Probleme des Säuglings (vor allem die Entwicklung eines neonatalen Entzugssyndroms) sowie die Notwendigkeit einer engmaschigen ärztlichen Betreuung des Neugeborenen genau aufgeklärt werden [126]. Im Rahmen eines gemeinsamen „informed consent“, also einer gemeinsamen Vereinbarung zwischen Arzt und Patientin, sollte ein regelmäßiges Screening auf den Konsum von Opioiden und Opiaten während der Schwangerschaft stattfinden.
Diagnostik der Heroinabhängigkeit
Die Diagnose einer Heroinabhängigkeit oder einer opioidbezogenen Störung erfolgt anhand des klinischen Befunds und eines entsprechenden positiven Befunds im Urin.
Therapie der Opioidabhängigkeit in der Schwangerschaft
Da während eines Opioidentzugs mit einer ausgeprägten vegetativen und psychischen Entzugssymptomatik gerechnet werden muss, die in der Folge zu Uteruskontraktionen und schweren fetalen Komplikationen bis hin zu Fehl- und Frühgeburten führen kann, kann ein Entzug opioidabhängiger Schwangerer aus therapeutischer Sicht nicht empfohlen werden. Stattdessen gelten die Schwangerschaft und auch ein großzügig gefasster Zeitraum im Anschluss daran als Indikation zur Opioidsubstitution, beispielsweise mit Methadon. Ziel der Substitution ist es, eine stabile Schwangerschaftsentwicklung und eine bestmögliche postnatale Adaptation (Anpassung an die neue Situation) zu gewährleisten [66, 74, 81]. Substituierte Schwangere zeigen im Gegensatz zu nichtsubstituierten Schwangeren hinsichtlich der medizinischen Versorgung eine bessere Compliance und signifikant erniedrigte perinatale Morbiditäts- und Mortalitätsraten. Im Durchschnitt sind die Neugeborenen methadonsubstituierter Mütter größer als die Kinder nichtsubstituierter Frauen, dennoch zeigen die Kinder insgesamt im Vergleich zu gesunden Kontrollen ebenfalls ein retardiertes Größenwachstum [66].
Zur Substitutionsbehandlung stehen in Deutschland aktuell zur Verfügung:
- racemisches Methadon (D/L-Methadon, z.B. Methadonhydrochlorid-Lösung NRF 29.1., Kategorie C, Abb. 2),
- das enantiomerenreine Levomethadon (L-Polamidon®, Kategorie C),
- Buprenorphin (z.B. Subutex®, Kategorie C, Abb. 2) und
- Buprenorphin in Kombination mit Naloxon (Suboxone®, Kategorie C).
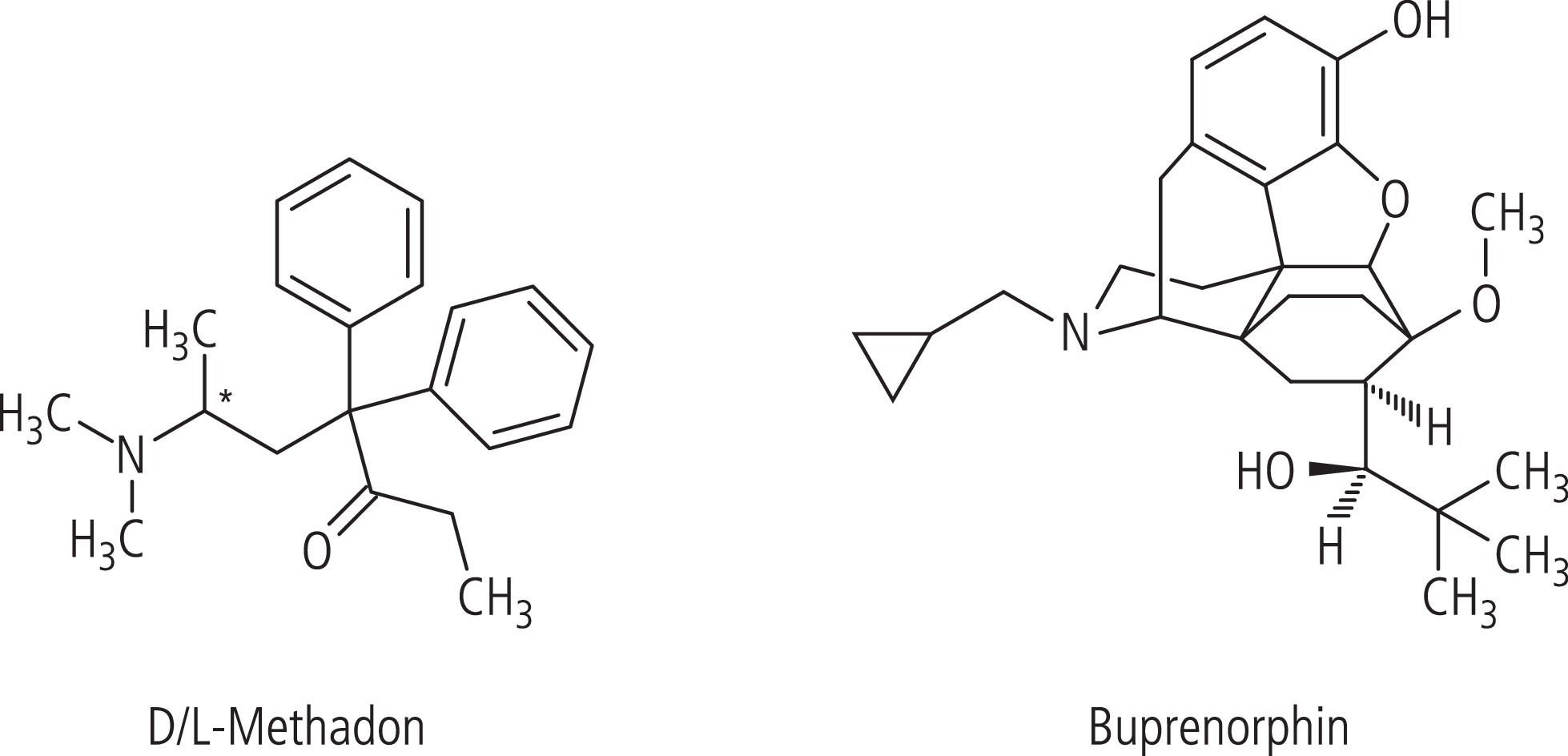
Abb. 2. D/L-Methadon und Buprenorphin
Methadon und Levomethadon sind reine μ-Opioidrezeptor-Agonisten, während Buprenorphin an μ-Opioidrezeptoren als Partialagonist und an κ-Opioidrezeptoren als Antagonist wirkt. Bei dem Kombinationspräparat soll der Zusatz des Opioidrezeptor-Antagonisten Naloxon dazu dienen, eine ausschließlich orale Anwendung zu gewährleisten (Naloxon führt bei Opioidabhängigen bei intravenöser oder nasaler Applikation zu vegetativen Entzugssymptomen); die Kombination ist aber aktuell nicht zur Substitution schwangerer Patientinnen zugelassen [Fachinformation], weil es tierexperimentelle Hinweise auf eine Reproduktionstoxizität gibt und entsprechende Daten für den Einsatz beim Menschen bisher fehlen. Laut Wong et al. kann im Falle einer Nichtverfügbarkeit von Methadon zur Substitution von opiatabhängigen Schwangeren alternativ auf retardierte Opioide zurückgegriffen werden [126].
Bezüglich der Frage, mit welchem Wirkstoff in der Schwangerschaft substituiert werden sollte, ist die Datenlage noch unklar. Laut Lacroix et al. gelten sowohl Methadon/Levomethadon als auch Buprenorphin als in der Schwangerschaft sicher einsetzbar [72]. Dagegen deuten Studienergebnisse der Arbeitsgruppe Fischer darauf hin, dass das neonatale Entzugssyndrom bei einer Substitution mit Buprenorphin weniger stark ausgeprägt ist als bei einer Substitution mit Methadon [24, 61, 62, 65]. Dennoch konstatierten Jones et al., dass Entzugssymptome und das Craving (Verlangen nach dem Suchtstoff) bei intensiv abhängigen Patientinnen der klinischen Erfahrung nach durch Methadon besser kupiert werden als durch Buprenorphin, weshalb die Entscheidung, mit welchem Substitut behandelt werden sollte, immer auch im Rahmen einer Einzelfallabwägung getroffen werden sollte [62].
Im Verlauf der Schwangerschaft kann es aufgrund der Gewichtszunahme der Schwangeren und einer Zunahme des Plasmavolumens erforderlich werden, die Dosis des Substitutionsmittels zu erhöhen, etwa zur Vermeidung von Entzugssymptomen oder zusätzlichem Heroinbeikonsum durch die Patientin. Eine solche Dosisanpassung kann vorsichtig in kleinen Schritten vorgenommen werden (z.B. bei Methadon-Lösung in 1-ml-Schritten, bei Buprenorphin in 1- bis 2-mg-Schritten). In einer Untersuchung mit Substitutionspatienten zeigte sich, dass Patienten mit geringem bis mittlerem Heroinbeikonsum mit signifikant niedrigeren Dosierungen von Methadon bzw. Levomethadon behandelt wurden als Patienten ohne Heroinbeikonsum [122]; dies spricht dafür, die Dosis des Substitutionsmittels nicht zu knapp zu bemessen, da ein Heroinbeikonsum im Zweifelsfall durch eine höhere Dosierung des Substitutionsmittels sicherer verhindert werden kann.
Bei einer Therapie mit Methadon ist im Falle einer Kombination mit anderen Wirkstoffen zu beachten, dass Methadon in der Leber durch Cytochrom-P450-Enzyme (CYP) abgebaut wird (Methadon: CYP2B6, CYP2C19, CYP3A4, CYP2D6; Levomethadon: CYP2C19, CYP2B6, CYP3A4, CYP2D6 [12, 54]) und dass die Funktion dieser Enzyme durch andere Wirkstoffe beeinflusst werden kann [104]. Der Metabolismus des racemischen Methadons ist stereoselektiv: CYP2B6 metabolisiert bevorzugt D-Methadon, CYP2C19 bevorzugt L-Methadon und CYP3A4 hat keine besondere Präferenz [12]. Der Methadon-Plasmaspiegel kann infolge einer pharmakokinetischen Interaktion bei einer Kombination mit Cimetidin, hormonellen Kontrazeptiva, Fluoxetin, Paroxetin sowie einigen Antimykotika und Antiarrhythmika erhöht sein. Umgekehrt können Wirkstoffe wie Carbamazepin, Phenobarbital, Phenytoin, Rifampicin oder Flunitrazepam den Methadon-Plasmaspiegel und damit die Wirkstärke sowie die Wirkungsdauer von Methadon verringern, wodurch Entzugssyndrome ausgelöst werden können [Fachinformation L-Polamidon®, 12].
In einer prospektiven Kohortenstudie mit 117 methadonsubstituierten schwangeren Frauen aus Irland zeigte sich auch, dass eine schrittweise Methadon-Dosisreduktion während der Schwangerschaft zu keinem geringeren Auftreten eines neonatalen Entzugssyndroms führte [19].
Buprenorphin wird sowohl über CYP2C8 als auch vor allem über CYP3A4 abgebaut. Dabei führen CYP3A4-Inhibitoren und -Induktoren zu Wechselwirkungen mit Buprenorphin [Fachinformation Subutex® (Juli 2010), 12, 104]. Bei gemeinsamer Einnahme von Buprenorphin mit Ketoconazol zeigte sich eine Erhöhung des Buprenorphin-Spiegels. Patienten, die zusätzlich zu Buprenorphin mit CYP3A4-Inhibitoren wie Ketoconazol, Gestoden, Makrolid-Antibiotika, den HIV-Protease-Inhibitoren Ritonavir, Indinavir oder Saquinavir behandelt werden, sollten deshalb genau überwacht und gegebenenfalls mit einer geringeren Buprenorphin-Dosis behandelt werden. Bezüglich einer Buprenorphin-Wechselwirkung mit CYP3A4-Induktoren liegen bisher keine klaren Daten vor, sodass bei Patienten, die mit CYP3A4-Induktoren wie Phenobarbital, Carbamazepin, Phenytoin und Rifampicin therapiert werden, ebenfalls eine vermehrte Kontrolle empfohlen wird. Darüber hinaus wird eine Wechselwirkung zwischen Buprenorphin und Phenprocoumon mit der Folge einer Purpura vermutet [Fachinformation].
Insbesondere bei Kombination von Opioiden mit Psychopharmaka sind darüber hinaus pharmakodynamische Interaktionen zu berücksichtigen. So können sich gemeinsame Wirkungen von Opioiden und manchen Antidepressiva oder Neuroleptika auf die QTc-Zeit sowie gemeinsame atemdepressive Wirkungen von Opioiden (z.B. D/L-Methadon, Levomethadon, Buprenorphin) und Benzodiazepinen addieren. In diesem Zusammenhang sei erwähnt, dass Levomethadon und Buprenorphin die QTc-Zeit in geringerem Maße verlängern als das racemische Methadon und im Vergleich dazu über ein sichereres kardiales Profil verfügen [12].
Mit neonatalen Entzugssyndromen wie einer Atemdepression und zerebralen Krampfanfällen muss auch unter einer Substitutionstherapie gerechnet werden, jedoch treten diese verglichen mit heroininduzierten Entzugssyndromen infolge der längeren Haltswertzeit von Methadon im Zweifelsfall ein bis zwei Wochen später auf [66]. Da ein postnataler Opioidentzug für den Säugling (unbehandelt) tödlich enden kann, sollte die Geburt bereits dann in einem Neonatalzentrum mit Intensiveinheit erfolgen, wenn der Verdacht eines nur sporadischen Heroinkonsums der Mutter während der Schwangerschaft im Raum steht; dies gilt erst recht bei Geburt unter Substitutionsbedingungen. Die Säuglinge methadon- oder buprenorphinsubstituierter Mütter sollten nach der Geburt unter Umständen mehrere Wochen lang intensivmedizinisch beobachtet werden, da bei ihnen eine Entzugssymptomatik, die entsprechend beobachtet und behandelt werden muss, häufig und auch verspätet auftritt.
Spätestens zu diesem Zeitpunkt muss die weitere Planung für Mutter und Kind erfolgen, und zwar meist multidisziplinär. Im Rahmen einer Einzelfallabwägung muss gegebenenfalls das Jugendamt hinzugezogen werden. In einigen Fällen ist eine Trennung von Mutter und Kind, teils auch die Freigabe des Säuglings zur Adoption, notwendig. Andererseits ist auch ein gemeinsames betreutes Wohnen von Mutter und Kind als Möglichkeit zu prüfen.
Begleitende Suchtstoffe
Tabak
Toxizität. Zigarettenkonsum während der Schwangerschaft führt zu einer Inkorporation von Begleitsubstanzen wie Aceton, Kohlenstoffmonoxid (CO), Radon, Ammoniak, Naphthalin, Teer, Formaldehyd und Cadmium, wobei Nicotin und andere toxische Substanzen plazentagängig sind [71]. Die Plazenta übernimmt als hochsensibles Organ die Funktion einer suffizienten Sauerstoff- und Nährstoffversorgung des Ungeborenenen. Es konnte gezeigt werden, dass eine chronische plazentäre Belastung mit Rauchbestandteilen zu einer verminderten Perfusion und einem häufigeren Infarktgeschehen der Plazenta beiträgt [48, 125]. Aus der dadurch resultierenden Minderversorgung des Fetus kann es zu intrauterinen Wachstums- und Entwicklungsverzögerungen kommen. So wurde ein vermehrtes Auftreten kindlicher Fehlbildungen wie Gastroschisis (ein Vorfall von Darmschlingen, verursacht durch eine Fehlbildung der Bauchwand) und Lippen-Kiefer-Gaumenspalten beobachtet [17, 49]. Weiterhin besteht ein erhöhtes Risiko für eine vorzeitige Plazentaablösung, die zum intrauterinen Tod des Fetus führen kann [125]. Darüber hinaus wurden bei Kindern rauchender Mütter kanzerogene Effekte wie die vermehrte Entwicklung von Hirntumoren, Leukämien oder Lymphomen im Zusammenhang mit einer fetalen Aufnahme oben genannter Substanzen beschrieben [108]. Während der Frühschwangerschaft ist eine höhere Rate von Fehlgeburten beschrieben, während ab dem zweiten Trimenon insbesondere plazentäre Komplikationen und die Gefahr einer vorzeitigen Wehentätigkeit im Vordergrund stehen [125].
Diagnostik. Hinsichtlich der Diagnostik des Tabakrauchens ist zwischen Missbrauch oder Abusus (nicht abhängiges Rauchen) und abhängigem Rauchen zu unterscheiden. Mithilfe des Fagerström-Tests (Tab. 3) zum Selbstausfüllen durch den Patienten kann das Ausmaß der Abhängigkeit einfach und schnell ermittelt werden [7].
Tab. 3. Fagerström-Test zur Abschätzung der Nicotinabhängigkeit [7]
|
Fragen und Antwortmöglichkeiten |
|
Wann rauchen Sie Ihre erste Zigarette nach dem Aufstehen?
|
|
Finden Sie es schwierig, das Rauchen zu unterlassen, wenn es verboten ist?
|
|
Auf welche Zigarette würden Sie nicht verzichten wollen?
|
|
Wie viele Zigaretten rauchen Sie im Allgemeinen pro Tag?
|
|
Rauchen Sie in den ersten Stunden nach dem Aufstehen im Allgemeinen mehr als am Rest des Tages?
|
|
Kommt es vor, dass Sie rauchen, wenn Sie krank sind und tagsüber im Bett bleiben müssen?
|
Therapie. Aufgrund der genannten massiven potenziellen Auswirkungen des Rauchens auf die Entwicklung des Fetus und den Verlauf der Schwangerschaft sollte der Schwangeren unbedingt zur Abstinenz hinsichtlich des Zigarettenkonsums geraten werden. Als therapeutische Hilfe sollte den Schwangeren in erster Wahl zu verhaltenstherapeutisch strukturierten Raucherentwöhnungsprogrammen geraten werden, wie sie in der Regel von allen größeren psychiatrischen Universitäts- und Suchttherapiezentren, aber auch von internistischen und pulmologischen Kliniken angeboten werden. Es wurden positive Effekte auf eine anhaltende Tabakabstinenz durch Entspannungstechniken, Kontingenzmanagment, körperliches Training und verhaltenstherapeutisch organisierte Gruppenprogramme beschrieben [4, 5].
Alternativ kann bei einem exzessiven Suchtverhalten eine Nicotinersatztherapie in Form von Nicotin-Pflastern, -Kaugummis oder -Lutschtabletten (z.B. Nicotinell®, Nicorette®) unter Abwägung von Risiken und Nutzen durchgeführt werden [4, 22, 126]. Hierbei ist zu beachten, dass Nicotin in der Schwangerschaft in der Regel schneller abgebaut wird als bei Nichtschwangeren, sodass die für nichtschwangere Patienten empfohlenen Dosierungen bei Schwangeren häufig zu niedrig sind [26, 38]. Für eine Effektivität und Sicherheit der Nicotinersatztherapie in der Schwangerschaft liegt allerdings bis heute keine ausreichende Datenlage vor [22].
Eine medikamentöse, rückfallprophylaktische Therapie der Nicotinsucht, wie sie mittlerweile bei nichtschwangeren Erwachsenen mit Bupropion (Zyban®, Kategorie C) oder Vareniclin (Champix®, Kategorie C) angeboten wird, ist während der Schwangerschaft nicht geeignet [Rote Liste, Fachinformationen], da hierfür nur unzureichende Daten vorliegen [18].
Insgesamt beträgt die Sechs-Monats-Abstinenzrate bei abhängigen Rauchern nach qualifizierter Entwöhnungsbehandlung etwa 9% [98], in einigen anderen Studien wurden etwa 20% angegeben. Bei Schwangeren sind daher engmaschige Kontrollen des Rauchverhaltens zu empfehlen, beispielsweise eine Bestimmung des Nicotin-Metaboliten Cotinin in Blut oder Urin, alternativ CO-Messungen in der Ausatemluft [38].
Alkohol
Toxizität. Chronischer Alkoholkonsum während der Schwangerschaft führt beim Fetus zu unterschiedlichen Ausprägungen des sogenannten fetalen Alkoholsyndroms (FAS). Unter einem FAS wird das syndromale Auftreten einer Vielzahl unterschiedlicher Fehlbildungen wie Mikroenzephalie (Gehirnminderentwicklung) mit geistiger Retardierung, Herz- und Organfehlbildungen sowie Gesichtsfehlbildungen mit weit auseinanderstehenden Augen, nivelliertem Philtrum (nur schwach ausgeprägte Rinne in der Mitte der Oberlippe) und schmalem Oberlippenrot verstanden [63].
Innerhalb der Frühschwangerschaft greifen alkoholbedingte Noxen in die hochsensible Entwicklungsphase der Organogenese ein. Dabei kann der übermäßige Alkoholkonsum während des ersten Trimenons zu schwerwiegenden geistigen Behinderungen auch ohne schwerwiegende, begleitende makroskopische Auffälligkeiten des Fetus führen, sodass man als Subform des fetalen Alkoholsyndroms vom ARND-Syndrom (alcohol related neurodevelopment disorder) spricht [105].
Kinder alkoholkranker Mütter zeigen in unterschiedlicher Ausprägung typische, strukturell veränderte Gesichtszüge, sodass die Diagnose eines FAS auch phänoptypisch gestellt werden kann und gesellschaftlich häufig mit einer für das betroffene Kind massiv belastenden Stigmatisierung als „Säuferkind“ einhergeht. Bei den betroffenen Kindern wurde ferner ein erhöhtes Auftreten des Aufmerksamkeitsdefizit-/Hyperaktivitätssyndroms und anderer Verhaltensauffälligkeiten beschrieben [23, 114].
Nichtteratogene Schwellenwerte sind für Alkohol nicht bekannt [48].
Diagnostik. Diagnostisch ist zu klären, ob es sich um einen Missbrauch (riskanter Konsum >20 g Alkohol bei Frauen), um einen Abusus oder eine Abhängigkeit handelt, da besonders im Falle eines Abhängigkeitssyndroms eine vermehrte klinische psychische wie somatische Instabilität der Mutter vorliegen kann. Hilfreich für die Diagnose einer Alkoholerkrankung sind neben dem klinischen Befund verschiedene Laborparameter (z.B. Gamma-Glutamyltransferase, MCV, MCH, CDT-Wert) sowie die Bestimmung von Alkohol in Blut und Urin.
Entzugstherapie. Therapeutisch wird werdenden Müttern eine strikte Alkoholkarenz empfohlen [48]. Bei einem bestehenden Abhängigkeitssyndrom muss mit dem Auftreten einer umfassenden Entzugssymptomatik und gegebenenfalls mit Entzugskrampfanfällen bis hin zum Delir gerechnet werden, die eine kurzfristige medikamentöse Behandlung mit Benzodiazepinen (für einige Tage) notwendig werden lässt [101]. Dabei existieren bisher die meisten Erfahrungen zum Einsatz von Diazepam (z.B. Valium®, Achtung: Kategorie D [56]), Einzelheiten siehe in Teil II dieses Beitrags. Zu diesem Schluss kommen auch die Autoren eines Übersichtsbeitrags [52], indem sie zur medikamentösen Behandlung eines Alkoholentzugs am ehesten Diazepam empfehlen. Für einen Alkoholentzug ist eine stationäre Behandlung der Mutter notwendig, zudem muss eine begleitende Substitution von Vitamin B1 (Thiamin) und Elektrolyten wie Kalium und Magnesium erfolgen.
Zur Frage einer Entzugsbehandlung mit Clomethiazol (Distraneurin®) während der Schwangerschaft kann aufgrund einer bisher unvollständigen Datenlage keine Stellungnahme abgegeben werden; teratogene Effekte der Substanz sind jedoch bisher nicht bekannt [48, 110].
Rückfallprophylaktische Therapie. Grundsätzlich ist für die rückfallprophylaktische Therapie zu bemerken, dass es sich hierbei um eine den individuellen Bedürfnissen des suchtkranken Patienten angepasste multimodale Therapie handeln sollte, also um eine Kombination von psychiatrisch-psychotherapeutischen, besonders verhaltenstherapeutischen Therapieregimen in Kombination mit rückfallprophylaktischer medikamentöser Therapie und vielfältigen psychosozialen Therapien einschließlich der Teilnahme an Selbsthilfegruppen. Dabei muss die rückfallprophylaktische Therapie jeweils in Rahmen eines suchttherapeutischen Gesamtkonzepts eingesetzt werden.
Die medikamentöse Unterstützung einer Alkoholabstinenz mit Disulfiram (Antabus®, Kategorie C) ist bei nichtschwangeren Patienten im Rahmen eines Gesamtkonzepts hochwirksam [25, 124]. Dieses Arzneimittel ist seit Mai 2011 in Deutschland leider nicht mehr auf dem Markt; innerhalb Europas ist es in der Schweiz, in Frankreich und in Österreich weiterhin zugelassen. Disulfiram ist allerdings bei Schwangeren im ersten Trimenon kontraindiziert und wird auch im Verlauf der Schwangerschaft seitens der Fachinformation nicht empfohlen.
Für die rückfallprophylaktische „Anti-Craving“-Behandlung mit Acamprosat (Campral®, Kategorie C) liegen noch zu wenige Daten vor, sodass die Einnahme bei bestehender Schwangerschaft generell nicht empfohlen werden kann; in Tierversuchen hat sich jedoch bisher keine Feto-Teratogenität der Substanz bestätigt. Eine Acamprosat-Einnahme als Off-Label-Medikation zur Verhinderung potenzieller gravierender Auswirkungen auf den Fetus im Falle eines fortgesetzten Alkoholkonsums sollte daher im Rahmen einer Einzelfallentscheidung sehr sorgfältig abgewogen werden [1]. Solange noch keine Humandaten zur Teratotoxizität vorliegen, sollten jedoch nichtmedikamentöse Therapieregime bevorzugt werden [Fachinformation].
Seit Januar 2011 steht in Deutschland mit Naltrexon (Adepend®, Kategorie C) eine weitere Möglichkeit der medikamentösen rückfallpräventiven Unterstützung bei Alkoholabhängigen zur Verfügung. Klinische Daten über die Anwendung von Naltrexon während der Schwangerschaft liegen bisher nicht vor. Von einer Einnahme während der Schwangerschaft muss zum jetzigen Zeitpunkt aufgrund der Ergebnisse tierexperimenteller Studien zur Reproduktionstoxizität unbedingt abgeraten werden [Fachinformation].
Psychotherapeutische Ansätze gewinnen an Bedeutung, vor allem im Anschluss an die akute Entzugsbehandlung, wenn eine Eingliederung der Betroffenen in längerfristig angelegte Entwöhnungsprogramme oder suchtspezifische Langzeittherapien stattfindet. Im Zentrum psychotherapeutischer Arbeit mit Alkoholpatienten stehen – wie bei Suchtpatienten generell – verhaltenstherapeutische Interventionen wie Selbstmanagment-Therapie, Psychoedukation, soziales Kompetenztraining, Teilnahme an Selbsthilfegruppen, familientherapeutische Ansätze und zum Teil auch tiefenpsychologische Ansätze, etwa die Bearbeitung von inneren Grundannahmen und des daraus resultierenden eigenen Selbstbilds.
Zur suchttherapeutischen Langzeittherapie kann auch die zusätzliche Therapie der Patienten mit Antidepressiva gehören, da eigene Multicenterstudien des Norddeutschen Suchtforschungsverbunds mit 565 alkoholabhängigen Patienten ergaben, dass mehr als 50% dieser Patienten an anderen psychischen Erkrankungen leiden. Dabei kamen besonders Angst- und depressive Störungen häufig vor. Bei Frauen überwogen Angststörungen, die dann mit besonders häufigen Entgiftungsbehandlungen und schweren Entzugssymptomen einhergingen [112]. Zur Therapie opioidabhängiger Schwangerer mit Antidepressiva und den damit verbundenen Risiken siehe Teil II des Beitrags.
Unter Ausreizung aller therapeutischen Möglichkeiten stellt die Alkholabhängigkeit eine chronische Erkrankung mit begrenztem Heilungserfolg dar, bei der aber immerhin durchschnittlich 50% der Betroffenen nach Entzugs- und Entwöhnungstherapie langfristig abstinent bleiben können.
Psychostimulanzien
Toxizität. Amphetamine und Cocain sind plazentagängig und können eine Vasokonstriktion bewirken, unter anderem in der Plazenta. Dadurch steigt die Gefahr einer plazentären Minderperfusion bis hin zu regionalen Gewebsinfarkten. Die Folgen für das Ungeborene sind vielfältig und beinhalten mentale und körperliche Entwicklungsverzögerungen, Frühgeburten, ein verringertes Geburtsgewicht der Neugeborenen [47] bis hin zu organischen Fehlbildungen (bei exzessivem Drogenkonsum). In seltenen Fällen kommt es zum intrauterinen Absterben des Fetus [16]. Unter der Einnahme von Cocain und Crack wurden vorzeitige Plazentaablösungen, vorzeitige Blasensprünge sowie kardiale und neurologische Fehlbildungen beobachtet [16, 75, 32].
Cocain ist plazentagängig und wird vom Fetus metabolisiert. Im Falle eines regelmäßigen Cocain-Konsums seitens der Mutter entwickeln die Säuglinge nach der Geburt ein Entzugssyndrom mit vielfältigen Begleiterscheinungen wie psychomotorischer Agitation, Tachypnoe, Tachykardien und Schlafstörungen [96].
Hinsichtlich der Einnahme von Psychostimulanzien steht häufig ein polytoxikomanes Konsumverhalten im Vordergrund, sodass fetale Fehlbildungen und intrauterine Entwicklungsstörungen kausal nur sehr eingeschränkt auf die Einnahme spezifischer Drogen zurückgeführt werden können. Es konnte jedoch ein Zusammenhang zwischen der Einnahme von Cocain während der Frühschwangerschaft und einem vermehrten Auftreten von schweren fetalen Fehlbildungen wie Mikrozephalie, urogenitalen, kardialen und gastrointestinalen Veränderungen gefunden werden [75].
Nichtteratogene Schwellenwerte sind auch für Psychostimulanzien nicht bekannt [48].
Diagnostik. Die Diagnose einer psychostimulanzienbezogenen Störung kann nur anhand anamnestischer Daten, dem klinischen somatischen und psychiatrischen Befund sowie dem Urinbefund erfolgen.
Therapie. Therapeutisch wird den Müttern eine sofortige Abstinenz, also eine stationäre Entzugsbehandlung empfohlen. Bei Entzugssymptomen, die im Zweifelsfall neben den ausgeprägten psychischen Entzugssymptomen auch zu massiven vital bedrohlichen Komplikationen wie zerebralen Krampfanfällen, hypertensiven Krisen und vegetativen Entgleisungen führen können, kann unter Berücksichtigung der Verhältnismäßigkeit eine kurzzeitige Therapie mit Benzodiazepinen (Achtung FDA-Kategorie D, siehe Teil II) erwogen werden [101].
Im Anschluss an die Entzugsbehandlung sollte das Abstinenzverhalten zunächst weiter engmaschig psychiatrisch, gynäkologisch und allgemeinmedizinisch begleitet werden. Die medikamentöse Unterstützung einer Cocainabstinenz mit Disulfiram (Antabus®, Kategorie C) ist bei nichtschwangeren Patienten im Rahmen eines Gesamtkonzepts nach mehreren neuesten Publikationen (z.B. [124]) wirksam; in Deutschland war es aber bisher zu keinem Zeitpunkt dafür zugelassen. Grundsätzlich und besonders bei fortgesetzter Einnahme von Cocain und Amphetaminen während der Schwangerschaft sollten zumindest engmaschige gynäkologische sonographische Kontrollen und, wenn möglich, eine psychiatrische und allgemeinmedizinische Behandlung durchgeführt werden.
Die Geburt des Kindes sollte in einem Krankenhaus mit Neonatalzentrum stattfinden, um im Falle einer fetalen Entzugssymptomatik postpartal handlungsfähig zu sein.
Es gibt Hinweise darauf, dass ein Cocainkonsum während der Schwangerschaft als Prädiktor für spätere gewalttätige Übergriffe der Mutter gegenüber dem Kind gelten könnte [33]. Eine anschließende engmaschige und längerfristig anhaltende Betreuung der Mutter und des Säuglings durch ein interdisziplinäres Behandlerteam inklusive Ärzten, Psychologen, Hebammen und Sozialarbeitern ist daher grundsätzlich bei Suchtpatientinnen, aber ganz besonders bei Patientinnen mit Cocainkonsum während der Schwangerschaft, von großer Bedeutung.
Eine rückfallprophylaktische Therapie mit Desipramin (in Deutschland außer Handel, Kategorie C) und Fluoxetin (z.B. Fluctin®, Kategorie C) sowie mit Disulfiram (Kategorie C, mit Tagesdosierungen von über 250 mg) wurde bezüglich des Konsums von Cocain grundsätzlich als effektiv beschrieben [88, 111], diese Wirkstoffe können jedoch bei Schwangeren nicht eingesetzt werden (siehe Teil II des Beitrags).
Cannabis
Toxizität. Die Daten zu fetalen Komplikationen durch einen Cannabiskonsum während der Schwangerschaft sind bisher uneinheitlich. So konnte bisher keine Korrelation zwischen einem fortgesetzten Cannabiskonsum während der Schwangerschaft und einer erhöhten Fehlbildungsrate der Feten gefunden werden. Es gibt jedoch klare Hinweise auf eine erhöhte perinatale Sterblichkeit. Neugeborene von Frauen, die vor und während der Schwangerschaft Cannabis konsumiert hatten, zeigten darüber hinaus ein erhöhtes Risiko für ein erniedrigtes Geburtsgewicht, für eine Körperlänge unterhalb der dritten Perzentile sowie für die Entwicklung perinataler Komplikationen, sodass vermehrt intensivmedizinische Überwachungen notwendig wurden [52]. Zudem konnten in Tierversuchen durch Tetrahydrocannabinol (THC) Chromosomenbrüche induziert werden [48, 68]. In In-vitro-Untersuchungen wurde ferner eine Inhibition der Plazentaentwicklung durch Hemmung der Trophoblasten gezeigt, jedoch ist die klinische Relevanz dieser Ergebnisse bisher unklar [68]. Unter regelmäßigem Konsum von Marihuana war die CO-Blutkonzentration im Vergleich zu tabakrauchenden Schwangeren bis zum Fünffachen erhöht, weiterhin wurde unter Einfluss von Tetrahydrocannabinol ein Absinken der fetalen Herzfrequenz gefunden [110].
Im Langzeitverlauf zeigten Kinder von Frauen, die während der Schwangerschaft regelmäßig Marihuana konsumiert hatten, verminderte kognitive Leistungen und reduzierte Gedächtnisleistungen [40, 39, 59].
Was die fetalen Risiken eines Cannabiskonsums während der Schwangerschaft betrifft, besteht laut Gerardin et al. noch ein erheblicher Informationsmangel bei den interdisziplinären Behandlerteams [44].
Arzneimittel, die cannabinoidartige Substanzen (z.B. Tetrahydrocannabinol, Cannabis, Cannabinol) enthalten, können seit einer Änderung der betäubungsmittelrechtlichen Vorschriften im Mai 2011 in Deutschland zur Therapie unterschiedlicher Erkrankungen zugelassen werden. Eine Zuordnung nach den FDA-Kriterien gibt es bisher aber nicht.
Diagnostik. Die Diagnose einer cannabisbezogenen Störung kann nur anhand von anamnestischen Daten, dem klinischen somatischen und psychiatrischen Befund sowie dem Urinbefund erfolgen.
Therapie. Vor dem Hintergrund der aktuell noch ungeklärten Risikolage und den bereits existierenden Hinweisen auf eine mögliche Beeinträchtigung der fetalen Entwicklung durch einen Cannabiskonsum während der Schwangerschaft wird aus ärztlicher Sicht auf die Notwendigkeit einer strikten Cannabisabstinenz hingewiesen [48].
Im Falle eines regelmäßigen vorangegangenen Substanzmissbrauchs sollte ein Entzug unter kontrollierten medizinischen Bedingungen im stationären Setting stattfinden. Zur Kupierung einer auftretenden Entzugssymptomatik und von psychotischen Symptomen mit Angst- und Panikattacken kann dabei auf Benzodiazepine, vorrangig Diazepam (Kategorie D), für einen kurzen Zeitraum oder mehrere einzelne Gaben zurückgegriffen werden [101, 110]. Bei einem Entzug von Cannabinoiden ist zu beachten, dass der Urin der Patienten besonders nach chronischem oder täglichem Gebrauch von Cannabinoiden noch wochenlang nach der letzten Einnahme positiv sein kann und auch Entzugssymptome entsprechend über Wochen bis Monate andauern können [13, 111].
Eine rückfallspezifische Medikation hinsichtlich der Einnahme von Cannabinoiden existiert bisher nicht. Bei Nichtschwangeren könnte eine antidepressive Therapie wirksam sein, da viele Cannabiskonsumenten an einem amotivationalen Syndrom leiden. Zur Therapie einer schweren Depression bei Schwangeren siehe Teil II.
Begleitend zum Cannabiskonsum wird häufig ausgeprägtes Tabakrauchen beobachtet. In diesem Falle ist das Risiko für eine intrauterine fetale Schädigung deutlich erhöht und ein sofortiges Beenden und eine entsprechen Entzugsbehandlung des Cannabis- und Tabakkonsums unbedingt zu empfehlen.
Sedativa
Toxizität. Innerhalb der Sedativa wird zwischen Hypnotika (Barbiturate und Benzodiazepine) und Tranquillanzien (Benzodiazepine) unterschieden, wobei Barbiturate heute eine eher untergeordnete Rolle spielen. Unter der regelmäßigen Einnahme von Benzodiazepinen während des ersten Trimenons der Schwangerschaft wird eine Zunahme insbesondere kardialer und orofazialer Fehlbildungen beim Fetus diskutiert [79].
Wenn während der Spätschwangerschaft regelmäßig Benzodiazepine eingenommen werden, muss beim Säugling nach der Geburt mit der Entwicklung eines Floppy-Infant-Syndroms gerechnet werden. Darunter versteht man eine generalisierte massive Muskel- und Atemschwäche des Säuglings mit Temperaturregulationsstörungen als Folge einer fetalen Aufnahme der grundsätzlich plazentagängigen Benzodiazepine; die Symptomatik kann dosisabhängig unterschiedlich stark ausgeprägt sein und über mehrere Tage anhalten [3]. Auch mit einer zeitlich verzögerten Entwicklung von vegetativen Entzugssymptomen in Form von Tachypnoe, Tachykardie, vermehrtem Schwitzen und Zittern beim Säugling muss gerechnet werden, weshalb die Geburt auch in diesem Fall zur Gewährleistung einer ausreichenden Versorgung des Neugeborenen in einem Neonatalzentrum erfolgen sollte [117].
Die Arbeitsgruppe Leppee et al. fand heraus, dass ein Drittel von knapp 900 schwangeren, hospitalisierten Frauen während der Schwangerschaft Diazepam eingenommen hatten; ein derart hoher Prozentsatz einer Diazepam-Einnahme während der Schwangerschaft spricht dafür, dass die nachgewiesene Gefährdung der Ungeborenen durch die Einnahme von Benzodiazepinen in der Schwangerschaft in der Praxis zu wenig beachtet wird [73]. Diazepam wird von der FDA in Kategorie D eingestuft: dem Wirkstoff wird also ein erhöhtes fetales Risiko attestiert und dennoch wird von einer Einnahme in der Schwangerschaft nicht grundsätzlich abgeraten – die Einnahme muss daher individuell im Rahmen eines Risiko-Nutzen-Vergleichs diskutiert werden.
Diagnostik. Die Diagnostik von Abusus oder Abhängigkeit erfolgt aus einem positiven Urinbefund für Benzodiazepine und dem klinischen Befund. Ein positiver Urinbefund bei klinisch unauffälligen, nicht sediert wirkenden Patienten mag im ersten Moment verwundern – diese Konstellation ist jedoch insbesondere bei Vorliegen einer Abhängigkeit nicht selten.
Therapie. Therapeutisch wird ein schrittweises (semilogarithmisches) Ausschleichen der Sedativa noch während der Schwangerschaft empfohlen; eingesetzt werden sollte hierfür noch am ehesten Diazepam [3]. Der Entzug sollte nur sehr langsam und unbedingt unter kontrollierten medizinischen Bedingungen (vorrangig im stationären Setting) erfolgen.
Zusammenfassung und Konsequenzen
Für alle hier genannten Suchtstoffe existieren für den Fall eines Konsums während der Schwangerschaft keine Grenzwerte für die Entwicklung von Akut- oder Langzeitschäden bei den betroffenen Kindern. Es hat sich jedoch gezeigt, dass der Konsum der einzelnen Suchtstoffe während der Schwangerschaft mit einer erhöhten Prävalenz des plötzlichen Kindstods (Sudden Infant Death Syndrome) beim Neugeborenen einhergeht [14, 79, 97, 118].
Zusammengefasst ist daher bei schwangeren opioidabhängigen Frauen eine meist stationäre Entzugsbehandlung der Beikonsumsubstanzen zu empfehlen (Tab. 4); eine Ausnahme ist die Raucherentwöhnung, die auch ambulant erfolgen kann. Für die Behandlung der Opioidabhängigkeit selbst ist eine Substitutionstherapie mit Methadon/Levomethadon oder Buprenorphin klar indiziert, da ein Opioidentzug während der Schwangerschaft mit deutlich größeren Risiken für das Ungeborene einhergeht als die Einnahme von Substitutionsopioiden.
Tab. 4. Therapie von Substanzabhängigkeiten während der Schwangerschaft
|
Suchtstoff |
Therapie, Hinweise zur Geburt und zur Versorgung des Neugeborenen |
|
Heroin |
Substitution mit Opioiden! Einschleichende medikamentöse Therapie mit Buprenorphin (Kategorie C), Levomethadon oder D/L- Methadon (Kategorie C) unter Absetzen von Heroin. Möglicherweise Reduktion des Risikos für ein neonatales Entzugssyndrom durch Substitution mit Buprenorphin gegenüber einer Substitution mit Methadon (Datenlage unklar). Bei intensivabhängigen Patientinnen kann eine Substitution mit Methadon notwendig werden, da wirksamere Kupierung der Entzugssymptomatik als mit Buprenorphin. Geburt muss in einem Krankenhaus mit der Möglichkeit einer pädiatrischen Intensivversorgung erfolgen, da schwere neonatale Entzugssymptome zu vitaler Gefährdung des Neugeboren führen können. |
|
Tabak |
Abstinenz! Für Entwöhnung: Strukturierte Raucherentwöhnungsprogramme. Bei exzessivem Suchtverhalten ist eine Nicotinersatztherapie unter Nutzen-Risiko-Abwägung in Betracht zu ziehen (Cave: Datenlage rar). |
|
Alkohol |
Abstinenz! Stationäre Entzugsbehandlung: Symptomorientiert; kurzfristige Therapie mit Benzodiazepinen (z.B. Diazepam, Kategorie D) möglich, bei deliranter Symptomatik Diazepam plus antipsychotische Therapie mit Haloperidol (Kategorie C). Zusätzlich Gabe von Thiamin (Vitamin B1), Elektrolyten und Magnesium. Rückfallprophylaxe bei Abstinenz: Arzneimittel bei unklarer Datenlage generell nicht zu empfehlen. Bei schwerster Suchterkrankung kann nach dem 1. Trimenon die Einnahme von Acamprosat (Kategorie C) unter sorgfältiger Risiko-Nutzen-Abwägung in Betracht gezogen werden. Suchtspezifische Langzeittherapien und Entwöhnungstherapien mit verhaltenstherapeutischen, psychoedukativen und tiefenpsychologisch fundierten Therapieangeboten sind zu empfehlen. |
|
Psychostimulanzien (Amphetamine und Cocain) |
Abstinenz! Entzugsbehandlung: Möglichst frühzeitige stationäre Aufnahme; symptomorientiert, kurzfristige Therapie mit Benzodiazepinen (z.B. Diazepam, Kategorie D) möglich. Rückfallprophylaxe bei Abstinenz: verhaltenstherapeutische Maßnahmen, Psychoedukation. Keine rückfallprophylaktische medikamentöse Therapie bei Schwangeren möglich. Im Anschluss an die Geburt ist eine engmaschige und längerfristige interdisziplinäre Betreuung von Mutter und Kind notwendig. |
|
Cannabis |
Abstinenz! Entzugsbehandlung: Symptomorientiert, bei Angst- und Panikzuständen im stationären, im Verlauf gegebenenfalls in teilstationärem Rahmen medikamentös unterstützte kurzfristige Anxiolyse mit Benzodiazepinen (z.B. Diazepam, Kategorie D). Bei schwerer depressiver Symptomatik ist unter Risiko-Nutzen-Abwägung gegebenenfalls eine medikamentöse antidepressive Therapie in Betracht ziehen (siehe Teil II des Beitrags) |
|
Sedativa |
Abstinenz! Entzugsbehandlung: Langsamer Entzug (semilogarithmisch) durch schrittweise Reduktion der konsumierten Substanzmenge unter stationären Bedingungen. Geburt muss in Neonatalzentrum erfolgen, da ein Benzodiazepinkonsum in der Spätschwangerschaft zu einem „Floppy-Infant-Syndrom“ mit vitaler Gefährdung des Säuglings führen kann. |
Aus ärztlicher Sicht stellt ein Drogenkonsum der Mutter während der Schwangerschaft per se keine alleinige Indikation zur Abtreibung dar. Dennoch sollte bei opioidabhängigen Schwangeren gynäkologischerseits eine intensivierte sonographische Diagnostik des Ungeborenen insbesondere während des zweiten Trimenons erfolgen, um eventuelle schwere Fehlbildungen frühzeitig zu erkennen und mögliche Konsequenzen mit der Mutter zu besprechen. Durch pränatale Ultraschalluntersuchungen ist es jedoch nachvollziehbarerweise nicht möglich, eine spätere geistige Entwicklungsverzögerung oder eine mentale Retardierung beim Kind festzustellen.
Literatur
1. Adde-Michel C, Hennebert O, Laudenbach V, Marret S, et al. Effect of acamprosate on neonatal excitotoxic cortical lesions in in utero alcohol-exposed hamsters. Neurosci Lett 2005;374:109–12.
2. Arshad M, El-Kamary SS, Jhaveri R. Hepatitis C virus infection during pregnancy and the newborn period – are they opportunities for treatment? J Viral Hepat 2011;18:229–36.
3. AWMF-Leitlinien für Sedativa/Benzodiazepine: www.awmf.org/leitlinien/detail/ll/076-009.html.
4. AWMF-Leitlinien für Tabakbedingte Störungen. Leitlinie Tabakentwöhnung. [Artikel] // www.sucht.de/tl_files/pdf/11_05_03.pdf.5.Batra A. [Tobacco dependence – evidence-based treatment strategies] Z Arztl Fortbild Qualitatssich 2002;96:281–6.
6. Berle JO, Solberg DK, Spigset O. [Treatment of bipolar disorder during pregnancy and in the postpartum period] Tidsskr Nor Laegeforen 2011;131:126–9.
7. Bleich S, Havemann-Reinecke U, Kornhuber J. Fagerström-Test für Nikotinabhängigkeit. Göttingen: Beltz Test GmbH, 2002.
8. Bodén R, Lundgren M, Brandt L, Reutfors J, et al. Risks of adverse pregnancy and birth outcomes in women treated or not treated with mood stabilisers for bipolar disorder: population based cohort study. BMJ 2012;345:e7085. doi: 10.1136/bmj.e7085.
9. Bohus M, editor. Borderline-Störung. Göttingen: Hogrefe Verlag für Psychologie, 2002.
10. Bonnet U, Scherbaum N. Evidenzbasierte Behandlung der Cannabisabhängigkeit. Dt Ärzteblatt 2005;102:A3334–41.
11. Brzozka MM, Falkai P, Havemann-Reinecke U. Für Schizophrenie braucht man Drei. Suchtmed 2009;11:98–103.
12. Brünen S, Vincent PD, Baumann P, Hiemke C, et al. Therapeutic drug monitoring (TDM) for drugs used in the treatment of substance related disorders. Literature review using a TDM appropriateness rating scale. Ther Drug Monit 2011;33:561–72.
13. Budney AJ, Hughes JR, Moore BA, Vandrey R. Review of the validity and significance of cannabis withdrawal syndrome. Am J Psychiatry 2004;161:1967–77.
14. Burns L, Conroy E, Mattick RP. Infant mortality among women on a methadone program during pregnancy. Drug Alcohol Rev 2010;29:551–6.
15. Chambers CD, Hernandez-Diaz S, Van Marter LJ, et al. Selective serotonin-reuptake inhibitors and risk of persistent pulmonary hypertension of the newborn. N Engl J Med 2006;354:579–87.
16. Chasnoff IJ, Burns WJ, Schnoll SH, Burns KA. Cocaine use in pregnancy. N Engl J Med 1985;313:666–9.
17. Chung KC, Kowalski CP, Kim HM, Buchman SR. Maternal cigarette smoking during pregnancy and the risk of having a child with cleft lip/palate. Plast Reconstr Surg 2000;105: 485–91.
18. Clark SM, Nakad R. Pharmacotherapeutic management of nicotine dependence in pregnancy. Obstet Gynecol Clin North Am 2011;38:297–311.
19. Cleary B, Reynolds K, Eogan M, O’Connell M, et al. Methadone dosing and prescribed medication use in a prospective cohort of opioid-dependent pregnant women. Addiction 2012; doi: 10.1111/add.12078 [Epub ahead of print].
20. Cohen LS, Friedman JM, Jefferson JW, Johnson EM, et al. A reevaluation of risk of in utero exposure to lithium. JAMA 1994;271:146–50.
21. Cole JA, Modell JG, Haight BR, Cosmatos IS, et al. Bupropion in pregnancy and the prevalence of congenital malformations. Pharmacoepidemiol Drug Saf 2007;16: 474–84.
22. Coleman T, Chamberlain C, Cooper S, Leonardi-Bee J. Efficacy and safety of nicotine replacement therapy for smoking cessation in pregnancy: systematic review and meta-analysis. Addiction 2011;06:52–61.
23. Coles CD, Platzman KA. Behavioral development in children prenatally exposed to drugs and alcohol. Int J Addict 1993;28: 1393–433.
24. Coyle MG, Salisbury AL, Lester BM, Jones HE, et al. Neonatal neurobehavior effects following buprenorphine vs. methadone exposure. Addiction 2012;107(Suppl 1):63–73.
25. De Sousa A. A one-year pragmatic trial of naltrexone vs. disulfiram in the treatment of alcohol dependence. Alcohol Alcohol 2004;39:528–31.
26. Dempsey DA, Benowitz NL. Risks and benefits of nicotine to aid smoking cessation in pregnancy. Drug Saf 2001;24:277–322.
27. Deutsch-Österreichische Leitlinien zur HIV-Therapie bei Schwangeren und Neugeborenen. www.rki.de/DE/Content/InfAZ/H/HIVAIDS/Therapie/Leitlinien/PDF__D__A__schwanger.html (Zugriff am 24.10.2011).
28. Diav-Citrin O, Shechtman S, Ornoy S, et al. Safety of haloperidol and penfluridol in pregnancy: a multicenter, prospective, controlled study. J Clin Psychiatry 2005;66:317–22.
29. Djulus J, Koren G, Einarson TR, et al. Exposure to mirtazapine during pregnancy: a prospective, comparative study of birth outcomes. J Clin Psychiatry 2006;67:1280–4.
30. Driessen M, Schulte S, Luedecke C, et al. Trauma and PTSD in patients with alcohol, drug, or dual dependence: a multi-center study. Alcohol Clin Exp Res 2008;32:481–8.
31. Drogen- und Suchtbericht 2011, www.drogenbeauftragte.de/fileadmin/dateien-dba/Service/Publikationen/Drogen_und_Suchtbericht_2011_110517_Drogenbeauftragte.pdf (Zugriff am 24.10.2011).
32. Dusick AM, Covert RF, Schreiber MD, et al. Risk of intracranial hemorrhage and other adverse outcomes after cocaine exposure in a cohort of 323 very low birth weight infants. J Pediatr 1993;122:438–45.
33. Eiden RD, Schuetze P, Colder CR, Veira Y. Maternal cocaine use and mother-toddler aggression. Neurotoxicol Teratol 2011;33: 360–9.
34. Einarson A, Choi J, Einarson TR, Koren G. Incidence of major malformations in infants following antidepressant exposure in pregnancy: results of a large prospective cohort study. Can J Psychiatry 2009;54:242–6.
35. Empfehlung der ständigen Impfkommission des Robert-Koch-Institut Stand April 2011 www.rki.de/cln_160/nn_199630/SharedDocs/FAQ/Impfen/AllgFr__AllgemeineFragen/FAQ08.html (Zugriff am 24.10.2011).
36. Ericson A, Kallen B, Wiholm B. Delivery outcome after the use of antidepressants in early pregnancy. Eur J Clin Pharmacol 1999;55:503–8.
37. Ferger B, Havemann-Reinecke U, Kuschinsky K. Dopamin und Suchterkrankungen. Med Monatsschr Pharm 1997;20:300–9.
38. Florescu A, Ferrence R, Einarson T, Selby P, et al. Methods for quantification of exposure to cigarette smoking and environmental tobacco smoke: focus on developmental toxicology. Ther Drug Monit 2009;31:14–30.
39. Fried PA, Watkinson B. 36- and 48-month neurobehavioral follow-up of children prenatally exposed to marijuana, cigarettes, and alcohol. J Dev Behav Pediatr 1990;11:49–58.
40. Fried PA, Watkinson B, Gray R. Differential effects on cognitive functioning in 13- to 16-year-olds prenatally exposed to cigarettes and marihuana. Neurotoxicol Teratol 2003;25:427–36.
41. Galbally M, Roberts M, Buist A. Mood stabilizers in pregnancy: a systematic review. Aust N Z J Psychiatry 2010;44:967–77.
42. Gentile S. Drug treatment for mood disorders in pregnancy. Curr Opin Psychiatry 2011;24:34–40.
43. Gentile S. Selective serotonin reuptake inhibitor exposure during early pregnancy and the risk of birth defects. Acta Psychiatr Scand 2011;123:266–75.
44. Gerardin M, Victorri-Vigneau C, Louvigne C, Rivoal M, et al. Management of cannabis use during pregnancy: an assessment of healthcare professionals’ practices. Pharmacoepidemiol Drug Saf 2011;20:464–73. doi: 10.1002/pds.2095.
45. Glaeske B. Psychotrope und andere Arzneimittel mit Missbrauchs- und Abhängigkeitspotenzial. In: Deutsche Hauptstelle für Suchtfragen e.V. (Hrsg.). Jahrbuch Sucht 2009. Geesthacht: Neuland, 2009: 93–4.
46. Gold LH. Treatment of depression during pregnancy. J Womens Health Gend Based Med 1999;8:601–7.
47. Gouin K, Murphy K, Shah PS. Effects of cocaine use during pregnancy on low birthweight and preterm birth: systematic review and metaanalyses. Am J Obstet Gynecol 2011;204:340–12.
48. Günthert A. Substanzkonsum in der Schwangerschaft. In: Mann K, Havemann-Reinecke U, Gassmann R (Hrsg.). Jugendliche und Suchtmittelkonsum. Band 2, überarbeitete Auflage. Freiburg i. Br.: Lambertus, 2009: 126–39.
49. Haustein KO. Cigarette smoking, nicotine and pregnancy. Int J Clin Pharmacol Ther 1999;37:417–27.
50. Havemann-Reinecke U. Die Bedeutung zentraler dopaminerger Neurone für die Entwicklung von Abhängigkeit am Beispiel der Opioide. Aachen: Shaker Verlag, 2002.
51. Hayatbakhsh MR, Flenady VJ, Gibbons KS, Kingsbury AM, et al. Birth outcomes associated with cannabis use before and during pregnancy. Pediatr Res 2012;71:215–9. doi: 10.1038/pr.2011.25. Epub 2011 Dec 21.
52. Heberlein A, Leggio L, Stichtenoth D, Hillemacher T. The treatment of alcohol and opioid dependence in pregnant women. Curr Opin Psychiatry 2012;25:559–64.
53. Hernández-Díaz S, Smith CR, Shen A, Mittendorf R, et al.; North American AED Pregnancy Registry; North American AED Pregnancy Registry. Comparative safety of antiepileptic drugs during pregnancy. Neurology 2012;78:1692–9.
54. Hiemke C, Baumann P, Bergemann N, Conca A, et al. AGNP consensus guidelines for therapeutic drug monitoring in psychiatry. Update 2011. Pharmacopsychiatry 2011;44:195–235.
55. Hoell I, Amanzada A, Degner D, Havemann-Reinecke U. Therapie von schwangeren Patientinnen mit Abhängigkeit von Opioiden und begleitenden Suchtstoffen. Teil II: Therapie der Komorbiditäten. Med Monatsschr Pharm 2011;34:418–25.
56. Hoell I, Havemann-Reinecke U. Therapie von schwangeren Patientinnen mit Abhängigkeit von Opioiden und begleitenden Suchtstoffen. Teil I: Toxische Folgen und therapeutische Konsequenzen. Med Monatsschr Pharm 2011;34:363–74.
57. Hoffmann C, Rockstroh JK (editors). HIV 2010. Hamburg: Medizin Fokus Verlag, 2010.
58. Holmes LB, Mittendorf R, Shen A, Smith CR, et al. Fetal effects of anticonvulsant polytherapies: Different risks from different drug combinations. Arch Neurol 2011;68:1275–81 (doi:10.1001/archneurol.2011.133).
59. Huizink AC, Mulder EJ. Maternal smoking, drinking or cannabis use during pregnancy and neurobehavioral and cognitive functioning in human offspring. Neurosci Biobehav Rev 2006;30:24–41.
60. Inder D, Rehan HS, Yadav M, Manak S, et al. IFN-alpha-2a (Interferon) and ribavirin induced suicidal attempt in a patient of chronic HCV: A rare case report. Indian J Pharmacol 2011;43:210–211.
61. Jones HE, Heil SH, Baewert A, Arria AM, et al. Buprenorphine treatment of opioid-dependent pregnant women: a comprehensive review. Addiction 2012;107(Suppl 1):5–27.
62. Jones HE, Kaltenbach K, Heil SH, et al. Neonatal abstinence syndrome after methadone or buprenorphine exposure. N Engl J Med 2010;363:2320–31.
63. Jones KL, Smith DW. Recognition of the fetal alcohol syndrome in early infancy. Lancet 1973;302:999–1001.
64. Kaaja E, Kaaja R, Hiilesmaa V. Major malformations in offspring of women with epilepsy. Neurology 2003;60:575–9.
65. Kakko J, Heilig M, Sarman I. Buprenorphine and methadone treatment of opiate dependence during pregnancy: comparison of fetal growth and neonatal outcomes in two consecutive case series. Drug Alcohol Depend 2008;96:69–78.
66. Kandall SR, Doberczak TM, Jantunen M, Stein J. The methadone-maintained pregnancy. Clin Perinatol 1999;26:173–83.
67. Kaneko S, Battino D, Andermann E, et al. Congenital malformations due to antiepileptic drugs. Epilepsy Res 1999;33:145–58.
68. Khare M, Taylor AH, Konje JC, Bell SC. Delta9-tetrahydrocannabinol inhibits cytotrophoblast cell proliferation and modulates gene transcription. Mol Hum Reprod 2006;12:321–33.
69. Klier CM, Mossaheb N, Saria A, Schloegelhofer M, et al. Pharmacokinetics and elimination of quetiapine, venlafaxine, and trazodone during pregnancy and postpartum. J Clin Psychopharmacol 2007;27:720–2.
70. Koch L. SSRIs and congenital abnormalities. Nature Rev Endocrinol 2011;7:499.
71. Lackmann GM, Salzberger U, Tollner U, Chen M, et al. Metabolites of a tobacco-specific carcinogen in urine from newborns. J Natl Cancer Inst 1999;91:459–65.
72. Lacroix I, Berrebi A, Garipuy D, et al. Buprenorphine versus methadone in pregnant opioid-dependent women: a prospective multicenter study. Eur J Clin Pharmacol 2011;67:1053–9.
73. Leppee M, Culig J, Eric M, Sijanovic S. The effects of benzodiazepines in pregnancy. Acta Neurol Belg 2010;110:163–7.
74. Little BB, Snell LM, Klein VR, Gilstrap LC, et al. Maternal and fetal effects of heroin addiction during pregnancy. J Reprod Med 1990;35:159–62.
75. Little BB, Wilson GN, Jackson G. Is there a cocaine syndrome? Dysmorphic and anthropometric assessment of infants exposed to cocaine. Teratology 1996;54:145–9.
76. Lopez M, Coll O. Chronic viral infections and invasive procedures: risk of vertical transmission and current recommendations. Fetal Diagn Ther 2010;28:1–8.
77. Malm H, Artama M, Gissler M, Ritvanen A. Selective serotonin reuptake inhibitors and risk for major congenital anomalies. Obstet Gynecol 2011;118:111–20.
78. McCance-Katz EF. Drug interactions associated with methadone, buprenorphine, cocaine, and HIV medications: Implications for pregnant women. Life Sci 2011;88:953–8.
79. McElhatton PR. The effects of benzodiazepine use during pregnancy and lactation. Reprod Toxicol 1994;8:461–75.
80. Mulder EJ, Ververs FF, de Heus R, Visser GH. Selective serotonin reuptake inhibitors affect neurobehavioral development in the human fetus. Neuropsychopharmacology 2011;36:1961–71. Epub 2011 Apr 27 (doi: 10.1038/npp.2011.67).
81. Naeye RL, Blanc W, Leblanc W, Khatamee MA. Fetal complications of maternal heroin addiction: abnormal growth, infections, and episodes of stress. J Pediatr 1973;83:1055–61.
82. Najavits LM. Seeking safety protocol for men and women. Psychiatr Serv 2007;58:1376.
83. Norddeutscher Suchtforschungsverbund: www.nsfev.de.
84.Nordeng H, Lindemann R, Perminov KV, Reikvam A. Neonatal withdrawal syndrome after in utero exposure to selective serotonin reuptake inhibitors. Acta Paediatr 2001;90:288–91.
85. Nulman I, Koren G, Rovet J, Barrera M, et al Neurodevelopment of children following prenatal exposure to venlafaxine, selective serotonin reuptake inhibitors, or untreated maternal depression. Am J Psychiatry 2012;169:1165–74.
86. O’Reardon JP, Cristancho MA, von Andreae CV, Cristancho P, et al. Acute and maintenance electroconvulsive therapy for treatment of severe major depression during the second and third trimesters of pregnancy with infant follow-up to 18 months: case report and review of the literature. J ECT 2011;27:e23–6.
87. Oberlander TF, Warburton W, Misri S, Riggs W, et al. Major congenital malformations following prenatal exposure to serotonin reuptake inhibitors and benzodiazepines using population-based health data. Birth Defects Res B Dev Reprod Toxicol 2008;83:68–76.
88. Oliveto A, Poling J, Mancino MJ, et al. Randomized, double blind, placebo-controlled trial of disulfiram for the treatment of cocaine dependence in methadone-stabilized patients. Drug Alcohol Depend 2011;113:184–91.
89. Ornoy A, Segal J, Bar-Hamburger R, Greenbaum C. Developmental outcome of school-age children born to mothers with heroin dependency: importance of environmental factors. Dev Med Child Neurol 2001;43:668–75.
90. Ozkan H, Cetinkaya M, Koksal N, Yapici S. Severe fetal valproate syndrome: combination of complex cardiac defect, multicystic dysplastic kidney, and trigonocephaly. J Matern Fetal Neonatal Med 2011;24:521–4.
91. Palmsten K, Hernandez-Diaz S. Can nonrandomized studies on the safety on antidepressants during pregnancy convincingly beat confounding, chance, and prior beliefs? Epidemiology 2012;23:686–8.
92. Pariante CM, Seneviratne G, Howard L. Should we stop using tricyclic antidepressants in pregnancy? Psychol Med 2011;41:15–7.
93. Parry BL, Curran ML, Stuenkel CA, et al. Can critically timed sleep deprivation be useful in pregnancy and postpartum depressions? J Affect Disord 2000;60:201–12.
94. Pedersen LH, Henriksen TB, Bech BH, Licht RW, et al. Prenatal antidepressant exposure and behavioral problems in early childhood – a cohort study. Acta Psychiatr Scand 2012; doi: 10.1111/acps.12032. [Epub ahead of print]
95. Pedersen LH, Henriksen TB, Vestergaard M, Olsen J, et al. Selective serotonin reuptake inhibitors in pregnancy and congenital malformations: population based cohort study. BMJ 2009;339:b3569.
96. Peters H, Theorell CJ. Fetal and neonatal effects of maternal cocaine use. J Obstet Gynecol Neonatal Nurs 1991;20:121–6.
97. Pinho AP, Nunes ML. Epidemiological profile and strategies for diagnosing SIDS in a developing country. J Pediatr (Rio J ) 2011;87:115–22.
98. Puente D, Cabezas C, Rodriguez-Blanco T, et al. The role of gender in a smoking cessation intervention: a cluster randomized clinical trial. BMC Public Health 2011;11:369.
99. Reis M, Källén B. Delivery outcome after maternal use of antidepressant drugs in pregnancy: an update using Swedish data. Psychol Med 2010;40:1723–33.
100. Robert-Koch-Institut zur Inzidenz von Hepatitis A: www.rki.de/cln_116/nn_468098/DE/Content/Infekt/EpidBull/Archiv/2008/44__08,templateId=raw,property=publicationFile.pdf/44_08.pdf (Zugriff am 24.10.2011).
101. Rohde A, Schaefer C. Psychopharmakotherapie in Schwangerschaft und Stillzeit. Möglichkeiten und Grenzen. Stuttgart: Thieme, 2006: 1.
102. Rupprecht R, Soyka M, Grohmann R, Rüther E, et al. Zur Problematik der Kombination von Clozapin mit Benzodiazepinen. Der Nervenarzt 2004;75:857–60.
103. Saatcioglu O, Tomruk NB. The use of electroconvulsive therapy in pregnancy: a review. Isr J Psychiatry Relat Sci 2011;48:6–11.
104. Saber-Tehrani AS, Bruce RD, Altice FL. Pharmacokinetic drug interactions and adverse consequeces between psychotropic medications and pharmacotherapy for the treatment of opioid dependence. Am J Drug Alcohol Abuse 2011;37:1–11.
105. Sampson PD, Streissguth AP, Bookstein FL, et al. Incidence of fetal alcohol syndrome and prevalence of alcohol-related neurodevelopmental disorder. Teratology 1997;56:317–26.
106. Sarkola T, Eriksson CJ, Niemela O, Sillanaukee P, et al. Mean cell volume and gamma-glutamyl transferase are superior to carbohydrate-deficient transferrin and hemoglobin-acetaldehyde adducts in the follow-up of pregnant women with alcohol abuse. Acta Obstet Gynecol Scand 2000;79:359–66.
107. Sasadeusz JJ, Dore G, Kronborg I, Barton D, et al. Clinical experience with the treatment of hepatitis C infection in patients on opioid pharmacotherapy. Addiction 2011;106:977–84.
108. Sasco AJ, Vainio H. From in utero and childhood exposure to parental smoking to childhood cancer: a possible link and the need for action. Hum Exp Toxicol 1999;18:192–201.
109. Schäfer I, Langeland W, Hissbach J, et al. Childhood trauma and dissociation in patients with alcohol dependence, drug dependence, or both – A multi-center study. Drug Alcohol Depend 2010;109:84–9.
110. Schäfer C, Spielmann H, Vetter L. Arzneimittelverordnung in Schwangerschaft und Stillzeit. 7. Auflage. München: Elsevier/Urban & Fischer, 2006.
111. Schmidt LG, Gastpar M, Falkai P, Gaebel W (editors). Evidenzbasierte Suchtmedizin. Behandlungsleitlinie Substanzbezogene Störungen. Köln: Deutscher Ärzte-Verlag, 2006.
112. Schneider U, Altmann A, Baumann M, et al. Comorbid anxiety and affective disorder in alcohol-dependent patients seeking treatment: the first multicentre study in Germany. Alcohol Alcohol 2001;36:219–23.
113. Slone D, Siskind V, Heinonen OP, Monson RR, et al. Antenatal exposure to the phenothiazines in relation to congenital malformations, perinatal mortality rate, birth weight, and intelligence quotient score. Am J Obstet Gynecol 1977;128:486–8.
114. Spohr HL, Willms J, Steinhausen HC. Prenatal alcohol exposure and long-term developmental consequences. Lancet 1993;341:907–10.
115. Stauber RE, Jauk B, Fickert P, Hausler M. Increased carbohydrate-deficient transferrin during pregnancy: relation to sex hormones. Alcohol Alcohol 1996;31:389–92.
116. Stephansson O, Kieler H, Haglund B, Artama M, et al. Selective serotonin reuptake inhibitors during pregnancy and risk of stillbirth and infant mortality. JAMA 2013;309:48–54.
117. Sutton LR, Hinderliter SA. Diazepam abuse in pregnant women on methadone maintenance. Implications for the neonate. Clin Pediatr (Phila) 1990;29:108–11.
118. Thomas DB. Cleft palate, mortality and morbidity in infants of substance abusing mothers. J Paediatr Child Health 1995;31:457–60.
119. Udechuku A, Nguyen T, Hill R, Szego K. Antidepressants in pregnancy: a systematic review. Aust N Z J Psychiatry 2010;44:978–96.
120. Watts DH, Williams PL, Kacanek D, Griner R, et al.; for the Pediatric HIV/AIDS Cohort Study. Combination antiretroviral use and preterm birth. J Infect Dis 2012 [Epub ahead of print Nov 29].
121. Wedekind D, Havemann-Reinecke U. Sucht, psychiatrische Komorbidität und das serotonerge System. Nervenheilkunde 2009;28:509–13.
122. Wedekind D, Jacobs S, Karg I, et al. Psychiatric comorbidity and additional abuse of drugs in maintenance treatment with l- and d,l-methadone. World J Biol Psychiatry 2008;9:1–10.
123. Wedekind D, Jacobs S, Poser W, Rüther E, et al. Comorbidity in heroin and cocaine addiction. German Journal of Psychiatry 2009;12:1–8.
124. Weinshenker D. Cocaine sobers up. Nat Med 2010;16:969–70.
125. Werler MM. Teratogen update: smoking and reproductive outcomes. Teratology 1997;55:382–8.
126. Wong S, Ordean A, Kahan M. Substance use in pregnancy. J Obstet Gynaecol Can 2011;33:367–84.
Modifizierter Nachdruck aus Med Monatsschr Pharm 2011;34:363–74.
Prof. Dr. Ursula Havemann-Reinecke, Dr. Imke Hoell, Klinik für Psychiatrie und Psychotherapie, Universitätsmedizin Göttingen, Von-Siebold-Str. 5, 37075 Göttingen, E-Mail: u.havemann-reinecke@med.uni-goettingen.de, imke.hoell@med.uni-goettingen.de
Treatment of polytoxicomanic, opioid addicted pregnant women. Part I. Toxic effects and therapeutic consequences
Opioid dependent patients often are dependent from the illegal consumption of heroin and, in addition, perform a polytoxicomanic way of consuming drugs. They suffer of various somatic and psychiatric diseases. Moreover, pregnancies of drug addicted women are classified as high-risk pregnancies. With respect to the particular consumed drug substances other than opioids during pregnancy variable forms of teratogenic and toxic effects can be assigned to the baby. Critical values of maternal substance abuse referring to fetal impairment do not exist. With regard to the possible teratogenic and toxic fetal effects of maternal consume of alcohol, tobacco, sedativa, cannabis, cocaine and amphetamines, withdrawal treatment of polytoxicomanic pregnant patients under inpatient medical supervision including medication if necessary represent the first-line-treatment. With respect to smoking, it is possible to detoxicate the patients also by an outpatient treatment. However, referring to heroin addiction, a maintenance therapy with L-methadone, D/L-methadone or buprenorphine should be preferred since fetal withdrawal symptoms of opioids otherwise can cause severe complications which even can lead to the loss of the fetus and also increase the risks for the mother. Increasing the dose of the opioid substitute may be necessary, for example, to avoid premature uterus contractions. It is to be pointed out that substitution treatment with methadone or buprenorphine also improve the medicinal compliance and psychosocial circumstances of the pregnant patients. Subsequent to delivery, the maintenance treatment should initially be pursued over a further period of time. In the follow-up, the question of continuing with maintenance treatment or starting a withdrawal treatment of opioids should be discussed on an individual basis. To sum up, proceeded interdisciplinary care during pregnancy and afterwards by all the professions involved like general practioners as well as social workers, gynaecologists, paediatrists, pharmacists, psychologists and psychiatrists should be ensured. Futhermore, diagnosis and therapy of the comorbid psychiatric and infectious diseases like hepatitis A, B, C and HIV are necessary and described (see Part II. Comorbidity and their treatment).
Key words: Pregnancy, teratogenic effects, drugs, opioids, heroine, alcohol, tobacco smoking, psychostimulants, cannabinoids, polytoxicomania, drug addiction therapy
Psychopharmakotherapie 2013; 20(01)
