Gisa Ellrichmann und Ralf Gold, Bochum
Dr. med. Gisa Ellrichmann, Prof. Dr. med. Ralf Gold, Neurologische Klinik, St. Josef-Hospital, Klinikum der Ruhr-Universität Bochum, Gudrunstraße 56, 44791 Bochum, E-Mail: Gisa.Ellrichmann@ruhr-uni-bochum.de
Zurzeit existieren zahlreiche Möglichkeiten zur Therapie der multiplen Sklerose (MS), einer chronischen Erkrankung des Zentralnervensystems, die trotz verschiedener Behandlungsansätze unverändert die häufigste neurologische Ursache von Behinderungen bei jungen Erwachsenen ist. Die Zahl der verfügbaren Immuntherapien für die schubförmige MS hat besonders in den vergangenen 15 Jahren zugenommen. In der aktualisierten Leitlinie zur Diagnose und Therapie der multiplen Sklerose [22] wurde das Stufenschema für den Einsatz der bestehenden MS-Therapien in seiner Grundstruktur bestätigt und um neue Therapiemöglichkeiten erweitert.
Bereits seit Anfang der 1990er-Jahre wurden beginnend mit Natalizumab Arzneimittel mit neuen Applikationswegen als Alternative zu den Interferonen und Glatirameracetat mit subkutaner bzw. intramuskulärer Applikation entwickelt. Der Wunsch von MS-Patienten nach einer regelmäßig anzuwendenden, sicheren und wirksamen oralen Behandlung erlangt zunehmend an Bedeutung. Seit einigen Jahren werden zahlreiche orale Immuntherapeutika zur Behandlung der schubförmigen MS entwickelt. Wenn diese in den nächsten Jahren die Zulassung erlangen, ergänzen sie die bisher verfügbaren Therapieoptionen, sodass das therapeutische Repertoire der behandelnden Ärzte im klinischen Alltag deutlich erweitert wird.
Mit Teriflunomid (Abb. 1) wird derzeit ein vielversprechender oral verfügbarer Wirkstoff, der sowohl antiinflammatorische als auch antiproliferative Aktivität besitzt, als neue MS-Therapie in klinischen Studien untersucht.
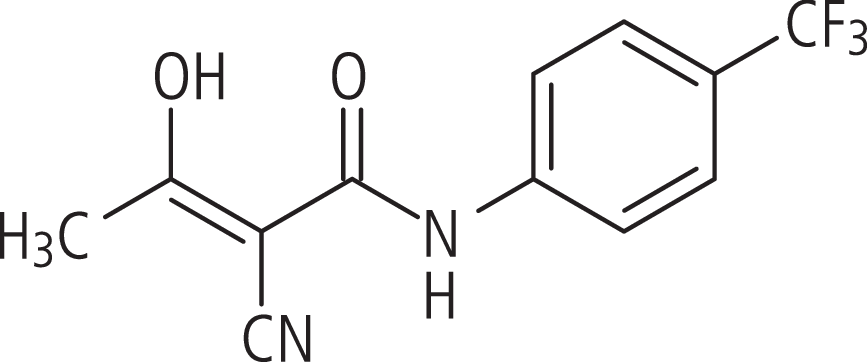
Abb. 1. Teriflunomid
Wirkungsmechanismus
Teriflunomid ist der aktive Metabolit von Leflunomid, einem langwirksamen Antirheumatikum, das bereits als Basistherapie in der Behandlung der rheumatoiden Arthritis und der Psoriasis-Arthritis eingesetzt wird [11, 13, 17]. Leflunomid wird in der Darmwand und der Leber in Teriflunomid umgewandelt, welches reversibel das mitochondriale Enzym Dihydroorotat-Dehydrogenase (DHODH) hemmt und so die Pyrimidin-Synthese beeinflusst [4, 8, 9]. Auf proliferierende B- und T-Zellen wirkt dies zytostatisch.
Teriflunomid hemmt ferner die Aktivität einer Tyrosinkinase, wodurch die T-Zell-Proliferation sowie die Aktivierung und Produktion von Zytokinen vermindert werden [5, 20]. Eine neuere Studie ergab, dass Teriflunomid die Interaktion zwischen T-Zellen und Antigen-präsentierenden Zellen (antigen-presenting cell, APC), die entscheidend zur T-Zell-Immunantwort beiträgt, beeinflusst [21]. Möglicherweise hat Teriflunomid darüber hinaus durch Hemmung des Tumornekrosefaktors alpha (TNF-α) einen Einfluss auf die Signalübertragung im NF-κB(Nuclear factor kappa B)-Signalweg [14].
Pharmakokinetik
Teriflunomid ist im Plasma zu 99,3% an Proteine gebunden. Ausgeschieden wird es über die Fäzes (hier überwiegend nicht metabolisiert) und über den Urin, primär in Form von 4-Trifluoromethyl-anilin-oxalsäure [12]. Beim Menschen beträgt die Halbwertszeit etwa zwei Wochen. Die Elimination kann durch Gabe von Colestyramin oder Aktivkohle beschleunigt werden; dies sollte besonders bei Eintritt einer ungeplanten Schwangerschaft unter Teriflunomid durchgeführt werden. Aufgrund der überwiegend hepatischen Elimination ist eine Niereninsuffizienz keine Kontraindikation, in dieser Situation bedarf es jedoch erhöhter Vorsicht. Teriflunomid hemmt das Cytochrom-P450-Isoenzym 2C9, wodurch bei einer begleitenden Medikation mit Warfarin oder Phenprocoumon deren gerinnungshemmende Wirkung erhöht werden kann [3].
Präklinische Studien
Studien an Tieren mit experimenteller Autoimmun-Enzephalomyelitis (EAE), einem etablierten Tiermodell der MS, ließen nach Gabe von Teriflunomid (bzw. Leflunomid) einen deutlichen positiven Effekt auf den klinischen Verlauf erkennen [10]. Die Wirksamkeit der Substanz konnte nicht nur in verschiedenen Tiermodellen, sondern auch auf immunhistochemischer und elektrophysiologischer Ebene sowie in vitro bestätigt werden [15, 19].
Klinische Studien
Auf eine 2006 veröffentliche Phase-II-Studie (Proof of concept) folgte ein ausführliches Phase-III-Studienprogramm, das die mittlerweile abgeschlossenen Studien TEMSO, TOWER und TENERE sowie die noch laufende TOPIC-Studie beinhaltet (Tab. 1).
Tab. 1. Übersicht über aktuelle große Phase-III-Studien mit Teriflunomid. Der Wirkstoff wird in zwei Dosierungen bei verschiedenen Verlaufsformen der multiplen Sklerose (MS) untersucht, verglichen wird mit Plazebo und Interferon beta-1a.
|
Studie |
Verlaufsform |
Anzahl der Patienten |
Behandlungsgruppen |
Primärer Endpunkt |
Sekundäre Endpunkte |
|
TEMSO (Teriflunomide multiple sclerosis oral) |
RMS |
1088 |
|
Jährliche Schubrate |
Behinderungsprogression (EDSS) MRT: Volumenveränderung Fatigue (FIS) |
|
TOWER (Teriflunomide oral in people with relapsing MS) |
RMS |
1169 |
|
Jährliche Schubrate |
Behinderungsprogression (EDSS) Fatigue (FIS) Lebensqualität (SF-36) |
|
TENERE (A multicenter, randomized, parallel-group, rater-blinded study comparing the effectiveness and safety of teriflunomide and interferon beta-1a in patients with relapsing multiple sclerosis) |
RMS |
324 |
|
„Time to Failure“ |
Jährliche Schubrate Fatigue (FIS) Zufriedenheit (TSQM) |
|
TOPIC (An international, multi-center, randomized, double-blind, placebo-controlled, parallel group study to evaluate the efficacy and safety of two year treatment with teriflunomide 7 mg once daily and 14 mg once daily versus placebo in patients with a first clinical episode suggestive of MS) |
CIS |
ca. 780 |
|
Entwicklung einer manifesten MS (klinisch basierte Diagnose) |
Entwicklung einer manifesten MS (MRT-basierte Diagnose) Jährliche Schubrate Behinderungsprogression (EDSS) MRT: Volumenveränderung Fatigue (FIS) |
RMS: Relapsing MS; CIS: Clinically Isolated Syndrome; s.c. subkutan; EDSS: Expanded Disability Status Scale; MRT: Magnetresonanztomographie; FIS: Fatigue Impact Scale; SF-36: Short Form-36; TSQM: Treatment Satisfaction Questionnaire for Medication
TEMSO
In der TEMSO-Studie, einer randomisierten, doppelblinden, Plazebo-kontrollierten Phase-III-Studie, wurde Teriflunomid (7 und 14 mg/Tag) bei schubförmiger multipler Sklerose untersucht [16]. Die Studie lief über einen Zeitraum von gut zwei Jahren (108 Wochen). Eingeschlossen wurden 1088 Patienten mit schubförmig verlaufender MS mit oder ohne Progredienz im Alter zwischen 18 und 55 Jahren mit einem EDSS(Expanded disability status scale)-Score ≤5,5.
Im primären Endpunkt, der jährlichen Schubrate, ließ sich unter der Behandlung mit Teriflunomid in beiden Dosierungen eine signifikante Reduktion gegenüber Plazebo nachweisen: In der Plazebo-Gruppe lag die jährliche Schubrate bei 0,54, in beiden Verum-Gruppen ergab sich eine Rate von 0,37 (jeweils p<0,001 für Verum vs. Plazebo). Bei den mit Teriflunomid behandelten Patienten war die Zeit, die bis zum Auftreten des ersten Schubs verstrich, länger und der Anteil der Patienten ohne Schub höher als unter Plazebo (53,7 bzw. 56,5 vs. 45,6% ; p=0,01 bzw. p=0,003 für 7 bzw. 14 mg/Tag vs. Plazebo).
In der MRT-Bildgebung war die Anzahl der MS-typischen Gadolinium-aufnehmenden T1-Läsionen je Scan nach Einnahme von Teriflunomid signifikant gegenüber Plazebo verringert (0,57 bzw. 0,26 vs. 1,33; jeweils p<0,001 für 7 bzw. 14 mg/Tag vs. Plazebo). Die Gesamtgröße aller Läsionen war nach Einnahme von 7 mg/Tag Teriflunomid um 39,4% gegenüber Plazebo verringert, nach Einnahme von 14 mg/Tag Teriflunomid um 67,4%; diese Ergebnisse würden für die höhere Dosis sprechen. Das Gehirnparenchym als Maß für eine Hirnatrophie war in allen Gruppen nur unwesentlich gegenüber dem Ausgangswert bei Studienbeginn verändert.
TOWER
In der internationalen, doppelblinden, Plazebo-kontrollierten Phase-III-Studie TOWER wurde die Wirksamkeit und Sicherheit von Teriflunomid (7 und 14 mg/Tag) bei 1169 Patienten mit schubförmiger MS untersucht. Primärer Endpunkt war wie in der TEMSO-Studie die jährliche Schubrate [1]. Daten dieser Studie wurden bis März 2012 erhoben. Nach ersten Informationen des Herstellers zeigte sich bei Einnahme von Teriflunomid im Vergleich zu Plazebo eine Reduktion der jährlichen Schubrate um 22,3 bzw. 36,3% (7 bzw. 14 mg/Tag), wodurch die Ergebnisse der TEMSO-Studie bestätigt wurden [7]. Ausführliche Analysen wurden noch nicht veröffentlicht.
TENERE
Um die Wirksamkeit von Teriflunomid (7 und 14 mg/Tag) direkt mit der von Interferon beta-1a (3-mal wöchentlich 44 mg s.c.) vergleichen zu können, wurde die multizentrische TENERE-Studie durchgeführt [2]. Teilnehmer waren 324 Patienten mit schubförmiger MS. Der primäre Endpunkt war definiert als „Time to Failure“, also als Zeit bis zum Auftreten eines Schubs oder einer unregelmäßigen Einnahme der Studienmedikation, die anderweitig begründet wurde. Nach ersten Informationen des Herstellers ergaben sich keine signifikanten Unterschiede zwischen den Gruppen: Der primäre Endpunkt wurde von 48,6 bzw. 37,8% der Patienten unter Teriflunomid (7 bzw. 14 mg/Tag) erreicht im Vergleich zu 42,3% in der Interferon-Gruppe [6]. Auch hier steht die ausführliche Präsentation der Ergebnisse noch aus.
TOPIC
Die TOPIC-Studie ist eine internationale, multizentrische, randomisierte, doppelblinde, Plazebo-kontrollierte Studie zur Beurteilung der Wirksamkeit und Sicherheit von Teriflunomid bei Patienten mit klinisch isoliertem Syndrom (Clinically isolated syndrome, CIS). Analysiert wird die Zeit bis zur Diagnose einer klinisch manifesten MS. Die Rekrutierung der Patienten ist noch nicht abgeschlossen, geplant sind etwa 780 Teilnehmer [18].
Nebenwirkungen
An relevanten Nebenwirkungen wurde in der TEMSO-Studie neben Diarrhö, Schwindel, Hautreaktionen und leichtem Haarausfall, die jeweils in allen Gruppen vorkamen (Tab. 2), eine Erhöhung der Alanin-Aminotransferasewerte (ALT) beobachtet. Eine bis zu 3-fache Erhöhung der ALT wiesen in allen Gruppen ähnlich viele Studienteilnehmer auf (6,3 bzw. 6,7 vs. 6,7% für 7 bzw. 14 mg/Tag vs. Plazebo). Eine Verdopplung der Werte wurde in den Verum-Gruppen häufiger beobachtet als unter Plazebo (54 bzw. 57,3 vs. 35,9%).
Tab. 2. Übersicht über mögliche Nebenwirkungen unter der Einnahme von Teriflunomid [16]
|
Symptome |
Plazebo [%] |
Teriflunomid 7 mg [%] |
Teriflunomid 14 mg [%] |
|
Diarrhö |
8,9 |
14,7 |
17,9 |
|
Schwindel |
7,2 |
9,0 |
13,7 |
|
Hautveränderungen und/oder Haarausfall |
3,3 |
10,3 |
13,1 |
|
Erhöhung der Alanin-Aminotransferase (ALT) |
6,7 |
12,0 |
14,2 |
Schwerwiegende opportunistische Infektionen wurden bei keinem Teilnehmer festgestellt. Im Plazebo-Arm trat einmalig eine ausgeprägte Herpes-zoster-Infektion auf. Nach Einnahme von Teriflunomid wurden drei Fälle einer Pyelonephritis dokumentiert [16].
Trotz doppelter antikonzeptiver Maßnahmen kam es in den Studien bis zur Datenerhebung am 1. Juni 2011 zu 41 ungewollten Schwangerschaften unter Teriflunomid. Hierunter waren 10 gesunde Neugeborene, 21 gewollte Schwangerschaftsabbrüche und 9 Spontanaborte. 5 Schwangerschaften waren zum Zeitpunkt der Datenerhebung noch nicht beendet. Bei allen ausgetragenen Schwangerschaften wurde Teriflunomid im ersten Trimenon eliminiert (z.B. durch Colestyramin).
Fazit
Teriflunomid ist nach den bisher verfügbaren Daten eine interessante Alternative zu den bisher verfügbaren MS-Therapeutika. Im Falle einer Zulassung würde es die Möglichkeiten zur Behandlung von MS-Patienten mit schubförmigem Verlauf erweitern. Die Studienergebnisse zur klinischen Wirksamkeit und zur magnetresonanztomographisch nachgewiesenen Wirkung auf die Entzündungsherde scheinen für eine Eingruppierung als Basistherapeutikum zu sprechen; die Entscheidung der Zulassungsbehörden bleibt aber abzuwarten.
Schlussfolgerung
Die Entwicklung neuer MS-Medikamente erlaubt nicht nur eine alternative, orale Applikationsform, sondern bietet auch Wirkstoffe mit neuen Angriffspunkten und Wirkungsmechanismen. Zum aktuellen Zeitpunkt scheinen einige Neuentwicklungen wirksamer und besser verträglich zu sein als die bisher zur Verfügung stehenden Therapieoptionen. Kritische Analysen sind jedoch auch hier, wie bei anderen neuen Wirkstoffen, von fundamentaler Bedeutung. Ein vollständiges Verdrängen der etablierten Basistherapeutika ist aktuell nicht abzusehen. Neben Fingolimod, der ersten oral verfügbaren Substanz, die zur Behandlung der schubförmigen MS zugelassen wurde, sind eine Reihe weiterer oral verfügbarer Medikamente zur MS-Therapie in der klinischen Prüfung. Teriflunomid ist ohne Zweifel ein vielversprechender Wirkstoff, dessen Wirksamkeit bei gleichzeitig gutem Sicherheitsprofil in ausführlichen Studien belegt wurde.
Eine abschließende Risiko-Nutzen-Bewertung der neuen Therapieprinzipien ist erst nach jahrelanger Erfahrung im klinischen Alltag und gleichzeitig engmaschiger Betreuung der Patienten möglich. Die Behandlung der MS ist und bleibt komplex, bedarf stetiger Kontrollen und sollte sich nicht nur auf die medikamentöse Behandlung konzentrieren.
Interessenkonflikte
GE: Es bestehen keine Interessenkonflikte.
RG hat Redner- und Beraterhonorare sowie Forschungsunterstützung von Bayer, BiogenIdec, Merck Serono, Novartis und TEVA erhalten.
Literatur
1. A multi-center double-blind parallel-group placebo-controlled study of the efficacy and safety of teriflunomide in patients with relapsing multiple sclerosis (TOWER). http://clinicaltrials.gov/show/NCT00751881 (Zugriff am 03.09.2012).
2. A multi-center, randomized, parallel-group, rater-blinded study comparing the effectiveness and double-blind parallel-group placebo-controlled study of the efficacy and safety of teriflunomide and interferon beta-1a in patients with relapsing multiple sclerosis (TENERE). http://clinicaltrials.gov/show/NCT00883337 (Zugriff am 03.09.2012).
3. Beaman JM, Hackett LP, Luxton G, Illett KF. Effect of hemodialysis on leflunomide plasma concentrations. Ann Pharmacother 2002;36:75–7.
4. Bruneau JM, Yea CM, Spinella-Jaegle S, Fudali C, et al. Purification of human dihydro-orotat dehydrogenase and its inhibition by A771726, the active metabolite of leflunomide. Biochem J 1998;336:299–303.
5. Cherwinski HM, McCarley D, Schatzman R, Devens B, et al. The immunosuppressant leflunomide inhibits lymphocyte progression through cell cycle by a novel mechanism. J Pharmacol Exp Ther 1995;272:460–8.
6. Genzyme, a Sanofi Company. Genzyme reports positive top-line results of TENERE study of oral teriflunomide in relapsing multiple sclerosis. Press Release, December 2011.
7. Genzyme, a Sanofi Company. Genzyme reports positive top-line results of TOWER, a pivotal phase III trial for AubagioTM (teriflunomide) in relapsing multiple sclerosis. Press Release, June 2012.
8. Gold R, Wolinsky JS. Pathophysiology of multiple sclerosis and the place of teriflunomide. Acta Neurol Scand 2011;124: 75–84.
9. Greene S, Watanabe K, Braatz-Trulson J, Lou L. Inhibition of dihydro-orotate dehydrogenase by the immunosuppressive agent leflunomide. Biochem Pharmacol 1995;50:861–7.
10. Korn T, Magnus T, Toyka K, Jung S. Modulation of effector cell functions in experimental autoimmune encephalomyelitis by leflunomide – mechanisms independent of pyrimidine depletion. J Leukoc Biol 2004;76:950–60.
11. Li EK, Tam L, Tomlinson B. Leflunomide in the treatment of rheumtoid arthritis. Clin Ther 2004;26:447–59.
12. Limsakun T, Menguy-Vacheron F. Pharmacokinetics of oral teriflunomide, a novel oral disease-modifying agent under investigation for the treatment of MS [Poster]. Annual Meeting of the American Academy of Neurology (AAN), Toronto, April 15, 2010.
13. Maddison P, Kiely P, Kirkham B, Lawson T, et al. Leflunomide in rheumatoid arthritis: recommendations through a process of consensus. Rheumatology (Oxford) 2005;44:280–6.
14. Manna SK, Aggarwal BB. Immunosuppressive leflunomide metabolite (A771726) blocks TNF-dependent nuclear factor-kappa B activation and gene expression. J Immunol 1999;162:2095–102.
15. Merrill JE, Hanak S, Pu S, Liang J, et al. Teriflunomide reduces behavioral, electrophysiological, and histopathological deficits in the Dark Agouti rat model of experimental autoimmune encephalomyelitis. J Neurol 2009;256:89–103.
16. O’Connor P, Wolinsky JS, Confavreux C, Comi G, et al. Randomized trial of oral teriflunomide for relapsing multiple sclerosis. N Engl J Med 2011;365:1293–303.
17. Osiri M, Shea B, Robinson V, Suarez-Almazor M, et al. Leflunomide for treating rheumatoid arthritis: a systematic review and meta-analysis. J Rheumatol 2003;30:1182–90.
18. Phase III study with teriflunomide versus placebo in patients with first clinical symptom of multiple sclerosis (TOPIC), estimated study completion: December 2018, currently recruiting patients. http://clinicaltrials.gov/show/NCT00622700 (Zugriff am 03.09.2012).
19. Sweitzer SM, DeLeo JA. The active metabolite of leflunomide, an immunosuppressive agent, reduces mechanical sensitivity in a rat mono-neuropathy model. J Pain 2002;3:360–8.
20. Xu X, Williams JW, Bremer EG, Finnegan A, et al. Inhibition of protein tyrosine phosphorylation in T cells by a novel immunosuppressive agent, leflunomide. J Biol Chem 1995;270:12398–403.
21. Zeyda M, Poglitsch M, Geyeregger R, Smolen JS, et al. Disruption of the interaction of T cells with antigen-presenting cells by the active leflunomide metabolite teriflunomide: involvement of impaired integrin activation and immunologic synapse formation. Arthritis Rheum 2005;52:2730–9.
22. DGN/KKNMS Leitlinie zur Diagnose und Therapie der MS Online-Version, Stand 17.07.2012 (www.dgn.org/images/stories/dgn/leitlinien/LL_MS_Neu/dgn-kknms_ms-ll_20120717_frei.pdf, Zugriff am 30.7.2012).
Ellrichmann, Gold · Teriflunomid
Teriflunomide: an alternative to established MS therapies?
Since the last two decades, therapy for relapsing multiple sclerosis (MS) has dramatically improved. Immunomodulatory therapies of the first generation, including interferon beta and glatiramer acetate, remain as a standard therapy in relapsing-remitting MS. To improve quality of life and long-term acceptance by patients, a number of new drugs for MS therapy, especially those which are orally available, could enlarge the arsenal of approved drugs for MS within the next years. Different substances have already broadened the therapeutic options, others may become an alternative to the current injectable first-line treatment for relapsing MS. This allows an increasing individualization of MS-treatment. In particular, there is a need for safe and effective oral options. One of these orally administered drugs is teriflunomide which is discussed in this article.
Key words: Multiple sclerosis, teriflunomide, oral drugs
Psychopharmakotherapie 2012; 19(05)
