Aiden Haghikia, Bochum/Oxford, und Ralf Gold, Bochum
Fortschritte in der Diagnostik
Die Diagnostik der multiplen Sklerose (MS) basiert nach wie vor auf mehreren Säulen. Dabei handelt es sich unverändert vor allem eine klinisch-neurologische Diagnose, die den Ausschluss von möglichen Differenzialdiagnosen erfordert [4]. Die bewährten Zusatzdiagnostika wie die Serologie und die elektrophysiologische Untersuchung – mit den visuell evozierten Potenzialen (VEP), den motorisch evozierten Potenzialen (MEP) und den somatosensibel evozierten Potenzialen (SSEP) – haben weiterhin einen hohen Stellenwert. Dank der rasanten technischen Entwicklung und des gewachsenen klinischen Erfahrungsschatzes ist die Magnetresonanztomographie (MRT) jedoch die Methode, die am meisten dazu beiträgt, dass die Diagnose der MS rascher gestellt werden kann als früher. Und sie ist die Methode, die für die wiederholten Revisionen der Diagnosekriterien verantwortlich ist.
Magnetresonanztomographie
Nach den 2010 revidierten McDonald-Kriterien [14] kann die Diagnose der MS mithilfe der MRT-Bildgebung in manchen Fällen direkt bei der ersten klinischen Präsentation gesichert werden, sodass bereits zu diesem Zeitpunkt eine immunmodulierende Therapie eingeleitet werden kann. Die überarbeiteten McDonald-MRT-Kriterien, auf die in der neuen DGN/KKNMS-Leitlinie [4] Bezug genommen wird, sollen nicht nur die Absicherung der Diagnose vereinfachen, sondern auch die Sensitivität erhöhen und die Abgrenzung von differenzialdiagnostisch zu erwägenden Krankheitsbildern verbessern. Letzteres betrifft vor allem die Neuromyelitis optica (NMO) und Krankheiten aus dem Formenkreis der NMO.
In den neuen McDonald-Kriterien werden zusätzlich die pädiatrische MS und Besonderheiten bei MS-Patienten mit asiatischem und lateinamerikanischem Hintergrund berücksichtigt.
Eine wesentliche Änderung betrifft die Dissemination der Läsionen im Raum. In den vorherigen Diagnosekriterien wurden im T2-gewichteten MRT neun Läsionen in drei für die MS typischen Regionen im zentralen Nervensystem (ZNS) gefordert. Jetzt reicht für die Diagnosesicherung einer MS – basierend auf Ergebnissen neuer prospektiver Studien – je eine T2-Läsion in zwei MS-typischen ZNS-Regionen aus. Auch bei der erforderlichen zeitlichen Dissemination gab es eine Veränderung: Im Gegensatz zu den älteren Kriterien, in denen der Nachweis einer neuen Kontrastmittel-aufnehmende Läsion frühestens 30 Tage nach dem initialen MRT gefordert wurde, reicht es jetzt für die Diagnosestellung aus, wenn neben den oben beschriebenen T2-Läsionen gleichzeitig eine Kontrastmittel-aufnehmende Läsion vorliegt (Abb. 1).
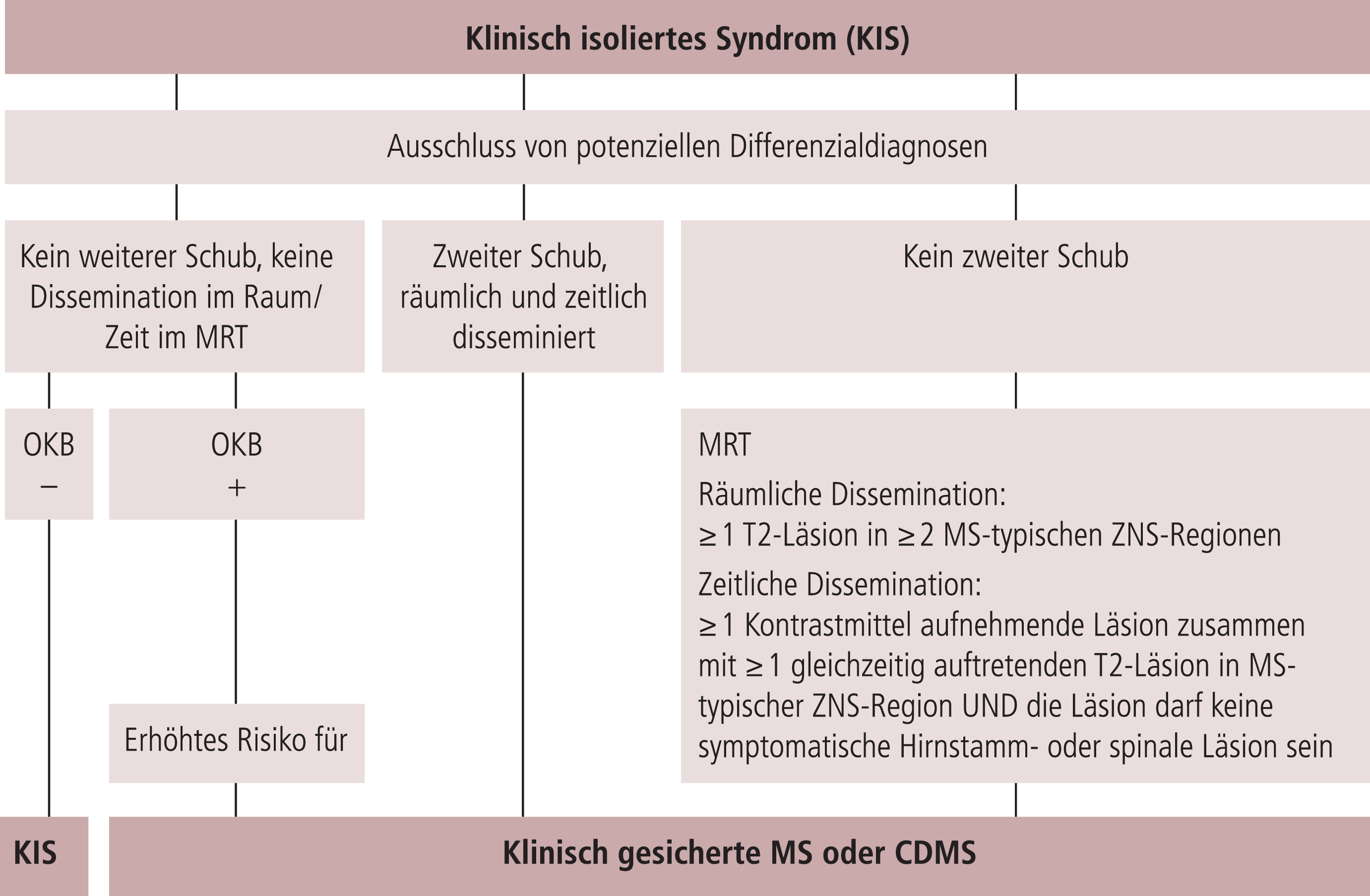
Abb. 1. Algorithmus zur Diagnose der multiplen Sklerose (MS) nach den 2010 revidierten McDonald-Kriterien [14]. CDMS: clinically definded MS (klinisch gesicherte MS); OKB: oligoklonale Banden
Serologie
Die erforderlichen serologischen Untersuchungen sind in der neuen Leitlinie detailliert aufgelistet und wurden um die Bestimmung von Antikörpern gegen Aquaporin 4 (AQP4) erweitert [4]. Aquaporin-4-Antikörper treten bei mehr als der Hälfte der Patienten mit Neuromyelitis optica auf. Sie sind inzwischen sowohl für das pathophysiologische Verständnis dieser Erkrankung als auch als Diagnosekriterium etabliert und eignen sich besonders gut zur Abgrenzung einer NMO von der spinalen Form der MS.
Liquordiagnostik
Der angloamerikanischen Tradition folgend wurde die Bedeutung der Lumbalpunktion zur Prüfung des Liquors auf eine intrathekale Antikörpersynthese in der neuen Leitlinie weiter abgeschwächt. Die Liquoruntersuchung ist allerdings weiterhin eine feste diagnostische Stütze, wie es übrigens in fast ganz Europa der Fall ist. Der Nachweis bzw. das Fehlen von oligoklonalen Banden (OKB) ist insbesondere bei der Abgrenzung der MS von der NMO nützlich, vor allem bei Aquaporin-4-Antikörper-negativen Patienten. Die oligoklonalen Banden sind außerdem auch weiterhin dem MRT als prädiktiver Marker für die Konversion vom klinisch isolierten Syndrom zur gesicherten MS überlegen (Abb. 1) [4, 11,16].
Sonderformen der MS
In der revidierten Leitlinie wird zur NMO, den Erkrankungen aus dem Formenkreis der NMO und der akuten disseminierten Enzephalomyelitis (ADEM) Stellung genommen. So beinhaltet die Leitlinie detaillierte Algorithmen zur Diagnose und Therapie der NMO.
Bei der Diagnosestellung dieser Sonderformen der MS beziehungsweise bei der Abgrenzung dieser Erkrankungen von der MS spielen neben den erwähnten AQP4-Antikörpern auch die klinische Präsentation (z.B. eine isolierte Optikusneuritis und/oder spinale Symptomatik) sowie die Bildgebung (z.B. langstreckige spinale Läsionen) maßgeblich eine Rolle [4].
Neue Aspekte in der MS-Therapie
Die Basistherapeutika Interferon beta und Glatirameracetat
Obwohl die unterschiedlichen Interferon-beta(IFN-β)-Präparate und Glatirameracetat (GA) inzwischen als Immunmodulatoren in der Langzeitbehandlung der MS etabliert sind und keine Änderungen im Umgang mit diesen Substanzen zu erwarten sind, wurden zwei interessante Aspekte aus klinischen Studien in die neuen Therapieempfehlungen (Abb. 2) aufgenommen [4]:
- IFN-β und GA sind in ihrer Wirksamkeit gleichwertig
- Bei Patienten mit klinisch isoliertem Syndrom verzögern sowohl die IFN-b-Präparate als auch GA bei frühem Einsatz die Konversion zur klinisch gesicherten MS.
Lange Zeit wurde ein Unterschied in der Wirksamkeit von IFN-β und GA angenommen. Jetzt wurden zwei Head-to-Head-Studien durchgeführt, in denen subkutanes Interferon beta-1a (Rebif®, 3-mal wöchentlich 44 µg) [10] bzw. subkutanes Interferon beta-1b (Betaferon®, 250 oder 500 µg alle 2 Tage) [13] direkt mit Glatirameracetat (20 mg/Tag, Copaxone®) verglichen wurden. In beiden Studien zeigten sich nach zwei Jahren keine wesentlichen Unterschiede zwischen der Wirksamkeit des Interferons und der des Glatirameracetats. In der Studie mit Interferon beta-1b war die 500-mg-Dosierung des Interferons nicht besser wirksam als die zugelassene Standard-Dosierung mit 250 mg.
Die zweite Änderung der Empfehlungen für die Basistherapeutika betrifft die Frühtherapie, die vielerorts bereits gängige Praxis ist: Für den frühestmöglichen Therapiebeginn noch vor dem zweiten Schub liegen jetzt für sämtliche IFN-β-Präparate und Glatirameracetat Daten aus prospektiven klinischen Studien und damit Klasse-I-Evidenzen vor [3, 5, 8, 9].
Unklar bleibt, ob es Patienten gibt, die auf eine dieser Therapien besser anspechen als auf eine andere, sodass im Fall von leichten Schüben eine Umstellung auf das andere Basistherapeutikum (anstelle einer Eskalationstherapie) vertretbar erscheint.
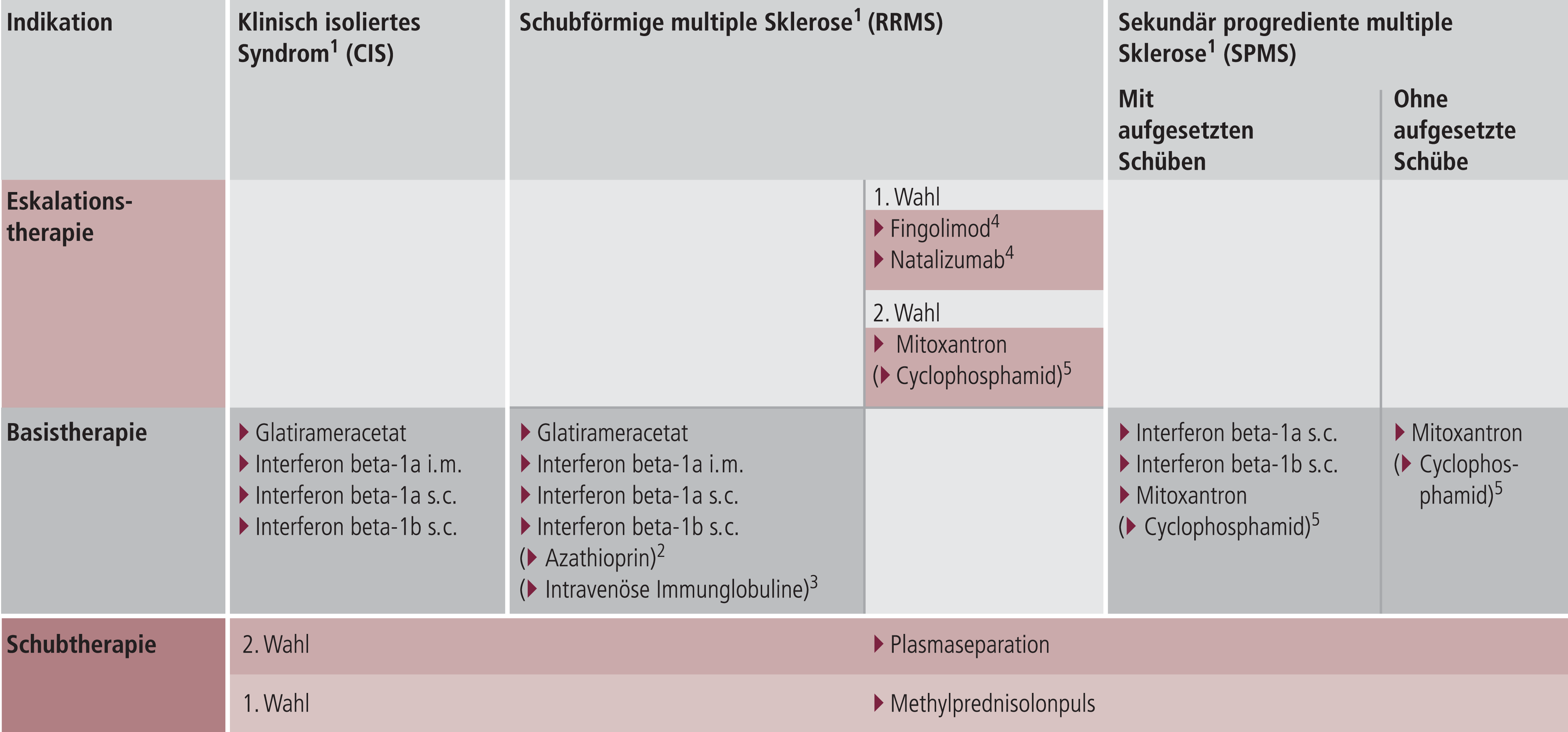
Abb. 2. Stufenschema zur Therapie der multiplen Sklerose (MS) nach der S2e-Leitlinie der Deutschen Gesellschaft für Neurologie (DGN) und des Krankheitsbezogenen Kompetenznetzwerks Multiple Sklerose (KKNMS) [4]. 1: Wirkstoffe in alphabetischer Reihenfolge. Die Darstellung impliziert innerhalb der jeweiligen Indikationsgruppe keine Überlegenheit eines Wirkstoffs gegenüber einem anderen. 2: Zugelassen, wenn Interferon beta nicht möglich ist oder unter Azathioprin ein stabiler Verlauf erreicht wird. 3: Einsatz nur postpartal im Einzelfall gerechtfertigt, insbesondere vor dem Hintergrund fehlender Behandlungsalternativen. 4: Fingolimod und Natalizumab haben neben der Zulassung zur Eskalationstherapie auch eine Zulassung zur Behandlung therapienaiver Patienten bei mindestens zwei behindernden Schüben mit Krankheitsprogression innerhalb der letzten 12 Monate und mindestens einer Gadolinium-anreichernden Läsion bzw. einer signifikanten Zunahme der T2-Läsionen im MRT. 5: Zugelassen für bedrohlich verlaufende Autoimmunkrankheiten, somit lediglich für fulminante Fälle als Ausweichtherapie vorzusehen, idealerweise nur an ausgewiesenen MS-Zentren. CIS: Clinically Isolated Syndrom; RRMS: Relapsing-Remitting Multiple Sclerosis; SPMS: sekundär progrediente MS; i.m.: intramuskulär; s.c.: subkutan
Eskalationstherapie mit Natalizumab
Noch während des klinischen Studienprogramms zu Natalizumab traten drei Fälle einer Natalizumab-assoziierten progressiven multifokalen Leukenzephalopathie (PML) auf, die zunächst zum Rückruf des Medikaments vom Markt geführt haben. Doch seit der Wiedereinführung und Zulassung zur Therapie der hochaktiven MS 2006 hat sich Natalizumab (Tysabri®) als Eskalationstherapie etabliert. Mit bislang rund 250 Fällen bei knapp 100000 weltweit behandelten MS-Patienten ist die PML unverändert eine eher seltene Nebenwirkung der Natalizumab-Therapie, die allerdings aufgrund des lebensbedrohlichen Verlaufs und der Gefahr von irreversiblen Residuen gefürchtet ist. Trotz intensiver Forschungsbemühungen konnte die Ursache für das Auftreten der PML bei MS-Patienten noch immer nicht aufgeklärt werden und es ist nicht möglich, Risikopatienten im Vorfeld einer Therapie sicher zu identifizieren.
Derzeit scheinen die Therapiedauer und eine vorangegangene immunsuppressive Therapie die wichtigsten Risikofaktoren für das Auftreten einer Natalizumab-assoziierten PML zu sein. Ausgehend von Daten aus Langzeitbeobachtungsprogrammen des Herstellers wurde das Risiko, unter Natalizumab-Therapie eine PML zu entwickeln, bei Patienten mit einer Infusionsdauer von insgesamt 25 bis 48 Monaten und einer immunsuppressiven Vortherapie mit bis zu 1:90 berechnet [1]. Dennoch haben sich die Experten des Committee for Medicinal Products for Human Use (CHMP) der europäischen Zulassungsbehörde (EMA) und die amerikanische Zulassungsbehörde (FDA) nach mehreren Re-Evaluationen des Risiko-Nutzen-Profils von Natalizumab zugunsten des therapeutischen Antikörpers entschieden.
In diesem Zusammenhang muss erwähnt werden, dass es zumindest einen Faktor gibt, der einen hohen negativ prädiktiven Wert zu besitzen scheint, sodass es hiermit gelingt, Patienten zu identifizieren, die ein sehr geringes Risiko haben, unter Natalizumab eine PML zu entwickeln: Es handelt sich um einen negativen Nachweis von Antikörpern gegen das JC-Virus im Serum. JCV-Antikörper gelten als das pathogenetische Korrelat der PML. Für die Untersuchung auf JCV-Antikörper wurde eigens ein sogenannter Enzyme-linked Immunosorbent Assay (ELISA) entwickelt, der in zwei Stufen mit hoher Sensitivität und Spezifität Antikörper gegen eines der immundominanten Epitope des JCV-Kapsid-Proteins erkennt. Interessenterweise wiesen alle Patienten, die unter Natalizumab eine PML entwickelten und von denen Serumproben aus der Zeit vor dem Auftreten der PML auffindbar waren, hohe JCV-Antikörper-Titer auf [6]. Dieser Umstand erscheint zunächst aus virusbiologischer Sicht paradox, da man bei einer höheren Antikörperantwort eine niedrigere Viruslast erwarten würde. Allerdings stimmt diese Beobachtung gut mit bisherigen immunologischen Arbeiten überein, nach denen die humorale Immunantwort gegen das JCV keine entscheidende Rolle zu spielen scheint. Die funktionale Bedeutung des ELISA-Tests bleibt damit allerdings noch unbeantwortet. Wie das Ergebnis einer Langzeitstudie zeigt, scheint das Risiko einer PML bei JCV-Antikörper-negativen Patienten mit etwa 0,1:1000 auf einem sehr niedrigen Niveau zu liegen [1]. Die Aussagekraft des Tests wird allerdings dadurch eingeschränkt, dass bis zu 2% der Antikörperbefunde falsch negativ ausfallen.
In die revidierte Leitlinie wurden detaillierte Hinweise zur Anwendung des JCV-Antikörper-Tests sowie zu den notwendigen Sicherheitsmaßnahmen und Untersuchungen vor Beginn einer Natalizumab-Therapie, bei der Umstellung von anderen immunmodulierenden Therapien auf Natalizumab, aber auch während der Natalizumab-Therapie aufgenommen. Auch Maßnahmen zur frühzeitigen Erkennung von PML im Rahmen der Pharmakovigilanz werden erläutert [4].
Nach den bisherigen Erfahrungen mit Natalizumab-assoziierter PML hängen die Überlebenswahrscheinlichkeit und das Ausmaß der klinischen Residuen im Falle einer Erkrankung vor allem davon ab, wann die PML erkannt wird und wann Gegenmaßnahmen eingeleitet werden. Schon bei den ersten Fällen einer PML nach Markteinführung zeigte sich, dass vor allem die Eliminierung des Antikörpers aus dem Körper mittels Plasmapherese oder Immunadsorption und die Handhabung des sogenannten Immunrekonstitutions-Syndrom (IRIS) – der Reaktion des wieder erstarkten Immunsystems – , entscheidend für den Therapieerfolg der PML sind [17]. Unter diesen Voraussetzungen hat die Natalizumab-assoziierte PML mit einer Überlebensrate von mehr als 80% und dem Fortbestand von leichten Residuen in rund 15% der Fälle eine wesentlich bessere Prognose als etwa die PML bei HIV-Patienten [7].
Fingolimod: Der Beginn einer neuen Ära mit oralen MS-Therapien
Fingolimod (Gilenya®, 0,5 mg täglich) wurde 2011 als erstes Medikament aus einer ganzen Reihe von oralen Substanzen, die sich derzeit in verschiedenen Stadien der klinischen Prüfung befinden, zur Therapie der MS zugelassen. Über einen Sphingosin-1-Phosphat-Rezeptor-vermittelten Mechanismus führt Fingolimod dazu, dass Immunzellen die sekundären Lymphorgane, vor allem die Lymphknoten, nicht verlassen können. Damit können auch potenziell autoreaktive Zellen nicht zum Zielorgan gelangen und zu entzündlichen Reaktionen führen [15]. Der Substanz wird zudem – basierend auf Daten aus experimentellen Arbeiten – eine remyelinisierende Eigenschaft zugesprochen, die allerdings im humanen Organismus noch bestätigt werden muss [12].
Aufgrund seiner in klinischen Studien nachgewiesenen starken Wirksamkeit wurde Fingolimod zwar vom Hersteller zunächst als Basistherapie vorgesehen (wofür es in den USA durch die FDA auch zugelassen wurde). Aufgrund der in den Studien aufgetretenen Nebenwirkungen wurde es in Deutschland und Europa durch die EMA aber lediglich als Eskalationstherapie und für die Behandlung von therapienaiven Patienten mit hochaktiver MS zugelassen.
In einer der beiden zulassungsrelevanten Phase-III-Studien kam es zu zwei tödlich verlaufenden Herpes- bzw. Varicella-Zoster-Enzephalitiden [2]. Zudem traten bei mehreren Patienten bereits nach der ersten Dosis kardiologische Nebenwirkungen (z.B. Bradykardien, Bradyarrhythmien) auf. Daher müssen vor Beginn und während der Therapie mit Fingolimod besondere Vorkehrungen getroffen und Sicherheitsuntersuchungen durchgeführt werden. Diese beinhalten unter anderem eine kardiologische Abklärung und eine EKG-Untersuchung zum Ausschluss von Rhythmus- und Erregungsüberleitungsstörungen. Die Testung auf Serum-Antikörper gegen Varicella-Zoster-Viren (VZV) und eine VZV-Impfung bei negativem Antikörper-Nachweis sollen dazu beitragen, das Risiko von Fingolimod-assoziierten Infektionen oder Enzephalitiden zu verringern. Die Auswertung von Daten der Postmarketing-Phase von mehr als 36000 Patienten lieferte keine Hinweise auf bisher unbekannte schwere Nebenwirkungen.
Diese Aspekte und entsprechende Hinweise auf Sicherheits- und Verlaufsuntersuchungen, die bei einer Therapie mit Fingolimod durchgeführt werden müssen, finden sich im Detail in der revidierten Leitlinie [4].
Kinderwunsch, Schwangerschaft und Stillzeit bei MS-Patientinnen
Die Erfahrung lehrt uns, dass die Anwendung von Arzneimitteln in der Schwangerschaft vor allem für das Ungeborene unvorhersehbare und folgenschwere Nebenwirkungen haben kann. Daher ist beim Umgang mit schwangeren Frauen zu Recht höchste Vorsicht geboten. Diese Haltung und der Umstand, dass mit schwangeren Frauen selbstverständlich keine klinischen Studien durchgeführt werden dürfen, bergen allerdings die Gefahr einer medizinischen Unterversorgung von schwangeren Frauen und chronisch kranken Frauen mit Kinderwunsch. Im Falle der multiplen Sklerose ist es schon allein wegen der Geschlechterverteilung und dem üblichen Erkrankungsalter überflüssig, die Relevanz des Themas zu betonen. Es ist zwar bekannt, dass die Schwangerschaft bei MS-Patientinnen zumindest ab dem zweiten Trimenon einen gewissen Schutz vor einer Krankheitsaktivität darstellt, doch das gilt längst nicht für alle Betroffenen und wenn doch, meldet sich die Krankheit spätestens nach der Geburt und dann meist mit Vehemenz zurück.
Die Autoren der revidierten Leitlinie haben sich nun dieses schwierigen und teilweise kontrovers behandelten Themas angenommen. Als Diskussionsgrundlage werden hierbei in Ermangelung von Studiendaten auch Erfahrungsberichte und Fallserien mit peripartal akzidentiell verabreichten Arzneimitteln oder nach gründlicher Abwägung bewusst applizierter Medikation herangezogen. Allgemein gilt:
- Immunmodulierende Therapien sollten vor einer geplanten Schwangerschaft abgesetzt werden – bei einer ungeplanten Schwangerschaft direkt nachdem diese festgestellt wurde.
- Unter immunsuppressiver Therapie ist eine strenge Kontrazeption zu beachten.
In der Leitlinie wird noch differenzierter zu den einzelnen Substanzen Stellung genommen und es werden Sonderfälle diskutiert, etwa die Fortführung einer Therapie bei Kinderwunsch bis zum positiven Nachweis einer Schwangerschaft, das Vorgehen bei starker Krankheitsaktivität und die Therapie von Schüben während der Schwangerschaft. Weitere Themen sind Aspekte der Fertilität und Reproduktionsmedizin bei MS [4].
Symptomatische Therapie der MS
Neben einer Immuntherapie zur Verminderung der entzündlichen Krankheitsaktivität oder einer allgemeinen Immunprophylaxe spielt die symptomatische Therapie bei der Behandlung der MS eine immense Rolle. Ziel der symptomatischen Therapie ist es, Körperfunktionen so weit als möglich wieder herzustellen und residuale Symptome zu lindern.
Die Funktionsausfälle bei der MS sind so breit gefächert wie das Auftreten der Läsionen im ZNS: Sie reichen von der Spastik bis zu kognitiven Störungen, von der Blasenstörung bis zur Ataxie und Fatigue. Daher gehen wir an dieser Stelle nicht auf einzelne, in der Leitlinie vorgestellte Therapien ein. Die Vielfalt der Funktionsdefizite bedingt eine große Palette an vorgeschlagenen Therapiemöglichkeiten – mit höchst unterschiedlichen Qualitätsansprüchen, was die klinische Validierung betrifft. In der Leitlinie wird jeweils auf den Evidenzgrad der einzelnen Therapiemöglichkeiten verwiesen [4].
Interessenkonflikte
AH hat keinen Interessenkonflikt über den Zeitraum der letzten zwei Jahre zu berichten.
RG hat Redner- und Beraterhonorare sowie Forschungsunterstützung von Bayer, BiogenIdec, MerckSerono, Novartis und TEVA erhalten.
Literatur
1. Bloomgren G, Richman S, Hotermans C, et al. Risk of natalizumab-associated progressive multifocal leukoencephalopathy. N Engl J Med 2012;366:1870–80.
2. Cohen JA, Barkhof F, Comi G, et al. Oral fingolimod or intramuscular interferon for relapsing multiple sclerosis. N Engl J Med 2010;362:402–15.
3. Comi G, Martinelli V, Rodegher M, et al. Effect of glatiramer acetate on conversion to clinically definite multiple sclerosis in patients with clinically isolated syndrome (PreCISe study): a randomised, double-blind, placebo-controlled trial. Lancet 2009;374: 1503–11.
4. DGN/KKNMS Leitlinie zur Diagnose und Therapie der MS Online-Version, Stand 17.07.2012 (www.dgn.org/images/stories/dgn/leitlinien/LL_MS_Neu/dgn-kknms_ms-ll_20120717_frei.pdf, Zugriff am 30.7.2012).
5. Filippi M, Rovaris M, Inglese M, et al. Interferon beta-1a for brain tissue loss in patients at presentation with syndromes suggestive of multiple sclerosis: a randomised, double-blind, placebo-controlled trial. Lancet 2004;364:1489–96.
6. Gorelik L, Lerner M, Bixler S, et al. Anti-JC virus antibodies: implications for PML risk stratification. Ann Neurol 2010;68:295–303.
7. Kappos L, Bates D, Edan G, et al. Natalizumab treatment for multiple sclerosis: updated recommendations for patient selection and monitoring. Lancet Neurol 2011;10:745–58.
8. Kappos L, Freedman MS, Polman CH, et al. Long-term effect of early treatment with interferon beta-1b after a first clinical event suggestive of multiple sclerosis: 5-year active treatment extension of the phase 3 BENEFIT trial. Lancet Neurol 2009;8:987–97.
9. Kinkel RP, Dontchev M, Kollman C, et al. Association between immediate initiation of intramuscular interferon beta-1a at the time of a clinically isolated syndrome and long-term outcomes: A 10-year follow-up of the controlled high-risk avonex multiple sclerosis prevention study in ongoing neurological surveillance. Arch Neurol 2011;69:183–90.
10. Mikol DD, Barkhof F, Chang P, et al. Comparison of subcutaneous interferon beta-1a with glatiramer acetate in patients with relapsing multiple sclerosis (the rebif vs. glatiramer acetate in relapsing MS disease [REGARD] study): a multicentre, randomised, parallel, open-label trial. Lancet Neurol 2008;7:903–14.
11. Miller DH, Chard DT, Ciccarelli O. Clinically isolated syndromes. Lancet Neurol 2012;11:157–69.
12. Miron VE, Jung CG, Kim HJ, et al. FTY720 modulates human oligodendrocyte progenitor process extension and survival. Annal Neurol 2008;63:61–71.
13. O’Connor P, Filippi M, Arnason B, et al. 250 microg or 500 microg interferon beta-1b versus 20 mg glatiramer acetate in relapsing-remitting multiple sclerosis: a prospective, randomised, multicentre study. Lancet Neurol 2009;8:889–97.
14. Polman CH, Reingold SC, Banwell B, et al. Diagnostic criteria for multiple sclerosis: 2010 revisions to the McDonald criteria. Ann Neurol 2011;69:292–302.
15. Schwab SR, Cyster JG. Finding a way out: lymphocyte egress from lymphoid organs. Nat Immunol 2007;8:1295–301.
16. Tumani H, Deisenhammer F, Giovannoni G, et al. Revised McDonald criteria: the persisting importance of cerebrospinal fluid analysis. Ann Neurol 2011;70:520; author reply 521.
17. Wenning W, Haghikia A, Laubenberger J, et al. Treatment of progressive multifocal leukoencephalopathy associated with natalizumab. N Engl J Med 2009;361:1075–80.
Dr. Aiden Haghikia, Neurologische Klinik, St. Josef-Hospital, Klinikum der Ruhr-Universität Bochum, Gudrunstraße 56, 44791 Bochum und Nuffield Department of Clinical Neurosciences, Weatherall Institute of Molecular Medicine, John Radcliffe Hospital, University of Oxford, Oxford, OX3 9DS, United Kingdom, E-Mail: aiden.haghikia@ndm.ox.ac.uk
Prof. Dr. med. Ralf Gold, Neurologische Klinik, St. Josef-Hospital, Klinikum der Ruhr-Universität Bochum, Gudrunstraße 56, 44791 Bochum
S2-guidelines for multiple sclerosis: new therapeutic and diagnostic aspects
Multiple sclerosis (MS) is a rapidly evolving field of translational medicine, where research efforts of the last decades have resulted in diagnostic and therapeutic advances available now in the clinical setting. Therefore, it is not surprising that since the last MS consensus guidelines of the German Society of Neurology (DGN) in 2008 the major diagnostic criteria have undergone thorough revision and the number of approved drugs has increased. Numerous promising therapeutics are at late stage clinical trials. In addition, valuable experience on existing therapeutic principles has accumulated with extended patient years on treatment and monitoring programs have given relevant insight on risk-benefit profiles of newer MS drugs. Growing clinical experience and recent findings on so far unknown mechanisms of action have also led to considerable changes in the use and precautions of applied MS drugs.
Increasing therapeutic options provide treating neurologists the privilege and ability for to choose the right drug according to their MS patients’ needs. At the same time new treatment options add to complexity and new questions that these drugs create, often not even related to the neurologic disease: How and to what extent do these drugs impair the immune system? How do they interact with other drugs, e.g. symptomatic medication? When to stop therapy before pregnancy and when to start again, especially in a disease that mostly affects young women?
The revised and extended MS consensus guidelines of the German Society of Neurology summarized in this article include recent proceedings in the field of MS, neuromyelitis optica, acute disseminated encephalomyelitis, and provide background information in addition to detailed recommendations on application and safety measures of MS therapeutics based on highest available evidence class. Furthermore, the guidelines now contain chapters on symptomatic therapies and consider pregnancy as well as other important non-neurological aspects of MS. Here, we focus only on few selected aspects that are new in the revised guidelines.
Key words: Multiple sclerosis, guidelines DGN 2012, diagnosis, therapy
Psychopharmakotherapie 2012; 19(05)
