Bernhard J. Steinhoff, Kehl-Kork
Standard der Epilepsietherapie ist nach wie vor die chronische antiepileptische Pharmakotherapie, somit also die Vorbeugung epileptischer Anfälle durch kontinuierliche, meist orale Applikation [11]. Mittlerweile steht neben den klassischen Antiepileptika eine Vielzahl neuer Substanzen zur Verfügung, von denen in Deutschland als erste Vigabatrin im Jahre 1992 eingeführt wurde [11]. Im Gegensatz zu anderen neurologischen Indikationen wie der Therapie des Morbus Parkinson oder der Migränebehandlung eint neue Antiepileptika nicht ein gemeinsames Wirkprinzip, wie dies bei den genannten Erkrankungen für Dopaminagonisten oder Triptane zutrifft. Vielmehr handelt es sich bei den neuen Antiepileptika um eine heterogene Gruppe verschiedenster Moleküle mit verschiedensten Wirkprinzipien, die sich letztlich zunächst nur anhand des Einführungsdatums nach 1992 als Gruppe zusammenfassen lassen.
Wenige neue Antiepileptika wiesen selektive Mechanismen auf, beispielsweise Vigabatrin über die irreversible Hemmung der GABA-Aminotransferase oder Tiagabin über die Blockade der Wiederaufnahme von Gamma-Aminobuttersäure (GABA) im synaptischen Spalt [11]. Auch Gabapentin, Pregabalin und Levetiracetam definieren sich zum Teil über einen spezifischen Wirkungsmechanismus: Gabapentin und Pregabalin modulieren Calciumkanäle durch die Besetzung spezifischer Bindungsstellen am Kanal [11, 12], Levetiracetam wirkt über die Bindung einer sogenannten SV2A-Rezeptor-Bindungsstelle [11]. Die letzten in Deutschland eingeführten neuen Antikonvulsiva, Lacosamid und Retigabin, zeichneten sich im Vergleich zu anderen Arzneimitteln ebenfalls durch einen spezifischen, nur diesen Substanzen eigenen Mechanismus aus, nämlich einerseits die langsame Inaktivierung von Natriumkanälen durch Lacosamid und andererseits die Öffnung inhibitorischer Kaliumkanäle durch Retigabin [11].
Es ist eine verlockende Idee, dass die etwa 30% pharmakotherapieresistenten Epilepsiepatienten möglicherweise eher durch Antiepileptika erfolgreich behandelt werden können, die einen von den etablierten Mechanismen differenziellen Effekt ausüben. Neben den bereits genannten Mechanismen spielt unter etablierten Antikonvulsiva unter Einbeziehung der neuen Substanzen Lamotrigin, Oxcarbazepin und Eslicarbazepinacetat die Blockade spannungs- und gebrauchsabhängiger Natriumkanäle, darüber hinausgehend die Wirkung auf weitere spannungsabhängige Ionenkanäle, dabei insbesondere Calciumkanäle, sowie der aktivierende Einfluss auf inhibitorische Neurotransmitter, insbesondere GABA, die wesentliche Rolle. Eine denkbare und potenziell wichtige antikonvulsive Wirkweise ist sicher der hemmende Einfluss auf exzitatorische Neurotransmitter, hier vor allem Glutamat.
Die bisher verfügbaren Antikonvulsiva haben nur zum Teil und dann eher schwach ausgeprägte antiglutamaterge Effekte. Dies gilt vor allem für Felbamat und Topiramat [11]. Mit Perampanel wird nun erstmals eine antiglutamaterge spezifisch wirksame Substanz in die Epilepsietherapie eingeführt, deren Zulassung zur Zusatztherapie von Patienten mit fokalen epileptischen Anfällen ab einem Alter von 12 Jahren seitens der europäischen Zulassungsbehörde erfolgt ist. Die hier vorgelegte Übersichtsarbeit fasst den Wirkungsmechanismus, die wesentlichen pharmakologischen Eigenschaften und die Ergebnisse der Zulassungsstudien zusammen.
Substanz und Wirkungsmechanismus
Perampanel (Abb. 1) ist ein oral aktiver, nichtkompetitiver und hoch selektiver Antagonist am Alpha-Amino-3-hydroxy-5-methyl-4-isoxazolpropionsäure(AMPA)-Rezeptor, der als Antiepileptikum in den letzten Jahren in klinischer Prüfung war [5]. AMPA-Rezeptoren finden sich vorwiegend an der postsynaptischen Membran exzitatorischer Synapsen im Gehirn. Sie weisen eine Glutamatbindungsstelle auf und leiten glutamatvermittelte postsynaptische Signale weiter [10]. Man geht davon aus, dass im menschlichen hippokampalen und neokortikalen Gewebe bei Epilepsien eine Hypersensitivität von AMPA-Rezeptoren und eine erhöhte Anzahl von Glutamatbindungsstellen vorliegen [13, 14]. Aus diesem Grund erwartet man von AMPA-Rezeptorantagonisten ein therapeutisches antikonvulsives Potenzial [9, 10].
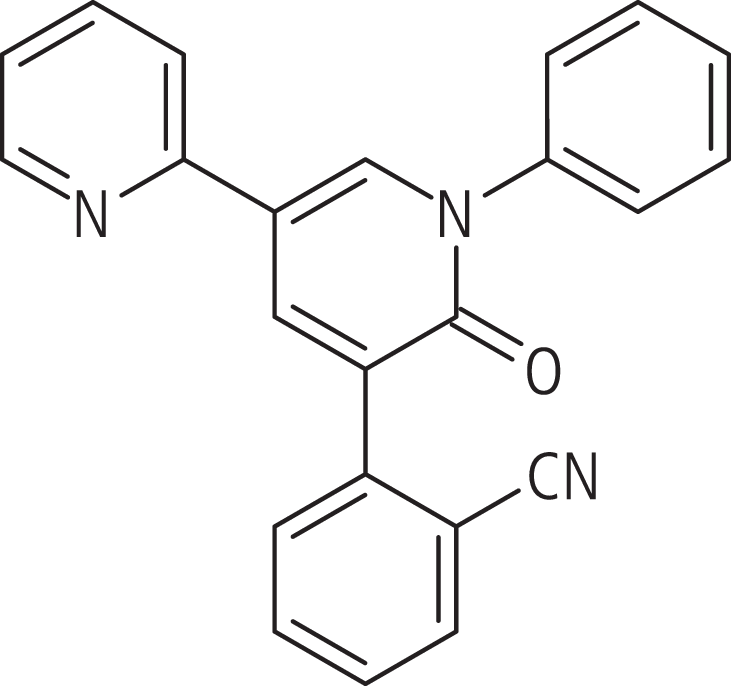
Abb. 1. Perampanel
Perampanel hemmt wahrscheinlich den durch Glutamat induzierten Anstieg der intrazellulären Calciumkonzentration, wodurch die neuronale Exzitabilität abnimmt [8]. Es konnte gezeigt werden, dass Perampanel nicht mit anderen ionotropen Glutamatrezeptoren wie dem N-Methyl-D-Aspartat(NMDA)-Rezeptor oder Kainat-Rezeptoren relevant interagiert [5, 10] und keine Phencyclidin-artigen Störwirkungen auf das Verhalten induziert, wie sie unter Einfluss verschiedener NMDA-Rezeptorantagonisten beobachtet wurden, [10]. Neben Perampanel befindet sich mit Talampanel ein anderer AMPA-Rezeptorantagonist ebenfalls in klinischer Prüfung als Antiepileptikum [2].
Experimentelle Pharmakologie und Toxikologie [5]
Perampanel wurde in verschiedenen präklinischen Modellen eingesetzt [5]. Im Maximal-Elektroschock-Modell, das als Indikator für eine Wirksamkeit gegen generalisierte tonisch-klonische Anfälle beim Menschen sprechen soll [12], wurde an Mäusen eine hohe Wirksamkeit nachgewiesen [5]. Gleiches gilt für audiogene Anfälle der Maus [5], die ebenfalls als Modell für generalisierte tonisch-klonische Anfälle angesehen werden. Perampanel unterdrückt Pentylentetrazol-induzierte Anfälle der Maus, woraus sich auf einen therapeutischen Effekt auf klonische Anfälle schließen lässt. In allen drei klassischen präklinischen Anfallsmodellen waren die erforderlichen Dosen für eine Anfallskontrolle niedriger als für die traditionellen Antikonvulsiva Carbamazepin und Valproinsäure. Im Amygdala-Kindling-Modell der Ratte, dem klassischen Modell für mesial-temporale Epileptogenese, erhöhte Perampanel die Nachentladungsschwelle dosisabhängig ebenso wie die Anfallsdauer der motorischen Anfallsphase und die Dauer der Nachentladungen. Im 6-Hz-Elektroschock-Modell der Maus, in dem zahlreiche verfügbare Antikonvulsiva unwirksam sind, war ebenfalls eine hohe Wirksamkeit von Perampanel nachweisbar. Die antikonvulsive Aktivität nimmt üblicherweise ab, wenn die Stimulationsintensität 22 mA überschreitet. Nur wenige Antikonvulsiva inhibieren Anfälle bei einer Stimulationsintensität von 44 mA. Dosisabhängig ließ sich mit Perampanel auch unter diesen Stimulationsintensitäten ein inhibitorischer Effekt nachweisen. Perampanel wirkte dagegen nicht im klassischen Absencen-Modell der Strasbourg-Ratte.
Pharmakokinetik [1]
Perampanel wird rasch und komplett aus dem Gastrointestinaltrakt resorbiert. Bei gesunden Probanden ergab sich eine maximale Plasmakonzentration im Mittel eine Stunde nach Einnahme, wobei dieser Zeitraum zwischen 15 Minuten und zwei Stunden variierte. Nahrung reduzierte die maximale Plasmakonzentration, nicht aber das Ausmaß der Resorption. Die absolute Bioverfügbarkeit liegt nahe 100%.
Perampanel wird zu 95% an Plasmaproteine gebunden. Es wird umfangreich metabolisiert, wobei die wesentlich involvierten Cytochrome CYP3A4 und/oder CYP3A5 sind. Die Perampanel-Konzentration wird durch die Inhibition von CYP3A kaum, wohl aber durch eine massive Induktion von CYP3A4 beeinflusst, was sich in Interaktionsstudien niederschlug. Die Clearance von Perampanel steigt unter Einfluss von Carbamazepin um das Dreifache und unter Einfluss von Phenytoin und Oxcarbazepin um das Zweifache. Unter Einfluss von Ketoconazol, einem potenten CYP3A-Inhibitor, kommt es dagegen nur zu einem leichten Anstieg der Konzentration und zu einer Verlängerung der Halbwertszeit um 15%. Perampanel selbst ist kein potenter Enzyminduktor oder -inhibitor. Es hat keinen signifikanten Einfluss auf die Clearance von Clonazepam, Levetiracetam, Phenobarbital, Phenytoin, Topiramat und Zonisamid. Die Clearance von Oxcarbazepin wird um 26% reduziert. Die Clearance von Carbamazepin, Clobazam, Lamotrigin und Valproinsäure wird unter der höchsten untersuchten Perampanel-Dosis zwar signifikant, aber nur im Ausmaß von unter 10% verändert. Unter einer Tagesdosis von 4 mg und 8 mg wurde kein Effekt von Perampanel auf Levonorgestrel oder Ethinylestradiol berichtet, während unter Tagesdosen von 12 mg die maximale Plasmakonzentration und die Konzentration über 24 Stunden von Levonorgestrel um etwa 40% fiel.
Perampanel wird fast komplett über den CYP3A-Metabolismus eliminiert. Die mittlere Halbwertszeit beträgt 105 Stunden. Sie wird in Kombination mit Carbamazepin auf 25 Stunden gesenkt. Üblicherweise wird das Plasmafließgleichgewicht 14 Tage nach Beginn der Eindosierung erreicht. Perampanel wird zu 70% fäkal und zu 30% mit dem Urin eliminiert.
Die Pharmakokinetik ist linear. Im Dosisbereich zwischen 2 und 12 mg wurde die Dosisproportionalität gezeigt.
Es wird empfohlen, dass Perampanel einmal täglich vor dem Zubettgehen eingenommen wird. Unter Einfluss von Nahrung wird die maximale Plasmakonzentration reduziert und erst zwei Stunden nach Einnahme erreicht. Eine fettreiche Mahlzeit senkt die Resorptionsrate: Die maximale Konzentration wird um 40% gesenkt, während das Resorptionsausmaß, die Konzentration über 24 Stunden und die Halbwertszeit nicht verändert werden. Man kann vermutlich daraus schließen, dass Plasmakonzentrationsspitzen, die für die Verträglichkeit eher störend und für die Wirksamkeit überflüssig sind, bei Einnahme von Perampanel nach Nahrungsaufnahme in der Praxis vermieden werden.
Phase-II-Studien [6]
Mit Perampanel wurden zwei Phase-II-Studien durchgeführt, um die maximal tolerierte Dosis zu ermitteln. Dabei handelte es sich um doppelt verblindete, Plazebo-kontrollierte Studien bei erwachsenen Patienten mit epileptischen Anfällen fokalen Ursprungs [6]. Die Patienten waren 18 bis 70 Jahre alt. In der ersten Studie wurden sie für 12 Wochen mit Plazebo oder Perampanel behandelt, wobei die Dosis über acht Wochen aufdosiert wurde und eine vierwöchige Erhaltungsphase folgte. In dieser Studie wurde Perampanel bis zu 4 mg pro Tag entweder einmal oder zweimal pro Tag gegeben. In der zweiten Studie erhielten Patienten Plazebo oder einmalig pro Tag appliziertes Perampanel bis zu einer maximalen Dosis von 12 mg für 16 Wochen, mit einer Aufdosierung über 12 Wochen und einer Erhaltungsperiode über 4 Wochen. Insgesamt wurden 153 Patienten in der ersten Studie randomisiert (Perampanel zweimal täglich bei 51 Patienten, einmal täglich bei 51 Patienten und Plazebo bei 51 Patienten). In der zweiten Studie wurden 48 Patienten eingeschlossen (Perampanel 38 Patienten, Plazebo 10 Patienten). In der ersten Studie ergaben sich keine Verträglichkeitsunterschiede zwischen Plazebo und Perampanel, und zwar unabhängig davon, ob Perampanel einmal oder zweimal pro Tag gegeben wurde. In der zweiten Studie vertrugen die meisten Patienten Dosen von mehr als 6 mg Perampanel in einmal täglicher Applikation. In beiden Studien waren die häufigsten Störwirkungen zentralnervöser Art und überwiegend mäßig ausgeprägt. Aus diesen Studien wurde auf einen anzustrebenden Dosierungsbereich zwischen 4 und 12 mg pro Tag bei einmal täglicher Gabe geschlossen und die nachfolgenden drei entscheidenden Zulassungsstudien entsprechend konzipiert.
Ergebnisse der zulassungsrelevanten Phase-III-Studien [3, 4, 8]
Perampanel wurde bei Patienten mit schwer behandelbaren Epilepsien ab einem Alter von 12 Jahren als Zusatzmedikation in insgesamt drei randomisierten, Plazebo-kontrollierten, multizentrischen Studien getestet. Die Basismedikation bestand dabei aus ein bis drei Antiepileptika.
In zwei Studien wurde eine Perampanel-Tagesdosis von 8 mg bzw. 12 mg mit Plazebo verglichen [3, 4], in der dritten Studie Dosen von 2 mg, 4 mg und 8 mg mit einem zusätzlich gegebenen Scheinmedikament [8]. Alle drei Studien führten letztlich in eine offene Weiterbeobachtung, in der dann als Maximaldosis 12 mg möglich waren.
In den Zulassungsstudien wurde die Behandlung mit Perampanel immer in einer Dosis von 2 mg pro Tag begonnen. Je nach Randomisierung wurde dann wöchentlich in Schritten von 2 mg gesteigert. Die Erhaltungsdosis wurde über 13 Wochen beobachtet, ehe in einer Transitionsphase von vier Wochen schließlich in die offene Weiterbehandlung übergegangen werden konnte.
In allen drei Studien waren die primären Zielvariablen entsprechend den unterschiedlichen Vorgaben der amerikanischen und der europäischen Zulassungsbehörde
- die mediane Änderung der Anfallsfrequenz über 28 Tage im Vergleich zur Vorbeobachtungsphase bzw.
- die Responderrate, also die Zahl von Patienten, die eine Anfallsreduktion um mindestens 50% erfuhren.
Sekundäre Zielvariablen waren die mediane Veränderung der Frequenz von komplex-fokalen und sekundär generalisierten Anfällen und die umfangreiche Erfassung von Sicherheitsparametern einschließlich Laborparametern und EKG.
Studie 306 [8]
In der Studie 306 betrugen die Zieldosen von Perampanel 2 mg, 4 mg und 8 mg. Die Studie wurde in Europa, Asien und Australien durchgeführt. 878 Patienten wurden rekrutiert, 712 randomisiert. Letztlich betrugen die Behandlungsstärken n=185 in der Plazebo-Gruppe, n=180 in der 2-mg-Gruppe, n=172 in der 4-mg-Gruppe und n=169 in der 8-mg-Gruppe. In diesen Gruppen betrug die Rate an Studienbeendern 89,7%, 85,6%, 91,9% und 85,8%. Ein Studienabbruch aufgrund von Störwirkungen erfolgte in 3,2% der Fälle unter Plazebo, in 5,6% der Fälle unter einer angestrebten Erhaltungsdosis von 2 mg Perampanel, in 2,9% unter 4 mg Perampanel und in 6,5% unter 8 mg Perampanel. Die demographischen Merkmale waren in allen Behandlungsgruppen ähnlich. Die Dauer der Epilepsie betrug im Mittel 19,1 Jahre. 14,7% der Patienten nahmen zum Zeitpunkt des Studieneinschlusses ein Antiepileptikum ein, 85,3% zwei oder drei Antiepileptika. Die mediane Anfallshäufigkeit während der Vorbeobachtungsperiode von sechs Wochen lag je nach Behandlungsgruppe zwischen 9,3 und 10,9 Anfällen pro 28 Tage.
Wirksamkeit. Die mediane Änderung der Anfallshäufigkeit betrug unter Plazebo 10,7%, unter 2 mg Perampanel 13,6%, unter 4 mg Perampanel 23% und unter 8 mg Perampanel 30,8%. Für 4 mg und 8 mg Perampanel waren diese Unterschiede statistisch signifikant (p=0,003 bzw. p<0,001). Die Responderrate betrug unter Plazebo 17,9%, unter 2 mg Perampanel 20,6%, unter 4 mg Perampanel 28,5% und unter 8 mg Perampanel 34,9%. Für 4 mg Perampanel und 8 mg Perampanel waren diese Unterschiede statistisch signifikant (p=0,013 bzw. p<0,001). Um einen Responder zu erzielen, waren 37 Behandlungen mit 2 mg Perampanel, 8 Behandlungen mit 4 mg Perampanel und 6 Behandlungen mit 8 mg Perampanel notwendig (Numbers needed to treat).
Anfallsfreiheit wurde bei 1,2% der Patienten unter Plazebo, bei 1,9% unter 2 mg Perampanel, bei 4,4% unter 4 mg Perampanel und bei 4,8% unter 8 mg Perampanel erreicht. Zusätzliche Untersuchungen des globalen klinischen Eindrucks sprachen ebenfalls für einen positiven Effekt von Perampanel unter 4-mg- und unter 8-mg-Dosen.
Verträglichkeit. Schwindel und Schläfrigkeit waren die Störwirkungen, die am häufigsten zu einer Dosisreduktion führten. Generell wurden Schwindel, Schläfrigkeit, Erschöpfung und Gangstörungen unter Perampanel mindestens doppelt so häufig beobachtet wie unter Plazebo. Für Schwindel deutete sich eine Dosis-Wirkungs-Beziehung an. Kopfschmerzen wurden von 9 bis 11% der Patienten unter Perampanel berichtet, allerdings berichteten auch 8,6% der Patienten unter Plazebo über diese Störwirkung. Unerwünschte Ereignisse, die zu einem Abbruch der Behandlungen führten, traten bei 3,8% unter Plazebo, bei 6,7% unter 2 mg Perampanel, bei 2,9% unter 4 mg Perampanel und bei 7,1% unter 8 mg Perampanel auf. Die am häufigsten zum Abbruch der Behandlung führenden Störwirkungen waren unter Perampanel Schwindel, Anfälle und Erschöpfung. Eine Verschlechterung der Anfallssituation, die als eine mehr als 50%ige Zunahme der Anfälle gegenüber der Vorbeobachtungsperiode definiert war, wurde unter Plazebo bei 15%, unter 2 mg Perampanel bei 11%, unter 4 mg Perampanel bei 8% und unter 8 mg Perampanel ebenfalls bei 8% der Patienten beobachtet.
Studie 305 [4]
In diese Studie, in der Plazebo mit Perampanel in einer Erhaltungsdosis von 8 mg bzw. 12 mg verglichen wurde, wurden 496 Teilnehmer rekrutiert und letztlich 389 randomisiert. In der Plazebo-Gruppe waren 136 Patienten, in der 8-mg-Gruppe 129 Patienten und in der 12-mg-Gruppe 121 Patienten. Studienbeender waren 88,2%, 83,7% und 76,9%; 11,8%, 16,3% und 23,1% der Patienten brachen die Studie ab. Ein Abbruch aufgrund von unerwünschten Ereignissen erfolgte unter Plazebo bei 2,9%, unter 8 mg Perampanel bei 8,5% und unter 12 mg Perampanel bei 19% der Patienten.
Die Zielvariablen waren identisch mit denen der Studie 306. Die mediane prozentuale Änderung der Anfallshäufigkeit betrug unter Plazebo 9,7%, unter 8 mg Perampanel 30,5% und unter 12 mg Perampanel 17,6%. Für beide untersuchten Perampanel-Dosen war dieser Unterschied statistisch signifikant (p=0,0008 bzw. p=0,0105). Die Responderraten betrugen unter Plazebo 14,7%, unter 8 mg Perampanel 33,3% und unter 12 mg Perampanel 33,9%. Auch bezüglich dieses Kriteriums waren die Unterschiede statistisch signifikant (0,0018 bzw. 0,0006). Anfallsfreiheit wurde in der Erhaltungsphase unter Plazebo bei 1,7%, unter 8 mg Perampanel bei 2,8% und unter 12 mg Perampanel bei 6,5% der Patienten erreicht. Die globale Evaluation der klinischen Effizienz sprach signifikant für Perampanel.
Störwirkungen traten unter Plazebo bei 68,4%, unter 8 mg Perampanel bei 86,8% und unter 12 mg Perampanel bei 86,0% der Patienten auf. Die Rate schwerwiegender Störwirkungen betrug 5,1%, 7,8% und 9,9%. Die häufigsten unerwünschten Ereignisse (mit einer Häufigkeit von mehr als 10%) betrafen Schwindel, Müdigkeit, Erschöpfung und Kopfschmerzen, wobei erneut Kopfschmerzen in der Plazebo-Gruppe gleich häufig berichtet wurden. Die häufigsten unerwünschten Ereignisse, die zu einer Dosisänderung oder einem Studienabbruch führten, waren Schwindel, Müdigkeit, Kopfschmerzen, Erschöpfung, Ataxie und Asthenie.
Studie 304 [3]
Auch in dieser multizentrischen, doppelblinden, Plazebo-kontrollierten Studie wurde Perampanel in einer Erhaltungsdosis von 8 mg oder 12 mg mit Plazebo bei Patienten verglichen, die mindestens 12 Jahre alt waren, an therapieresistenten Epilepsien mit Anfällen fokalen Ursprungs erkrankt waren und mindestens ein bis drei Antiepileptika als Basismedikation einnahmen. Die Patienten wurden im Verhältnis 1:1:1 randomisiert. Nach einer Vorbeobachtungsperiode von sechs Wochen mit stabiler Medikation folgte eine sechswöchige Aufdosierungsphase mit nachfolgend dreizehnwöchiger Erhaltungsperiode. Die primären Zielvariablen waren zu den anderen beiden zulassungsrelevanten Studien identisch. Von 534 rekrutierten Patienten wurden letztlich 390 randomisiert. In der Plazebo-Gruppe waren 121 Patienten, 133 Patienten wurden mit 8 mg Perampanel und 134 Patienten mit 12 mg Perampanel behandelt. Die Studie beendeten 87,6%, 85,7% und 74,6%, entsprechend betrugen die Quoten der Studienabbrecher 12,4%, 14,3% und 25,4%. Aufgrund von unerwünschten Ereignissen brachen in der Plazebo-Gruppe 5,8%, in der 8-mg-Gruppe 6,8% und in der 12-mg-Gruppe 17,9% der Patienten ab.
In dieser Studie war hinsichtlich der Wirksamkeit der hohe Anteil von erfolgreichen Therapien unter Plazebo bemerkenswert und statistisch relevant. Die mediane prozentuale Abnahme der Anfallshäufigkeit betrug unter Plazebo 21,0%, unter 8 mg Perampanel 26,3% und unter 12 mg Perampanel 34,5%. Die Ergebnisse unter Perampanel waren statistisch signifikant besser (p=0,0261 bzw. 0,0158). Dies galt nicht hinsichtlich der Zielvariable der Responderrate, die für Plazebo 26,4%, für 8 mg Perampanel 37,6% und für 12 mg Perampanel 36,1% betrug. Perampanel war hinsichtlich dieser Zielvariable nur im Trend, aber nicht signifikant besser (p=0,0076 bzw. 0,091). Die Zahl der Behandlungen bis zu einem erfolgreichen Ergebnis im Sinne eines Responders (Numbers needed to treat) betrug 9 bzw. 10. Die Anfallsfreiheitsquoten betrugen 0% für Plazebo, 2,6% für 8 mg Perampanel und 2,0% für 12 mg Perampanel. Eine globale klinische Verbesserung wurde statistisch signifikant nur unter 8 mg Perampanel beschrieben. Die ungewöhnlich hohe Plazebo-Rate erklärte sich zum großen Teil dadurch, dass in bestimmten Ländern (Mittel- und Südamerika) extrem hohe Plazebo-Raten beobachtet wurden, die sich mit hoher Wahrscheinlichkeit methodisch negativ auf die Datenqualität und letztlich auch auf das Wirksamkeitsergebnis auswirkten.
Störwirkungen wurden generell bei 82,6% unter Plazebo, 88,0% unter 8 mg Perampanel und 91,8% unter 12 mg Perampanel beobachtet. Unerwünschte Ereignisse, die zu einer Dosisreduktion oder einem Abbruch führten, wurden unter Plazebo bei 5,0%, unter 8 mg Perampanel bei 22,6% und unter 12 mg Perampanel bei 33,6% berichtet. Schwerwiegende unerwünschte Ereignisse traten in einer Häufigkeit von 5,0%, 6,0% und 6,7% auf. Die häufigsten unerwünschten Ereignisse mit einer Häufigkeit von mindestens 10% betrafen Schwindel, Müdigkeit, Kopfschmerzen (neuerlich mit einer hohen Plazebo-Rate, die sich von Perampanel nicht unterschied), Stürze, Irritabilität und Ataxie.
Die Wirksamkeitsergebnisse und die zusammengefassten Störwirkungen der drei zulassungsrelevanten Studien werden in den Tabellen 1, 2 und 3 wiedergegeben.
Tab. 1. Wirksamkeit von Perampanel in den Zulassungsstudien
|
Studie |
Plazebo |
Verum |
|||
|
2 mg |
4 mg |
8 mg |
12 mg |
||
|
Mediane Änderung der Anfallshäufigkeit |
|||||
|
Krauss et al., 2012 [8] |
–10,7% |
–13,6 |
–23,3% |
–30,8% |
– |
|
p-Wert |
– |
n. s. |
0,003 |
<0,001 |
|
|
French et al., 2012 [4] |
–9,7% |
– |
– |
–30,5% |
–17,6% |
|
p-Wert |
– |
– |
– |
0,0008 |
0,0105 |
|
French et al., 2012 [3] |
–21,0% |
– |
– |
–26,3% |
–34,5% |
|
p-Wert |
– |
– |
– |
0,0261 |
0,0158 |
|
Responderrate |
|||||
|
Krauss et al., 2012 [8] |
17,9% |
20,6% |
28,5% |
34,9% |
– |
|
p-Wert |
– |
n. s. |
0,013 |
<0,001 |
|
|
French et al., 2012 [4] |
14,7% |
– |
– |
33,3% |
33,9% |
|
p-Wert |
– |
– |
– |
0,0018 |
0,0006 |
|
French et al., 2012 [3] |
26,4% |
– |
– |
37,6% |
36,1% |
|
p-Wert |
– |
– |
– |
0,076; |
0,091; |
n. s.: nicht signifikant
Tab. 2. Unerwünschte Ereignisse in allen drei Zulassungsstudien
|
Plazebo |
Verum |
||||
|
2 mg |
4 mg |
8 mg |
12 mg |
||
|
Unerwünschte Ereignisse gesamt [%] |
66,5 |
61,7 |
64,5 |
81,2 |
89,0 |
|
Schwindel [%] |
9,0 |
10,0 |
16,3 |
31,8 |
42,7 |
|
Müdigkeit („somnolence“) [%] |
7,2 |
12,2 |
9,3 |
15,5 |
17,6 |
|
Kopfschmerzen [%] |
11,3 |
8,9 |
11,0 |
11,4 |
13,3 |
|
Erschöpfung („fatigue“) [%] |
4,8 |
4,4 |
7,6 |
8,4 |
12,2 |
|
Irritabilität [%] |
2,9 |
3,9 |
4,1 |
6,7 |
11,8 |
|
Stürze [%] |
3,4 |
1,1 |
1,7 |
5,1 |
10,2 |
|
Übelkeit [%] |
4,5 |
2,2 |
2,9 |
5,8 |
7,8 |
|
Nasopharyngitis [%] |
4,1 |
3,9 |
5,2 |
5,3 |
4,3 |
|
Infektionen des oberen Respirationstrakts [%] |
2,7 |
6,1 |
3,5 |
3,2 |
3,9 |
|
Ataxie [%] |
0,0 |
0,0 |
0,6 |
3,2 |
8,2 |
|
Gleichgewichtsstörung [%] |
0,5 |
0,0 |
0,0 |
5,1 |
3,1 |
Tab. 3. Unerwünschte Ereignisse in allen drei Zulassungsstudien, die zu Dosisänderungen (>2%) oder zum Studienabbruch (>1%) führten
|
Plazebo (n=442) |
Verum |
||||
|
2 mg (n=180) |
4 mg (n=172) |
8 mg (n=431) |
12 mg (n=255) |
||
|
Unerwünschte Ereignisse gesamt [%] |
66,5 |
61,7 |
64,5 |
81,2 |
89,0 |
|
Schwindel |
|||||
|
4 (0,9) |
0 |
6 (3,5) |
37 (8,6) |
42 (16,5) |
|
4 (0,9) |
1 (0,6) |
1 (0,6) |
9 (2,1) |
11 (4,3) |
|
Müdigkeit („Somnolence“) |
|||||
|
2 (0,5) |
0 |
0 |
17 (3,9) |
13 (5,1) |
|
1 (0,2) |
1 (0,6) |
0 |
2 (0,5) |
7 (2,7) |
|
Erschöpfung („Fatigue“) |
|||||
|
1 (0,2) |
0 |
1 (0,6) |
8 (1,9) |
3 (1,2) |
|
0 |
2 (1,1) |
2 (1,2) |
1 (0,2) |
2 (0,8) |
|
Irritabilität |
|||||
|
0 |
0 |
0 |
1 (0,2) |
8 (3,1) |
|
1 (0,2) |
0 |
0 |
1 (0,2) |
3 (1,2) |
|
Ataxie |
|||||
|
0 |
0 |
0 |
5 (1,2) |
7 (2,7) |
|
0 |
0 |
0 |
3 (0,7) |
4 (1,6) |
Die Ergebnisse der Studien führten zur Zulassung von Perampanel seitens der europäischen Zulassungsbehörde für die Zusatzbehandlung von Patienten ab einem Alter von 12 Jahren, bei denen trotz einer antiepileptischen Basismedikation weiterhin Anfälle fokalen Ursprungs auftreten. Die Studienergebnisse sind in dreierlei Hinsicht interessant:
- Es wird klar gezeigt, dass Perampanel als erster selektiver, nichtkompetitiver AMPA-Rezeptorantagonist als Zusatzmedikation bei schwer behandelbaren fokalen Epilepsien wirksam ist. Dies lässt hoffen, dass mit Perampanel eine zusätzliche effiziente Möglichkeit zur Therapie schwer behandelbarer Epilepsien zur Verfügung gestellt wird.
- Es zeigt sich auch im Entwicklungsprogramm von Perampanel, dass die Auswahl von Studienzentren bei multizentrischen Studien essenziell sein kann. In der Studie 304 waren die Ergebnisse von Perampanel letztlich deswegen schlechter als in den anderen Studien, weil die Rate von Plazebo-Respondern deutlich höher war. Dies wiederum ließ sich auf die besonders hohen Erfolgsquoten unter Plazebo in Mittel- und Südamerika zurückführen. Es bleibt zu hoffen, dass auch bei zukünftigen Entwicklungsprogrammen mehr auf die Qualität der Studienzentren als unter Umständen auf das Tempo der Rekrutierung geachtet wird.
- Die Wirksamkeitsdaten deuten an, dass zwischen 8 mg Perampanel und 12 mg Perampanel ein Plateau besteht. Die höhere Störwirkungsrate unter 12 mg ist wesentlich für dieses Resultat bei einer Intention-to-treat-Analyse verantwortlich. Trotzdem zeigt die Post-hoc-Analyse, dass Patienten durchaus von einer höheren Dosierung (12 mg) profitieren können. Entsprechend wurde auch das Zulassungsdossier formuliert.
Besondere Aspekte der Verträglichkeit
Aufgrund des neuen Wirkungsmechanismus der Substanz hat man in den Zulassungsstudien besonderen Wert auf eine sehr umfangreiche Verträglichkeitsprüfung gelegt. In keiner der drei Zulassungsstudien wurden relevante Laborauffälligkeiten oder EKG-Veränderungen gesehen. Die Rate von allergischen Hautausschlägen war niedrig, sie betrug unter Plazebo 1,6%, unter 2 mg Perampanel 1,1%, unter 4 mg 2,3%, unter 8 mg 2,8% und unter 12 mg 2,0%. Psychiatrische unerwünschte Ereignisse waren selten, was im Kontext des Wirkungsmechanismus vom Perampanel von größerer Bedeutung ist. Schlaflosigkeit wurde unter Plazebo bei 3,6% der Patienten beobachtet, die entsprechenden Häufigkeiten betrugen für 2 mg, 4 mg, 8 mg und 12 mg Perampanel 1,1%, 1,2%, 3,5% und 4,3%. Für Angst betrugen diese Quoten (Plazebo, 2 mg, 4 mg, 8 mg, 12 mg Perampanel) 1,1%, 2,2%, 1,7%, 3,0% und 3,5%, für Aggression 0,5%, 0,6%, 0,6%, 1,6% und 3,1%, für Depression 1,6%, 0,6%, 0,6%, 0,7% und 2,4%. Gedächtnisstörungen traten bei 1,1% der Patienten unter Plazebo auf, die Häufigkeit betrug unter 2 mg Perampanel 1,1%, unter 4 mg 0%, unter 8 mg 1,2% und unter 12 mg 2,0%.
Zusätzlich Ergebnisse aus der offenen Weiterbehandlungsstudie [7]
Offensichtlich war die Häufigkeit von zentralnervösen unerwünschten Ereignissen niedriger, wenn – wie in der Transition zur offenen Weiterbehandlung – die Dosierung alle zwei Wochen und nicht jede Woche um 2 mg Perampanel gesteigert wurde. In der Konversionsphase erreichten mehr als 91% der Patienten Dosishöhen von 10 mg oder 12 mg, was dafür spricht, dass unter diesen Bedingungen eher noch höhere Dosen erreicht werden können. Unerwünschte Effekte, die zu einer Studienbeendigung bzw. zu einem Therapieende führten, waren unter diesen Bedingungen mit 11,7% eher selten. Vergleicht man die mediane Anfallsreduktion der Patienten, die während der Studien Verum erhalten hatten, mit den Patienten, die in der verblindeten Studienphase mit Plazebo behandelt wurden und dann auf Perampanel in der offenen Weiterbehandlung eingestellt wurden, ergibt sich auch im Langzeitverlauf von einem Jahr hinsichtlich der Wirksamkeit kein Unterschied. Die mediane prozentuale Anfallsreduktion nach einem Jahr betrug bei Patienten, die während der gesamten Zeit mit Verum behandelt wurden 48,8% und bei den vormals mit Plazebo behandelten Patienten 49,2%.
Interessenkonflikte
BS gibt folgende potenziellen Interessenkonflikte an: Honorare für die Beratung oder Teilnahme an einem Expertenbeirat von Eisai, GlaxoSmithKline und UCB; Honorare für Vorträge, Stellungnahmen oder Artikel von Bial, Desitin, Eisai, GlaxoSmithKline und UCB; Forschungsbeihilfe für die Einrichtung von Bial, Carbamed, Desitin, Eisai, GlaxoSmithKline, Novartis und UCB, sonstige Unterstützung für die Einrichtung von Desitin, Eisai, GlaxoSmithKline, Novartis und UCB.
Literatur
1. Bialer M, Johannessen SI, Levy RH, Perucca E, et al. Progress report on new antiepileptic drugs: a summary of the Tenth Eilat Conference (EILAT X). Epilepsy Res 2010;92:89–124.
2. Chappell AS, Sander JW, Brodie MJ, Chadwick D, et al. A crossover, add-on trial of talampanel in patients with refractory partial seizures. Neurology 2002;58:1680–2.
3. French J, Krauss GL, Biton V, Squillacote D, et al. Adjunctive perampanel for refractory partial-onset seizures: randomized phase III study 304. Neurology 2012;79:589–96.
4. French JA, Krauss GL, Steinhoff BJ, Squillacote D, et al. Evaluation of adjunctive perampanel in patients with refractory partial-onset seizures: Results of randomized global phase III study 305. Epilepsia 2012. Im Druck. doi: 10.1111/j.1528-1167.2012.03638.x. (Epub ahead of print).
5. Hanada T, Hashizume Y, Tokuhara N, Takenaka O, et al. Perampanel: a novel, orally active, noncompetitive AMPA-receptor antagonist that reduces seizure activity in rodent models of epilepsy. Epilepsia 2011;52:1331–40.
6. Krauss GL, Bar M, Biton V, Klapper JA, et al. Tolerability and safety of permapanel: two randomized dose-escalation trials. Acta Neurol Scand 2012;125:8–15.
7. Krauss GL, Perucca E, Ben-Menachem E, Kwan P, et al. Perampanel, a selective, non-competitive a-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid receptor antagonist, as adjunctive therapy for refractory partial-onset seizures: interim results from phase III extension study 307. Epilepsia. Im Druck. doi: 10.1111/j.1528-1167.2012.03648.x. (Epub ahead of print).
8. Krauss GL, Serratosa JM, Villanueva V, Endziniene M, et al. Randomized phase III study 306: adjunctive perampanel for refractory partial-onset seizures. Neurology 2012;78:1408–15.
9. Meldrum BS, Rogawski MA. Molecular targets for antiepileptic drug treatment. Neurotherapeutics 2007;4:18–61.
10. Rogawski MA. Revisiting AMPA receptors as an antiepileptic drug target. Epilepsy Curr 2011;11:56–63.
11. Steinhoff BJ. Pharmakotherapie der Epilepsie. Klin Neurophys 2012;43:131–7.
12. Steinhoff BJ, Herrendorf G, Bittermann H-J, Kurth C. Neue Antiepileptika: Gabapentin. Epilepsie-Blätter 1995;8:3–11.
13. Vollmar W, Gloger J, Berger E. RNA editing (R/G site) and flip-flop splicing of the AMPA receptor subunit GluR2 in nervous tissue of epilepsy patients. Neurobiol Dis 2004;15:371–9.
14. Zilles K, Qu MS, Köhling R, Speckmann EJ. Ionotropic glutamate and GABA receptors in human epileptic tissue: quantitative in vitro receptor autoradiography. Neuroscience 1999;94:1051–61.
Prof. Dr. Bernhard J. Steinhoff, Epilepsiezentrum Kork, Landstraße 1, 77694 Kehl-Kork, E-Mail: bsteinhoff@epilepsiezentrum.de
The new antiepileptic drug perampanel
Antiepileptic drug (AED) treatment is still the golden standard of epilepsy treatment. In general, various antiepileptic modes of action are possible. Although it is obvious that the antiglutamatergic reduction of hyperexcitability should be a major strategy, currently licenced AEDs do not or hardly address this option.
For the first time, with perampanel, a selective, non-competitive alpha-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid (AMPA) receptor antagonist is now available that has specific antiglutamatergic effects.
The European regulation authorities approved perampanel for the add-on treatment of epilepsies of focal origin in patients with difficult-to-treat epilepsies and a minimum age of 12 years.
This review summarizes all relevant preclinical and clinical data including pharmacology and pivotal phase III trials.
Key words: Epilepsy, antiepileptic drug treatment, glutamate, perampanel
Psychopharmakotherapie 2012; 19(05)
