Dr. Dr. Tanja Neuvians, Ladenburg
Teriflunomid ist der aktive Metabolit von Leflunomid (z.B. Arava®), das seit mehr als zehn Jahren für die Behandlung der rheumatoiden Arthritis zugelassen ist. Teriflunomid hemmt die Dihydroorotat-Dehydrogenase – das Schlüsselenzym der De-novo-Pyrimidin-Synthese – und damit die Aktivierung, Proliferation und Funktion von Lymphozyten; Zellen, die sich langsam teilen und exogene Pyrimidinquellen nutzen, sind von dieser Wirkung weniger stark betroffen. An der Wirksamkeit von Teriflunomid scheinen noch andere Mechanismen beteiligt zu sein, etwa eine Hemmung der Aktivierung des Transkriptionsfaktors NF-kB [1, 2].
In einer Phase-II-Studie wiesen Patienten mit schubförmiger multipler Sklerose nach oraler Einnahme von Teriflunomid eine geringere Krankheitsaktivität und einen besseren klinischen Verlauf auf als die Patienten der Plazebo-Gruppe [3].
Studiendesign
In die Phase-III-Studie TEMSO (Teriflunomide multiple sclerosis oral) wurden Patienten zwischen 18 und 55 Jahren eingeschlossen, die an multipler Sklerose (MS) mit schubförmigem Verlauf mit oder ohne Progression litten. Sie hatten mindestens einen Schub im letzten Jahr oder mindestens zwei Schübe in den letzten zwei Jahren und ihr Behinderungsgrad entsprach einem Score von weniger als 5,5 auf der Expanded Disability Status Scale (EDSS). Sie wurden in drei Gruppen randomisiert und bekamen einmal täglich
- Plazebo (n=363),
- 7 mg Teriflunomid (n=365) oder
- 14 mg Teriflunomid (n=358).
Die Einnahme erfolgte doppelblind über 108 Wochen. In regelmäßigen Abständen wurden klinisch-neurologische Untersuchungen und Magnetresonanztomographien (MRT) durchgeführt. Da im Zusammenhang mit einer Anwendung von Leflunomid schwere Leberschäden und Pankreatitiden auftraten, wurden bei den Studienteilnehmern Ultraschalluntersuchungen des Bauchraums und Kontrollen der entsprechenden Laborparameter durchgeführt.
Primäres Studienziel war eine Reduktion der jährlichen Schubfrequenz. Zu den sekundären Endpunkten zählten ein verringertes Fortschreiten der Behinderung, gemessen als Veränderung des EDSS-Scores, und das Gesamtvolumen der Entzündungsherde im MRT.
Ergebnisse
Zwischen September 2004 und März 2008 wurden 1088 Patienten in die Studie aufgenommen, 796 schlossen sie planmäßig ab. Mehr als 90% der Teilnehmer litten an einer schubförmig-remittierenden MS, die übrigen an einer sekundär progredienten oder einer progredient-schubförmigen MS. Die mittlere Erkrankungsdauer betrug knapp neun Jahre, der mittlere EDSS-Score rund 2,7 Punkte. Weniger als 30% der Teilnehmer wurden in den vorangegangenen zwei Jahren mit krankheitsmodifizierenden Basistherapeutika behandelt.
Teriflunomid reduzierte die Anzahl der Schübe dosisunabhängig von 0,54 Schüben pro Patientenjahr unter Plazebo auf 0,37 Schübe pro Patientenjahr (jeweils p<0,001). Das Risiko eines Schubs war somit bei Einnahme von Teriflunomid gegenüber Plazebo um etwa 31% verringert.
Eine über mindestens 12 Wochen anhaltende, bestätigte Zunahme der körperlichen Behinderung trat in der Plazebo-Gruppe bei 27,3% der Patienten auf, unter 7 mg Teriflunomid bei 21,7% der Patienten und unter 14 mg bei 20,2% der Patienten (Abb. 1). Das Risiko für eine anhaltende Behinderungsprogression war gegenüber Plazebo unter der niedrigeren Teriflunomid-Dosis um 23,7% (p<0,08) und unter der höheren Teriflunomid-Dosis um 29,8 % (p<0,03) vermindert.
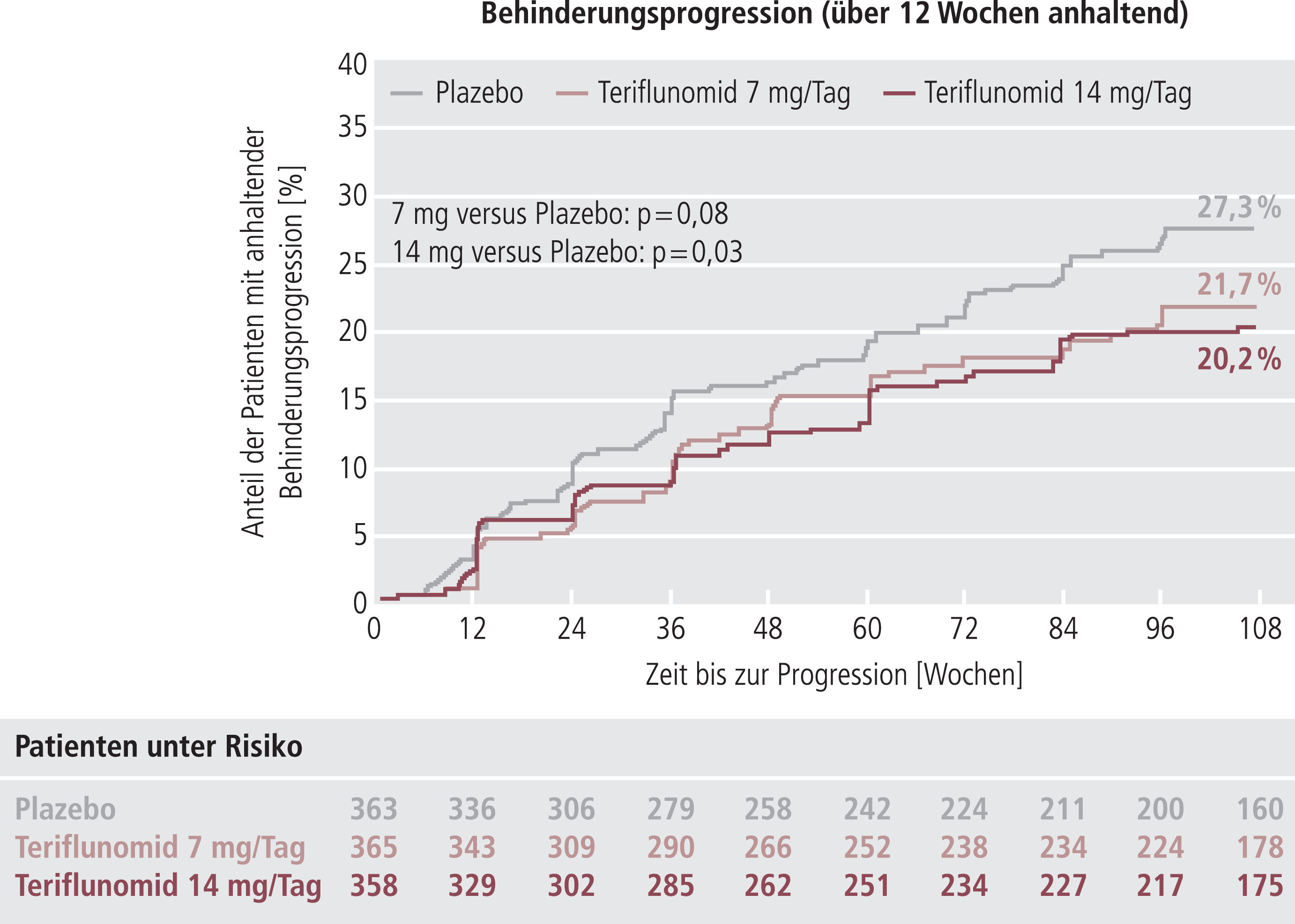
Abb. 1. Anteil der Patienten mit bestätigter, über mindestens 12 Wochen anhaltender Behinderungsprogression, ermittelt anhand der EDSS(Expanded disability status scale)-Scores in der TEMSO-Studie [1]
Das Gesamtvolumen der Entzündungsherde im MRT stieg unter Teriflunomid deutlich weniger als in der Plazebo-Gruppe (+2,21 ml), dabei war die 14-mg-Dosis (+0,72 ml; p<0,001) wirksamer als die 7-mg-Dosis (+1,31 ml; p<0,03). Teriflunomid reduzierte die Zahl der aktiven Entzündungsherde, es hatte aber keinen Einfluss auf die Gehirnatrophie. Auch auf Erschöpfungserscheinungen wirkte es sich nicht aus.
Unerwünschte Ereignisse traten in allen drei Studiengruppen etwa gleich oft auf (Tab. 1). Die häufigsten unerwünschten Ereignisse, die in beiden Teriflunomid-Gruppen gegenüber Plazebo verstärkt vorkamen und bei denen ein Dosiseffekt deutlich wurde, waren Durchfall, Übelkeit, Haarausfall und erhöhte Alanin-Aminotransferase-(ALAT-)Werte. Leicht erhöhte ALAT-Werte (≥1-fach über der Norm) waren unter Teriflunomid häufiger als in der Plazebo-Gruppe (54 bzw. 57,3% vs. 35,9%), dagegen waren stark erhöhte ALAT-Werte (≥3-fach über der Norm) in allen drei Gruppen gleich häufig (6,3 bis 6,7%) und zum Teil auf andere Erkrankungen zurückzuführen. Die Pankreaswerte (Amylase- und Lipasespiegel) blieben in allen drei Gruppen im Normbereich. Schwere Infektionen traten in allen Gruppen etwa gleich häufig auf (1,6 bzw. 2,5% vs. 2,2%).
Tab. 1. Häufigkeit unerwünschter Ereignisse (UE) in der TEMSO-Studie [n (%)] (Auswahl) [1]
|
Plazebo (n=360) |
Teriflunomid 7 mg/Tag (n=368) |
Teriflunomid 14 mg/Tag (n=358) |
|
|
Alle UE |
315 (87,5) |
328 (89,1) |
325 (90,5) |
|
Schwerwiegende UE |
46 (12,8) |
52 (14,1) |
57 (15,9) |
|
Diarrhö |
32 (8,9) |
54 (14,7) |
64 (17,9) |
|
Erhöhte Alamin-Aminotransferase-Werte |
24 (6,7) |
44 (12,0) |
51 (14,2) |
|
Übelkeit |
26 (7,2) |
33 (9,0) |
49 (13,7) |
|
Haarausdünnung oder verminderte Haardichte |
12 (3,3) |
38 (10,3) |
47 (13,1) |
Die Zahl der Neutrophilen und Lymphozyten sank im Mittel nur wenig (≤1,0/nl bzw. ≤0,3/nl), allerdings unter der höheren Teriflunomid-Dosis tendenziell stärker als unter der niedrigeren Teriflunomid-Dosis und Plazebo. Die Werte sanken innerhalb der ersten drei Monate der Therapie, anschließend stabilisierte sich die Zellzahl. Unter Teriflunomid traten drei Fälle einer moderaten Neutropenie (<0,9/nl) auf.
Diskussion
Die Behandlung mit Teriflunomid hat bei Patienten mit schubförmiger multipler Sklerose eine zwar mäßige, aber anhaltende Wirkung, die mit einer Reduktion der Schubrate um rund 30% in der gleichen Größenordnung wie die der bisher verfügbaren Basistherapeutika liegt. Im Unterschied zu diesen kann Teriflunomid aber oral verabreicht werden. Die höhere Dosis (14 mg/Tag) scheint insbesondere im Hinblick auf das Fortschreiten der Behinderung von Vorteil zu sein. Nebenwirkungen, die auf Teriflunomid zurückzuführen waren, waren selten so schwer, dass sie zum Abbruch der Therapie führten [1].
Teriflunomid ist zu mehr als 99% an Plasmaproteine gebunden und hat eine Plasmahalbwertszeit von fast zwei Wochen. Es kann jedoch mithilfe von Colestyramin, das den enterohepatischen Kreislauf durchbricht, innerhalb weniger Tage aus dem Körper eliminiert werden. Dies ist beispielsweise notwendig, wenn eine Schwangerschaft nach Einnahme der Substanz geplant oder eingetreten ist, da Teriflunomid potenziell teratogene Wirkungen hat [2].
Die langfristige Sicherheit von Teriflunomid kann noch nicht beurteilt werden. Bei Rheumapatienten, die mit Leflunomid behandelt wurden, wurden in 1,9 Millionen Patientenjahren zwei Fälle einer lebensbedrohlichen progressiven multifokalen Leukenzephalopathie gemeldet. Ob dieses Risiko auch bei Teriflunomid besteht, wird sich erst in längerfristigen Studien mit höheren Patientenzahlen zeigen [1].
Fazit
Die Ergebnisse der TEMSO-Studie zeigen, dass Teriflunomid ein wirksames, oral anwendbares Therapeutikum für Patienten mit schubförmiger multipler Sklerose mit und ohne Progredienz ist. Es ist zwar im indirekten Vergleich nicht besser wirksam als die bisherigen Basistherapeutika, es ist aber durch die einmal tägliche Einnahme einer Tablette einfacher anzuwenden. Daten zur Verträglichkeit bei einer Anwendungsdauer von mehr als zwei Jahren liegen zurzeit noch nicht vor.
Quellen
1. O’Connor P, et al. Randomized trial of oral teriflunomide for relapsing multiple sclerosis. N Engl J Med 2011;365:1293–303.
2. Warnke C, et al. Review of teriflunomide and its potential in the treatment of multiple sclerosis. Neuropsychiatr Dis Treat 2009;5: 333–40.
3. O’Connor PW, et al. A Phase II study of the safety and efficacy of teriflunomide in multiple sclerosis with relapses. Neurology 2006;66:894–900.
Psychopharmakotherapie 2012; 19(02)
