Mathias Mäurer, Bad Mergentheim
Die derzeitigen MS-Basistherapeutika Interferon beta (IFN-β) und Glatirameracetat müssen als subkutane oder intramuskuläre Injektion verabreicht werden. Die Selbstverabreichung, aber auch die Applikation durch Dritte, ist für die Patienten immer mit einer gewissen Selbstüberwindung verbunden. Darüber hinaus kommen lokale Reaktionen an den Einstichstellen wie Rötungen, Juckreiz sowie schmerzhafte Schwellungen und Verhärtungen hinzu, die insbesondere die Langzeitanwendung erschweren. Neben diesen „Unannehmlichkeiten“ der regelmäßigen Anwendung ist vor allem die häufig nur partielle Wirksamkeit der Substanzen ein wichtiger Grund für eine mangelnde Adhärenz bei MS-Patienten.
Nach Erhebung des Deutschen MS-Registers hatten mehr als 30% der Patienten mit schubförmiger MS zum Zeitpunkt der Befragung bereits eine Immuntherapie abgebrochen. Als Gründe wurden in rund 30% der Fälle eine scheinbare Unwirksamkeit der Therapie und in der Hälfte der Fälle Nebenwirkungen angegeben [13]. Die absolute Zahl der Behandlungsabbrüche konnte in den letzten Jahren durch konsequente Aufklärung über den natürlichen Krankheitsverlauf und eine intensivere Betreuung durch geschulte MS-Schwestern zwar deutlich reduziert werden, aber es besteht nach wie vor ein großer Bedarf für wirksamere Therapien mit einer patientenfreundlicheren Anwendung.
Mit der Entwicklung oral applizierbarer MS-Therapeutika wird nun die Forderung nach einer patientenfreundlicheren Darreichungsform erfüllt. Um den klinischen Stellenwert der neuen Wirkstoffe bestimmen zu können, ist jedoch eine umfassende Bewertung ihres Sicherheits- und Verträglichkeitsprofils erforderlich. Dies gilt selbstverständlich nicht nur für die neuen oral applizierbaren MS-Therapeutika, sondern auch für die in der Entwicklung befindlichen neuen parenteral applizierbaren Substanzen, zu denen beispielsweise die monoklonalen Antikörper Alemtuzumab und Rituximab/Ocrelizumab gehören.
Thema des folgenden Artikels sind die oral applizierbaren Wirkstoffe, deren Zulassungsstudien bereits abgeschlossen sind oder die derzeit in Phase-III-Studien geprüft werden (Tab. 1). Die Wirksamkeit und das Sicherheitsprofil dieser Substanzen werden im Folgenden dargestellt.
Tab. 1. Orale MS-Therapeutika, die in Phase-III-Studien untersucht wurden oder werden
|
Wirkstoff |
Angenommene Wirkungsweise |
Zugelassen bei |
Phase-III-Studien mit MS-Patienten: Verlaufsform |
Hersteller |
|
Cladribin |
Immunsuppressivum, Adenosinanalogon |
Haarzell-Leukämie |
RRMS, CIS |
Merck Serono |
|
Fingolimod (FTY720) |
Immunmodulator, Sphingosin-1-Phosphat-Rezeptormodulator |
RRMS |
RRMS, PPMS |
Novartis |
|
Fumarsäureester (BG00012) |
Immunmodulator |
Psoriasis |
RRMS |
Biogen Idec |
|
Laquinimod |
Immunmodulator |
– |
RRMS |
Teva |
|
Teriflunomid |
Immunmodulator, Pyrimidinsynthese-Hemmer |
– |
RRMS, CIS |
Sanofi-Aventis |
RRMS: Schubförmige multiple Sklerose (Relapsing-remitting multiple sclerosis); CIS: klinisch isoliertes Syndrom, erstes demyelinisierendes Ereignis mit Hinweis auf MS; PPMS: primär progrediente MS
Cladribin
Cladribin (2-Chlor-2’-Desoxyadenosin) ist ein immunsuppressiv wirksames Adenosinanalogon. Das Prodrug wird durch Phosphorylierung in das aktive Triphosphat überführt, vorzugsweise in Lymphozyten und Monozyten mit einer hohen Phosphorylierungsrate. Die aktivierte Form wird anstatt des natürlichen Substrats in die DNS eingebaut, wodurch es zu einer Sörung der DNS-Synthese und -Reparatur kommt, was letztlich zum Zelluntergang führt. Klinisch resultiert daraus eine peripher messbare Lymphozytopenie. Die Substanz ist seit 1997 als intravenös zu applizierendes Chemotherapeutikum zur Therapie der Haarzell-Leukämie zugelassen.
Daten aus Phase-II-Studien zur oralen Applikation bei multipler Sklerose liegen nicht vor. In der bislang größten Phase-II-Studie mit Cladribin bei MS wurden 159 Patienten mit primär progredienter (PPMS, 30%) und sekundär progredienter MS (SPMS, 70%) eingeschlossen, denen Cladribin (zwei verschiedene Dosierungen) oder Plazebo in mehreren Zyklen intravenös verabreicht wurde. Nach 12 Monaten waren Anzahl und Größe der Kontrastmittel-aufnehmenden Läsionen in beiden Cladribin-Gruppen durchschnittlich um 90% gegenüber den Ausgangswerten verringert [18].
Cladribin wird derzeit in mehreren Phase-III-Studien bei MS-Patienten mit unterschiedlichen Verlaufsformen untersucht. Die doppelblinde Phase der CLARITY(Cladribine tablets in treating MS orally)-Studie ist mittlerweile abgeschlossen und ergab eine gute Wirksamkeit der Substanz gegenüber Plazebo. Die CLARITY-Studie war eine auf 96 Wochen ausgelegte randomisierte, Plazebo-kontrollierte, multizentrische Doppelblindstudie mit 1326 Patienten mit schubförmiger MS (Relapsing-remitting MS, RRMS). Cladribin wurde in dieser Studie in zwei verschiedenen oralen Dosierungen untersucht: eine Gesamtdosis von 3,5 mg/kg Körpergewicht (KG) und eine Gesamtdosis von 5,25 mg/kg KG. Die Einnahme von Cladribin oder Plazebo erfolgte jeweils in den ersten fünf Tagen eines 28-tägigen Zyklus, für vier Zyklen im ersten Behandlungsjahr und für zwei Zyklen im zweiten Behandlungsjahr. Die Teilnehmer der beiden Verum-Gruppen erhielten in den ersten 48 Wochen entweder vier Zyklen Cladribin (Hochdosis-Gruppe) oder zwei Zyklen Cladribin und zwei Zyklen Plazebo (Niedrigdosis-Gruppe); in den nachfolgenden 48 Wochen erhielten beide Verum-Gruppen zwei Zyklen Cladribin [9].
Wirksamkeit
In beiden Cladribin-Gruppen war die Anzahl der Schübe pro Jahr im Vergleich zu Plazebo signifikant verringert. In der Niedrigdosis-Gruppe war die jährliche Schubrate (primärer Endpunkt) um 58% niedriger als unter Plazebo, in der Hochdosis-Gruppe um 55%; sie betrug unter 3,5 mg/kg KG Cladribin 0,14 (95%-Konfidenzintervall[KI] 0,12–0,17), unter 5,25 mg/kg KG 0,15 (95%-KI 0,12–0,17) und unter Plazebo 0,33 (95%-KI 0,29–0,38), jeweils p<0,001 versus Plazebo (Abb. 1). Der Anteil schubfreier Patienten war unter Cladribin ebenfalls signifikant höher als unter Plazebo (79,7% bzw. 78,9% vs. 60,9% für 3,5 mg/kg KG bzw. 5,25 mg/kg KG; jeweils p<0,001).
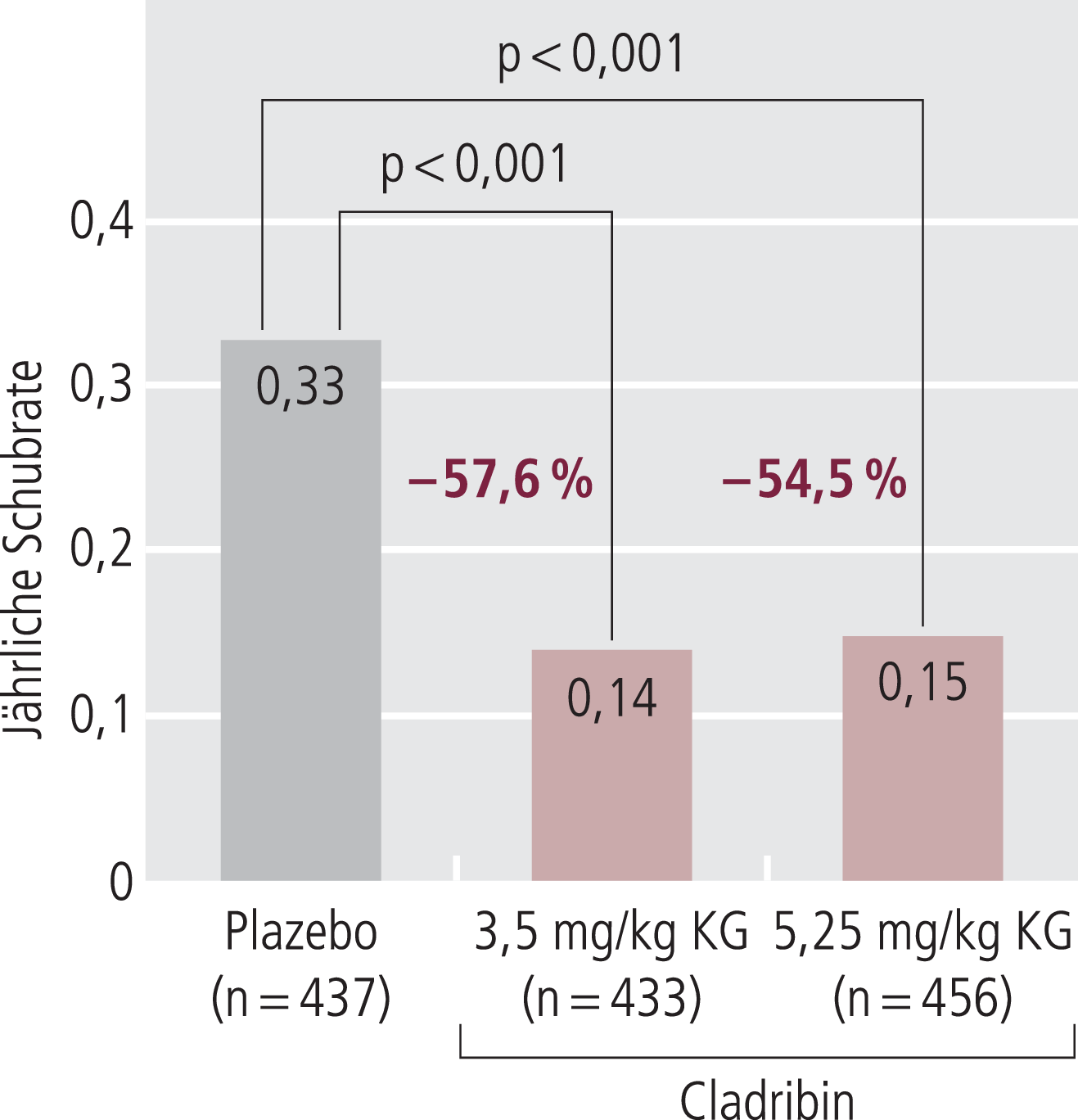
Abb. 1. Wirksamkeit von Cladribin auf die Schubrate (Anzahl der Schübe pro Jahr), verglichen mit Plazebo [9]
Hinsichtlich einer Verlangsamung der Behinderungsprogression zeigte Cladribin ebenfalls eine Überlegenheit gegenüber Plazebo. Während in der Plazebo-Gruppe 20,6% der Patienten eine über drei Monate bestätigte EDSS(Expanded disability status scale)-Progression hatten, war dies in den Cladribin-Gruppen nur bei 14,3% bzw. 15,1% (3,5 mg/kg KG bzw. 5,25 mg/kg KG) der Patienten der Fall; dies entspricht einer Reduktion von 33% bzw. 31% gegenüber Plazebo (p=0,02 bzw. p=0,03).
Wie schon in der vorangegangenen Phase-II-Studie zeigte sich auch in der CLARITY-Studie eine gegenüber Plazebo überlegene Wirksamkeit von Cladribin im Hinblick auf die MRT(Magnetresonanztomographie)-Parameter. So waren unter Cladribin verglichen mit Plazebo Gadolinium-aufnehmende Läsionen im T1-gewichteten MRT um 86% bzw. 88% (3,5 mg/kg KG bzw. 5,25 mg/kg KG) und T2-Läsionen um 73% bzw. 77% verringert. Bei allen MRT-Parametern waren die Unterschiede gegenüber Plazebo statistisch hochsignifikant (p<0,001) [9].
Sicherheit und Verträglichkeit
Erwähnenswert ist, dass die Therapie mit Cladribin von den meisten Patienten gut vertragen wurde. In der CLARITY-Studie brachen aufgrund intolerabler Nebenwirkungen nur 3,5% der Patienten unter der niedrigeren Cladribin-Dosis, 7,9% der Patienten unter der höheren Cladribin-Dosis und 2,1% der Patienten unter Plazebo die Therapie vorzeitig ab. Am häufigsten traten Lymphozytopenien, Kopfschmerzen, Nasopharyngitis und Infektionen der oberen Atemwege auf (Tab. 2).
Tab. 2. Häufigkeit unerwünschter Ereignisse [%] in der CLARITY-Studie (Auswahl) [9]
|
Plazebo |
Cladribin |
||
|
3,5 mg/kg KG (n=430) |
5,25 mg/kg KG (n=454) |
||
|
Alle unerwünschten Ereignisse |
73,3 |
80,7 |
83,9 |
|
Lymphozytopenie |
1,8 |
21,6 |
31,5 |
|
Kopfschmerzen |
17,2 |
24,2 |
20,7 |
|
Nasopharyngitis |
12,9 |
14,4 |
12,8 |
|
Infektionen der oberen Atemwege |
9,7 |
12,6 |
11,5 |
|
Schwere unerwünschte Ereignisse |
6,4 |
8,4 |
9,0 |
Die Inzidenz schwerer unerwünschter Ereignisse betrug unter Cladribin 8,4% bzw. 9,0% (3,5 mg/kg KG bzw. 5,25 mg/kg KG) und unter Plazebo 6,4%. Schwere Infektionen traten bei 2,3% bzw. 2,9% (3,5 mg/kg KG bzw. 5,25 mg/kg KG) der Patienten unter Cladribin und bei 1,6% der Patienten unter Plazebo auf. Darunter waren drei Fälle einer Herpes-Zoster-Infektion (ein Patient unter Cladribin 3,5 mg/kg KG und zwei Patienten unter Cladribin 5,25 mg/kg KG).
Neoplasien traten bei 1,4% der Patienten unter Cladribin 3,5 mg/kg KG und bei 0,9% der Patienten unter Cladribin 5,25 mg/kg KG auf; dabei handelte es sich um fünf benigne uterine Leiomyome, ein Zervixkarzinom im Initialstadium, je ein Melanom, Pankreaskarzinom und Ovarialkarzinom sowie ein myelodysplastisches Syndrom. Bei einer Patientin wurde neun Monate nach Studienende ein Chorionkarzinom diagnostiziert. Eine Systematik war dabei nicht zu erkennen. Unter Plazebo wurden keine Neoplasien beobachtet [9]
Zulassung
Trotz des guten Wirkungsprofils und des akzeptablen Sicherheitsprofils wurde im September 2010 bekannt gegeben, dass das Committee for Medicinal Products for Human Use (CHMP) der europäischen Arzneimittelbehörde (EMA) eine negative Empfehlung für die Zulassung von Cladribin ausgesprochen hat. Gegen diese Bewertung legte der Hersteller Widerspruch ein. Im Januar 2011 wurde aber bekannt gegeben, dass das Komitee bei seiner negativen Entscheidung blieb. Begründet wurde die Entscheidung damit, dass das Nutzen-Risiko-Verhältnis ungünstig sei und dass Bedenken insbesondere hinsichtlich der Langzeitsicherheit von Cladribin in der klinischen Anwendung bestünden. Dementsprechend kann in der nächsten Zeit in Europa nicht mit einer Zulassung dieser Substanz gerechnet werden. Die US-amerikanische Zulassungsbehörde (Food and Drug Administration, FDA) lehnte den Zulassungsantrag im März 2011 in der vorgelegten Form ab, auch sie verlangte weitere Daten zur Sicherheit des Wirkstoffs.
In Russland und Australien wurde die Substanz dagegen zugelassen.
Fingolimod (FTY720)
Fingolimod ist der erste Vertreter einer neuen Wirkstoffklasse: es ist ein Sphingosin-1-Phosphat(S1P)-Rezeptor-Modulator, der neben einer antiinflammatorischen Wirkung möglicherweise auch neuroprotektive oder neuroreparative Wirkungen entfaltet [4].
Fingolimod ist ein Prodrug: nach der oralen Einnahme wird es im Organismus durch die Sphingosin-Kinase phosphoryliert. Die aktive Form Fingolimod-Phosphat ist ein Analogon des natürlich vorkommenden Sphingosin-1-Phosphat (S1P); dieses Sphingolipid spielt eine entscheidende Rolle bei Entzündungsreaktionen und Reparaturmechanismen. Fingolimod-Phosphat bindet als funktionaler Antagonist an S1P-Rezeptoren: das sind transmembranöse G-Protein-gekoppelte Rezeptoren, die beispielsweise auf der Oberfläche von Lymphozyten vorkommen [2, 3]. Eine Bindung von Fingolimod-Phosphat an S1P-Rezeptoren führt zu einer Internalisierung dieser Rezeptoren. In der Folge stehen die Rezeptoren nicht mehr für eine Bindung des natürlichen Liganden zur Verfügung.
Wirkung auf Immunzellen
Eine Bindung von Sphingosin-1-Phosphat an S1P-Rezeptoren auf der Oberfläche von Lymphozyten ist für das Auswandern von Lymphozyten aus den Lymphknoten notwendig. Fingolimod verhindert diese Bindung und somit das Auswandern von CD4+-T-Zellen, CD8+-T-Zellen und B-Zellen, die alle für die Pathophysiologie der Entzündungsvorgänge wichtig sind. Die Zellen gelangen nicht zu entzündlichen Herden im ZNS, sondern werden im peripheren lymphatischen Gewebe zurückgehalten. Funktionell bleiben die Lymphozyten jedoch intakt. Unter der Therapie mit Fingolimod sinkt zwar die Zahl der T-Zellen im Blut um rund 70%, es ist aber zu beachten, dass nur rund 2% der gesamten T-Zell-Population im Blut zirkuliert [4].
Da weder die Aktivierung von T-Zellen noch die Funktion von T- und B-Gedächtniszellen beeinträchtigt sind, wird keine allgemeine Immunsuppression ausgelöst. Damit unterscheidet sich Fingolimod deutlich von den klassischen Immunsuppressiva.
Wirkungen auf andere Zellen
S1P-Rezeptoren konnten in unterschiedlichen Geweben und Organsystemen nachgewiesen werden, so auf vaskulären Endothelzellen, wo sie an der Regulation des vaskulären Tonus beteiligt sind, und auf atrialen Myozyten, wo sie eine Bedeutung für die Regulation der Herzfrequenz und die AV-Überleitung haben. Auch im ZNS werden S1P-Rezeptoren exprimiert, und zwar auf der Oberfläche von Astrozyten und Oligodendrozyten [4, 6, 14].
Letztlich ist die ubiquitäre Expression verschiedener Subtypen der S1P-Rezeptoren wahrscheinlich für einige der beobachteten unerwünschten Wirkungen von Fingolimod verantwortlich – sie beinhaltet auf der anderen Seite aber auch ein Potenzial für weitergehende erwünschte Wirkungen der Substanz. So weisen erste Studienergebnisse auf direkte zentrale Wirkungen von Fingolimod hin, das aufgrund seines lipophilen Charakters ZNS-gängig ist.
Die bisher ausschließlich tierexperimentellen Daten zeigen eine Unterstützung endogener Reparaturmechanismen durch Fingolimod [4]. Dabei scheint eine Reduktion der unerwünschten Astrogliose über eine Herunterregulierung von S1P1- und S1P3-Rezeptoren auf Astrozyten eine der wichtigsten neuroreparativen Wirkungen von Fingolimod zu sein [3, 22]. S1P-Rezeptoren scheinen darüber hinaus an der Regulation der Remyelinisierung und der Proliferation von Oligodendrozyten beteiligt zu sein [24]. Fingolimod unterstützt im Tiermodell der MS, der experimentellen Autoimmun-Enzephalitis (EAE-Modell), die Remyelinisierung und verbessert das Überleben der Oligodendrozyten, möglicherweise auch durch Interaktionen mit verschiedenen Wachstumsfaktoren [4, 20].
Wirksamkeit
Teil des Studienprogramms von Fingolimod sind die Phase-III-Studien TRANSFORMS (Trial assessing injectable interferon vs. Fingolimod oral in RRMS) und FREEDOMS (FTY720 research evaluating effects of daily oral therapy in multiple sclerosis), an denen Patienten mit schubförmiger MS teilnahmen, sowie die Phase-III-Studie INFORMS (FTY720 in patients with primary progressive multiple sclerosis) mit Patienten mit primär progressiv verlaufender MS. Die TRANSFORMS- und die FREEDOMS-Studie sind bereits abgeschlossen, sie ergaben eine signifikant höhere Wirksamkeit von Fingolimod sowohl gegenüber Plazebo als auch gegenüber der Vergleichssubstanz Interferon beta-1a.
In der TRANSFORMS-Studie wurde Fingolimod als erstes neues MS-Medikament im Rahmen einer Zulassungsstudie mit einer Standardtherapie, dem Interferon beta-1a, verglichen. 1292 RRMS-Patienten zwischen 18 und 55 Jahren erhielten im Rahmen der im Double-blind-Double-Dummy-Design durchgeführten Studie entweder Fingolimod (0,5 oder 1,25 mg/Tag) oder Interferon beta-1a (30 µg/Woche i.m., Avonex®). Primärer Endpunkt war die Reduktion der jährlichen Schubrate. Als sekundäre Endpunkte wurden weitere Krankheits- und Therapieaspekte wie der Anteil schubfreier Patienten, die Krankheitsaktivität sowie die Sicherheit und Verträglichkeit gemessen. Die Studiendauer betrug 12 Monate [5].
89% der eingeschlossenen Patienten beendeten die Studie. Die jährliche Schubrate war in beiden Fingolimod-signifikant niedriger als unter Interferon beta-1a: sie betrug in der 1,25-mg-Gruppe 0,20 (95%-KI 0,16–0,26), in der 0,5-mg-Gruppe 0,16 (95%-KI 0,12–0,21) und unter Interferon beta-1a 0,33 (95%-KI 0,26–0,42; jeweils p<0,001, Abb. 2); der Unterschied zwischen den beiden Fingolimod-Dosierungen war nicht signifikant [5].
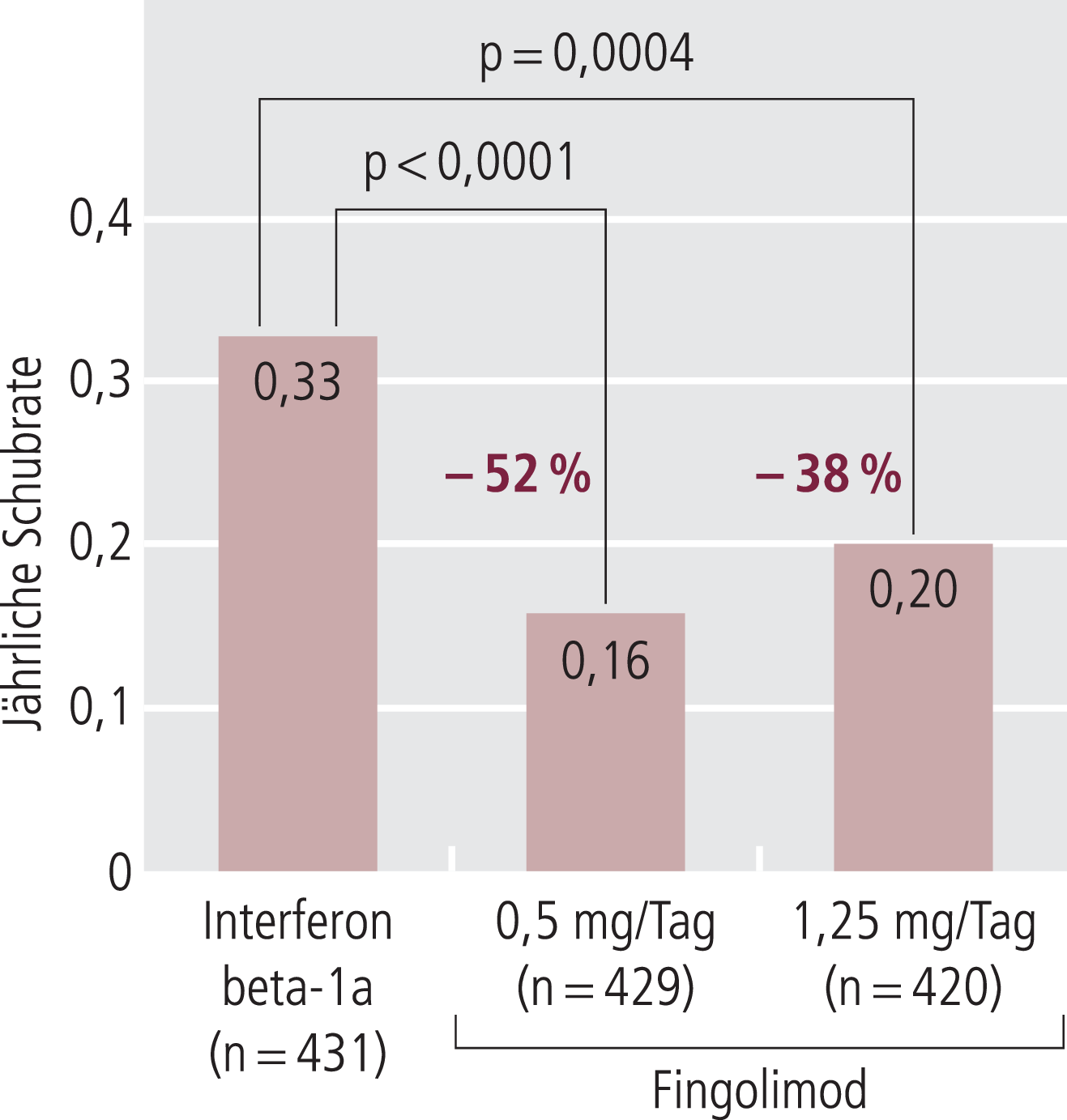
Abb. 2. Wirksamkeit von Fingolimod auf die Schubrate (Anzahl der Schübe pro Jahr), verglichen mit Interferon beta-1a (30 mg/Woche i.m.) [5]
In der FREEDOMS-Studie wurde Fingolimod ebenfalls in zwei Dosierungen (0,5 und 1,25 mg/Tag) bei 1272 Patienten über einen Zeitraum von 24 Monaten mit Plazebo verglichen [12]. Primärer Studienendpunkt war die Reduktion der jährlichen Schubrate. Als einer der sekundären Endpunkte wurde die Reduktion der Behinderungszunahme auf der EDSS-Skala gemessen.
81% der Patienten beendeten die Studie. In allen primären und sekundären Endpunkten war Fingolimod in beiden Dosierungen gegenüber Plazebo signifikant überlegen. Zwischen den beiden Fingolimod-Armen bestanden keine signifikanten Unterschiede in der Wirksamkeit. Die jährliche Schubrate betrug unter Fingolimod 0,5 mg/Tag 0,18 (95%-KI 0,15–0,22), unter Fingolimod 1,25 mg/Tag 0,16 (95%-KI 0,13–0,19) und unter Plazebo 0,40 (95%-KI 0,34–0,47), jeweils p<0,001 vs. Plazebo [12].
Das Risiko einer Behinderungsprogression war unter Fingolimod 0,5 mg/Tag um 30% und unter Fingolimod 1,25 mg/Tag um 32% niedriger als unter Plazebo (Hazard-Ratio 0,70 bzw. 0,68; jeweils p=0,02 vs. Plazebo). Die kumulative Wahrscheinlichkeit einer Behinderungsprogression (bestätigt nach drei Monaten) betrug unter Fingolimod 0,5 mg/Tag 17,7%, unter Fingolimod 1,25 mg/Tag 16,6% und unter Plazebo 24,1%. Während des Beobachtungszeitraums blieben der EDSS- und der MSFC(Multiple sclerosis functional composite)-Z-Score in beiden Fingolimod-Gruppen stabil oder verbesserten sich leicht, während sie sich in der Plazebo-Gruppe etwas verschlechterten (Tab. 3) [12].
Sicherheit und Verträglichkeit
Das Sicherheitsprofil von Fingolimod wurde bereits gut untersucht; die bisher aufgetretenen unerwünschten Ereignisse waren überwiegend dosisabhängig.
In der Phase-II-Studie, in der 281 Patienten mit schubförmiger MS eingeschlossen waren und über sechs Monate mit Fingolimod (0,5 oder 1,25 mg/Tag) oder Plazebo behandelt wurden, waren die häufigsten unerwünschten Ereignisse Infektionen der oberen Atemwege, Kopfschmerzen, Dyspnoe, Diarrhö und Übelkeit. Bei bis zu 12% der Patienten traten im Verlauf der Therapie erhöhte Leberwerte (Alaninaminotransferase = Glutamat-Pyruvat-Transaminase, Anstieg auf mindestens das 3-fache des Normwerts) auf; dies verlief klinisch asymptomatisch und war nach dem Absetzen reversibel [10]. Auch in der TRANSFORMS- und in der FREEDOMS-Studie waren Kopfschmerzen, Nasopharyngitis und Fatigue die unerwünschten Ereignisse, die unter Fingolimod und in den Kontrollgruppen am häufigsten auftraten (>10% der Patienten) [5, 12].
Studienabbrüche aufgrund von unerwünschten Ereignissen waren in der TRANSFORMS-Studie am häufigsten unter der höheren Fingolimod-Dosis (Fingolimod 1,25 mg/Tag: 10%; Fingolimod 0,5 mg/Tag: 5,6%; Interferon beta-1a: 3,7%). In der FREEDOMS-Studie brachen unter der höheren Fingolimod-Dosierung aufgrund unerwünschter Ereignisse 14,2% der Teilnehmer die Studie ab; unter der niedrigeren Fingolimod-Dosierung entsprach die Abbruchrate aufgrund unerwünschter Ereignisse derjenigen unter Plazebo (7,5% bzw. 7,7%) [5, 12].
Die Gesamtinzidenz von Infektionen (alle Schweregrade) war in den Phase-III-Studien unter allen drei Therapien (Fingolimod, Interferon beta-1a und Plazebo) etwa vergleichbar. In der TRANSFORMS-Studie wurden schwerwiegende Herpes-Infektionen sehr selten (0,2–0,7%) beobachtet. Bei zwei Patienten kam es unter Fingolimod unter der 1,25-mg-Dosis unter besonders ungünstigen Begleitumständen (falsche/verzögerte Diagnose bzw. Behandlung) zu einem letalen Verlauf einer Herpes-simplex-Enzephalitis und einer Varizella-Zoster-Enzephalitis [5].
Auch Neoplasien (lokal begrenzte Hautmalignome, Brustkrebs) traten in der TRANSFORMS-Studie sehr selten (bei jeweils weniger als 1% der behandelten Patienten) auf. In der FREEDOMS-Studie wurden maligne Veränderungen der Haut bei drei Patienten unter Fingolimod 1,25 mg/Tag und bei jeweils vier Patienten unter Plazebo bzw. Fingolimod 0,5 mg/Tag festgestellt. Andere maligne Neoplasien fanden sich bei einem Patienten unter Fingolimod 1,25 mg/Tag (Brustkrebs) gegenüber sechs Patienten in der Plazebo-Gruppe (drei Fälle von Brustkrebs, je ein Zervix-, Endometrium und Prostatakarzinom) [5, 12].
Ein Makulaödem entwickelten in der TRANSFORMS-Studie vier Patienten in der 1,25-mg-Gruppe und zwei Patienten in der 0,5-mg-Gruppe, es klang in vier der sechs Fälle binnen drei Monaten nach Absetzen des Präparats ab. In der FREEDOMS-Studie traten bei sieben Patienten Makulaödeme auf (alle unter Fingolimod 1,25 mg/Tag), sie waren in sechs Fällen binnen sechs Monaten nach Absetzen reversibel [5, 12].
Weitere wichtige Nebenwirkungen, die bei mit Fingolimod behandelten Patienten beobachtet wurden, waren eine vorübergehende und meist asymptomatische Verlangsamung der Herzfrequenz nach der ersten Einnahme von Fingolimod sowie eine geringe Erhöhung des Blutdrucks (um 2–3 mmHg). Dieser initiale negativ-chronotrope Effekt muss im Zusammenhang mit der Expression von S1P-Rezeptoren auf atrialen Myozyten gesehen werden [5, 12].
Zulassung
Fingolimod (Gilenya®) erhielt am 17. März 2011 die europäische Zulassung. Im Gegensatz zur amerikanischen Zulassungsbehörde (FDA) entschied sich die europäische Arzneimittelbehörde (EMA) gegen eine Zulassung von Fingolimod als Basistherapie; stattdessen wurde die Substanz als Therapie für hoch aktive MS-Patienten zugelassen, also entweder für Patienten, bei denen mit herkömmlichen Basistherapeutika keine Krankheitskontrolle erreicht wird, oder für Patienten, die von Beginn an einen aggressiven Verlauf aufweisen. Die Definition der hochaktiven MS entspricht hierbei den bereits bekannten Kriterien für eine Behandlung mit Natalizumab (Tysabri®). Das bedeutet, dass die europäische Zulassungsbehörde Fingolimod der Gruppe der Eskalationstherapien zugeordnet hat. Dies ist insofern bemerkenswert, als dass durch diese Bewertung in Europa weiterhin keine oral applizierbaren Arzneimittel für die Basistherapie der MS zur Verfügung stehen werden.
Fumarsäureester
Eine Mischung verschiedener Fumarsäureester (Dimethylfumarat, Ethylhydrogenfumarat) ist seit einigen Jahren als zur Therapie der Psoriasis zugelassen. Diese Hauterkrankung ist wie die MS T-Zell-vermittelt.
Zur Behandlung der multiplen Sklerose wird derzeit Dimethylfumarat (BG00012) eingesetzt. Der genaue Wirkungsmechanismus ist noch nicht vollständig geklärt. Die Substanz entfaltet ihre Wirkung unter anderem durch Interenz mit der NF-kB Signaltranduktionskaskade, wodurch eine verminderte Expression von Genen, die für wesentliche inflammatorisch wirksame Chemokine und Zytokine kodieren, hervorgerufen wird. Weiterhin aktivieren BG00012 und sein Metabolit Monomethylfumarat den Transkriptionsfaktor Nuclear-Factor-E2-related Factor-2 (Nrf2). Dieser Transkriptionsweg spielt für die oxidative Stressreaktion eine wichtige Rolle und ist in der Lage, Oligodendrozyten und Neuronen vor entzündlichen und metabolischen Schäden zu schützen.
Wirksamkeit
Dimethylfumarat (BG00012) befindet sich derzeit bei MS in der klinischen Prüfung. Die verblindete Phase der Phase-III-Studie läuft derzeit noch, so dass bezüglich der Wirksamkeit bisher nur Ergebnisse von Phase-II-Studien herangezogen werden können.
In einer Phase-IIb-Studie erhielten 257 RRMS-Patienten in 43 europäischen MS-Zentren randomisiert über sechs Monate Dimethylfumarat (120, 360 oder 720 mg/Tag) oder Plazebo [11]. Die mittlere Anzahl neuer Gadolinium-aufnehmender Entzündungsherde im MRT war unter der höchsten Dimethylfumarat-Dosis (720 mg/Tag) in den Wochen 12, 16, 20 und 24 gegenüber Plazebo um 69% verringert (1,4 vs. 4,5; p<0,0001). Weiterhin waren in diesem Studienarm neue oder vergrößerte T2-hyperintense Herde und neue T1-hypointense Herde in Woche 24 im Mittel signifikant seltener als unter Plazebo (2,2 vs. 4,2; p=0,0006 bzw. 0,8 vs. 1,7; p=0,014) [11].
In den beiden Phase-III-Zulassungsstudien sollen jeweils mehr als 1000 RRMS-Patienten eingeschlossen werden; BG00012 (480 oder 720 mg/Tag) wird in der einen Studie mit Plazebo verglichen (DEFINE-Studie), in der anderen mit Plazebo und Glatirameracetat (CONFIRM-Studie). Primärer Endpunkt ist jeweils die Reduktion der Schübe (Anteil der Teilnehmer ohne Schub bzw. Verringerung der Schubrate) nach zwei Jahren, sekundäre Endpunkte sind die Verringerung der Behinderungsprogression sowie die Verringerung der Läsionslast im MRT [7, 8].
Die Herstellerfirma BiogenIdec hat am 11. April 2011 in einer Pressemitteilung bekannt gegeben, dass die DEFINE Studie für die höher Dosierung positive Studienergebnisse für alle definierten Endpunkte zeigen konnte.
Sicherheit und Verträglichkeit
Die bisher aus den Phase-II-Studien und vor allem aus der mehrjährigen Anwendung bei Psoriasis bekannt gewordenen Sicherheitsdaten lassen darauf schließen, dass Fumarsäureester eine akzeptable Verträglichkeit und eine gute Langzeitsicherheit aufweisen; sie könnten sich gegebenenfalls auch für zukünftige Kombinationstherapien der MS eignen. Ein Problem bei der Anwendung ist sicherlich eine ausgeprägte Flush-Symptomatik, unter der fast alle Patienten litten, die mit Fumarsäureestern behandelt wurden [23].
Laquinimod
Das Chinolinderivat Laquinimod ist eine Weiterentwicklung des Wirkstoffs Linomid, dessen Erprobung bei der MS wegen Verträglichkeitsproblemen (vermehrtes Auftreten von Myokardinfarkten und Serositiden) nicht weiter verfolgt wird [21].
Laquinimod wirkt immunmodulatorisch, indem es die T-Zellinfiltration vermindert und bei der Entzündungsreaktion das Gleichgewicht der Zytokine in Richtung der durch T-Helferzellen vom Typ 2 (Th2-Zellen) vermittelten Immunantwort lenkt.
Wirksamkeit
Laquinimod wird gegenwärtig bei schubförmiger MS in zwei Phase-III-Studien untersucht: in der einen Studie wird es mit Plazebo verglichen (ALLEGRO-Studie), in der anderen mit Plazebo und dem aktiven Komparator Interferon beta-1a (BRAVO-Studie) [1, 20].
In einer Phase-II-Studie mit 306 Patienten mit RRMS wurde mit der höheren der beiden getesteten Dosierungen (0,1 oder 0,3 mg/Tag) eine signifikante Senkung der Gadolimium-anreichernden Läsionen (primärer Endpunkt) erreicht [17, 23].
Auf der diesjährigen Tagung der American Academy of Neurology wurden die 2-Jahres-Daten der ALLEGRO-Studie präsentiert [26]. Laquinimod in der Dosierung von 0,6 mg einmal pro Tag konnte bezüglich des primären Studienendpunkts eine 23%ige Reduktion der jährlichen Schubrate gegenüber Plazebo zeigen (p=0,0024). Darüber hinaus konnte eine Reduktion der Behinderungsprogression gemessen an der EDSS um 36% gegenüber Plazebo gezeigt werden (p=0,0122). Auch bei den Kernspinparametern konnte eine signifikante Überlegenheit von Laquinimod gegenüber Plazebo gezeigt werden, wobei insbesondere eine deutliche Verminderung der Hirnatrophie (33%, p<0,0001) bemerkenswert war.
Tab. 3. Behinderungsprogression: Mittelwerte (Standardabweichung) [12, 25]
|
Plazebo (n=418) |
Fingolimod |
p-Werte: |
||
|
0,5 mg/Tag (n=425) |
1,25 mg/Tag (n=429) |
|||
|
EDSS-Score* – Ausgangswert (Baseline) – Veränderung über 24 Monate |
2,49 (1,29) +0,13 (0,94) |
2,30 (1,29) 0,00 (0,88) |
2,41 (1,36) –0,03 (0,88) |
0,002 bzw. 0,002 |
|
MSFC-Z-Score† – Ausgangswert (Baseline) – Veränderung über 24 Monate |
–0,04 (0,76) –0,06 (0,57) |
+0,06 (0,60) +0,03 (0,39) |
–0,02 (0,75) +0,01 (0,40) |
0,01 bzw. 0,02 |
* EDSS: Expanded Disability Status Scale; eine Zunahme bedeutet Verschlechterung
† MSFC: Multiple Sclerosis Functional Composite; eine Abnahme bedeutet Verschlechterung
Sicherheit und Verträglichkeit
Die bisher bekannten Sicherheitsdaten sind als relativ günstig zu bewerten. Myokardinfarkte oder Serositiden wie bei der Vorgängersubstanz Linomid traten in den Phase-II-Studien unter Laquinimod nicht auf [23].
Diese günstigen Sicherheitsdaten bestätigten sich auch in der ALLEGRO-Studie. Lediglich eine häufigere Erhöhung der Leberenzyme war gegenüber Plazebo auffällig.
Teriflunomid
Teriflunomid ist der aktive Metabolit von Leflunomid, das bereits für die krankheitsmodifizierende Therapie der rheumatoiden Arthritis zugelassen ist. Die Substanz hemmt die Dihydroorotat-Dehydrogenase und damit die De-novo-Synthese von Pyrimidinen. Dadurch wird die Proliferation und Funktion von aktivierten Lymphozyten gehemmt, während hämatopoetische Stammzellen von der antiproliferativen Wirkung weitgehend unbeeinflusst bleiben.
Wirksamkeit
In einer doppelblinden Phase-II-Studie erhielten 157 Patienten mit schubförmiger MS und 22 Patienten mit sekundär progredienter MS über 36 Wochen Teriflunomid (7 oder 14 mg/Tag) oder Plazebo. Im primären Endpunkt, der kombinierten Zahl der aktiven Läsionen im MRT (neue und persistierende Gd-T1- und T2-Läsionen), war Teriflunomid gegenüber Plazebo signifikant überlegen: nach 36 Wochen waren diese unter Teriflunomid unter beiden Dosierungen um rund 60% seltener als unter Plazebo (7 mg/Tag: p<0,03; 14 mg/Tag: p<0,01). Unter der höheren Teriflunomid-Dosis war die Zunahme der Behinderung verglichen mit Plazebo signifikant geringer. Die Schubrate war zwar unter beiden Dosierungen niedriger als unter Plazebo, aber der Unterschied war nicht signifikant [16, 23].
Aufgrund dieser Ergebnisse wurde 2004 ein Phase-III-Studienprogramm gestartet. Teriflunomid wird nun als Monotherapie sowie als Zusatztherapie zu Interferon beta oder Glatirameracetat untersucht. Kürzlich wurde auf einem internationalen MS-Kongress kommuniziert, dass Teriflunomid die jährliche Schubrate gegenüber Plazebo um rund 30% signifikant verringert und dass die Behinderungsprogression mit der höheren Dosierung signifikant verzögert werden konnte [27].
Sicherheit und Verträglichkeit
Die Verträglichkeit von Teriflunomid wurde insgesamt als gut eingestuft. Nebenwirkungen, die häufiger in der Behandlungsgruppe als in der Plazebo-Gruppe auftraten, waren Durchfall, Übelkeit und eine Erhöhung der Leberenzyme, die in der Regel asymptomatisch waren und keinen Dosiseffekt zeigten. Darüber hinaus zeigten Teriflunomid-behandelte Patienten häufiger einen leichten Haarausfall, der jedoch nur selten zum Therapieabbruch führte. Die Rate der schweren unerwarteten Ereignisse betrug 12,8% in der Plazebo-Gruppe und 14,1% bzw. 15,9% in der 7-mg- bzw. 14-mg-Teriflunomid-Gruppe. Opportunistische Infektionen traten unter Teriflunomid nicht auf. Darüber hinaus zeigte sich auch kein Unterschied in der Häufigkeit schwerer Infektionen (2,2% Plazebo vs. 1,6% 7-mg- und 2,5% 14-mg-Gruppe). Eine leichte Verminderung der neutrophilen Granulozyten war in den ersten 3 Monaten zu beobachten, die dann auf einem Plateau verblieb. Vier Krebserkrankungen traten in der Studie auf, drei davon in der Plazebo-Gruppe.
Zusammenfassung/Ausblick
Nach den Bewertungen der europäischen Arzneimittelbehörde kann davon ausgegangen werden, dass 2011 nach der Zulassung von Fingolimod keine weiteren Substanzen für die Behandlung der multiplen Sklerose zugelassen werden.
Fingolimod wird allerdings keine Alternative zu den parenteral zu verabreichenden Basistherapien sein, wie es allgemein erwartet wurde – es wurde als Eskalationstherapie für hochaktive MS-Patienten zugelassen. Trotzdem bedeutet dies eine Bereicherung der Therapieoptionen bei schubförmiger MS, und für MS-Patienten zeichnet sich dementsprechend ein greifbarer Fortschritt ab. Cladribin wird trotz positiver Studienergebnisse vorerst nicht in Europa zur Behandlung der MS zur Verfügung stehen. Dimethylfumarat, Laquinimod und Teriflunomid befinden sich derzeit noch mitten in der klinischen Prüfung und die Ergebnisse können mit großem Interesse verfolgt werden.
Die unterschiedlichen Wirkungsmechanismen der Substanzen werden definitiv das Spektrum der MS-Therapeutika erweitern. Hieraus werden sich unter Umständen auch neue Impulse für sinnvolle Kombinationstherapien geben, die derzeit noch weitgehend fehlen.
Selbstverständlich müssen alle neuen Substanzen ihre Wirksamkeit und vor allem ihre Sicherheit in der praktischen Anwendung beweisen. Ein verantwortungsvoller Umgang mit diesen neuen Therapeutika, beispielsweise unter Ausnutzung von Risk-Management-Programmen, ist unentbehrlich.
Literatur
1. BRAVO Study: Laquinimod double blind placebo controlled study in RRMS patients with a rater blinded reference arm of Interferon β-1a (Avonex®). http://clinicaltrials.gov/ct2/show/NCT00605215 (Zugriff am 4.4.2011)
2. Brinkmann V, Lynch KR. FTY720: targeting G-protein-coupled receptors for sphingosine 1-phosphate in transplantation and autoimmunity. Curr Opin Immunol 2002;14:569–75.
3. Brinkmann V. FTY720 (fingolimod) in multiple sclerosis: therapeutic effects in the immune and the central nervous system. Br J Pharmacology 2009;158:1173–82.
4. Chun J, Hartung HP. Mechanism of action of oral fingolimod (FTY720) in multiple sclerosis. Clin Neuropharmacol 2010;33:91–101.
5. Cohen JA, Barkhof F, Comi G, Hartung HP, et al. Oral fingolimod or intramuscular interferon for relapsing multiple sclerosis. N Engl J Med 2010;362:402–15.
6. Dev KK, Mullershausen F, Mattes H, Kuhn RR, et al. Brain sphingosine-1-phosphate receptors: implication for FTY720 in the treatment of multiple sclerosis. Pharmacol Ther 2008;117:77–93.
7. Efficacy and safety of oral BG00012 in relapsing-remitting multiple sclerosis (DEFINE). http://clinicaltrials.gov/ct2/show/NCT00420212 (Zugriff am 4.4.2011)
8. Efficacy and safety study of oral BG00012 with active reference in relapsing-remitting multiple sclerosis (CONFIRM). www.clinicaltrials.gov/ct2/show/NCT00451451
9. Giovannoni G, Comi G, Cook S, Rammohan K, et al. A placebo-controlled trial of oral cladribine for relapsing multiple sclerosis. N Engl J Med 2010;362:416–26.
10. Kappos L, Antel J, Comi G, Montalban X, et al. Oral fingolimod (FTY720) for relapsing multiple sclerosis. N Engl J Med 2006;355:1088–91.
11. Kappos L, Gold R, Miller DH, Macmanus DG, et al. Efficacy and safety of oral fumarate in patients with relapsing-remitting multiple sclerosis: a multicentre, randomised, double-blind, placebo-controlled phase IIb study. Lancet 2008;372:1463–72.
12. Kappos L, Radue EW, O’Connor P, Polman C, et al. A placebo-controlled trial of oral fingolimod in relapsing multiple sclerosis. N Engl J Med 2010;362:387–401.
13. Khil L, Flachenecker P, Zettl UK, Elias W, et al. The German MS Registry: immunotherapy and drug discontinuation. Posterpräsentation auf der 25. Jahresversammlung des European Committee For Treatment And Research In Multiple Sclerosis (ECTRIMS), Düsseldorf, 9.-12. September 2009.
14. Klatt J, Hartung HP, Hohlfeld R. FTY720 (Fingolimod) als neue Therapiemöglichkeit der multiplen Sklerose. Der Nervenarzt 2007;78:1200–8.
15. Mehling M, Kappos L. Therapie der multiplen Sklerose. Teil 2: Ausblick auf mögliche zukünftige Therapieansätze. Schweiz Med Forum 2009;9:669–72.
16. O’Connor PW, Li D, Freedman MS, Bar-Or A, et al. A phase II study of the safety and efficacy of teriflunomide in multiple sclerosis with relapses. Neurology 2006;66: 894–900.
17. Polman C, Barkhof F, Sandberg-Wollheim M, Linde A, et al. Treatment with laquinimod reduces development of active MRI lesions in relapsing MS. Neurology 2005;64: 987–91.
18. Rice GP, Filippi M, Comi G. Cladribine and progressive MS: clinical and MRI outcomes of a multicenter controlled trial. Cladribine MRI Study Group. Neurology 2000;54:1145–55.
19. Safety and efficacy of orally administered laquinimod for treatment of relapsing remitting multiple sclerosis (RRMS) (ALLEGRO). http://clinicaltrials.gov/ct2/show/NCT00509145 (Zugriff am 4.4.2011)
20. Saini HS, Coelho RP, Goparaju SK, Jolly PS, et al. Novel role of sphingosine kinase 1 as a mediator of neurotrophin action in oligodendrocyte progenitors. J Neurochem 2005;95:1298–310.
21. Tan IL, Lycklama à Nijeholt GJ, Polman CH, Adèr HJ, et al. Linomide in the treatment of multiple sclerosis: MRI results from prematurely terminated phase-III trials. Mult Scler 2000;6:99–104.
22. Wu YP, Mizugishi K, Bektas M, Sandhoff R, et al. Sphingosine kinase 1/S1P receptor signaling axis controls glial proliferation in mice with Sandhoff disease. Hum Mol Genet 2008;17:2257–64.
23. Yaldizli Ö, Tettenborn B, Putzki N. Innovative orale Therapien der schubförmigen multiplen Sklerose. Neue Substanzen im Spannungsfeld von Wirksamkeit, Verträglichkeit und Sicherheit. Neurologie 2009;1:1–6.
24. Yu N, Lariosa-Willingham KD, Lin FF, Webb M, et al. Characterization of lysophosphatidic acid and sphingosine-1-phosphate-mediated signal transduction in rat cortical oligodendocytes. Glia 2004;45:17–27.
25. European Medicines Agency. Assessment report Gilenya, Procedure No. EMEA/H/C/2202 unter www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/002202/WC500104529.pdf (Zugriff am 6.4.2011).
26. Comi G. Oral laquinimod reduced relapse rate and delayed progression of disability in Allegro, a placebo-controlled phase III trial for relapsing-remitting multiple sclerosis. American Academy of Neurology 63rd Annual Meeting, Honolulu, Hawaii, 9. bis 16. April 2011.
27. 26th Congress of the European Committee for Treatment and Research in Multiple Sclerosis (ECTRIMS): Abstracts 79, P-982, P-431, and P-833. Presented October 14–15, 2010.
Priv.-Doz. Dr. Mathias Mäurer, Klinik für Neurologie, Caritas Krankenhaus Bad Mergentheim GmbH, Uhlandstraße 7, 97980 Bad Mergentheim, E-Mail: Mathias.Maeurer@ckbm.de
Efficacy and safety of oral MS-treatments
Since many years multiple sclerosis can be treated effectively using immunomodulatory medications. Yet, growing knowledge on MS pathogenesis, limited efficacy and apparent problems with adherence to current first-line therapies have led to the development of new oral substances. It can be expected from clinical data, that MS patients will not only profit from a more patient friendly application but also from a significant improvement of immunomodulatory efficacy. For the promising new sphingosine 1-phosphate receptor modulator fingolimod (FTY720) there are results from two phase III trials available. These results have led to a positive opinion of the EMA. Also a phase III study on the efficacy of the immunosuppressant cladribine, which shows positive results on relapse rates and disease progression, has been published. However the EMA did not see a favorable risk-benefit ration and refused the license of the substance. The following article summarizes efficacy and safety of those two new oral treatments and illustrates further developments on oral MS therapies.
Key words: Multiple sclerosis, oral, cladribine, fingolimod, FTY720
Psychopharmakotherapie 2011; 18(03)
