Susanne Stübner, Renate Grohmann, Eckart Rüther und Hans-Jürgen Möller, München
Die Frage nach einer Beeinflussung von medizinischem Fachpersonal durch die pharmazeutische Industrie und deren Werbekampagnen gibt immer wieder Anlass zu Fragen und zur Besorgnis.
Auf der einen Seite wurden Werbe-Effekte nachgewiesen (z.B. [5]). Auf der anderen Seite ist davon auszugehen, dass viele andere Faktoren in die Verordnungsprozesse einfließen: in der Klinik entsteht häufig der Eindruck, dass immer wieder Entscheidungen getroffen werden, die allgemeinen Strömungen durchaus entgegengesetzt sind.
Insofern stellte sich die Frage, ob sich eine Veränderung der Anwendungspraxis in Abhängigkeit von der Bewerbung eines Präparats erkennen lässt oder ob sich die tatsächliche Verordnung unabhängig davon entwickelt.
Unter der Hypothese, dass nach Ablauf des Patentschutzes eines Markenpräparats die offensive Werbekampagne des entsprechenden Pharmakonzerns erheblich nachlässt, könnte die Betrachtung der Anwendungshäufigkeiten dieses Wirkstoffs im Verlauf dieses Zeitraums indirekt Aufschluss über die Empfänglichkeit gegenüber der Werbung geben.
Vor diesem Hintergrund erfolgte eine Auswertung der im Rahmen des Projekts Arzneimittelsicherheit in der Psychiatrie (AMSP) ermittelten Anwendungshäufigkeiten.
Methoden
Das Projekt Arzneimittelsicherheit in der Psychiatrie (AMSP) ist ein Arzneimittelsicherheitsprogramm zur kontinuierlichen Erfassung von schweren und ungewöhnlichen unerwünschten Arzneimittelwirkungen bei stationären psychiatrischen Patienten unter den naturalistischen Bedingungen des klinischen Behandlungsalltags (Übersicht zu Projekt und Geschichte bei [2]). Das Projekt AMSP wurde 1993 an der Psychiatrischen Universitätsklinik in München gegründet und über weitere Kliniken in Deutschland, der Schweiz, Österreich, Belgien und Ungarn ausgedehnt. Das AMSP-Projekt ist allen Kliniken offen, die daran teilnehmen möchten. Derzeit nehmen am AMSP-Projekt 54 Institutionen teil, 33 davon in Deutschland (8 Universitätskliniken und 25 nichtuniversitäre Institutionen, darunter 11 Landes-/Bezirkskrankenhäuser und 14 psychiatrische Abteilungen von Allgemeinkrankenhäusern). Für die vorliegende Auswertung erfolgte eine Beschränkung auf die deutschen Institutionen.
Insgesamt werden durch das AMSP-System etwa 29000 Patienten pro Jahr überwacht, in Deutschland etwa 18000.
Die Daten über die Arzneimittelanwendungen in den teilnehmenden Kliniken und Institutionen basieren auf zwei Stichtags-Erhebungen pro Jahr. Alle Medikamente, die an diesen Tagen Anwendung finden, werden neben einigen Grundinformationen (Alter, Geschlecht und Diagnose) für jeden Patienten aufgelistet. Für psychiatrische Medikamente werden auch die Tagesdosierungen erfasst. Die Dokumentationen erfolgen anonymisiert. Eine detaillierte Darlegung der Methoden des AMSP-Projekts finden sich auch bei Engel et al. [1] und Grohmann et al. [2].
Die Daten der Stichtagserhebungen aller am AMSP-Projekt beteiligten Kliniken in Deutschland wurden ausgewertet für die Anwendungshäufigkeiten einzelner Präparate und deren Entwicklungen von 1993 bis 2008 (Darstellungen ab 1994).
Es wurden die Anwendungen der Wirkstoffe Amisulprid, Citalopram, Escitalopram, Mirtazapin, Risperidon und dessen Depotpräparat betrachtet. Für Amisulprid, Citalopram, Mirtazapin und Risperidon war der Patentschutz der Originalpräparate im Untersuchungszeitraum abgelaufen, und es waren Generika auf den Markt gekommen. Die prozentualen Anwendungshäufigkeiten wurden in Bezug auf alle Patienten, die mit der jeweiligen Substanzklasse behandelt wurden (Antidepressiva oder Antipsychotika), ermittelt.
Die Patente betreffen verschiedene Bereiche, darunter den eigentlichen Wirkstoff, also das Molekül, aber auch getrennt davon die Unterlagen der Zulassungsstudien. Die Zeitpunkte der Patentabläufe in Deutschland – in dem Sinne, dass ab diesem Zeitpunkt die Zulassung eines Generikums theoretisch erstmals möglich gewesen wäre – wurden bei den Originalherstellern Lundbeck, Sanofi-Aventis, Essex Pharma und Janssen-Cilag erfragt.
Ergebnisse
Insgesamt wurden im AMSP-Projekt bei zwei Stichtagserhebungen pro Jahr zwischen 1993 und 2008 an insgesamt 85 Kliniken in Deutschland die Medikationen von 88047 Patienten erfasst, darunter von 57696 Patienten mit Antipsychotika-Medikation und 41447 Patienten mit Antidepressiva-Medikation.
Die Abbildungen 1a–d zeigen die Entwicklungen der Anwendungspraxis von Amisulprid, Risperidon, Citalopram, Escitalopram und Mirtazapin.
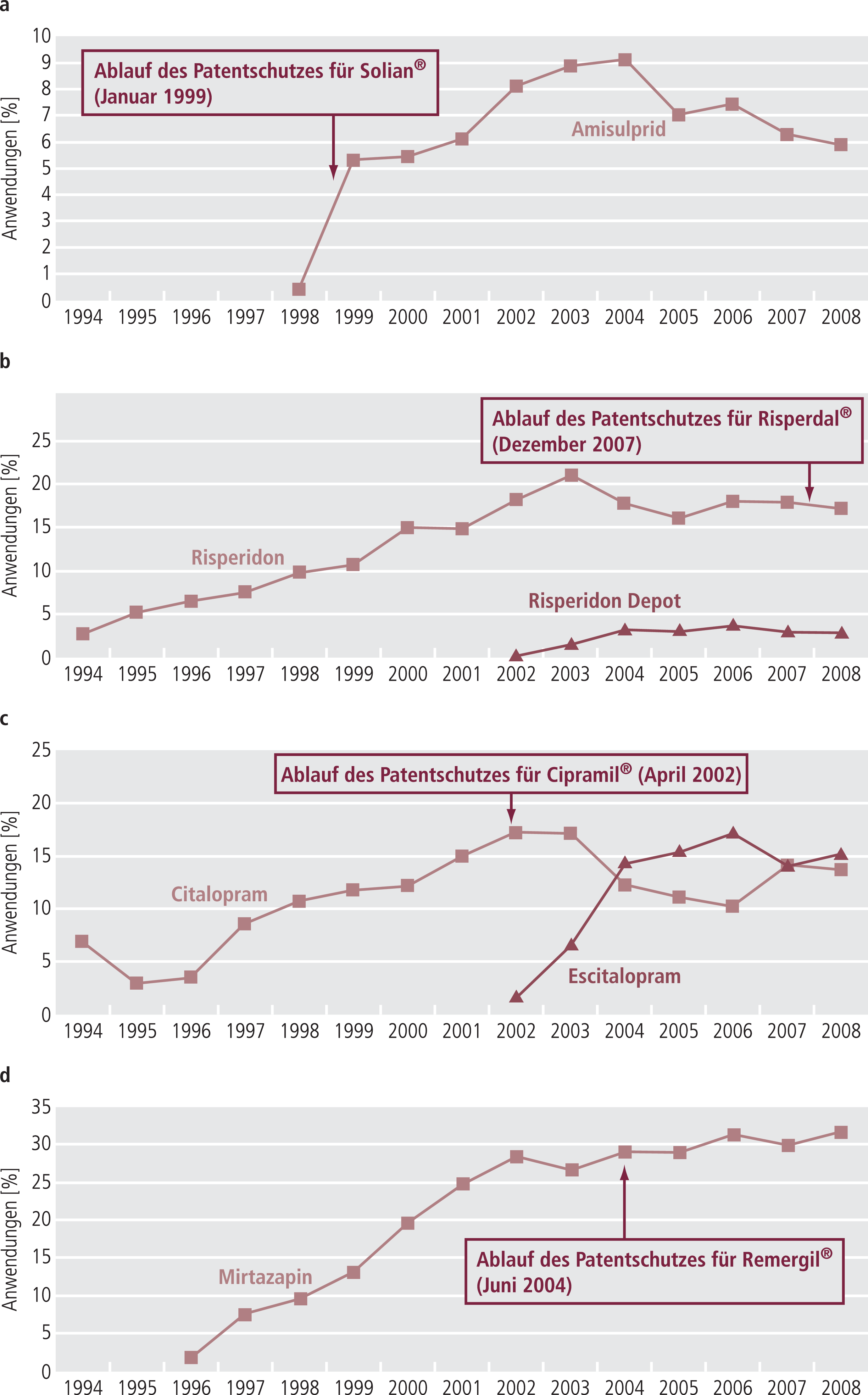
Abb. 1a–d. Anwendungen im Rahmen des AMSP-Projekts in Deutschland von 1994 bis 2008 [%]. Die prozentualen Anwendungen von Amisulprid, Risperidon und Risperidon-Depot beziehen sich auf alle Patienten, die mit Antipsychotika behandelt wurden (n=57969; AMSP Deutschland). Die prozentualen Anwendungen von Citalopram, Escitalopram und Mirtazapin beziehen sich auf alle Patienten, die mit Antidepressiva behandelt wurden (n=41447; AMSP Deutschland).
Amisulprid
Für Amisulprid (Patentablauf Solian® Januar 1999) zeigte sich von 1998 (in den vorangegangenen Jahren wurde es in keiner der am AMSP-Projekt teilnehmenden Kliniken angewendet) auf 1999 ein sprunghafter Anstieg der Anwendung von 0,37% auf 5,32% (bezogen auf alle mit Antipsychotika behandelten Patienten), dann eine langsamere Zunahme auf maximal 9,11% im Jahr 2004 und danach eine abnehmende Tendenz, wobei allerdings zuletzt noch eine höhere Anwendung vorlag als zum Zeitpunkt des Patentablaufs (Abb. 1a).
Risperidon
Risperidon (Patentablauf Risperdal® Dezember 2007) zeigte einen relativ kontinuierlichen Anstieg von 2,74% im Jahr 1994 auf maximal 20,93% im Jahr 2003 und sodann einen leichten Abfall bis auf minimal 16% im Jahr 2005, dann über den Patentablauf hinweg auf 17,22% im Jahr 2008 (bezogen auf alle Patienten je Jahr unter Antipsychotika). Der Rückgang der Risperidon-Gaben erfolgte gleichzeitig mit der Einführung eines Depotpräparats (Risperdal® Consta®). Dieses zeigte Anwendungen von etwa 3% konstant seit 2004 (Abb. 1b).
Citalopram
Für Citalopram (Patentablauf Cipramil® April 2002) fand sich ab 1995, nach einem leichten Abfall nach dem ersten Jahr auf 2,98%, ein kontinuierlicher Anstieg der Anwendungen auf bis zu 17,16% im Jahr 2002 (Patentablauf), die 2003 konstant blieben und sodann bis 2006 bis auf 10,19% fielen, jedoch dann erneut 2007 bis auf 14,16% stiegen (Abb. 1c).
Escitalopram
Etwa zeitgleich mit dem Patentablauf von Cipramil® wurde der Wirkstoff Escitalopram (Cipralex®) zugelassen, dessen Anwendung von 1,61% im Jahr 2002 sprunghaft auf 14,28% im Jahr 2004 stieg und dann bis 2006 langsamer auf 17,09% stieg. Es folgte dann ein mäßiger Rückgang auf einen Anteil von etwa 15% ab 2007 (Abb. 1c).
Mirtazapin
Die Anwendungen von Mirtazapin (Patentablauf Remergil® Juni 2004) stiegen kontinuierlich von 0,88% im Jahr 1996 auf 28,4% im Jahr 2002. 2003 erfolgte ein kleiner Einbruch auf eine Anwendung von 26,73%; diese stieg dann 2004 auf 29,04%. Danach erfolgte eine langsamere und schwankendere Steigerung bis auf 31,87% im Jahr 2008 (Abb. 1d).
Diskussion
Die im Rahmen des AMSP-Projekts erfassten Anwendungsdaten bei psychiatrischen Patienten in stationärer Behandlung wurden ausgewertet zur Frage etwaiger Veränderungen der relativen Verordnungshäufigkeit von Psychopharmaka nach Verlust des Patentschutzes des entsprechenden Präparats in Deutschland. Spätestens mit Auslaufen des Patentschutzes kann von einem Rückgang der Werbekampagnen der Originalhersteller ausgegangen werden.
Bei den exemplarisch betrachteten Wirkstoffen zeigten sich sehr unterschiedliche Verläufe. Dies lässt erkennen, dass die Anwendungen zumindest nicht ausschließlich werbungsabhängig erfolgen, sondern offenbar komplexere Prozesse zugrunde liegen.
Im Einzelnen zeigte sich für das Antipsychotikum Amisulprid nach dem Patentablauf für Solian® ein geringerer Anstieg und später ein Abfall der Anwendungen. Hier könnte ein Zusammenhang mit der Einführung von Konkurrenzpräparaten vermutet werden (z.B. Aripiprazol oder Quetiapin).
Auch das Antipsychotikum Risperidon (Risperdal®) zeigte etwa zur selben Zeit, das heißt in diesem Fall noch vor Ablauf des Patentschutzes, einen leichten Abfall der Anwendungen. Allerdings ist die Anwendungsentwicklung dieses Wirkstoffs wegen der Einführung eines Depotpräparats noch etwas komplizierter; wegen des erst Ende 2007 erfolgten Patentablaufs war zudem nur ein kurzer Zeitraum zu überblicken.
Der Verlauf der Anwendungen des Antidepressivums Citalopram wurde in Zusammenhang mit dem direkten Folge- und Konkurrenzpräparat Escitalopram betrachtet. Es zeigte sich ein Abfall der Anwendungen von Citalopram nach dem Patentablauf bei gleichzeitig erfolgter Zulassung von Escitalopram (dessen Patentschutz bis dato fortbesteht): In kurzer Zeit kam es zu einem Wechsel der Rangfolgen der Anwendungshäufigkeiten, die sich aber sodann erneut ablösten, um sich zuletzt bei etwa gleichen Anteilen einzupendeln. Diese Entwicklung legte die Vermutung nahe, dass es sich um klinisch unterschiedlich wirkende und eingesetzte Wirkstoffe handeln könnte, die deshalb in der klinischen Praxis beide ihren Stellenwert behaupten.
Das Antidepressivum Mirtazapin wurde nach Auslaufen des Patentschutzes für Remergil® sogar noch weiter zunehmend verordnet. Ein Grund hierfür könnte in dem sedierenden Wirkungsprofil vermutet werden, das in Deutschland besonders beliebt ist. Mirtazapin ist diesbezüglich ohne nennenswerte Konkurrenz unter den modernen Antidepressiva und kann als Folgepräparat der sedierenden trizyklischen Antidepressiva angesehen und eingesetzt werden.
Einflüsse von Werbungsaktivitäten können zwar anhand der Anwendungsverläufe vermutet werden, jedoch diese nicht ausschließlich damit erklärt und darauf zurückgeführt werden. Insgesamt ergeben die Betrachtungen der realen Anwendungen den Eindruck, dass andere Faktoren, zum Beispiel klinische Erfordernisse, wesentlich mitbestimmend sind, und dass es einige Zeit dauert, bis sich der klinische Stellenwert eines Präparats herausbildet.
Einige wesentliche Begrenzungen in der Aussagekraft der vorliegenden Auswertungen sind bei der Interpretation zu berücksichtigen:
- Patentierungen unterliegen komplexen Prozessen. Es sind nicht alle Faktoren, die den Zeitpunkt der Möglichkeit der Einführung von Generika beeinflussen, bekannt und datierbar.
- Auch Firmen, die Generika herstellen, betreiben Werbung. Dies findet zwar in der Regel nicht in dem Maße statt wie bei Einführung eines neuen Originalpräparats, jedoch kommen mitunter zahlreiche Folgepräparate auf den Markt, so dass hier auch von einer Summation kleinerer Werbeaktivitäten ausgegangen werden muss.
- Das Arzneimittelmarkt-System ist sehr komplex und aus naturwissenschaftlich-medizinischer Sicht nicht zu erklären. Es ist anzunehmen, dass außer der Werbung noch viele andere marktwirtschaftliche Größen – wie die Einführung von Konkurrenzpräparaten (diesbezüglich ergaben sich Hinweise aus den vorliegenden Daten), internationale Marktregelungen oder preisliche Veränderungen – ebenfalls Einfluss auf die Anwendungspraxis haben.
- Verschreibungsgewohnheiten dürften zudem auch von generellen zeitbedingten Strömungen und Gewohnheiten abhängig sein.
- Nicht zu vernachlässigen erscheint der Einfluss der Medien-Berichterstattung auf medizinisches Personal, aber auch auf die Patienten selbst und deren Bedürfnislage, was wiederum auf die Verschreiber einwirkt. In letzter Zeit wurden erste Untersuchungen zu dieser Thematik durchgeführt (z.B. [3]).
- Die Verzahnung von stationärer und ambulanter Behandlung ist sehr komplex. Die in Kliniken begonnenen Anwendungen werden oft anschließend im ambulanten Bereich weitergeführt. Dort spielen für Folgeverschreibungen auch die Vorgaben der Krankenkassen (Budgetierung) und der jeweiligen kassenärztlichen Verbände eine wichtige Rolle; es ist davon auszugehen, dass die Befürchtung von Regressen das Verordnungsverhalten der niedergelassenen Ärzte in einem besonderen Maße beeinflusst, zumal auch noch Zielvorgaben für die zu verschreibenden Anteile an sogenannten Leitpräparaten erfolgen. Die Verschreibungsgewohnheiten der kooperierenden niedergelassenen Ärzte dürften ihrerseits wiederum rückkoppelnde Effekte auf die Anwendungen in den Kliniken haben.
- Sowohl in Kliniken als auch im niedergelassenen Bereich gibt es unterschiedliche Handhabungen im Umgang mit den Pharmafirmen und ihren Vertretern; das generelle Empfangsverhalten gegenüber Pharmareferenten variiert zwischen den einzelnen Kliniken und niedergelassenen Kollegen erheblich. An niedergelassene Ärzte werden Muster ausgegeben; von größerer Bedeutung dürften aber die von Kliniken ausgehandelten Rabatte für Medikamente sein. Hinzu kommt, dass gerade den Universitätskliniken von den Firmen neu zugelassene Präparate teilweise unter dem Marktpreis zur Verfügung gestellt werden.
- Sowohl für die Annahme durch die behandelten Patienten als auch für die Anwendungsgewohnheiten der behandelnden Ärzte spielen Wirksamkeit, unerwünschte Wirkungen und Beeinflussung der Lebensqualität eine wesentliche Rolle. Aussagen zu diesen Faktoren können den vorliegenden Ergebnissen nicht entnommen werden und erfordern weiterführende Untersuchungsansätze.
Die vorliegenden Untersuchungen beruhen auf sehr großen Datensätzen, die aus überregionalen und heterogenen Institutionen gewonnen wurden. Deshalb kann von einer hohen Repräsentativität für den stationären Bereich in Deutschland ausgegangen werden.
Schlussfolgerungen und Ausblick
Die Unterschiede der Anwendungsverläufe legen die Interpretation nahe, dass die Verschreibungsgewohnheiten bei weitem nicht ausschließlich durch die Werbung beeinflusst werden, sondern den Entscheidungsprozessen komplexere Mechanismen zugrunde liegen, die weiterführend untersucht werden sollten.
Die Betrachtung tatsächlicher Behandlungsgewohnheiten in ihrer Gesamtheit lässt den Eindruck einer „experienced based medicine“ entstehen (siehe auch [4]), also einer Medizin, in der erworbene Erfahrungswerte eine wesentliche Berücksichtigung finden und Entscheidungsgrundlagen bilden.
Literatur
1. Engel R, Grohmann R, Rüther E, Hippius H. Research methods in drug surveillance. Pharmacopsychiatry 2004;37(Suppl 1):S12–5.
2. Grohmann R, Engel R, Rüther E, Hippius H. The AMSP drug safety program: Methods and global results. Pharmacopsychiatry 2004;37(Suppl 1):S4–11.
3. Lado E, Vacariza M, Fernandez-Gonzalez C, Gestal-Otero JJ, et al. Influence exerted on drug be escribing by patients’ attitudes and expectations and by doctors’ perception of such expectations: a cohort and nested case-control study. J Eval Clin Practice 2008;14:453–9.
4. Möller HJ. Is evidence sufficient for evidence-based medicine? Eur Arch Psychiatry Clin Neurosci 2009;259(Suppl 2):S167–72.
5. Wazana A. Physicians and the pharmaceutical industry: Is a gift ever just a gift? JAMA 2000;283:373–80.
Priv.-Doz. Dr. Susanne Stübner, Dr. Renate Grohmann, Prof. Dr. Eckart Rüther, Prof. Dr. Hans-Jürgen Möller, Klinik und Poliklinik für Psychiatrie und Psychotherapie der Ludwig-Maximilians-Universität München, Nussbaumstraße 7, 80336 München, E-Mail: Susanne.Stuebner@med.uni-muenchen.de
Does patent expiry influence administration rates?
Objective: Against the background of a debate of an influence of pharmaceutical industry on therapeutic staff the shifts of administration rates should be investigated according to promotion activities. The date of patent expiry was supposed to be connected with a ceasing of offensive advertising campaigns.
Methods: Administration rates were assessed within the multicenter drug surveillance program “Arzneimittelsicherheit in der Psychiatrie (AMSP)” and analyzed concerning several substances, of which the patent protection ended in the time of observation (amisulprid, citalopram, mirtazapine, risperidone), as well as concerning escitalopram and the depot preparation of risperidone.
Results: Between 1993 and 2008 the drug use data of 88,047 psychiatric inpatients at 85 hospitals in Germany were assessed. The administration rates of the single substances showed different courses. The date of termination of patent protection was usually recognizable, but did not define the processes completely; e.g. mirtazapine administrations increased continually.
Discussion: The courses of administrations indicate complex underlying processes. Methodological limitations have to be taken into account.
Key words: Drug surveillance program “Arzneimittelsicherheit in der Psychiatrie (AMSP)”, antipsychotics, antidepressants, promotion, patent protection
Psychopharmakotherapie 2011; 18(03)
