Gerd Laux, Wasserburg a. Inn/München, und die VIVALDI-Studiengruppe*
Mit einer Lebenszeitprävalenz von etwa 12 bis 17% gehören Depressionen zu den häufigsten psychischen Erkrankungen [1]. In Europa verursachen sie Gesundheitskosten in Höhe von 118 Milliarden Euro pro Jahr [26]. Depressionen sind häufig mit einer Desynchronisation zirkadianer Rhythmen verbunden: Patienten mit Depressionen weisen für unterschiedlichste physiologische Parameter wie Körperkerntemperatur, Cortisolfreisetzung, Melatoninsekretion und den Schlaf-Wach-Rhythmus abgeflachte, desynchronisierte oder phasenverschobene zirkadiane Rhythmen auf [27, 29]. Auch die bei Depressiven häufigen Schlaf- und Vigilanzstörungen sowie tageszeitlichen Schwankungen von Affekt und Antrieb deuten auf eine zirkadiane Rhythmusstörung hin: Drei Viertel dieser Patienten weisen Symptome einer Insomnie auf; Tagesmüdigkeit und Schläfrigkeit am Tage treten bei 40% der jüngeren und 10% der älteren Patienten auf [22]. Bislang verfügbare Antidepressiva zeigen zum Teil keine positiven Wirkungen auf Schlafstörungen oder können diese sogar noch verschlechtern [4].
Die verfügbaren antidepressiven Standardtherapien verstärken die Funktion der monoaminergen Systeme im Gehirn. Trizyklische Antidepressiva (TZA), selektive Serotonin-Wiederaufnahmehemmer (SSRI) und selektive Serotonin-Noradrenalin-Wiederaufnahmehemmer (SSNRI) sind zum Teil mit praktisch relevanten Nachteilen verbunden wie fehlender Wirkung auf Schlafstörungen, Absetzeffekten und Nebenwirkungen, die – wie beispielsweise gastrointestinale Störungen, sexuelle Dysfunktion und Gewichtszunahme – die Therapieadhärenz beeinträchtigen können [2, 4, 24]. Somit besteht nach wie vor erheblicher Bedarf an pharmakologischen Alternativen, die ohne gravierende beeinträchtigende Nebenwirkungen neben Stimmung und Antrieb auch den Schlaf-Wach-Rhythmus normalisieren.
Agomelatin verkörpert ein neues Therapieprinzip: Die Substanz wirkt als Agonist an den vorwiegend im Nucleus suprachiasmaticus (SCN) lokalisierten melatonergen MT1- und MT2-Rezeptoren, deren Exprimierung tageszeitlichen Schwankungen unterliegt, und als selektiver Antagonist an postsynaptischen serotonergen 5-HT2C-Rezeptoren. Diese 5-HT2c Rezeptoren befinden sich unter anderem im frontalen Kortex, Hippocampus, Thalamus sowie in hoher Dichte im Nucleus suprachiasmaticus [17]. Der synergistische Wirkungsmechanismus von Agomelatin wird sowohl mit der Normalisierung der depressiven Kernsymptome als auch mit der Regulation zirkadianer Rhythmen in Verbindung gebracht [23].
Die antidepressive Wirksamkeit von Agomelatin (25 bis 50 mg) wurde in randomisierten, kontrollierten Studien mit nahezu 6000 Patienten auch gegenüber etablierten Antidepressiva wie Venlafaxin, Sertralin und Fluoxetin nachgewiesen [6–8, 10, 11, 14]. Die antidepressive Wirksamkeit von Agomelatin erstreckt sich über alle Schweregrade der Depression und über das gesamte Spektrum der Symptome [9, 16, 20, 23]. Seine Wirkung setzte innerhalb der ersten ein bis zwei Wochen ein [7, 14]. Eine Langzeitstudie belegt, dass Agomelatin Rückfälle verhindert [5]. Schlafstörungen und Tagesmüdigkeit gingen unter der Therapie deutlich zurück. Im Vergleich zu Venlafaxin verbesserte Agomelatin Schlafqualität, Einschlafbereitschaft, Tagesbefindlichkeit sowie Tagesaktivität schon nach einer Woche signifikant [14], ohne jedoch durch sedierende Eigenschaften den normalen Schlaf-Wach-Rhythmus zu stören. In den Studien zeigte Agomelatin ein günstiges Sicherheits- und Verträglichkeitsprofil [3, 10, 12]. Ein Leberenzymanstieg wurde bei 1,1% der mit Agomelatin 25/50 mg behandelten Patienten registriert im Vergleich zu 0,7% in der Plazebo-Gruppe [3].
Um die in klinischen Studien nachgewiesene Wirksamkeit von Agomelatin hinsichtlich der depressiven Symptomatik und der gestörten zirkadianen Rhythmik sowie die Verträglichkeit im Praxisalltag zu überprüfen, wurde die nichtinterventionelle Studie VIVALDI konzipiert. Anders als in klinischen Studien können Effektivität und Sicherheit von Arzneimitteln in nichtinterventionellen Studien unter Praxisbedingungen an großen und heterogenen Patientenpopulationen evaluiert werden, wie sie für die Routineversorgung typisch sind.
Patienten und Methoden
In der multizentrischen nichtinterventionellen Studie VIVALDI behandelten 665 Fachärzte insgesamt 3356 depressive Patienten im Alter über 18 Jahren mit Agomelatin. Dazu zählten sowohl Patienten mit einer ersten depressiven Episode als auch Patienten mit einer wiederkehrenden depressiven Episode, die innerhalb der letzten drei Monate nicht medikamentös behandelt wurde, sowie depressive Patienten, bei denen die Therapie umgestellt wurde. Die Datenerhebung umfasste den Zeitraum von März 2009 bis Januar 2010. Der Beobachtungsplan sah vor, dass die Patienten etwa zwölf Wochen mit Agomelatin behandelt wurden. Während der Studie wurde die Behandlung zu vier Zeitpunkten (U1 bis U4) dokumentiert: bei der Aufnahmeuntersuchung sowie zwei, sechs und zwölf Wochen nach Therapiebeginn mit Agomelatin (Tab. 1).
Tab. 1. Untersuchungsablauf
|
Erhobene Parameter |
Eingangsvisite |
Kontrolle |
Kontrolle |
Abschluss- |
|
Aufklärung und schriftliches Einverständnis des Patienten |
X |
|||
|
Demographische Daten |
X |
|||
|
Anamnese und Diagnose |
X |
|||
|
Komorbiditäten |
X |
|||
|
Laborparameter |
X |
X |
X |
|
|
Vorbehandlung mit Antidepressiva |
X |
|||
|
Psychotrope und sonstige Komedikation |
X |
|||
|
Änderung der antidepressiven/ |
X |
X |
X |
|
|
svMADRS |
X |
X |
X |
X |
|
CGI-I |
X |
X |
X |
X |
|
CGI-S |
X |
X |
||
|
CircScreen |
X |
X |
X |
X |
|
Abschließende Beurteilung der Therapie |
X |
|||
|
Unerwünschte Ereignisse |
X |
X |
X |
|
|
svMADRS: Montgomery-Åsberg Depression Rating Scale – short version (Beurteilung des Schweregrads von Symptomen der Depression – vereinfachte Skala) CGI-I: Clinical Global Impression of Improvement Scale (Beurteilung der Zustandsänderung) CGI-S: Clinical Global Impression of Severity Scale (Beurteilung des Schweregrads der Krankheit) CircScreen: Patientenfragebogen zur zirkadianen Rhythmik |
||||
Jedes teilnehmende Zentrum konnte anschließend Patienten zur weiteren Dokumentation in ein Follow-up einschließen, das weitere neun Monate umfasste. Die hier vorgestellten Ergebnisse beziehen sich auf die Daten über zwölf Wochen.
In der Aufnahmeuntersuchung wurden demographische Parameter (Alter, Geschlecht, Größe, Gewicht, Body-Mass-Index), psychiatrische Anamnese (Anzahl depressiver Episoden in der Anamnese, Dauer der aktuellen Episode, stationäre Aufenthalte wegen der Depression, Suizidversuche), antidepressive Vorbehandlung, Komorbidität und Komedikation dokumentiert. Die Patienten erhielten unter Beachtung der Anwendungshinweise und der Fachinformation 25 mg Agomelatin einmal täglich beim Zubettgehen. Sofern nach zwei Wochen keine Besserung der Symptome eintrat, konnte die Dosis auf 50 mg einmal täglich erhöht werden.
Die Beurteilung der Effektivität von Agomelatin auf die depressive Symptomatik, die gestörte zirkadiane Rhythmik und den Schlaf erfolgte mit verschiedenen psychometrischen Bewertungsskalen: Der Schweregrad der Depression wurde zu Beobachtungsbeginn und bei den Kontroll- und Abschlussuntersuchungen mit einer modifizierten Version der Montgomery-Åsberg Depression Rating Scale (svMADRS) bestimmt. Sie beinhaltet alle zehn Items der Originalversion der MADRS. Jedes Item wird vom Arzt mit Hilfe einer sechsstufigen Skala beurteilt (0=keine Symptome, 6=extreme Symptome). Für den Einsatz im ambulanten Bereich bietet die svMADRS gegenüber der Standardversion den Vorteil, dass keine Ankerpunkte verwendet werden und dass die jeweiligen Symptome nicht definiert, sondern lediglich genannt werden [18]. Der Schweregrad der Depression wurde mit der Clinical Global Impression of Severity Scale (CGI-S) und die Zustandsänderung mit der Clinical Global Impression of Improvement Scale (CGI-I) bewertet.
Mithilfe des Patientenfragebogens CircScreen wurde der Effekt der Therapie auf den Schlaf-Wach-Rhythmus und die tageszeitlichen Schwankungen evaluiert. Der Selbstbeurteilungsbogen beinhaltet sieben Fragen zu Problemen, die während der vergangenen sieben Tage aufgetreten sind. Für die ersten fünf Fragen wird ein Summenscore von 0 bis 20 gebildet, wobei höhere Werte stärker ausgeprägten Störungen entsprechen. Frage 6 und 7 werden separat ausgewertet.
Zur Bewertung der Verträglichkeit von Agomelatin wurden die Inzidenz und Art unerwünschter Arzneimittelwirkungen sowohl in der Kontroll- als auch in der Abschlussuntersuchung dokumentiert, ebenso eine vorzeitige Beendigung der Therapie und deren Begründung. Ein weiteres Verträglichkeitskriterium waren Veränderungen der Lebertransaminasen Alanin-Aminotransferase (ALT) und Aspartat-Aminotransferase (AST) in Bezug auf Abweichungen vom Normwert zwischen U1 und U3 sowie zwischen U1 und U4. Am Ende des Beobachtungszeitraums erfolgte die Beurteilung der Wirksamkeit und Verträglichkeit durch den Arzt.
In die Auswertung wurden nur Patienten eingeschlossen, für die neben den Basisdaten (U1) Angaben zum Verlauf der Therapie vorlagen, also für mindestens eine der Untersuchungen U2 bis U4. Retrospektiv dokumentierte Patienten wurden nicht in die Datenanalyse einbezogen.
Ergebnisse
Von 3317 der insgesamt 3356 in die VIVALDI-Studie aufgenommen Patienten konnten die Wirksamkeitsdaten ausgewertet werden (2113 Frauen, 1161 Männer, 43 Patienten ohne Angaben). Die im Rahmen der Studie erfassten Baseline-Daten sind in Tabelle 2 wiedergegeben. Das mittlere Alter betrug 50,0 Jahre (18 bis 89). 36,4% der Patienten wiesen eine depressive Episode (F32) und 63,6% eine rezidivierende depressive Störung (F33) auf. Zwei Drittel der Patienten waren bereits seit einem Jahr und länger erkrankt. In der Anamnese dokumentierten die Ärzte durchschnittlich 4,5 depressive Episoden. Die aktuelle depressive Symptomatik bestand im Mittel seit acht Wochen. 38,1% der Patienten wiesen neuropsychiatrische Komorbiditäten auf; am häufigsten handelte es sich dabei um Angst- und Panikstörungen.
Tab. 2. Baseline-Daten
|
Geschlecht [n] |
Männer: 1161 (35,0%) Frauen : 2113 (63,7%) Keine Angabe: 43 (1,3%) |
|
|
Alter [Jahre] (Mittelwert) |
50,0±13,0 |
|
|
Altersgruppen |
<25 Jahre 25 bis <35 Jahre 35 bis <45 Jahre 45 bis <55 Jahre 55 bis <65 Jahre 65 bis <75 Jahre ≥75 Jahre |
102 (3,1%) 308 (9,4%) 647 (19,7%) 1026 (31,2%) 762 (23,2%) 363 (11,0%) 83 (2,5%) |
|
Gewicht (Mittelwert ± SD) |
Männer: 85,0±13,7 kg Frauen: 71,9±14,7 kg |
|
|
Body-Mass-Index (Mittelwert ± SD) |
Männer: 26,8±4,0 kg/m2 Frauen: 26,1±5,3 kg/m2 |
|
|
Familienstand [n] |
Alleinstehend Verwitwet In Partnerschaft |
951 (28,7%) 146 (4,4%) 2140 (64,5%) |
|
Diagnose [n] |
Depressive Episode Rezidivierende depr. Störung |
1202 (36,4%) 2104 (63,6%) |
|
Dauer der Erkrankung [n] |
<1 Jahr ≥1 Jahr |
1172 (38,0%) 1912 (62,0%) |
|
Anzahl der depressiven Episoden in der Anamnese |
4,5 (0 bis 30) |
|
|
Dauer der aktuellen Episode |
12,7 Wochen (1 bis 120) |
|
|
Stationäre Aufenthalte in der Anamnese [n] |
929 (28,3%) |
|
|
Suizidversuche in der Anamnese [n] |
235 (8,0%) |
|
|
Neuropsychiatrische Komorbiditäten [n] |
1265 (38,1%) |
|
|
Angst-/Panikstörungen Posttraumatisches Belastungssyndrom (PTBS) |
929 (28,0%)
|
|
|
Vorbehandlung mit Antidepressiva [n] |
1915 (57,7%) |
|
|
SSRI Trizyklische Antidepressiva Mirtazapin Venlafaxin |
1023 (30,8%) 812 (24,5%) 600 (18,1%) 408 (12,3%) |
|
Medikation
Mehr als Hälfte der Patienten (57,7%) waren bereits mit etablierten Antidepressiva vorbehandelt: ein Drittel (30,8%) hatte selektive Serotonin-Wiederaufnahmehemmer eingenommen. In 74,9% der Fälle erfolgte der Wechsel der antidepressiven Medikation aufgrund mangelnder Wirksamkeit und in 31,0% aufgrund mangelnder Verträglichkeit. 22,6% der Umstellungen auf Agomelatin erfolgten auf Wunsch der Patienten. Bei 26,7% der auf Agomelatin eingestellten Patienten handelte es sich um die erste Einstellung auf ein Antidepressivum. 55,4% der Patienten erhielten Agomelatin als Monotherapie, 30,1% kombiniert mit psychotropen Substanzen, 25,8% als Kombinationstherapie mit anderen Antidepressiva, 11,2% kombiniert mit anderen Antidepressiva und psychotropen Substanzen. Während der zwölfwöchigen Beobachtungszeit bekamen 997 Patienten (30,1%) eine psychotrope Komedikation, vorwiegend Neuroleptika (9,9%), Z-Substanzen (9,2%) und Benzodiazepine (8,9%). Bei 11,2% der Patienten wurden zusätzlich zu Agomelatin sowohl andere antidepressive als auch psychotrope Substanzen eingesetzt. Bei 314 Patienten (9,5%) wurde in der Beobachtungsperiode mindestens eine der antidepressiven oder psychotropen Begleitmedikationen abgesetzt; bei 478 Patienten (14,4%) verordneten die Ärzte im Verlauf der Studie eine zusätzliche antidepressive oder psychotrope Komedikation.
Während der ersten zwei Wochen nahmen nahezu alle Patienten täglich 25 mg Agomelatin ein. Im Verlauf der Beobachtungsstudie wurde ein Teil der Patienten (39,7%) auf die höhere Agomelatin-Dosis (50 mg/Tag) umgestellt. Bei der Abschlussuntersuchung wurden 58,3% der Patienten mit 25 mg/Tag Agomelatin behandelt; 39,7% der Patienten erhielten eine höhere Dosis, überwiegend 50 mg/Tag.
Veränderung des Schweregrads der Depression (svMADRS)
Ein svMADRS-Gesamtwert von 30 bis 60 entspricht einer schweren Depression, während ein Wert von 13 bis 21 eine leichte Symptomatik anzeigt. Eine Reduktion des svMADRS um mindestens 50% gilt als Response und ein Gesamtwert von weniger als 12 als Remission. Der mittlere Schweregrad der depressiven Symptomatik verbesserte sich unter Agomelatin von einem svMADRS-Summenscore von 30,6±8,7 bei der Eingangsuntersuchung auf einen Gesamtwert von 12,8±9,7 bei der Abschlussuntersuchung in Woche 12 (Abb. 1a). Im Mittel sank der svMADRS-Gesamtwert um 18,3 Punkte (57,7%) gegenüber dem Ausgangswert. Insgesamt zeigte sich bei 94,9% der Patienten eine Abnahme des svMADRS-Gesamtwert und somit eine Verbesserung des Schweregrads der Depression. Parallel dazu stiegen die Response- und Remissionsraten kontinuierlich an (Abb. 1b). Zwölf Wochen nach Therapiebeginn mit Agomelatin erfüllten 65,8% die Responsekriterien.

Abb. 1. Antidepressive Wirkung von Agomelatin. (a) Veränderung des svMADRS-Gesamtwerts im Zeitverlauf der zwölfwöchigen VIVALDI-Studie; (b) Response- und Remissionsraten (Response: Verbesserung des svMADRS um ≥50%; Remission: svMADRS-Gesamtwert ≤12); W: Woche
Eine antidepressive Wirkung von Agomelatin trat bei einem Teil der Patienten schon bei der ersten Kontrolluntersuchung nach zwei Wochen auf: Bei 12,3% besserte sich der svMADRS-Gesamtscore um mindestens 50%, so dass das Kriterium einer Response erfüllt wurde. Knapp die Hälfte der Patienten (48,4%) erreichte nach zwei Wochen eine Abnahme des svMADRS-Gesamtwerts um mindestens 20% und konnte somit als „early improvers“ klassifiziert werden.
Zu Beginn der VIVALDI-Studie wurde die Depression bei 56,9% der Patienten als schwer eingestuft (svMADRS-Gesamtwert: 30 bis 60), am Ende der zwölfwöchigen Behandlung mit Agomelatin sank diese Rate auf 6,6%. Nach zwölf Wochen war über die Hälfte der Patienten (54,8%) in Remission (svMADRS-Gesamtwert 0 bis 12). Eine relevante Verbesserung der Symptomatik und Veränderungen in den Schweregraden zeigten sich bei der ersten Kontrolluntersuchung nach zwei Wochen (Abb. 2).

Abb. 2. Veränderung des Schweregrads der Depression (svMADRS-Gesamtwert-Kategorien) im Beobachtungsverlauf; W: Woche
Auch bei der Analyse einzelner MADRS-Items bestätigte sich die antidepressive Wirksamkeit von Agomelatin. So erreichten 80,8% der Patienten eine Verbesserung für das Item reduzierter Schlaf, 73,0% für Traurigkeit, 72,0% für innere Spannung, 70,3% für Konzentrationsschwierigkeiten und 67,4% für Gefühlslosigkeit.
Verbesserung des klinischen Gesamteindrucks (CGI)
Der mittlere CGI-S-Wert sank von 4,7±0,8 zu Beginn der Therapie auf 3,2±1,3 nach zwölfwöchiger Agomelatin-Therapie (5 = Patient ist deutlich krank; 3 = Patient ist nur leicht krank). Der Anteil der Patienten in den Kategorien „überhaupt nicht krank“, „grenzwertig erkrankt“ und „leicht erkrankt“ nahm deutlich zu und entsprechend der Anteil der mäßig bis schwer kranken Patienten kontinuierlich ab (Abb. 3). Nach der CGI-I-Skala zeigten 22,8% der Patienten zwei Wochen nach Behandlungsbeginn mit Agomelatin eine Response (CGI-I ≤2) und 72,4% der Patienten nach zwölf Wochen. Ein Drittel (30,4%) der Patienten erreichte in Bezug auf den klinischen Gesamteindruck eine Remission (CGI-S ≤2).
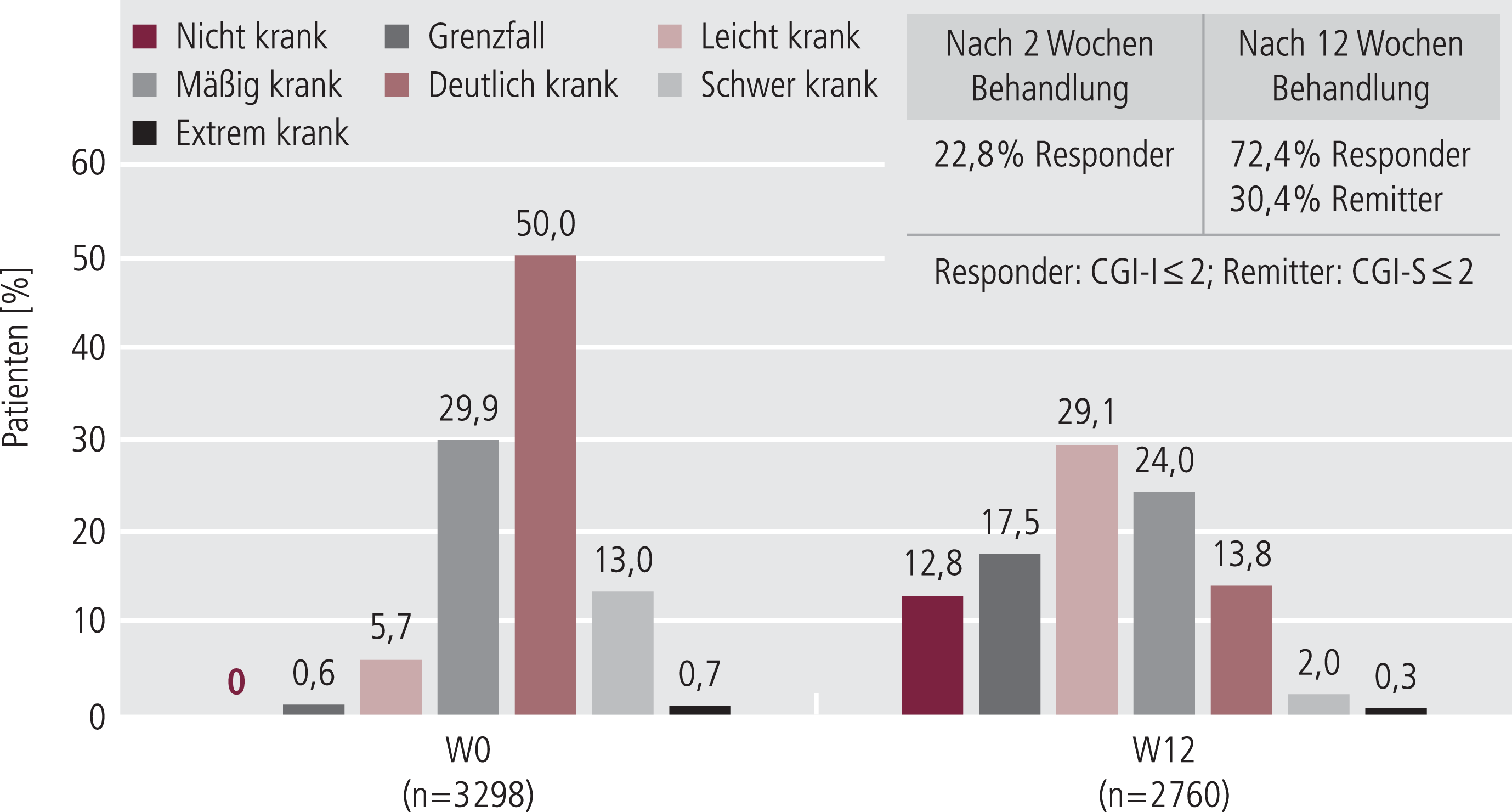
Abb. 3. Schweregrad der Krankheit gemäß CGI-S bei der Eingangsuntersuchung und nach 12 Wochen Agomelatin; W:Woche
Wirkung auf den Schlaf-Wach-Rhythmus
Nach zwei Wochen berichteten viele Patienten von einer Besserung der Schlafstörungen und der Tagesmüdigkeit (Abb. 4). Während 74,3% der Patienten bei der Aufnahmeuntersuchung in dem Selbstbeurteilungsfragebogen CircScreen häufige und sehr häufige Schwierigkeiten beim Einschlafen und 77,5% wiederholtes Aufwachen während der Nacht angaben, waren es bei der Abschlussuntersuchung jeweils nur noch 11,9% und 14,7%. Eine Verbesserung des Einschlafens im Vergleich zu Studienbeginn gaben 81,5% der Patienten an; 82,0% berichteten, besser durchschlafen zu können. Bei der Eingangsuntersuchung gaben zwei Drittel (65,7%) der Patienten an, in den frühen Morgenstunden häufig bis sehr häufig aufzuwachen und danach nicht wieder einschlafen zu können; in Woche 12 waren es nur noch 10,9%. Bei Baseline hatten 55,4% häufig/sehr häufig Schwierigkeiten, morgens richtig wach zu werden, nach zwölfwöchiger Behandlung mit Agomelatin nur noch 11,0%. Der Anteil der Patienten mit häufiger/sehr häufiger Tagesmüdigkeit ging von initial 62,0% auf 11,2% zurück. 60,9% der Patienten gaben am Ende des Beobachtungszeitraums an, ihre normalen Tagesaktivitäten häufig/sehr häufig ausführen zu können im Vergleich zu 33,2% zu Beginn der nichtinterventionellen Studie. Der mittlere Gesamtscore der ersten fünf Fragen des CircScreen-Fragebogens sank von 13,8±3,4 bei Baseline auf 6,1±4,2 nach zwölf Wochen. Eine Verbesserung des Gesamtscores wurde bei 92,4% der Patienten beobachtet. Zudem verbesserten sich insgesamt 56,6% der Studienteilnehmer in ihrer Alltagsfunktionalität (CircScreen, Frage 6). Der Anteil der Patienten, die sich während der letzten sieben Tage deprimiert gefühlt hatten (CircScreen, Frage 7), sank von 92,7% bei der Eingangsuntersuchung auf 41,4% bei der Abschlussuntersuchung nach zwölf Wochen.
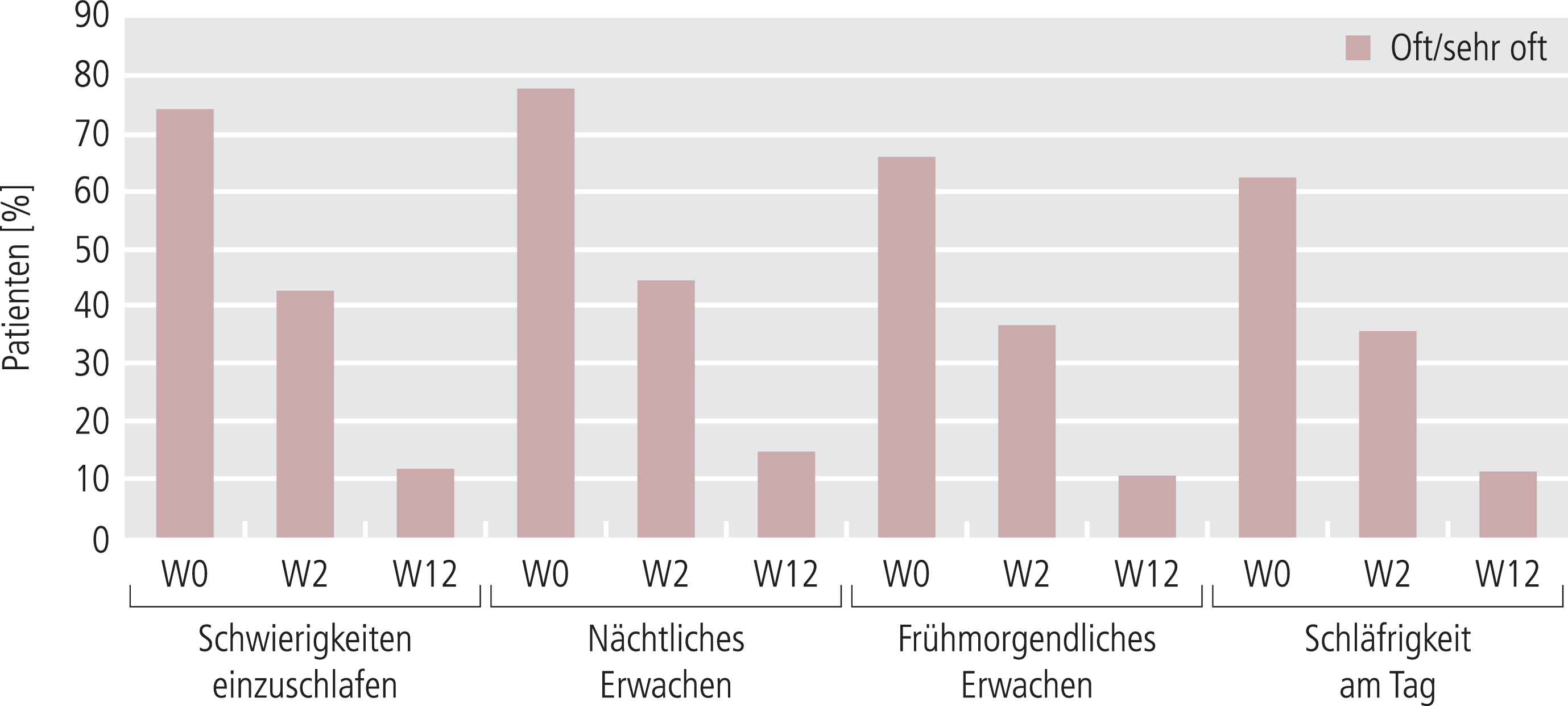
Abb. 4. Störungen des Schlafs und der tageszeitlichen Rhythmen (evaluiert mithilfe des Patientenfragebogens CircScreen); W: Woche
Beurteilung der Wirksamkeit und Verträglichkeit von Agomelatin
Bei der Abschlussuntersuchung beurteilten die Ärzte die Wirksamkeit von Agomelatin bei 67,3% der Patienten auf einer vierstufigen Skala als gut oder sehr gut.
Die Verträglichkeit wurde von nahezu allen Ärzten (93,2%) als sehr gut oder gut bewertet. Während der zwölfwöchigen Behandlung mit Agomelatin blieben das durchschnittliche Körpergewicht der Patienten (–0,1±2,7 kg) und der BMI (0,0±1,0) stabil. Die Analyse der unerwünschten Arzneimittelwirkungen (UAW) basiert auf den Daten von 3324 Patienten. Bei 334 Patienten (10,0%) wurden insgesamt 542 unerwünschte Arzneimittelwirkungen beobachtet. Von diesen unerwünschten Arzneimittelwirkungen wurden 526 (97,1%) als nicht schwerwiegend eingestuft. Am häufigsten waren Kopfschmerzen (1,7%), Übelkeit (1,4%) und Schwindel (0,9%). Ein sicherer Zusammenhang zwischen Agomelatin und einer unerwünschten Arzneimittelwirkung wurde bei 31 Patienten angenommen (0,9%). Für weitere 4,0% (n=132) der unerwünschten Arzneimittelwirkungen wurde ein Zusammenhang zu Agomelatin vom behandelnden Arzt als wahrscheinlich, für 2,7% (n=90) als möglich angesehen. Bei neun Patienten (0,3%) wurden insgesamt 16 schwerwiegende unerwünschte Arzneimittelwirkungen (sUAW) dokumentiert. In sechs dieser Fälle handelte es sich um Suizidgedanken, wobei in allen diesen Fällen kein kausaler Zusammenhang mit Agomelatin angegeben wurde. Mit einer Ausnahme hat sich jedes dieser schwerwiegenden unerwünschten Arzneimittelwirkungen wieder zurückgebildet. Bei der Ausnahme handelte es sich um einen 23-jährigen Patienten, der fünf Monate nach Therapiebeginn eine Manie entwickelte. Schon einige Wochen vor dem Auftreten der Manie hatte der Patient Agomelatin auf eigene Verantwortung abgesetzt. Bei dem Mann wurde eine bipolare Störung diagnostiziert, so dass die behandelnden Ärzte nicht von einem Zusammenhang mit Agomelatin ausgegangen sind.
Bei 2295 Patienten wurde die Alanin-Aminotransferase (ALT=GOT) zu Beginn der Behandlung und bei 1906 Patienten nach sechs Wochen bestimmt. Die Aspartat-Aminotransferase (AST=GPT) wurde bei 2235 Patienten bei der Aufnahmeuntersuchung und bei 1873 Patienten nach sechs Wochen bestimmt (Tab. 3). Der Anteil der Patienten mit über die Norm erhöhten Werten für die Lebertransaminase ALT stieg von 11,9% bei der Aufnahmeuntersuchung auf 14,6% nach zwölf Wochen; der Anteil der Patienten mit erhöhten AST-Werten stieg von 8,7% auf 10,8%. Einen ALT-Wert über dem Dreifachen des oberen Normwerts (>3 ULN) hatten bei der Aufnahmeuntersuchung 0,2% und nach zwölf Wochen 0,4% der Patienten; der Anteil der Patienten mit erhöhten AST-Werten >3 ULN war bei der Aufnahmeuntersuchung wie am Ende der Studie gleich (0,2%). Fünf Patienten, die bei Studienbeginn erhöhte Transaminasenwerte (ALT und/oder AST) unterhalb des 3-fachen oberen Normbereichs aufwiesen, entwickelten im Verlauf der Studien einen Anstieg über das Dreifache des oberen Normwerts.
Tab. 3. Lebertransaminasenwerte bei Aufnahme und im Verlauf der Studie
|
Kategorie |
V1 (Aufnahme) |
V3 (Woche 6) |
V4 (Woche 12) |
|||
|
n |
% |
n |
% |
n |
% |
|
|
ALT ≤ obere Norm |
2022 |
88,1 |
1651 |
86,6 |
1415 |
85,3 |
|
ALT > obere Norm, ≤ 3 x obere Norm |
268 |
11,7 |
251 |
13,2 |
236 |
14,2 |
|
ALT >3 x obere Norm |
5 |
0,2 |
4 |
0,2 |
7 |
0,4 |
|
AST ≤ obere Norm |
2041 |
91,3 |
1680 |
89,7 |
1463 |
89,2 |
|
AST > obere Norm, ≤3 x obere Norm |
189 |
8,5 |
190 |
10,1 |
174 |
10,6 |
|
AST >3 x obere Norm |
5 |
0,2 |
3 |
0,2 |
3 |
0,2 |
Insgesamt wurden bei acht Patienten (0,2%) erhöhte Transaminasenwerte als unerwünschte Arzneimittelwirkung berichtet; bei drei dieser Patienten standen keine Baseline-Werte zur Verfügung.
856 Patienten (25,8%) beendeten die Therapie vorzeitig. Als häufigster Grund für den Behandlungsabbruch wurde Patientenwunsch (13,5%), mangelnde Wirksamkeit (9,1%) und Unverträglichkeit (5,2%) angegeben. In 70,3% der Fälle gaben die behandelnden Ärzte an, nach Abschluss der nichtinterventionellen Studie eine Fortsetzung der Therapie mit Agomelatin zu planen.
Diskussion
Agomelatin ist das erste Antidepressivum, das als MT1-/MT2-Rezeptoragonist und selektiver 5-HT2C-Rezptorantagonist wirkt. Die Differenz im HAM-D-Score gegenüber Plazebo lag in den kontrollierten klinischen Studien zwischen 2,3 und 3,44 Punkten [9, 16, 23]. Die Inzidenz von Rückfällen wurde in einer 10-monatigen Studie unter Agomelatin um 54% im Vergleich zu Plazebo reduziert (p<0,0001) [5]. In direkten Vergleichsstudien mit verschiedenen SSRI und Venlafaxin konnte die antidepressive Wirksamkeit von Agomelatin bestätigt werden [6, 7, 11, 14]. In diesen Studien zeigte sich eine Verbesserung depressionsassoziierter Schlafstörungen bei einem Verträglichkeitsprofil überwiegend auf Plazebo-Niveau.
Die vorliegende nichtinterventionelle Beobachtungsstudie VIVALDI lieferte Effektivitäts- und Sicherheitshinweise für Agomelatin in der ambulanten Behandlung von depressiven Patienten unter naturalistischen Bedingungen. Die Durchführung dieser Untersuchung folgte den Empfehlungen der AGNP (Arbeitsgemeinschaft für Neuropsychopharmakologie und Pharmakopsychiatrie) zur Durchführung von Anwendungsbeobachtungen [15]. Hiernach können nichtinterventionelle Studien aus methodologischen Gründen keinen Wirksamkeitsnachweis liefern, jedoch bestätigende Effektivitätshinweise unter Alltags-(„real world“-)Bedingungen.
Die Baseline-Daten der in die Analyse einbezogenen Patienten bestätigen, dass es sich um eine sehr heterogene und für die tägliche Praxis repräsentative Population handelt. Ein Großteil der Studienteilnehmer (57,7%) war bereits mit Antidepressiva vorbehandelt; 38,1% wiesen neuropsychiatrische Komorbiditäten auf.
Die Verbesserung der depressiven Symptomatik, gemessen anhand der svMADRS-Skala, verlief nahezu linear, ausgehend von einem Baseline-Wert von 30,6 auf einen Wert von 12,8 bei der Abschlussuntersuchung. Nach zwei Wochen hatten 48,4% der Patienten eine Symptomreduktion im svMADRS von mindestens 20% erreicht („early improvers“). Nach sechs Wochen hatten sich 42,7% der Patienten um mindestens 50% im svMADRS-Gesamtwert verbessert und erfüllten damit die Responsekriterien. Jeder Dritte (33,2%) war zu diesem Zeitpunkt bereits remittiert (svMADRS-Gesamtwert ≤12). Bis zur Abschlussuntersuchung in Woche 12 stiegen die Response- und Remissionsraten noch weiter an (65,8% bzw. 54,8%). Gerade unter dem Aspekt, dass in der VIVALDI-Studie die meisten Patienten bereits mit etablierten Antidepressiva vorbehandelt waren, ist es bemerkenswert, dass unter Agomelatin mehr als jeder zweite Patient remittierte. Dabei wurden mehr als die Hälfte der Patienten über den gesamten Beobachtungszeitraum mit der niedrigeren Agomelatin-Dosis (25 mg/Tag) behandelt. Der rasche und kontinuierliche Anstieg der Response- und Remissionsraten zwischen Woche 6 und Woche 12 in der vorliegenden Studie wirft aber gleichzeitig die Frage auf, ob das Maximum der Wirksamkeit von Agomelatin am Ende der Hauptuntersuchung schon erreicht war. Die Auswertung der 9-monatigen Follow-up-Phase der VIVALDI-Studie wird zeigen, ob die Response- und Remissionsraten bei längerer Behandlung noch weiter steigen.
Parallel zur Linderung der affektiven Kernsymptome der Depression verbesserte Agomelatin in der vorliegenden Studie auch die vorbestehende Schlafstörung. Nahezu alle Patienten (92,4%) verbesserten sich im CircScreen-Gesamtscore. Schon zwei Wochen nach Beginn der Behandlung gaben die Patienten eine spürbare Verbesserung aller mit dem CircScreeen-Fragebogen erfassten subjektiven Schlafparameter an. Das leichtere Einschlafen und bessere Durchschlafen wirkte sich tagsüber in einer reduzierten Tagesmüdigkeit und verbesserten Tagesaktivität aus. Damit bestätigen die bei depressiven Patienten unter Praxisbedingungen erhobenen Daten zur Schlafqualität die Ergebnisse klinischer Studien. Im Gegensatz zu Venlafaxin (70–150 mg/Tag) führte Agomelatin (25–50 mg/Tag) in einer doppelblinden, randomisierten Studie bereits nach einwöchiger Therapie zu einer signifikanten Verbesserung des subjektiven Einschlafens und der subjektiven Schlafqualität [14]. Die verbesserte Schlafqualität war assoziiert mit einem Rückgang der Tagesmüdigkeit. In einer offenen polysomnographischen Studie konnte gezeigt werden, dass Agomelatin (25 mg/Tag) über 42 Tage bei depressiven Patienten die Schlafeffizienz verbessert und Einschlaflatenz verkürzt [25]. Insgesamt führte Agomelatin zu einer Reorganisation der Schlafarchitektur mit längeren Tiefschlafphasen in der ersten Nachthälfte und Leichtschlafstadien in der zweiten Nachthälfte, ohne den REM-Schlaf zu beeinflussen. Die bislang verfügbare Datenlage lässt darauf schließen, dass Agomelatin die bei depressiven Patienten häufig gestörte zirkadiane Rhythmik wieder normalisiert, ohne gleichzeitig durch sedierende Eigenschaften den normalen Schlaf-Wach-Rhythmus zu stören.
Die Response- und Remissionsraten (65,8% bzw. 54,8%) von Agomelatin in der vorliegenden Untersuchung entsprechen den Ergebnissen zweier Anwendungsbeobachtungen mit Escitalopram: Möller et al. fanden für den SSRI nach acht Wochen eine Responserate (Reduktion des svMADRS um ≥50%) von 69,7% und eine Remissionsrate (svMADRS ≤12) von 56,8% [19]; eine weitere Untersuchung ergab 72,9 bzw. 83,1% nach 16 Wochen [13]. Eine Besonderheit der VIVALDI-Studie im Vergleich zu den zuvor genannten Beobachtungsstudien war der Wirksamkeitsnachweis von Agomelatin auf die bei depressiven Patienten häufig gestörte zirkadiane Rhythmik und die damit assoziierten Schlafstörungen. Der Anteil der Patienten mit Tagesmüdigkeit ging während der Therapie mit Agomelatin von 62,0% auf 11,2% zurück, parallel dazu verbesserte sich die Tagesaktivität, was insbesondere für berufstätige Patienten eine hohe Relevanz hat. In einer Beobachtungsstudie mit Escitalopram bei berufstätigen Patienten wurden keine Daten zur Schlafqualität oder Tagesvigilanz erhoben [28].
Verträglichkeit
In kontrollierten Studien bewirkte Agomelatin nach vier- bis achtwöchiger Therapie keine klinisch relevanten Veränderungen von kardiovaskulären und Vital-Parametern (einschließlich EKG) und verhielt sich gewichtsneutral [10]. In einer randomisierten, doppelblinden Vergleichsstudie traten unter Agomelatin seltener gastrointestinale und zentralnervöse Nebenwirkungen auf als unter Venlafaxin. Auch die Abbruchrate aufgrund von Nebenwirkungen war unter Agomelatin geringer als unter dem SSNRI (4,2% versus 13,2%) [14]. Eine weitere Vergleichsstudie ergab, dass Agomelatin im Gegensatz zu Venlafaxin die sexuelle Funktion besser erhält [11]. Außerdem konnten bei abrupter Beendigung der Behandlung mit Agomelatin anders als bei Paroxetin keine Absetzsymptome beobachtet werden [21].
In den kontrollierten Studien wurde ein Leberenzymanstieg bei 1,1% der mit Agomelatin 25/50 mg behandelten Patienten registriert im Vergleich zu 0,7% in den Plazebo-Gruppen [10]. Diese Transaminasenanstiege normalisierten sich gewöhnlich nach Absetzen von Agomelatin. Um die Bedeutung eines Transaminasenanstiegs im praktischen Alltag zu bewerten, fanden in der vorliegenden Studie diesbezügliche Laborkontrollen besondere Beachtung. Die Kontrollen erfolgten entsprechend der Fachinformation bei der Aufnahmeuntersuchung sowie nach 6 und nach 12 Wochen [3]. Bei lediglich 0,1% und 0,2% der Patienten mit anfangs normalen Transaminasenwerten stiegen die ALT- bzw. AST-Werte über das Dreifache der Norm zum letzten Untersuchungszeitpunkt. Nach 12 Wochen wurde bei 7 bzw. 3 Patienten ein pathologischer Anstieg des ALT- bzw. AST-Wertes über das Dreifache der Norm gemessen. Dabei ist zu bedenken, dass 5 der 7 Patienten, die nach 12 Wochen einen ALT-Anstieg zeigten, schon bei der Aufnahmeuntersuchung ALT-Werte oberhalb der dreifachen Norm aufwiesen. Die AST-Werte lagen bei Baseline bei fünf Patienten im pathologischen Bereich. Nach 12 Wochen ging diese Zahl auf drei Patienten zurück. Laut Fachinformation hätten diese Patienten nicht in die Studie eingeschlossen werden dürfen. Insgesamt zeigen diese Daten eine geringe Häufigkeit von Leberwerterhöhungen, die ohne klinische Symptome beobachtet wurden. Für den Praxisalltag gilt natürlich, dass die Leberwertkontrolle entsprechend Fachinformation durchzuführen ist.
Unerwünschte klinische Arzneimittelwirkungen traten während der zwölfwöchigen Beobachtungszeit mit einer insgesamt relativ geringen Inzidenz (10,0%) auf; das Körpergewicht blieb konstant. Die häufigsten unerwünschten Arzneimittelwirkungen waren zentralnervöse Störungen, gastrointestinale Störungen, Kopfschmerzen, Übelkeit und Schwindel. Diese waren in der Regel vorübergehender Natur. Ein kausaler Zusammenhang mit Agomelatin wurde nur bei 31 Patienten (0,9%) angenommen.
Der hohe Anteil der Patienten (74,2%), die ihre Behandlung über zwölf Wochen fortgesetzt haben, spiegelt die hohe Therapieadhärenz für Agomelatin im Praxisalltag wider. Von den insgesamt 25,8% Therapieabbrüchen in VIVALDI fanden 9,3% in den ersten vier Wochen, 7,3% zwischen Woche 4 und 8, 4,2% zwischen Woche 8 und 12 und 2,8% nach 12 Wochen statt. Die Abbruchraten aufgrund von mangelnder Wirksamkeit (9,1%) und mangelnder Verträglichkeit (5,2%) sind für depressive Patienten im Praxisalltag als niedrig anzusehen.
Die Ergebnisse der nichtinterventionellen Studie VIVALDI bestätigen die zuvor in klinischen Studien mit Agomelatin belegte antidepressive Effektivität mit Wiederherstellung des gestörten Schlaf-Wach-Rhythmus sowie die gute Verträglichkeit und die hohe Therapieakzeptanz bei einer großen und heterogenen Patientenpopulation im Praxisalltag.
Literatur
1. Alonso J, Angermeyer MC, Bernert S, Bruffaerts R, et al. Prevalence of mental disorders in Europe: results from the European Study of the Epidemiology of Mental Disorders (ESEMeD) project. Acta Psychiatr Scand Suppl 2004;420:21–7.
2. Baghai TC, Volz HP, Möller HJ. Drug treatment of depression in the 2000s: an overview of achievements in the last 10 years and future possibilities. World J Biol Psychiatry 2006;7:198–222.
3. Fachinformation Valdoxan®, Servier Deutschland GmbH, Februar 2009.
4. Fava M. Daytime sleepiness and insomnia as correlates of depression. J Clin Psychiatry 2004;65(Suppl 16):27–32.
5. Goodwin G, Emsley R, Rembry S, Rouillon F, et al. Agomelatine prevents relapse in patients with major depressive disorder, without evidence of a discontinuation syndrome. J Clin Psychiatry 2009;70:1128–37.
6. Hale A, Corral R, Mencacci O, Saiz Ruiz J, et al. Superior antidepressant efficacy of agomelatine vs. fluoxetine in severe major depressive disorder patients: a randomised, doubleblind study. Eur Neuropsychopharmacol 2009;19(Suppl 3):S418.
7. Kasper S, Hajak G, Wulff K, Hoogendijk WJ, et al. Efficacy of the novel antidepressant agomelatine on the circadian rest-activity cycle and depressive and anxiety symptoms in patients with major depressive disorder: a randomized, double-blind comparison with sertraline. J Clin Psychiatry 2010;71:109–20.
8. Kasper S, Lemoine P. Comparative efficacy of the antidepressants agomelatine, venlafaxine and sertraline. Eur Neuropsychopharmacology 2008;18:S331–2.
9. Kennedy SH, Emsley R. Placebo-controlled trial of agomelatine in the treatment of major depressive disorder. Eur Neuropsychopharmacol 2006;16:93–100.
10. Kennedy SH, Rizvi SJ. Agomelatine in the treatment of major depressive disorder. CNS Drugs 2010;24:479–99.
11. Kennedy SH, Rizvi S, Fulton K, Rasmussen J. A double-blind comparison of sexual functioning, antidepressant efficacy, and tolerability between agomelatine and venlafaxine XR. J Clin Psychopharmacol 2008;28:329–33.
12. Laux G. Verträglichkeitsprofil von Agomelatin. Psychopharmakotherapie 2009;16(Suppl 19):11–4.
13. Laux G, Friede M. Escitalopram zur Behandlung von komorbider Angst und Depression. Ergebnisse einer Anwendungsbeobachtung. Psychopharmakotherapie 2009;16:106–13.
14. Lemoine P, Guilleminault C, Alvarez E. Improvement in subjective sleep in major depressive disorder with a novel antidepressant, agomelatine: Randomized, double-blind comparison with venlafaxine. J Clin Psychiatry 2007;68:1723–32.
15. Linden M, Baier D, Beitinger H, Kohnen R, et al. Leitlinien zur Durchführung von Anwendungsbeobachtungen (AWB) in der Psychopharmakotherapie. Nervenarzt 1994;65:638–44.
16. Lôo H, Hale A, D’Haenen H. Determination of the dose of agomelatine, a melatoninergic agonist and selective 5-HT2C antagonist, in the treatment of major depressive disorder: a placebo-controlled dose range study. Int Clin Psychopharmacol 2002;17:239–47.
17. Millan MJ, Gobert A, Lejeune F, Dekeyne A, et al. The novel melatonin agonist agomelatine (S20098) is an antagonist at 5-hydroxytryptamine2C receptors, blockade of which enhances the activity of frontocortical dopaminergic and adrenergic pathways. J Pharmacol Exp Ther 2003;306:954–64.
18. Möller H-J, Schnitker J. Einsatz einer modifizierten MADRS bei depressiven Patienten in einer prospektiven Kohortenstudie. Nervenarzt 2007;78:685–90.
19. Möller HJ, Friede M, Schmauß M. Behandlung der Depression mit Escitalopram. Ergebnisse einer großen Anwendungsbeobachtung. Psychopharmakotherapie 2007;14:149–56.
20. Montgomery SA, Kasper S. Severe depression and antidepressants: focus on a pooled analysis of placebo-controlled studies on agomelatine. Int Clin Psychopharmacol 2007;22:283–91.
21. Montgomery SA, Kennedy SH, Burrows GD, Lejoyeux M, et al. Absence of discontinuation symptoms with agomelatine and occurrence of discontinuation symptoms with paroxetine: a randomized, double-blind, placebo-controlled discontinuation study. Int Clin Psychopharmacol 2004;19:271–80.
22. Nutt D, Wilson S, Paterson L. Sleep disorders as core symptoms of depression. Dialogues Clin Neurosci 2008;10:329–36.
23. Olié JP, Kasper S. Efficacy of agomelatine, aMT1/MT2 receptor agonist with 5-HT2C antagonistic properties, in major depressive disorder. Int J Neuropsychopharmacol 2007;10:661–73.
24. Popoli M. Agomelatine. Innovative pharmacological approach in depression. CNS Drugs 2009;23(Suppl 2):27–34.
25. Quera Salva MA, Vanier B, Laredo J, Hartley S, et al. Major depressive disorder, sleep EEG and agomelatine: an open-label study. Int Neuropsychopharmacol 2007;10:691–7.
26. Sobocki P, Jonsson B, Angst J, Rehnberg C. Cost of depression in Europe. J Ment Health Policy Econ 2006;9:87–98.
27. Wehr TA, Wirz-Justice A. Circadian rhythm mechanisms in affective illness and in antidepressant drug action. Pharmacopsychiatria 1992;15:31–9.
28. Winkler D, Pjrek E, Klein N, Kasper S. Escitalopram bei berufstätigen Menschen. Ergebnisse einer Anwendungsbeobachtung an 2378 Patienten. Psychopharmakotherapie 2006;13:142–6.
29. Wirz-Justice A. Biological rhythm disturbances in mood disorders. Int Clin Psychopharmacol 2006;21(Suppl 1):S11–5.
*665 niedergelassene Fachärzte
Prof. Dr. med. Dipl.-Psych. Gerd Laux, Kliniken des Bezirks Oberbayern, Inn-Salzach-Klinikum, Klinikum für Psychiatrie, Psychotherapie, Psychosomatische Medizin und Neurologie, Gabersee 7, 83512 Wasserburg a. Inn, E-Mail: g.laux-isk@t-online.de
Treatment of depression with agomelatine in psychiatric practice: Results of the VIVALDI study
Agomelatine (Valdoxan®) is a melatonergic MT1- und MT2-receptor agonist and selective serotonergic 5-HT2C-antagonist. In experimental models of depression as well as in humans it has been shown that the substance resynchronizes disturbed circadian rhythms. Controlled clinical trials have demonstrated that agomelatine improves both the symptoms of major depression and the sleep-wake-disturbances.
In the observational study VIVALDI (Valdoxan improves depressive symptoms and normalizes circadian rhythms) the efficacy of agomelatine on depressive symptoms and sleep-wake rhythm and its tolerability were examined in depressed outpatients of German psychiatrists. A total of 3,317 patients were treated with agomelatine and observed for 12 weeks. Antidepressant efficacy was evaluated with the svMADRS (short version MADRS) and the Global Clinical Impression (CGI) scale. The effect on sleep and daytime functioning was assessed by a patient questionnaire (modified CircScreen).
During the course of the study the patients showed a clear improvement of the svMADRS total score from initially 30.6 to 12.8 after 12 weeks. After 12 weeks, 54.8% of the patients achieved remission (svMADRS ≤12). Sleep quality and daytime functioning improved as well. Daytime sleepiness improved in 78.2% of patients at week 12. Most of the physicians (93.2%) evaluated the tolerability of agomelatine as very good or good. Adverse reactions were reported by 10.0% of patients.
In conclusion, this study in the naturalistic setting confirms the improvements of depressive symptoms and sleep-wake cycle by agomelatine previously shown in randomised clinical trials in a typical patient’s population in psychiatric practice and out-patients psychiatric departments.
Key words: Agomelatine, depression, circadian rhythms, sleep disorders, non-interventional study
Psychopharmakotherapie 2011; 18(01)
