Bernhard F. Décard*, Bochum, Aiden Haghikia*, Bochum/Oxford, und Ralf Gold, Bochum
Eine Reihe neuer Medikamente zur Behandlung der multiplen Sklerose (MS) haben ihre Wirksamkeit in großen Phase-III-Studien gezeigt und stehen aktuell kurz vor ihrer klinischen Zulassung in Europa [38]. Gemeinsam ist diesen Therapien eine orale Darreichungsform und, soweit sich bisher anhand der aktuellen Datenlage abschätzen lässt, auch eine gute Verträglichkeit. Neben teilweise gänzlich neuen Wirkungsmechanismen scheinen einige der neuen Medikamente auch eine überlegene Wirksamkeit gegenüber den bisherigen, injizierbaren immunmodulatorischen Basistherapien (Interferon beta und Glatirameracetat) zu besitzen.
Eine interessante und vielversprechende Substanz ist hierbei das oral verfügbare Fingolimod, da es neben einem innovativen Wirkungsmechanismus auch eindrucksvolle positive klinische Ergebnisse gezeigt hat. Die bisher zugelassenen Therapien zur Behandlung der multiplen Sklerose haben insbesondere die inflammatorische Komponente der Erkrankung im Visier. Neue Arzneistoffe, die sowohl antiinflammatorische als auch neuroprotektive Eigenschaften besitzen, werden dringend benötigt; Fingolimod könnte zukünftig eine Therapieoption sein, die diese beiden Eigenschaften vereint.
Erst kürzlich wurde im Rahmen von zwei großen Doppelblind-Studien die Wirksamkeit und Sicherheit von Fingolimod in der Behandlung der schubförmigen multiplen Sklerose getestet. Sowohl gegenüber Plazebo (FREEDOMS-Studie) als auch im direkten Vergleich mit intramuskulär verabreichtem Interferon beta-1a (IFNb-1a) (TRANSFORMS-Studie) konnte bei mit Fingolimod behandelten Patienten eine signifikant reduzierte Schubrate und verminderte kernspintomographische Krankheitsaktivität nachgewiesen werden [8, 20]. Diese Therapieeffekte in der Behandlung der schubförmigen multiplen Sklerose werden vorwiegend darauf zurückgeführt, dass Fingolimod das Auswandern von enzephalitogenen Lymphozyten aus den sekundären Lymphknoten effektiv verhindert. Durch seine strukturelle Ähnlichkeit mit dem Lipidmediator Sphingosin beeinflusst Fingolimod Sphingolipid-Signalwege, die eine wesentliche Rolle bei der systemischen Zirkulation von Lymphozyten und deren Austritt aus peripher lymphatischen Geweben spielen (Abb. 1).
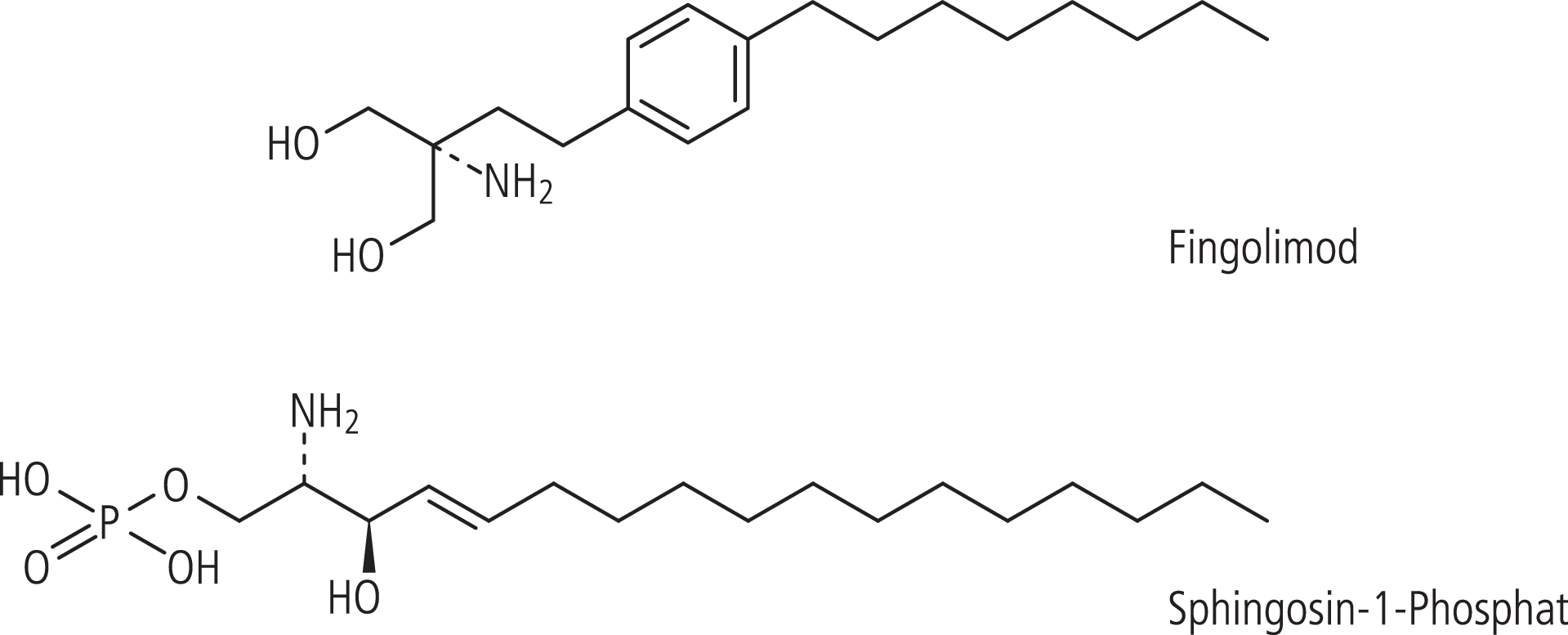
Abb. 1. Fingolimod und der endogene Sphingolipid-Botenstoff Sphingosin-1-phosphat (S1P)
Durch seine lipophile Struktur ist Fingolimod zudem in der Lage, die Blut-Hirn-Schranke zu überqueren, so dass im Rahmen der Behandlung von relevanten ZNS-Konzentrationen auszugehen ist. Die ZNS-assoziierten und mutmaßlich neuroprotektiven Effekte von Fingolimod sind aktuell Gegenstand intensiver Forschungsbemühungen [30, 31].
Tierexperimentelle Daten am Modell der experimentellen autoimmunen Neuritis (EAN) weisen zudem auf eine vielversprechende Wirkung von Fingolimod bei demyelinisierenden Polyneuropathien hin [44].
Wie bei anderen experimentellen Therapieansätzen, die bisher erfolgreich zur Behandlung der multiplen Sklerose eingesetzt wurden, sind die molekularen Wirkungsmechanismen von Fingolimod bisher noch unvollständig verstanden, so dass aktuell eine adäquate Risiko-Nutzen-Einschätzung nur bedingt möglich ist.
Nach einer Zusammenfassung der bisherigen Studienergebnisse versuchen die Autoren im Folgenden eine praxisrelevante Einschätzung für den künftigen klinischen Einsatz von Fingolimod zu geben. Für Leser, die einen tieferen Einblick in die molekularen Wirkungsmechanismen von Fingolimod gewinnen möchten, widmet sich dieser Übersichtsartikel zudem den physiologischen Grundlagen des Sphingolipid-Signalling und vermittelt einen Überblick zu peripheren immunologischen Wirkungsmechanismen sowie potenziell regenerativen und neuroprotektiven ZNS-assoziierten Effekten von Fingolimod.
Klinische Studienergebnisse und praxisrelevante Einschätzungen für den Einsatz von Fingolimod
Anfang dieses Jahres wurden die Ergebnisse zweier großer multizentrischer Phase-III-Studien (randomisiert, doppelblind, Plazebo-kontrolliert bzw. head-to-head) veröffentlicht, in denen das Wirk- und Sicherheitsprofil des oral verabreichten Fingolimod in der Therapie der schubförmig verlaufenden MS untersucht worden war [8, 20]. In der FREEDOMS-Studie (FTY720 research evaluation effects of daily oral therapy in multiple sclerosis) wurde die Wirkung von Fingolimod in den Dosierungen 0,5 mg bzw. 1,25 mg pro Tag gegen Plazebo bei 1033 Patienten (von 1272 ursprünglich eingeschlossenen) untersucht. In der TRANSFORMS (Trial assessing injectable interferon versus FTY720 oral in relapsing-remitting multiple sclerosis) wurde die Wirkung von Fingolimod in den Dosierungen 0,5 mg bzw. 1,25 mg pro Tag gegen IFNb-1a (Avonex®, Biogen Idec, Cambridge, USA) in einer Dosis von 30 µg einmal wöchentlich bei 1153 Patienten (von 1292 ursprünglich eingeschlossenen) bezüglich Schubrate, MRT-Aktivität und Progressionsrate untersucht. Dabei konnten die Ergebnisse der vier Jahre zuvor publizierten Phase-II-Studie zum größten Teil bestätigt werden, obwohl dort teilweise deutlich höhere Dosierungen getestet worden waren (1,25 mg bzw. 5 mg täglich gegen Plazebo) [19]. Eine Reduktion der jährlichen Schubrate von mehr als 50% und eine signifikante Reduktion der MRT-Aktivität (T2-Läsionslast und Anzahl Kontrastmittel aufnehmender Herde) wurde in beiden Studien registriert, interessanterweise nicht nur im Vergleich zu Plazebo, sondern auch zum Interferon-Präparat (in der niedrigeren Dosierung von 0,5 mg Fingolimod täglich). Weitere Details zum Wirkungsspektrum von Fingolimod aus der FREEDOMS- und der TRANSFORMS-Studie sind Tabelle 1 zu entnehmen.
Tab. 1. Ergebnisse der Phase-III-Studien mit Fingolimod – Wirkungsspektrum
|
FREEDOMS-Studie [20] |
TRANSFORMS-Studie [8] |
|||||
|
Fingolimod |
Plazebo |
Fingolimod |
IFNb-1a |
|||
|
1,25 mg/d (n=429) |
0,5 mg/d (n=425) |
(n=418) |
1,25 mg/d (n=420) |
0,5 mg/d (n=429) |
30 µg/Woche |
|
|
– Jährliche Schubrate |
0,16 |
0,18 |
0,40 |
0,20 |
0,16 |
0,33 |
|
– Anteil schubfreier Patienten |
74,7% |
70,4% |
45,6% |
79,8% |
82,6% |
69,3% |
|
– Wahrscheinlichkeit einer Behinderungsprogression innerhalb von 3 Monaten |
16,6% |
17,7% |
24,1% |
k. A. |
k. A. |
k. A. |
|
– Anteil Patienten ohne Kontrastmittel aufnehmende Läsionen im MRT |
89,8% |
89,7% |
65,1% |
91,2% |
90,1% |
80,8% |
|
– Anteil Patienten ohne neue oder ohne vergrößerte T2-Läsionen im MRT |
51,9% |
50,5% |
21,2% |
48,0% |
54,8% |
45,7% |
k. A. keine Angabe
Die zweite interessante Beobachtung betraf den anscheinend nicht dosisabhängigen Effekt von Fingolimod, so dass für den Zulassungsantrag zur Therapie der schubförmigen MS bei der US-amerikanischen Arzneimittelbehörde lediglich die niedrigste Dosierung von 0,5 mg täglich eingereicht wurde. Beweggrund für die Wahl der niedrigeren Dosierung war sicherlich auch das Auftreten teilweise massiver Nebenwirkungen (Informationen zum Nebenwirkungsspektrum aus der FREEDOMS- und der TRANSFORMS-Studie siehe Tab. 2) unter den höheren Dosierungen: unter täglicher Gabe von 1,25 mg Fingolimod traten zwei tödlich verlaufende Enzephalitiden auf (Herpes simplex und Varizella zoster), und das etwas häufigere Auftreten leichter viraler Infekte (vorwiegend broncho-pulmonal) unter den höheren Dosierungen (1,25 mg und 5 mg täglich) spricht zumindest für ein dosisabhängiges Nebenwirkungsprofil. Unter Therapie mit 0,5 mg Fingolimod zeigte sich zwar eine deutliche Reduktion der zirkulierenden Lymphozyten (um etwa 70%), ohne dass jedoch hiervon die Zahl der Neutrophilen oder der Effektor-Memory-T-Zellen beeinträchtigt gewesen wäre. Zudem fand sich kein Zusammenhang zwischen Lymphozyten-Zahl und Auftreten von schweren Infektionen, so dass niedrige Lymphozyten-Werte nicht zwingend ein erhöhtes Infektrisiko anzeigen und vice versa. Laborchemische Blutbildkontrollen sind daher nicht zwingend notwendig, allerdings sollte der behandelnde Arzt wissen, dass die Lymphozyten nach Beginn der Therapie relativ rasch abfallen und nach etwa einem Monat ein stabiles Level erreichen. Zusätzliche immunsuppressive Medikationen sollten unter Fingolimod-Therapie allerdings vermieden werden.
Tab. 2. Ergebnisse der Phase-III-Studien mit Fingolimod – Nebenwirkungsspektrum
|
FREEDOMS [20] |
TRANSFORMS [8] |
|||||
|
Fingolimod |
Plazebo |
Fingolimod |
IFNb-1a |
|||
|
1,25 mg/d (n=429) |
0,5 mg/d (n=425) |
(n=418) |
1,25 mg/d (n=420) |
0,5 mg/d (n=429) |
30 µg/Woche (n=431) |
|
|
Abbruch der Studie aufgrund von Nebenwirkungen |
14,2% |
7,5% |
7,7% |
10,0% |
5,6% |
3,7% |
|
Infektionen |
||||||
|
Letale Herpes-simplex- bzw. Herpes-zoster-Enzephalitiden |
– |
– |
– |
2 |
– |
– |
|
Nasopharyngitis |
26,1% |
27,1% |
27,5% |
22,1% |
20,5% |
20,4% |
|
Bronchitis |
9,1% |
8,0% |
3,6% |
k. A. |
k. A. |
k. A. |
|
Pneumonie |
1,9% |
0,9% |
0,7% |
k. A. |
k. A. |
k. A. |
|
Herpesvirus-Infekte |
5,8% |
8,7% |
7,9% |
5,5% |
2,1% |
2,8% |
|
Infekte des Urogenitaltrakts |
4,9% |
8,0% |
11,2% |
5,7% |
6,1% |
5,1% |
|
Kardiovaskuläre Nebenwirkungen |
||||||
|
Hypertension |
6,3% |
6,1% |
3,8% |
5,0% |
3,7% |
1,9% |
|
Bradykardien |
3,3% |
2,1% |
0,7% |
2,4% |
0,5% |
0 |
|
Atrioventrikulärer Block 1. Grades 2. Grades |
1,2% 0,2% |
0,5% 0 |
0,5% 0,2% |
0,5% 0,7% |
0,2% 0,2% |
0 0 |
|
Neoplasien |
||||||
|
Mammakarzinom |
0,2% |
0 |
0,7% |
0,5% |
0,5% |
0 |
|
Basalzellkarzinom |
0,2% |
0,9% |
0,7% |
0,5% |
0,7% |
0,2% |
|
Malignes Melanom |
0,2% |
0 |
0,2% |
0 |
0,7% |
0 |
|
Sonstige |
||||||
|
Lymphopenie |
5,4% |
3,5% |
0,5% |
1,0% |
0,2% |
0 |
|
Diarrhöen |
9,3% |
11,8% |
7,4% |
8,3% |
7,5% |
4,9% |
k. A. keine Angabe
Bei Auftreten von symptomatischen Bradykardien oder AV-Blockierungen nach erstmaliger Gabe von Fingolimod, wie sie in der Phase-III-Studie transient aufgetreten waren, oder bei Vorliegen einer eingeschränkten Metabolisierung im Rahmen von Leberfunktionsstörungen sollten kardiologische Untersuchungen beziehungsweise engmaschige Leberenzymkontrollen im Verlauf der Therapie erfolgen. Eine Therapie mit Fingolimod bei Patienten mit bereits bekannter koronarer Herzerkrankung oder Herzrhythmusstörungen ist unter Berücksichtigung der aktuellen Datenlage eher kritisch zu bewerten. Aufgrund der Gefahr von Torsade-de-pointes-Tachykardien sowie AV-Blockierungen sind unter Fingolimod-Therapie zudem Begleitmedikationen mit Antiarrhythmika zu vermeiden.
Aus den Studien geht zudem hervor, dass unter Therapie mit Fingolimod eine erhöhte Wachsamkeit bezüglich neu aufgetretener Makulaödeme und maligner Hautveränderungen geboten ist. Die FDA empfiehlt daher eine ophthalmologische Kontrolluntersuchung nach drei bis vier Monaten und einen zurückhaltenden Einsatz von Fingolimod bei Diabetikern. Hinweise für ein generell vermehrtes Auftreten von Malignomen bei einer täglichen Dosis von 0,5 mg Fingolimod ergeben sich aus der aktuellen Datenlage aber nicht.
Es bleibt abzuwarten, ob sich Fingolimod im klinischen Alltag insgesamt als sicheres Therapeutikum bewährt, wenn mehr Patientendaten vorliegen. Allerdings ist zu erwarten, dass der Hersteller Register mit kontrollierten Langzeitbeobachtungen, wie für neu zugelassene Medikamente inzwischen von Experten gefordert, führen wird.
Zusammengefasst handelt es sich bei Fingolimod um ein orales Therapeutikum, das mit einem neuartigen und spezifischen Wirkungsmechanismus sowie relativ geringen Nebenwirkungen seine Indikation in der Behandlung der schubförmigen MS nach momentaner Einschätzung am ehesten zwischen den klassischen Basistherapien (Beta-Interferone und Glatirameracetat) und den Eskalationstherapien (Natalizumab und Mitoxantron) im Therapieschema finden wird. Die FDA empfiehlt sogar den Einsatz von Fingolimod als First-Line-Medikation in der Behandlung der schubförmigen multiplen Sklerose.
Weitere klinische Studien werden Aufschluss über die potenziell neuroprotektive beziehungsweise regenerative Wirkung von Fingolimod geben. Für die primär progrediente MS wurde mit diesem Ziel bereits die INFORMS-Studie initiiert. Dabei können in Zukunft auch neue bildgebende Verfahren wie die Magnetization-Transfer-Ratio(MTR)- Imaging-Technik helfen, medikamentös bedingte regenerative Prozesse zu quantifizieren. Erst durch Therapiestudien wird sich zeigen, ob eine mögliche Erweiterung des Fingolimod-Einsatzbereichs, zum Beispiel für autoimmune Erkrankungen des peripheren Nervensystems, realisierbar ist.
Sphingosin-1-Phosphat und Sphingolipid-Signalling
Sphingolipid-Signalwege sind evolutionär hoch konserviert und beeinflussen durch Botenstoffe wie Ceramid, Sphingosin und Sphingosin-1-Phosphat (S1P) unter anderem wichtige den Zellzyklus regulierende und immunologische Prozesse [22, 42]. Die mannigfaltigen biologischen Wirkungen von S1P werden über fünf verschiedene und hochspezifische G-Protein-gekoppelte Rezeptoren (S1PR 1–5) vermittelt. Während S1P unter anderem pro-mitogene, anti-apoptotische und pro-inflammatorische Funktionen ausübt, haben Sphingosin und Ceramid entgegengesetzte Eigenschaften und wirken pro-apoptotisch und wachstumshemmend. Aufgrund dieser Erkenntnisse schlagen unter anderem die Autoren Spiegel und Milstien den Begriff eines zellulären Sphingolipid-Rheostat vor [9, 42]. Hinsichtlich der weiteren pleiotropen Effekte von S1P unter anderem auf zytoskelettale und kardiovaskuläre Funktionen sei hier auf weiterführende Literatur verwiesen [11].
Im Rahmen des zellulären Sphingolipid-Metabolismus entsteht Sphingosin als Abbauprodukt des membranständigen Sphingomyelin und kann durch Sphingosinkinasen intrazellulär zu S1P phosphoryliert werden. S1P wird von nahezu allen Zellen des menschlichen Körpers produziert und spielt eine wichtige Rolle in der embryonalen Entwicklung des Gefäß- und Nervensystems [33]. Für die Aufrechterhaltung und Kontrolle der S1P-Plasmakonzentrationen scheinen insbesondere Erythrozyten und in geringerem Maße auch Thrombozyten und Endothelzellen verantwortlich zu sein. Die S1P generierende Sphingosin-Kinase 1 (SK1) ist in ihrem inaktivierten Zustand im Zytoplasma lokalisiert und transloziert nach Aktivierung an die Plasmamembran und somit in räumliche Nähe des Substrats Sphingosin [16, 18, 36]. Eine Aktivierung der Sphingosin-Kinase 1 (SK1) ist für diverse Wachstumsfaktoren (unter anderem VEGF), aber auch pro-inflammatorische Zytokine wie TNF-alpha und Interleukin-1 beta beschrieben worden [37, 43]. Als Resultat lokaler pro-inflammatorischer Stimuli kann folglich eine exzessive Produktion von S1P mit konsekutiver auto- und parakriner Aktivierung von S1P-Rezeptoren auftreten.
Bei der Ausschleusung von S1P in den Extrazellulärraum scheinen Transportproteine aus der ATP-binding cassette-(ABC-)Familie eine entscheidende Rolle zu spielen [21, 32]. Im Plasma ist S1P aufgrund seiner Lipophilie an Albumin und Lipoproteine, insbesondere HDL, gebunden. Bedingt durch eine vermehrte Aktivität der S1P degradierenden S1P-Lyase in den lymphatischen Geweben besteht zwischen Serum und den lymphatischen Organen interessanterweise ein signifikanter Gradient [13, 41]. Während die physiologischen Gewebekonzentrationen von S1P in der Regel niedrig sind, finden sich im Plasma Konzentrationen, die deutlich über den Dissoziationskonstanten der S1P-Rezeptoren liegen [13]. Eine enge zeitliche und räumliche Kontrolle der S1P-Level in Geweben und Körperflüssigkeiten ist unter physiologischen Bedingungen entscheidend für eine gerichtete Migration von Zellen des Immunsystems.
Pharmakologische Wirkungsmechanismen von Fingolimod
Der immunsuppressive Sphingosin-1-Phosphat(S1P)-Rezeptor-Modulator Fingolimod wurde Anfang der 90er Jahre von japanischen Forschern durch Modifizierung des im Pilz Isaria sinclairii vorkommenden Wirkstoffs Myriocin synthetisiert [1]. Isaria sinclairii ist bereits lange in der traditionellen chinesischen Medizin bekannt und wird zum Erhalt der „ewigen Jugend“ eingesetzt. Nach oraler Aufnahme wird Fingolimod vorwiegend in der Leber durch die im Zellkern lokalisierte Sphingosin-Kinase 2 (SK2) zum biologisch aktiven Fingolimod-Phosphat (Fingolimod-P) phosphoryliert. Das phosphorylierte Fingolimod besitzt strukturelle Ähnlichkeiten mit dem ubiquitär vorkommenden Sphingolipid Botenstoff S1P [3, 6]. In S1P-Rezeptor-Bindungs-Assays konnte gezeigt werden, dass Fingolimod-Phosphat als hochaffiner Agonist an die Rezeptoren S1PR1 (IC50 0,3 nM), S1PR4 (0,6 nM) und S1PR5 (0,3 nM) und in geringerem Maße auch an den S1PR2 (3,1 nM) bindet [6, 23].
Immunologische Effekte von Fingolimod
Erste Erkenntnisse über immunsuppressive Wirkungen von Fingolimod wurden anhand von Transplantationsmodellen in Ratten gewonnen. Ratten, die mit Fingolimod in Dosen von 0,1 mg/kg Körpergewicht und höher behandelt wurden, zeigten eine signifikant verzögerte Abstoßungsreaktion von Hauttransplantaten und eine verminderte Graft-versus-Host-Reaktion (GvHR) [7, 14, 24].
In Mäusen, bei denen durch konditionalen Knock-out der S1PR1 auf hämatopoetischen Zellen fehlte, wurde ein Auswandern von reifen T-Zellen aus Lymphknoten vollständig verhindert. Die Behandlung von Wildtyp-Mäusen mit Fingolimod führte zu vergleichbaren Effekten und ist quasi mit einem temporären S1PR1-Knock-out-Status auf Lymphozyten zu vergleichen [25, 40]. Diese und weitere experimentelle Arbeiten weisen daraufhin, dass Fingolimod-Phosphat als funktioneller Antagonist des S1PR1 ein Auswandern von autoagressiven T-Lymphozyten in das ZNS verhindert (Abb. 2). Im Fall einer S1P-Rezeptorbindung wird der internalisierte Rezeptor wieder rasch an der Zelloberfläche exprimiert und steht für eine erneute Signaltransduktion zur Verfügung. Vereinbar mit der Rolle eines funktionellen Antagonisten führt die Bindung von Fingolimod-Phosphat hingegen nach endosomaler Internalisierung auch zu einer endgültigen proteosomalen Degradierung des Rezeptors [17, 34].
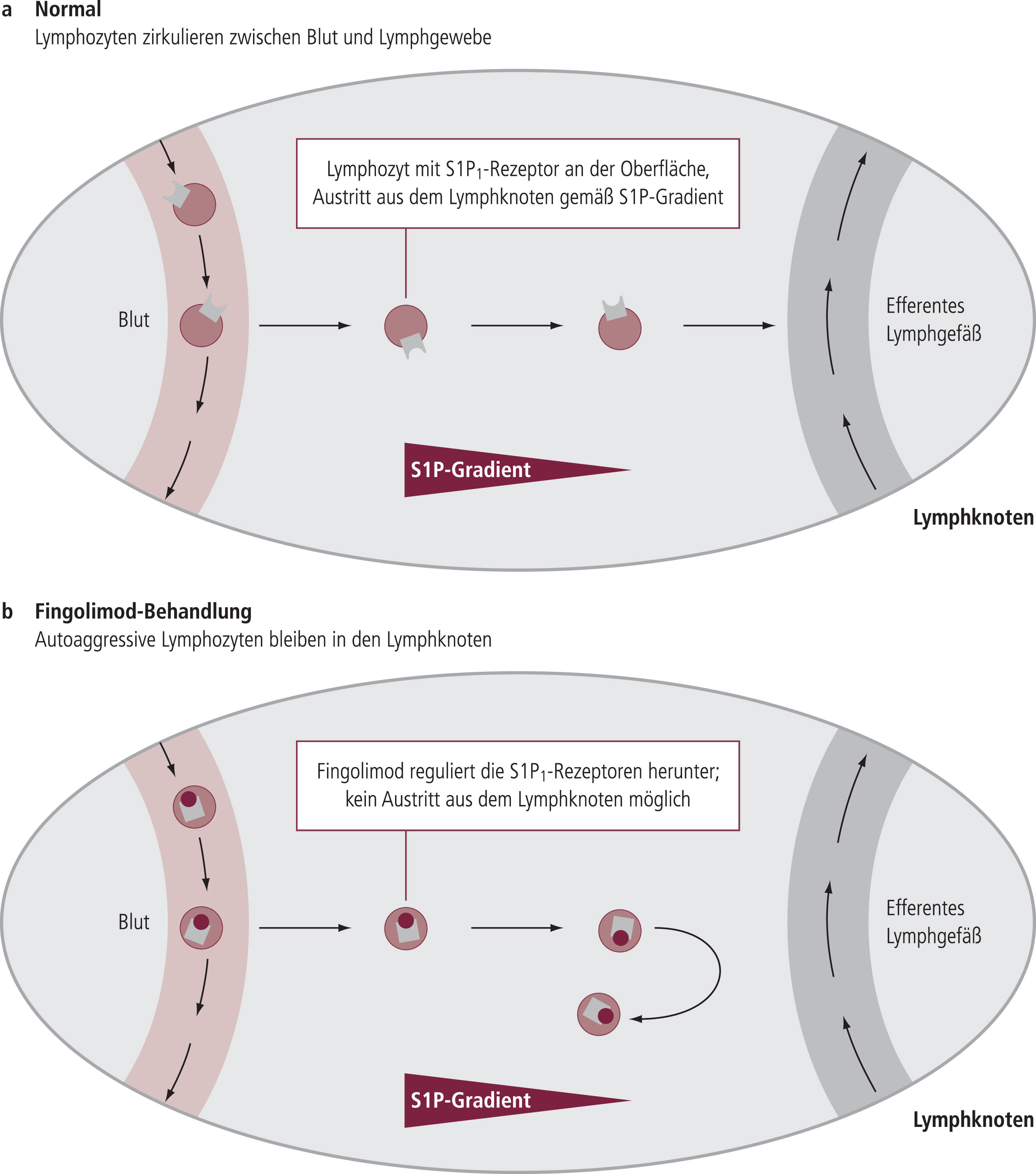
Abb. 2. Fingolimod verhindert den Austritt von Lymphozyten aus dem lymphatischen Gewebe
Interessanterweise beeinträchtigt Fingolimod weder die immunologische Funktion von Lymphozyten an sich noch die Motilität von im ZNS ansässigen T-Zellen [4, 35]. Diese Beobachtung könnte eine wichtige Bedeutung für die Aufrechterhaltung der immunologischen Überwachung im zentralen Nervensystem unter Fingolimod-Therapie haben. Von Relevanz ist außerdem, dass nach Absetzen von Fingolimod die funktionsfähigen Lymphozyten wieder rasch in der Zirkulation auftauchen; auch in diesem Punkt unterscheidet sich Fingolimod von klassischen Immunsuppressiva.
Arbeiten von Mehling et al. weisen zudem daraufhin, dass Fingolimod in der Behandlung der multiplen Sklerose vorzugsweise bestimmte Subpopulationen von CD4+-T-Zellen in den Lymphknoten zurückhält. Hierbei scheinen naive T-Zellen und zentrale Memory-T-Zellen, die den sogenannten „homing receptor“ CCR7 exprimieren, durch Behandlung mit Fingolimod am Auswandern gehindert zu werden, wohingegen die CCR7–-Effektor-Memory-T-Zellen weiterhin im Blut zu finden sind [26]. Ebenso werden langlebige T-Memory-Zellen nicht durch eine Behandlung mit Fingolimod beeinträchtigt. Des Weiteren deuten aktuelle Daten von Mehling et al. daraufhin, dass vor allem die Anzahl der im Blut zirkulierenden pro-inflammatorischen CD4+-Th17-Zellen durch Behandlung mit Fingolimod deutlich reduziert wurde [27]. Hiermit vereinbar fand sich im EAN-Modell der Ratte (GBS-Modell) nach Behandlung mit Fingolimod eine signifikante Reduktion von pro-inflammatorischen Th17-Zellen in den demyelinisierenden Läsionen des N. ischiadicus [45]. Interessanterweise korrelierte hierbei das Ausmaß der perivaskulären Th17-Infiltrate mit der Schwere der neurologischen Ausfälle im EAN-Modell. Diese Daten unterstützen die Hypothesen, dass Th17-Zellen und die von ihnen produzierten Zytokine in der Pathogenese der multiplen Sklerose und entzündlichen Polyneuropathien eine wichtige Rolle spielen könnten und dass Fingolimod ein Auswandern dieser pro-inflammatorischen Zellen in die Zielorgane zu verhindern scheint.
Neben der funktionell antagonistischen Wirkung auf S1PR1 von Lymphozyten gibt es seit längerem Hinweise, dass Fingolimod-Phosphat auch agonistische Effekte auf Endothelzellen von lymphatischen Organen ausübt [23, 39]. Durch eine persistierende Aktivierung des S1PR1 auf Endothelzellen im Sinus von Lymphknoten wird eine Erhöhung der Barrierefunktion vermittelt. Diese agonistische Wirkung von Fingolimod-Phosphat auf Endothelzellen scheint einen weiteren Mechanismus darzustellen, der ein reduziertes Auswandern der Lymphozyten aus den lymphatischen Organen erklärt [5]. Die Dualität von funktionell antagonistischer (Lymphozyten) und agonistischer Wirkweise (Endothel) könnte zudem erklären, warum die pharmakologischen Effekte von Fingolimod nicht durch einen reinen Antagonisten imitiert werden können.
Des Weiteren gibt es Hinweise aus experimentellen Arbeiten, dass Fingolimod auch inhibitorische Wirkungen auf die S1P degradierende S1P-Lyase besitzt und die immunologischen Wirkungen von Fingolimod unter Umständen auch durch direkte Beeinflussung des S1P-Metabolismus und des S1P-Gewebe-Gradienten vermittelt werden [2, 12]. Eine Inhibition der S1P-Lyase und die dadurch vermittelte Aufhebung des S1P-Gewebe-Gradienten führen interessanterweise zu ähnlichen immunologischen Effekten wie Fingolimod-Phosphat; dies stellt somit einen weiteren Ansatzpunkt für zukünftige Therapien zur Behandlung von Autoimmunerkrankungen dar [41].
Die bisher dargelegten Wirkungen von Fingolimod beziehen sich im Wesentlichen auf die peripheren immunologischen Effekte, so dass zu klären bleibt, welche Mechanismen von Fingolimod im zentralen Nervensystem eine Rolle spielen und zu therapeutischen Effekten in der Behandlung der multiplen Sklerose führen. Durch seine lipophile Struktur ist Fingolimod ohne Probleme in der Lage, die Blut-Hirn-Schranke zu überwinden [10]. Neben den peripheren immunsuppressiven Wirkungen, die vorwiegend auf ein vermindertes Einwandern von antigenspezifischen und enzephalitogenen T-Zellen in das ZNS zurückgeführt werden, scheint Fingolimod in der Behandlung der multiplen Sklerose auch direkte neuroprotektive und regenerative Effekte im zentralen Nervensystem auszuüben (Abb. 3) [31].
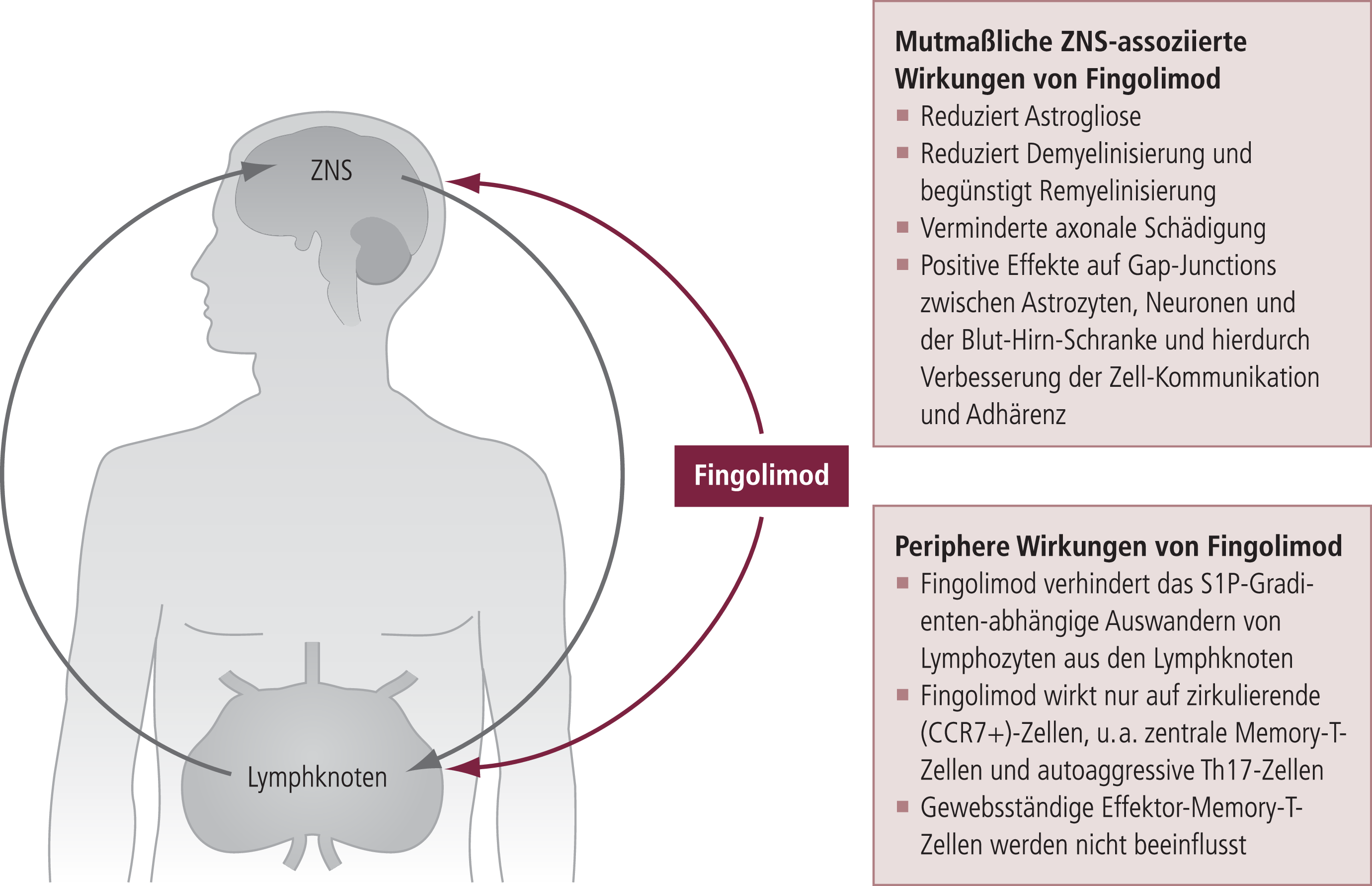
Abb. 3. Dualer Wirkansatz von Fingolimod: periphere und mutmaßliche ZNS-assoziierte Wirkungen. Die hellgrauen Pfeile symbolisieren den physiologischen Weg von Lymphozyten. Fingolimod verhindert das von einem S1P-Gradienten abhängige Auswandern von Lymphozyten aus den Lymphknoten und vermittelt mutmaßliche neuroprotektive und regenerative Effekte im ZNS.
Die neuroprotektive Komponente des Fingolimod und dessen möglicher Einsatz in anderen neuroimmunologischen Erkrankungen
Betrachtet man die vorliegenden Erkenntnisse über die bekannten Signalwege des S1P und die physiologische Verteilung seiner Rezeptoren, überrascht es eigentlich nicht, dass die Wirkungsmechanismen des Fingolimod über die Immunmodulation hinausgehen.
Eine der ersten Arbeiten, die sich mit der Rolle von Sphingosinen im zentralen Nervensystem befasste, konnte die Expression des Rezeptors S1PR5 auf Oligodendrozyten zeigen [15]. Zudem wurde diesem Signalweg eine wichtige Rolle für die oligodendroglialen Differenzierungs- und Reifungsphasen sowie für deren Überleben im Zellverband zugesprochen. Dabei scheint S1P über den S1PR5 in Oligodendrozyten-Vorläuferzellen eher zu einem Rückgang der für die Myelinisierung wichtigen Zellausläufer zu führen, wohingegen in reifen Oligodendrozyten das Überleben über diesen Signalweg gesichert wird.
In Folgearbeiten, die dieser Fragestellung weiter nachgingen, konnte vor allem die Gruppe um den kanadischen Forscher Jack Antel den stadienabhängigen Nachweis von S1PR1- und S1PR3-mRNS in humanen Oligodendrozyten und deren Vorläuferzellen (oligodendrocytic progenitor cells, OPCs) erbringen [28, 29]. Rezeptor-vermittelte Antworten von Fingolimod, wie Myelinisierung, Reifung und Zellüberleben, scheinen dabei einem streng dosis- und zeitabhängigen Schema zu folgen. So führt die längere Behandlung reifer Oligodendrozyten mit niedrigen Konzentrationen von Fingolimod zu einer S1PR5-vermittelten Ausdehnung von Zellausläufern, also dem Markscheiden bildenden Zellteil. Dagegen führt Fingolimod in OPCs bei verlängerter Behandlungszeit über den S1PR1 zu deren Reifung und letztendlich zur Myelinisierung, also über den Rezeptor, der vorwiegend für den lymphozytären Wirkungsmechanismus (s. o.) zuständig ist.
Eine interessante und neuartige Wirkweise des Fingolimod, die direkte Relevanz für neuroregenerative und -protektive Prozesse hat, wurde kürzlich in einem toxischen In-vitro-Modell gezeigt. Dabei wurden murine organotypische Gehirnschnitte verwendet, die in diesem Fall den zerebellären Zellverband inklusive der Gliazellen, Neurone, Axone und deren Markscheiden widerspiegeln [30]. Der mögliche Einfluss des peripheren Immunsystems auf die primär zentralnervösen Zellen wird in diesem Modell effektiv ausgeschlossen und der direkte Einfluss des Fingolimod kann besser beurteilt werden. Um das Regerationspotenzial dieser Gehirnschnitte zu analysieren, wurde Lysolecithin appliziert, was zu einer isolierten Demyelinisierung führt, ohne die Axone zu beschädigen. Morphologisch und funktionell konnte gezeigt werden, dass zwar eine gewisse spontane Remyelinisierung der Axone als Ausdruck der Regenerationsfähigkeit des Gewebes stattfindet, jedoch die mit Fingolimod behandelten Gehirnschnitte eine viel höhere Rate an überlebenden OPCs und deren Ausreifung sowie eine funktionelle Remyelinisierung aufweisen. Dabei konnte auch gezeigt werden, dass diese Wirkungsmechanismen von Fingolimod am ehesten von den „glialen“ Sphingosin-1-Phosphat-Rezeptoren S1PR3 und S1PR5 vermittelt werden [30]. Zeitgleich zur Förderung der Remyelinisierung in den toxisch entmarkten Gehirnschnitten wurde eine deutliche Reduktion der sonst für die „Sklerose-“ oder Narbenbildung verantwortlichen Astrozytose, aber auch ein Rückgang der lokalen Entzündungszellen, der Mikroglia, beobachtet.
Fingolimod in Stichpunkten
– Fingolimod ist der erste Wirkstoff einer neuen Substanzklasse von Immunsuppressiva, die Sphingolipid-Signalwege modulieren.
– Fingolimod verhindert das S1P-Gradienten-abhängige Auswandern von Lymphozyten aus sekundär lymphatischen Organen und führt laborchemisch zu einer deutlichen Lymphopenie.
– Fingolimod hat in vitro direkte neuroregenerative Effekte.
– Fingolimod reduziert die Schubrate und Krankheitsprogression bei schubförmig verlaufender multipler Sklerose und scheint im direkten Vergleich mit Interferon beta-1a i.m. überlegen zu sein.
– Typische Nebenwirkungen von Fingolimod sind Lymphopenie, Infekte der oberen Atemwege und eine transiente Bradykardie.
– Weitere klinische Erfahrungen sind notwendig, um mögliche Kausalzusammenhänge zwischen der Einnahme von Fingolimod und dem Auftreten von Makulaödemen, bösartigen Hautveränderungen und Reaktivierungen von Herpes-Infektionen zu untersuchen.
Bereits in vorklinischen, tierexperimentellen Arbeiten wurde ein positiver Effekt des Fingolimod auf den Krankheitsverlauf der experimentellen autoimmunen Enzephalomyelitis (EAE), des klassischen Tiermodells der MS, beobachtet [6]. Allerdings wurde aufgrund der beobachteten Lymphopenie der gebesserte Krankheitsverlauf der EAE bei Behandlung mit Fingolimod dessen immunsuppressiver Wirkung zugesprochen. Wie kürzlich durchgeführte experimentelle Arbeiten zeigen konnten, führt interessanterweise auch die Behandlung der experimentellen autoimmunen Neuritis (EAN), des Tiermodells der chronisch entzündlichen autoimmunen Neuritis, mit Fingolimod und strukturell ähnlichen S1P-Rezeptor-Modulatoren zu einem deutlich besseren Verlauf der Erkrankung [44, 46]. Auch in diesen Arbeiten wurde die Wirkung mit dem deutlich reduzierten Auftreten von infiltrierenden Entzündungszellen in peripheren Nerven erklärt; eine mögliche Förderung der Markscheiden-Regeneration durch die Schwann-Zellen wurde nicht untersucht. Dennoch zeigen diese Ergebnisse mögliche neue Therapieindikationen von Fingolimod für autoimmun bedingte Erkrankungen auch des peripheren Nervensystems auf und könnten nach klinischer Prüfung den Einsatzbereich für Fingolimod erweitern.
Literatur
1. Adachi K, Chiba K. FTY720 story. Its discovery and the following accelerated development of sphingosine 1-phosphate receptor agonists as immunomodulators based on reverse pharmacology. Perspect Medicin Chem 2008;1:11–23.
2. Bandhuvula P, Tam YY, Oskouian B, Saba JD. The immune modulator FTY720 inhibits sphingosine-1-phosphate lyase activity. J Biol Chem 2005;280:33697–700.
3. Billich A, Bornancin F, Devay P, Mechtcheriakova D, et al. Phosphorylation of the immunomodulatory drug FTY720 by sphingosine kinases. J Biol Chem 2003;278:47408–15.
4. Brinkmann V, Chen S, Feng L, Pinschewer D, et al. FTY720 alters lymphocyte homing and protects allografts without inducing general immunosuppression. Transplant Proc 2001;33:530–1.
5. Brinkmann V, Cyster JG, Hla T. FTY720: sphingosine 1-phosphate receptor-1 in the control of lymphocyte egress and endothelial barrier function. Am J Transplant 2004;4:1019–25.
6. Brinkmann V, Davis MD, Heise CE, Albert R, et al. The immune modulator FTY720 targets sphingosine 1-phosphate receptors. J Biol Chem 2002;277:21453–7.
7. Chiba K, Hoshino Y, Suzuki C, Masubuchi Y, et al. FTY720, a novel immunosuppressant possessing unique mechanisms. I. Prolongation of skin allograft survival and synergistic effect in combination with cyclosporine in rats. Transplant Proc 1996;28:1056–9.
8. Cohen JA, Barkhof F, Comi G, Hartung HP, et al. Oral fingolimod or intramuscular interferon for relapsing multiple sclerosis. N Engl J Med 2010;362:402–15.
9. Cuvillier O, Pirianov G, Kleuser B, Vanek PG, et al. Suppression of ceramide-mediated programmed cell death by sphingosine-1-phosphate. Nature 1996;381:800–3.
10. Foster CA, Howard LM, Schweitzer A, Persohn E, et al. Brain penetration of the oral immunomodulatory drug FTY720 and its phosphorylation in the central nervous system during experimental autoimmune encephalomyelitis: consequences for mode of action in multiple sclerosis. J Pharmacol Exp Ther 2007;323:469–75.
11. Fyrst H, Saba JD. An update on sphingosine-1-phosphate and other sphingolipid mediators. Nat Chem Biol 2010;6:489–97.
12. Hla T. Immunology. Dietary factors and immunological consequences. Science 2005;309:1682–3.
13. Hla T, Venkataraman K, Michaud J. The vascular S1P gradient-cellular sources and biological significance. Biochim Biophys Acta 2008;1781:477–82.
14. Hoshino Y, Suzuki C, Ohtsuki M, Masubuchi Y, et al. FTY720, a novel immunosuppressant possessing unique mechanisms. II. Long-term graft survival induction in rat heterotopic cardiac allografts and synergistic effect in combination with cyclosporine A. Transplant Proc 1996;28:1060–1.
15. Jaillard C, Harrison S, Stankoff B, Aigrot MS, et al. Edg8/S1P5: an oligodendroglial receptor with dual function on process retraction and cell survival. J Neurosci 2005;25:1459–69.
16. Jarman KE, Moretti PA, Zebol JR, Pitson SM. Translocation of sphingosine kinase 1 to the plasma membrane is mediated by calcium- and integrin-binding protein 1. J Biol Chem 2010;285:483–92.
17. Jo E, Sanna MG, Gonzalez-Cabrera PJ, Thangada S, et al. S1P1-selective in vivo-active agonists from high-throughput screening: off-the-shelf chemical probes of receptor interactions, signalling, and fate. Chem Biol 2005;12:703–15.
18. Johnson KR, Becker KP, Facchinetti MM, Hannun YA, et al. PKC-dependent activation of sphingosine kinase 1 and translocation to the plasma membrane. Extracellular release of sphingosine-1-phosphate induced by phorbol 12-myristate 13-acetate (PMA). J Biol Chem 2002;277:35257–62.
19. Kappos L, Antel J, Comi G, Montalban X, et al. Oral fingolimod (FTY720) for relapsing multiple sclerosis. N Engl J Med 2006;355:1124–40.
20. Kappos L, Radue EW, O’Connor P, Polman C, et al. A placebo-controlled trial of oral fingolimod in relapsing multiple sclerosis. N Engl J Med 2010;362:387–401.
21. Kim RH, Takabe K, Milstien S, Spiegel S. Export and functions of sphingosine-1-phosphate. Biochim Biophys Acta 2009;1791:692–6.
22. Maceyka M, Milstien S, Spiegel S. Sphingosine-1-phosphate: the Swiss army knife of sphingolipid signalling. J Lipid Res 2009;50(Suppl):S272–6.
23. Mandala S, Hajdu R, Bergstrom J, Quackenbush E, et al. Alteration of lymphocyte trafficking by sphingosine-1-phosphate receptor agonists. Science 2002;296:346–9.
24. Masubuchi Y, Kawaguchi T, Ohtsuki M, Suzuki C, et al. FTY720, a novel immunosuppressant, possessing unique mechanisms. IV. Prevention of graft versus host reactions in rats. Transplant Proc 1996;28:1064–5.
25. Matloubian M, Lo CG, Cinamon G, Lesneski MJ, et al. Lymphocyte egress from thymus and peripheral lymphoid organs is dependent on S1P receptor 1. Nature 2004;427:355–60.
26. Mehling M, Brinkmann V, Antel J, Bar-Or A, et al. FTY720 therapy exerts differential effects on T cell subsets in multiple sclerosis. Neurology 2008;71: 261–7.
27. Mehling M, Lindberg R, Raulf F, Kuhle J, et al. Th17 central memory T cells are reduced by FTY720 in patients with multiple sclerosis. Neurology 2010;75:403–10.
28. Miron VE, Hall JA, Kennedy TE, Soliven B, et al. Cyclical and dose-dependent responses of adult human mature oligodendrocytes to fingolimod. Am J Pathol 2008;173:1143–52.
29. Miron VE, Jung CG, Kim HJ, Kennedy TE, et al. FTY720 modulates human oligodendrocyte progenitor process extension and survival. Ann Neurol 2008;63:61–71.
30. Miron VE, Ludwin SK, Darlington PJ, Jarjour AA, et al. Fingolimod (FTY720) enhances remyelination following demyelination of organotypic cerebellar slices. Am J Pathol 2010;176:2682–94.
31. Miron VE, Schubart A, Antel JP. Central nervous system-directed effects of FTY720 (fingolimod). J Neurol Sci 2008;274:13–7.
32. Mitra P, Oskeritzian CA, Payne SG, Beaven MA, et al. Role of ABCC1 in export of sphingosine-1-phosphate from mast cells. Proc Natl Acad Sci U S A 2006;103:16394–9.
33. Mizugishi K, Yamashita T, Olivera A, Miller GF, et al. Essential role for sphingosine kinases in neural and vascular development. Mol Cell Biol 2005;25:11113–21.
34. Oo ML, Thangada S, Wu MT, Liu CH, et al. Immunosuppressive and anti-angiogenic sphingosine 1-phosphate receptor-1 agonists induce ubiquitinylation and proteasomal degradation of the receptor. J Biol Chem 2007;282:9082–9.
35. Pinschewer DD, Ochsenbein AF, Odermatt B, Brinkmann V, et al. FTY720 immunosuppression impairs effector T cell peripheral homing without affecting induction, expansion, and memory. J Immunol 2000;164:5761–70.
36. Pitson SM, Moretti PA, Zebol JR, Lynn HE, et al. Activation of sphingosine kinase 1 by ERK1/2-mediated phosphorylation. EMBO J 2003;22:5491–500.
37. Pitson SM, Moretti PA, Zebol JR, Xia P, et al. Expression of a catalytically inactive sphingosine kinase mutant blocks agonist-induced sphingosine kinase activation. A dominant-negative sphingosine kinase. J Biol Chem 2000;275:33945–50.
38. Rammohan KW, Shoemaker J. Emerging multiple sclerosis oral therapies. Neurology 2010;74(Suppl 1): S47–53.
39. Sanchez T, Estrada-Hernandez T, Paik JH, Wu MT, et al. Phosphorylation and action of the immunomodulator FTY720 inhibits vascular endothelial cell growth factor-induced vascular permeability. J Biol Chem 2003;278:47281–90.
40. Sanna MG, Wang SK, Gonzalez-Cabrera PJ, Don A, et al. Enhancement of capillary leakage and restoration of lymphocyte egress by a chiral S1P1 antagonist in vivo. Nat Chem Biol 2006;2:434–41.
41. Schwab SR, Pereira JP, Matloubian M, Xu Y, et al. Lymphocyte sequestration through S1P lyase inhibition and disruption of S1P gradients. Science 2005;309:1735–9.
42. Spiegel S, Milstien S. Sphingosine-1-phosphate: an enigmatic signalling lipid. Nat Rev Mol Cell Biol 2003;4:397–407.
43. Xia P, Wang L, Moretti PA, Albanese N, et al. Sphingosine kinase interacts with TRAF2 and dissects tumor necrosis factor-alpha signaling. J Biol Chem 2002;277:7996–8003.
44. Zhang Z, Zhang ZY, Fauser U, Schluesener HJ. FTY720 ameliorates experimental autoimmune neuritis by inhibition of lymphocyte and monocyte infiltration into peripheral nerves. Exp Neurol 2008;210:681–90.
45. Zhang ZY, Zhang Z, Schluesener HJ. FTY720 attenuates lesional interleukin-17(+) cell accumulation in rat experimental autoimmune neuritis. Neuropathol Appl Neurobiol 2009;35:487–95.
46. Zhang ZY, Zhang Z, Zug C, Nuesslein-Hildesheim B, et al. AUY954, a selective S1P(1) modulator, prevents experimental autoimmune neuritis. J Neuroimmunol 2009;216:59–65.
*Diese Autoren haben gleichwertig zum Manuskript beigetragen
Dr. Bernhard F. Décard, Prof. Dr. Ralf Gold, Neurologische Klinik der Ruhr-Universität Bochum im St. Josef-Hospital, Gudrunstraße 56, 44791 Bochum, E-Mail: b.decard@klinikum-bochum.de Dr. Aiden Haghikia, Neurologische Klinik der Ruhr-Universität Bochum im St. Josef-Hospital, Gudrunstraße 56, 44791 Bochum und Weatherall Institute of Molecular Medicine, Department of Clinical Neurology, University of Oxford
Fingolimod (FTY720) in use for neuroimmunologic disorders
A series of novel drugs about to be approved for the treatment of multiple sclerosis (MS) has just passed or is being subject of phase III clinical trials. A common feature of the majority of them is the oral usage and according to the available data their presumable safety. Furthermore, they promise to be superior over the so far available injectable drugs beta-interferon (IFNb) and glatirameracetate (GLAT) and exert new pharmacomechanisms. Recently, the results of two approval studies on effect and safety of fingolimod (FTY720) were released: both studies showed a significant reduction of relapse rate and MRI activity in fingolimod treated MS patients compared to either placebo (FREEDOMS study) or intramuscular injected IFNb-1a (TRANSFORMS study). Based on the benefit-risk assessment of fingolimod (0,5 mg/day), the FDA supports the use of this novel therapeutic option as first-line therapy in the treatment of patients with relapsing multiple sclerosis.
In this article the authors summarize the present study results and try to assess a clinical outlook for the use of fingolimod. Furthermore we provide an overview of so far elicited sphingolipid-signalling pathways and the involvement of fingolimod in immunologic and non-immunologic or neuroprotective mechanisms.
Key words: Fingolimod, FTY720, multiple sclerosis, neuroimmunology, sphingosine-1-phosphate, S1P
Psychopharmakotherapie 2010; 17(05)
