Hermann Stefan, Erlangen
Epilepsien stellen als häufige neurologische Erkrankung ein großes Belastungspotenzial für Betroffene und deren Angehörige dar. Durch die bisher verfügbaren Antiepileptika sind etwa 70% der Patienten befriedigend behandelbar. Es bleibt jedoch ein großer Anteil von Patienten, bei denen die Anfallskontrolle nicht ausreichend ist oder unerwünschte Nebenwirkungen auftreten. Allergische Hautreaktionen, Stevens-Johnson-Syndrom, Knochenmarkstoxizität und Hyponatriämien gehören zum Nebenwirkunsspektrum bereits vorhandener Substanzen aus der Dibenzazepin-Carbamid-Gruppe und waren Anlass für die Entwicklung neuer Wirkstoffe durch Abwandlung der chemischen Struktur.
Eslicarbazepinacetat hat mit den bereits vorhandenen Molekülen Carbamazepin und Oxcarbazepin den Dibenzazepin-Kern mit dem Carboxamid-Substituenten gemein, weist jedoch an Position 10/11 eine abweichende Struktur auf (Abb. 1). Während Carbamazepin in einem ersten Schritt durch Oxidierung zu Carbamazepin-10,11-epoxid verstoffwechselt wird, entsteht aus Oxcarbazepin durch Hydroxylierung das Monohydroxyderivat (MHD), und zwar entstehen im Verhältnis 1:4 die Enantiomere R-Licarbazepin und S-Licarbazepin. Die Stereoisomere unterscheiden sich in ihrer pharmakologischen Wirkung. So weist S-Licarbazepin im MES(maximaler Elektroschock)-Modell eine effektive Anfallskontrolle von 100±0,0% auf, R-Licarbazepin dagegen nur von 5,9±1,8% [6]. S-Licarbazepin wurde deshalb weiterentwickelt und erhielt als Wirkstoff den internationalen Freinamen (INN) Eslicarbazepin. Eslicarbazepinacetat ist sein Essigsäureester; es wird im Verlauf eines First-Pass-Metabolismus fast vollständig zu Eslicarbazepin hydrolysiert (Abb. 1) [2, 9].
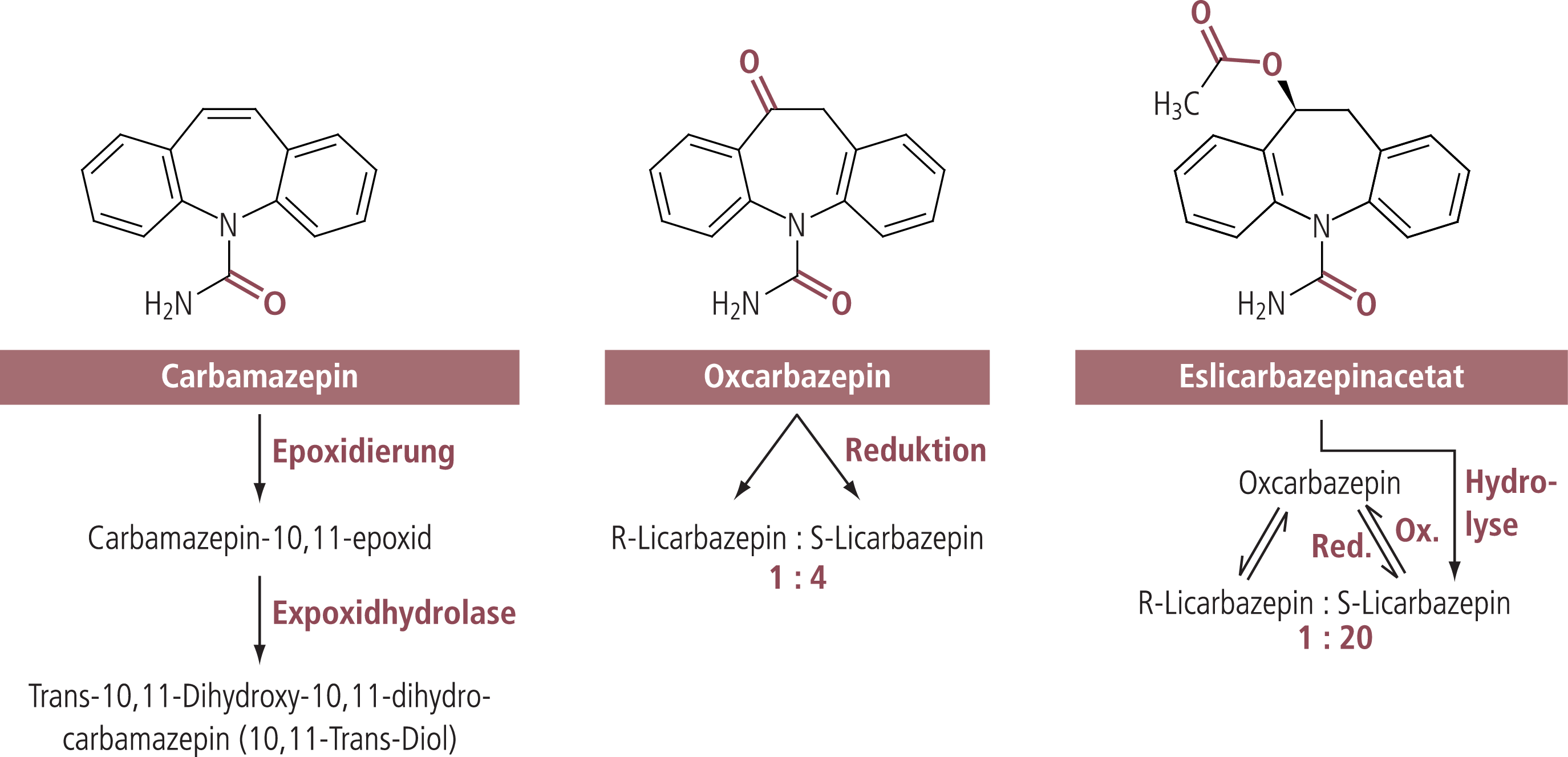
Abb. 1. Chemische Struktur von Carbamazepin, Oxcarbazepin und Eslicarbazepinacetat
Der exakte Wirkungsmechanismus von Eslicarbazepinacetat (ESL) ist nicht im Detail entschlüsselt. Als Wirkung wird eine kompetitive Bindung an der Rezeptor-Site 2 spannungsabhängiger Natriumkanäle angenommen, die zu einer Stabilisierung (Verlängerung des inaktivierten Zustands) des Natriumkanals führt und damit eine funktionelle Selektivität für die Hemmung repetitiver neuronaler Entladungen erreicht [8]. Eslicarbazepinacetat hat in mehreren Tiermodellen zur Abschätzung seiner antikonvulsiven Potenz protektive Eigenschaften gezeigt, beispielsweise im maximalen Elektroschocktest und in einem Modell zur Kindling-Epileptogenese [13]. Im Modell zur Kindling-Epileptogenese verzögerte sich das Kindling durch die intraperitoneale Gabe von Eslicarbazepinacetat in Dosierungen von 30 und 100 mg/kg. Die Schwelle zur Auslösung generalisierter Anfälle erhöhte sich um 217% bzw. 280% [22]. Gegenüber verschiedenen Chemokonvulsiva (Pentetrazol [Metrazol], Bicucullin, Picrotoxin und 4-Aminopyridin) weist Eslicarbazepinacetat antikonvulsive Wirksamkeit auf [4] (Tab. 1). Das Verhältnis zwischen Wirksamkeit und Toxizität zeigt einen günstigen protektiven Index (>117 im Vergleich zu 62,4 bei Oxcarbazepin und 32,8 bei Carbamazepin) [6].
Tab. 1. Wirksamkeit von Eslicarbazepinacetat in verschiedenen Tiermodellen
|
MES-Test |
|
(Maximaler Elektroschock bei Mäusen; Modell für sekundär generalisierte Anfälle) – In 100% bzw. 90,6±9,4% der untersuchten Fälle durch 15 mg/kg Eslicarbazepinacetat [Benes et al., J Med Chem 1999;42:2582–7. Learmonth et al. Eur J Med Chem 2001;36:227–36] |
|
Hippocampale Mikroperfusion mit Chemokonvulsiva |
|
(Modell für fokale Anfälle) – Picrotoxin: in 75% der untersuchten Fälle durch 30 mg/kg Eslicarbazepinacetat – Latrunculin A: in 100% der untersuchten Fälle durch 10 mg/kg Eslicarbazepinacetat |
|
Kindling |
|
(Modell für Epileptogenese) – Corneal Kindling: signifikante Verzögerung des Kindlings durch 30 bzw. 100 mg/kg Eslicarbazepinacetat; Erhöhung der Schwelle für generalisierte Anfälle um 217 bzw. 280% – Amygdala-Kindling: signifikante Erhöhung der Anfallsschwelle durch 200 bzw. 300 mg/kg Eslicarbazepinacetat auf 289 bzw. 1319% |
Pharmakokinetik
Nach oraler Gabe wird Eslicarbazepinacetat durch Hydrolyse im First-Pass-Metabolismus rasch und umfassend durch intestinale und hepatische Esterasen hauptsächlich zu Eslicarbazepin verstoffwechselt [2]. Die Bioverfügbarkeit beträgt 90% [20]. Es liegt eine konzentrationsunabhängige Bindung an Plasmaproteine ≤30% vor [23]. Eslicarbazepin wird zum größten Teil unverändert oder (zu etwa einem Drittel) als inaktives Glucuronid-Konjugat ausgeschieden; beide Formen machen gemeinsam etwa 93% aller im Urin nachgewiesenen Metaboliten aus [20]. Nur ein geringer Teil (1%) wird zu Oxcarbazepin metabolisiert [1]. Dieses wird teilweise zu R-Licarbazepin verstoffwechselt. Im Verlauf des Abbaus von Eslicarbazepinacetat ergibt sich deshalb ein Verhältnis R-Licarbazepin zu S-Licarbazepin von 1:20 [1, 4]. Der Zeitpunkt der Plasmaspitzenkonzentration (tmax) liegt zwischen ein bis vier Stunden nach oraler Gabe, im Mittel bei drei Stunden. Der Steady-State wird nach vier bis fünf Tagen erreicht, die effektive Halbwertszeit wird mit 20 bis 24 Stunden angegeben. Die Pharmakokinetik ist unabhängig von Nahrungsaufnahme, Alter oder Geschlecht (Tab. 2).
Tab. 2. Pharmakokinetische Kenngrößen von Eslicarbazepinacetat
|
Bioverfügbarkeit 90%a |
|
tmax 1 bis 4 Stunden nach oraler Gabeb |
|
Konzentrationsabhängige Bindung an Plasmaproteine ≤30%c |
|
Steady State nach 4 bis 5 Tagend,e |
|
Effektive Halbwertszeit 20 bis 24 Stundenb,d |
|
Lineare Pharmakokinetikd |
|
Dosisproportionalität im Bereich zwischen 400 und 2400 mgd |
|
Nahezu vollständig renale Elimination (93% der Ausgangssubstanz finden sich als Eslicarbazepin oder Eslicarbazepinglucuronid im Urin)d,e,f |
|
Pharmakokinetik unabhängig von Nahrungsaufnahmea, Alterf,g oder Geschlechth |
aMaia et al. Drugs R D 2005;6:201–6. bAlmeida, Soares-da-Silva. Drugs R D 2003;4:269–84. cVaz-da-Silva et al. Epilepsia 2005;46:191. dAlmeida, Soares-da-Silva. J Clin Pharmacol 2004;44:905–18. eMaia et al. Int J Clin Pharmacol Ther 2008;46:119–30. fAlmeida et al. J Clin Pharmacol 2005;45:1062–6. gAlmeida et al. J Clin Pharmacol 2008;48:966–77. hFalcao et al. Biopharm Drug Dispos 2007;28:249–56.
Da die Ausscheidung fast vollständig renal erfolgt, ist bei eingeschränkter Nierenfunktion (Creatinin-Clearance ≤60 ml/min) eine Dosisreduzierung erforderlich [12]. Bei Patienten mit leichter oder mäßiger Leberfunktionsstörung ist keine Dosisanpassung erforderlich [13].
Der Vergleich der Steady-State-Pharmakokinetik von Eslicarbazepinacetat nach einmal oder zweimal täglicher Verabreichung über acht Tage zeigte, dass die mittlere Plasmakonzentration bei einmal täglicher Gabe um 33% höher lag als bei zweimal täglicher Gabe [3]. Aufgrund der relativ langen Halbwertszeit kann Eslicarbazepinacetat als einmal tägliche Gabe verabreicht werden.
Interaktionen
Aufgrund der bisherigen Datenlage ist von einem nur geringen Interaktionspotenzial mit anderen Antiepileptika auszugehen. Eslicarbazepinacetat weist eine nur geringe oder keine relevante Wirkung auf die Aktivität der meisten Cytochrom-P450-(CYP-)Isoenzyme (CYP1A2, CYP2A6, CYP2B6, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A4, CYP4A9/11), UDP-Glucuronosyltransferasen (UGT1A) und der Epoxidhydrolase auf. Die CYP2C9-vermittelte Tolbutamid-4-Hydroxylierung wird um 38% gehemmt und UGT1A1 um 39% aktiviert.
Es fand sich keine signifikante Beeinflussung der Plasmaspiegel von Carbamazepin, Levetiracetam, Lamotrigin, Topiramat oder Valproinsäure durch 400 und 800 mg Eslicarbazepinacetat. Mit 1200 mg Eslicarbazepinacetat zeigte sich eine geringe Beeinflussung des Verhältnisses von Lamotrigin und Topiramat [7, 15]. Eslicarbazepinacetat verursacht eine geringe Abnahme der systemischen Exposition gegenüber Topiramat [21]. Dosisanpassungen sind bei Komedikation von Eslicarbazepinacetat mit Lamotrigin oder Topiramat im Allgemeinen nicht erforderlich.
Valproinsäure, Gabapentin, Clobazam oder Levetiracetam beeinflussten die Clearance von Eslicarbazepinacetat bei Dosierungen zwischen 400 mg und 1200 mg/Tag nicht. Allerdings erschien die Clearance durch Carbamazepin und Phenobarbital sowie Lamotrigin und Topiramat erhöht [14, 15]. Diese Zunahme wurde aber nicht als klinisch relevant beurteilt.
Die Kombination von Eslicarbazepinacetat mit Phenytoin führte im Mittel zu einem 31- bis 33%igen Abfall der Verfügbarkeit von Eslicarbazepinacetat und einem 31- bis 35%igen Anstieg der Phenytoin-Exposition. Bei Kombinationstherapie könnte also hier eine Dosisanpassung der Medikamente erforderlich sein [13].
Hinsichtlich Digoxin ergaben sich keine Hinweise für Interaktionen, bei S-Warfarin zeigte sich ein geringer, aber statistisch signifikanter Einfluss (Abnahme der Warfarin-Exposition um 23%). Daher sollte bei Kombinationstherapie der Gerinnungswert gemessen werden. Die Serumkonzentration von Ethinylestradiol und Levonorgestrol wird bei Kombination mit Eslicarbazepinacetat (1200 mg/Tag) reduziert. Daher ist eine nichthormonelle Antikonzeption zu empfehlen.
Klinische Erfahrungen
Eslicarbazepinacetat wurde bisher in der Add-on-Therapie bei Patienten mit fokalen Epilepsien im Erwachsenenalter eingesetzt. Hierbei handelt es sich um eine Phase-II-Studie und drei Phase-III-Studien, die als multizentrische, randomisierte, doppelblinde, Plazebo-kontrollierte Studie oder als Follow-up-Beobachtung zum Langzeitverlauf duchgeführt wurden (Phase II: BIA-2093-201, Phase III: BIA-2093-301, -302, -303) [5, 10, 11, 17]. Eine Übersicht über die Phase-III-Studien gibt Abbildung 2. Nach einer retrospektiven Baseline-Phase zur Ermittlung der durchschnittlichen Anfallsfrequenz wurde aufdosiert, je nach Studie mit unterschiedlicher Geschwindigkeit und Zieldosis – zwischen 400 und 1200 mg/Tag – oder Plazebo, später schließlich abdosiert. Teilnehmen konnten Patienten in der Altersgruppe von 18 bis 65 Jahren mit schwer behandelbarer fokaler Epilepsie (mindestens vier oder mehr fokale Anfälle pro Monat trotz Behandlung mit ein oder zwei anderen Antiepileptika).

Abb. 2. Studien-Designs der Phase III 1) [10], 2) [5], 3) [17]; QD: einmal täglich; AED: Antiepileptikum
In der ersten Studie (Phase II) waren Patienten mit Carbamazepin und Oxcarbazepin ausgeschlossen [11]. Die Dosierung in dieser Studie erfolgte als Einmal- oder Zweimalgabe. Insgesamt nahmen 143 Patienten teil. Die Ansprechrate, bestimmt als mindestens 50%ige Abnahme der Anfallsfrequenz pro 4-Wochen-Zeitraum, lag bei täglicher Einmalgabe signifikant höher als mit Plazebo (54% vs. 28%; p=0,008). Die Ansprechrate mit Zweimalgabe (41%) war im Vergleich mit Plazebo nicht signifikant verschieden. Anfallsfreiheit wurde mit Eslicarbazepinacetat (einmal und zweimal tägliche Gabe) signifikant häufiger erreicht als mit Plazebo (24% vs. 9%). Nebenwirkungen (Kopfschmerz, Schwindel, Übelkeit) waren bei Zweimalgabe häufiger als bei Einmalgabe. Insgesamt gab es eine niedrige Inzidenz dosisabhängiger Nebenwirkungen mit überwiegend leichter bis moderater Intensität.
Aufgrund der Ergebnisse der Phase-II-Studie mit vorteilhafter Wirkung und günstigem Nebenwirkungsprofil bei Einmalgabe wurden die Phase-III-Studien nur mit einmal täglicher Verabreichung durchgeführt. Dabei war die Einnahme von Oxcarbazepin oder Felbamat ein Ausschlusskriterium. Bei allen drei im Design vergleichbaren, randomisierten, doppelblinden, Plazebo-kontrollierten, multizentrischen Phase-III-Studien wiesen die mit Eslicarbazepinacetat 800 und 1200 mg in Add-on-Therapie behandelten Patienten in der 12-wöchigen Erhaltungsphase signifikant niedrigere Anfallshäufigkeiten auf als die Patienten in der Plazebogruppe (Abb. 3) [5, 10, 17]. Die gepoolte Analyse der Phase-III-Studien ergab bei Patienten mit 1200 mg Eslicarbazepinacetat eine Responderrate von 44% (p<0,001) im Vergleich zu 22% unter Plazebo. Zwischen Plasma-Eslicarbazepin-Konzentration und Wirksamkeit schien ein Zusammenhang zu bestehen. So wurde in der kombinierten Analyse Anfallsfreiheit bei 400 mg in 1,6%, bei 800 mg in 3,8% und bei 1200 mg in 7,5% der Fälle erreicht.
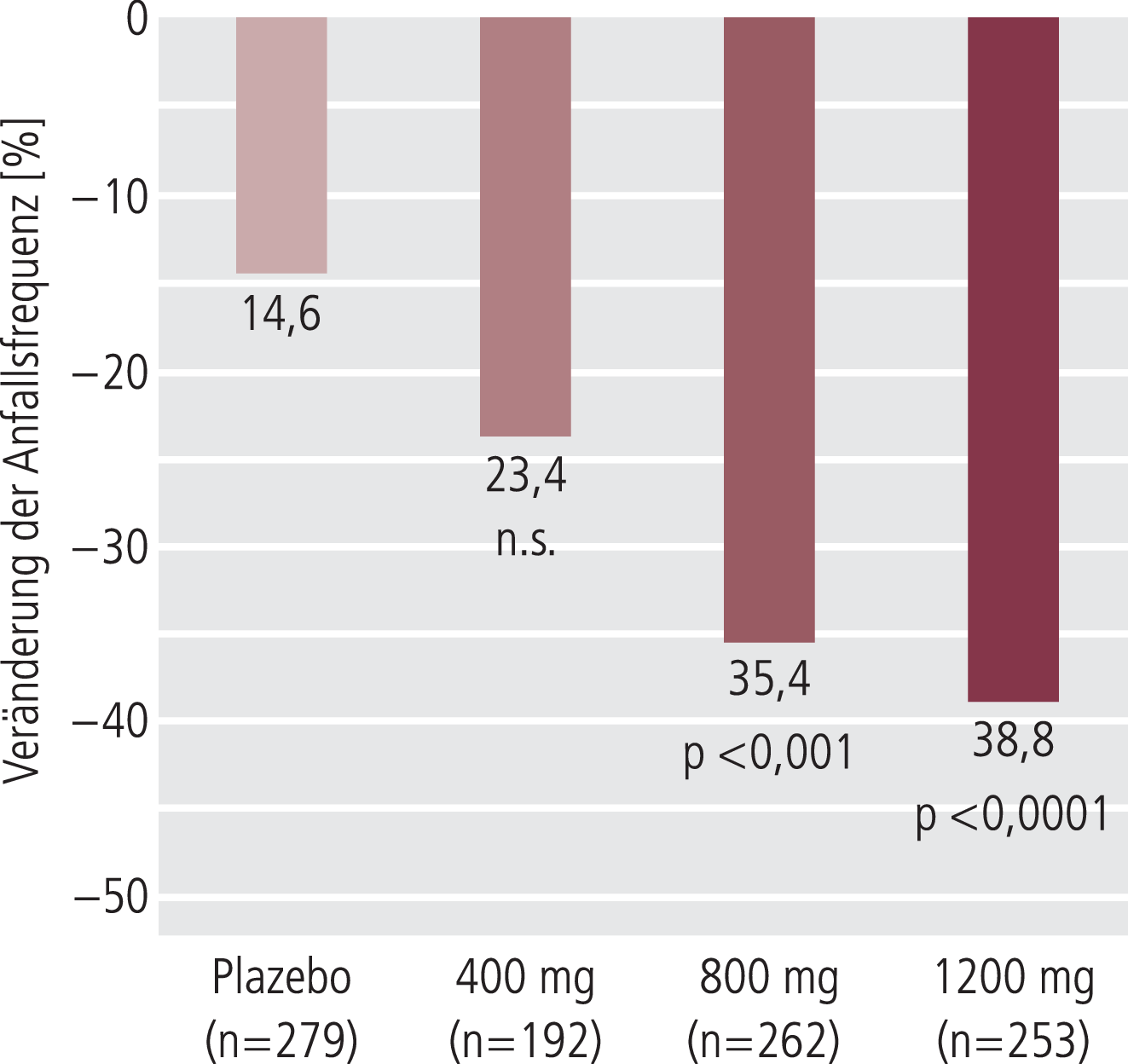
Abb. 3. Relative Abnahme der Anfallsfrequenz (Median) über die 12-wöchige Erhaltungsphase unter 400, 800, 1200 mg Eslicarbazepinacetat im Vergleich zu Plazebo (kombinierte Analyse der drei Phase-III-Studien, Intention-to-treat-Population) [nach 12]
Als unerwünschte Ereignisse fanden sich hauptsächlich zentralnervöse Nebenwirkungen in Form von Schwindelgefühl, Kopfschmerzen oder Müdigkeit (13,7%, 10,8%, 9,8%) bei der höchsten Dosierung von 1200 mg/Tag Eslicarbazepinacetat (Plazebo: 2%, 5% und 2%). Die zentralnervösen Nebenwirkungen waren in 94% leicht bis mäßig (Studie -301).
Ein Natriumspiegel ≤125 mmol/l wurde bei vier Patienten registriert. Diese Patienten erhielten zusätzlich Carbamazepin in einer Dosierung von ≥1000 mg als Begleitmedikation und hatten einen Natriumspiegel von ≤135 mmol/l vor Eindosierung von Eslicarbazepinacetat.
In der offenen Verlängerung der Studien -301, -302 und -303 wiesen die Patienten nach einem Jahr eine deutliche und anhaltende Reduktion der Anfallshäufigkeit auf (Retentionsrate 73,5%) [16, 18, 19]. Hierbei war die mittlere relative Anfallsreduktion konstant.
Therapie mit Eslicarbazepinacetat in der Praxis
Bisher liegen nur begrenzte Erfahrungen mit der Kombinationstherapie von Eslicarbazepinacetat bei fokalen Epilepsien vor. Sie beziehen sich zurzeit auf das Erwachsenenalter. Empfohlen wird eine Initialdosis von 400 mg, die nach ein bis zwei Wochen auf 800 mg als Einmalgabe abends angehoben werden kann. Weitere Dosiserhöhungen auf 1200 mg sind je nach Anfallsreduktion und Verträglichkeit möglich. Bei der Therapie mit Eslicarbazepinacetat ist von drei Ausgangssituationen auszugehen:
- Zusatztherapie bei bestehender Vorbehandlung
- Umstellung von Oxcarbazepin auf Eslicarbazepinacetat in Kombinationsbehandlung
- Umstellung von Carbamazepin auf Eslicarbazepinacetat in Kombinationstherapie
Bei Hinzufügen von Eslicarbazepinacetat zur Medikation bei Patienten, die nicht mit Carbamazepin und Oxcarbazepin behandelt wurden, sind die Dosierungsempfehlungen relativ einfach umzusetzen. Allerdings sind die Tabletten für die Feindosierung noch nicht optimal geeignet, da die Dosierungsschritte zu groß sind.
Bei Umstellung von Oxcarbazepin auf Eslicarbazepinacetat werden Umstellungsdosierungen im Verhältnis 0,7:1 bis 1:1 empfohlen. Hier müssen noch weitere Erfahrungen gesammelt werden, insbesondere bei hoher Oxcarbazepin-Dosierung von 2400 mg, da eine äquivalente Eslicarbazepinacetat-Dosierung ein Off-Lable-Use wäre.
Bezüglich Nebenwirkungen ist zu vermerken, dass Hyponatriämien nach Zulassung bisher nur selten beobachtet wurden.
Literatur
1. Almeida L, Soares-da-Silva P. Safety, tolerability, and pharmacokinetic profile of BIA 2-093, a novel putative antiepileptic, in a rising multiple-dose study in young healthy humans. J Clin Pharmacol 2004;44:905–18.
2. Almeida L, Falcao A, Maia J, Mazur D, et al. Single-dose and steady-state pharmacokinetics of eslicarbazepine acetate (BIA2-093) in healthy elderly and young subjects. J Clin Pharmacol 2005;45:1062–6.
3. Almeida L, Falcao A, Maia J, Vaz-da-Silva P. Steady-state pharmacokinetics of once-daily and twice-daily regimens of eslicarbazepineacetate (BIA 2-093) in healthy subjects. (Abstract No. 2.102). Epilepsia 2006;47(Suppl 4):154.
4. Almeida L, Soares-da-Silva P. Eslicarbazepine acetate (BIA 2-093). Neurotherapeutics 2007;4:88–96.
5. Ben-Menachem E, Gabbai AA, Hufnagel A, Maia J, et al. Eslicarbazepine as adjunctive therapy in adult patients with partial epilepsy. Epilepsy Res 2010;89:278–85.
6. Benes J, Parada A, Figueirodo AA, Alves PC, et al. Anticonvulsant and sodium channel blocking properties of novel 10,11-dihydro-5H-dibenz[b,f]azepine-5-carboxamide derivates. J Med Chem 1999;42:2582–7.
7. Bialer M, Falcao A, Maia J, Almeida L, et al. Investigation of the influence of eslicarbazepine acetate on the plasma concentration of concomitant antiepileptic drugs in partial epilepsy (Abstract No. E397). Epilepsia 2009;50(Suppl 4):156. Plus poster presented at the 8th European Congress on Epileptology (ECE), Berlin, Germany, Sep 21–25, 2008.
8. Bonifacio MJ, Sheridan RD, Parada A, Cunha RA, et al. Interaction of the novel anticonvulsant BIA 2-093 with voltage-gated sodium channels: comparison with carbamazepine. Epilepsia 2001;42:600–8.
9. De Boer HM, Mula M, Sander JW. The global burden and stigma of epilepsy. Epilepsy Behav 2008;12:88–96.
10. Elger C, Halász P, Maia J, Almeida L, et al. Efficacy and safety of eslicarbazepine acetate as adjunctive treatment in adults with refractory partial-onset seizure: a randomized, double-blind, placebo-controlled, parallel-group phase III study: Epilepsia 2009;50:454–63.
11. Elger C, Bialer M, Cramer JA, Maia J, et al. Eslicarbazepine acetate: a double blind, add-on, placebo-controlled exploratory trial in adult patients with partial onset seizures. Epilepsia 2007;48:497–504.
12. European Medicines Agency, CHMP assessment report for Zebinix: 2009: Available from URL: www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/000988/WC500047229.pdf (letzter Zugriff 24.08.2010).
13. European Medicines Agency. Zebinix (eslicarbazepine acetate): summary of product characteristics. Available from URL:www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Product_Information/human/000988/WC500047225.pdf (letzter Zugriff 24.08.2010)
14. Falcao A, Fuseau E, Fabre M, Maia J, et al. Population pharmacokinetics of AEDs after co-administration with eslicarbazepine acetate in adult patients with refractory partial epilepsy (Abstract No. 3.203). Epilepsia 2008;49(Suppl 7):430.
15. Fusseau E, Fabre M, Falcao A, Maia J, et al. Population pharmacokinetics of eslicarbazepine acetate in adult patients with refractory partial seizures (Abstract No. 3.207). Epilepsia 2008;49(Suppl 7):432.
16. Gabbai A, Ben-Menachem E, Maia J, Almeida L, et al. Long-term treatment of partial epilepsy with eslicarbazepine acetate (ESL): results of an one-year open-label extension of study BIA-2093-302 (Abstract No. 3.208). Epilepsia 2008;49(Suppl 7):432–3.
17. Gil-Nagel A, Lopes-Lima J, Almeida L, Maia J, et al. Efficacy and safety of 800 and 1 200 mg eslicarbazepine acetate as adjunctive treatment in adults with refractory partial-onset seizures. Acta Neurol Scand 2009;120:281–7.
18. Halasz P, Elger C, Guekht A, Maia J, et al. Long-term treatment of partial epilepsy with eslicarbazepine acetate (ESL): results of a one-year open-label extension to study BIA-2093-301 (Abstract No. 3.213). Epilepsia 2008;49(Suppl 7):435–6.
19. Lopes-Lima J, Gil-Nagel A, Maia J, Almeida L, et al. Longterm treatment of partial epilepsy with eslicarbazepine acetate (ESL): results of a one-year open-label extension of study BIA-2093-303 (Abstract No. 3.227). Epilepsia 2008;49(Suppl 7):441–2.
20. Maia J, Almeida L, Falcao A, Soares E, et al. Effect of renal impairment on the pharmacokinetics of eslicarbazepine acetate. Int J Clin Pharmacol Ther 2008;46:119–30.
21. Nunes T, Sicard E, Almeida L, Huguet J, et al. Pharmacokinetic interaction between eslicarbazepine acetate and topiramate in healthy volunteers (Abstract No. T225). Epilepsia 2009;50(Suppl 4):108. Plus poster presented at the 8th European Congress on Epileptology (ECE), Berlin, Germany, Sep 21–25, 2008.
22. Potschka H, Pekcec A, Soares-da-Silva P. Inhibition of kindling progression by eslicarbazepine acetate and licarbazepine. (Abstract No. p071) Epilepsia 2007;48(Suppl 7):2–177.
23. Vaz-da-Silva M, Costa R, Soares E, Maia J, et al. Effect of eslicarbazepine acetate on the pharmacokinetics of digoxin in healthy subjects: Fundam Clin Pharmacol 2009;23:509–14.
Prof. Dr. med. Hermann Stefan, Zentrum Epilepsie Erlangen, Neurologie Klinik, Schwabachanlage 6, 91054 Erlangen, E-Mail: hermann.stefan@uk-erlangen.de
Eslicarbazepine acetate: A further pharmacological development as adjunctive therapy of focal epilepsy
Within the last two decades a multitude of antiepileptic drugs of the so-called new generation has been introduced. Because of a more favourable pharmacokinetic and a better side effect profile some of these newer formulations have replaced the role of older substances as best choice in the broad treatment spectrum of epilepsies. Now, since October 2009 a new antiepileptic drug, eslicarbazepine acetate (ESL), has been released in Germany for adjunctive therapy of focal epilepsy in adults. Contrary to other new antiepileptic drugs whose novel anticonvulsant efficacy promised possible therapeutic progress, ESL – as a result of consequent development of dibenzazepine formulations, which also carbamazepine and oxcarbazepine belong to – represents a substance of reliable and good efficacy in the treatment of focal epilepsy. Compared with those preceding drugs ESL by its pharmacological optimization of the initial substances promises many advantages regarding tolerability and handling in every day work. Efficacy and tolerability of ESL have been evaluated in three extended randomised double-blind studies. The results of all three studies consistently document besides a favourable profile of tolerability a significant advantage of efficacy of ESL in once daily application compared to a placebo group of patients with pharmacoresistant epilepsy. Data from prolonged open studies over a 12 months period document a persistent seizure reduction with ESL associated with a positive effect on quality of life and mood.
This article presents an overview of pharmacological characteristics, current data of the relevant studies referring to efficacy, safety and tolerability.
Key words: Antiepileptic therapy, pharmacological further development, eslicarbazepine acetat, profile of side effects
Psychopharmakotherapie 2010; 17(05)
