Priv.-Doz. Dr. Dieter Angersbach, Wolfratshausen
Blonanserin ist ein neues, seit 2008 in Japan und Süd-Korea zugelassenes, atypisches Antipsychotikum, das strukturell nicht mit anderen bereits zugelassenen Substanzen verwandt ist. Wie andere neue Antipsychotika (z. B. Olanzapin, Ziprasidon, Aripiprazol, Paliperidon), ist Blonanserin ein potenter Antagonist von 5-HT2- und D2-Rezeptoren und ein schwächerer Antagonist von α1-Rezeptoren. Die Substanz bindet nicht an Histamin- und Muscarin-Rezeptoren. Wegen des selektiven pharmakologischen Profils wird eine gute Verträglichkeit erwartet. Blonanserin (AD 5432) wurde in Japan entwickelt; bei japanischen Patienten zeigte die Substanz in einem doppelblinden Plazebo-kontrollierten Vergleich mit Haloperidol gute Wirksamkeit in der Behandlung sowohl von positiven als auch von negativen Symptomen.
In der vorliegenden Doppelblindstudie wurden nun Wirksamkeit und Verträglichkeit von Blonanserin in drei verschiedenen Dosierungen im Vergleich zu Plazebo und Haloperidol bei nicht-japanischen Patienten untersucht.
Die Studie wurde von Juni bis Dezember 2003 von 37 Zentren in den USA und einigen europäischen Ländern durchgeführt.
Studiendesign
Eingeschlossen wurden Patienten im Alter von 18 bis 65 Jahren, die wegen der Exazerbation einer Schizophrenie, diagnostiziert nach DSM-IV-TR, weniger als 2 Wochen zuvor stationär aufgenommen worden waren. Der Score der Positive and Negative Syndrome Scale (PANSS) betrug wenigstens 70, wobei ein Score von ≥4 für die Items Wahnvorstellung, Halluzinationen, desorganisiertes Verhalten und ungewöhnliche Denkinhalte erforderlich war.
Aufgrund des klinischen Gesamteindrucks, Teil Schweregrad der Erkrankung (Clinical global impression – severity of illness, CGI-S), mussten die Patienten wenigstens „mäßig krank“ (Score≥4) sein.
Ausschlusskriterien waren unter anderen: Therapieresistenz, Substanzabhängigkeit/-missbrauch und andere schwerwiegende Erkrankungen.
Die Patienten wurden nach einer einfachblinden Plazebo-Auswaschphase von 4–7 Tagen randomisiert einer 6-wöchigen doppelblinden Behandlung zugewiesen. Dabei gab es fünf Behandlungsgruppen: Blonanserin 2,5 mg/Tag (n=61), 5 mg/Tag (n=58) oder 10 mg/Tag (n=64), 10 mg/Tag Haloperidol (n=60) und Plazebo (n=64). Die Patienten blieben für wenigsten 2 Wochen nach dem Einschluss noch in stationärer Behandlung.
Der primäre Wirksamkeitsparameter war die mittlere Änderung des PANSS-Scores vom Einschluss bis Woche 6 der Behandlung. Sekundäre Wirksamkeitsparameter waren unter anderen die Änderungen der Positiv- und Negativsubscores der PANSS, der Anteil der Patienten mit einer Änderung des PANSS-Scores um ≥20%, ≥40%, ≥60% und ≥80, sowie die mittlere Änderung des CGI-S-Scores. Die Beurteilung der Wirksamkeit wurde wöchentlich vorgenommen.
Ebenfalls wöchentlich wurden die Berichte von Nebenwirkungen registriert und das Auftreten und der Schweregrad von extrapyramidal-motorischen Symptomen mithilfe der Abnormal Involuntary Movement Scale, der Simpson Angus Extrapyramidal Side Effect Scale und der Barnes Akathisia Scale beurteilt. Zur Beurteilung der Verträglichkeit wurden weiterhin 14-täglich verschiedene körperliche Untersuchungen (einschließlich Feststellung des Körpergewichts) und Laboruntersuchungen vorgenommen.
Wirksamkeit
Von den 307 eingeschlossenen Patienten beendeten 228 (74,3%) die Studie protokollgemäß. Die Abbrüche wegen Unverträglichkeit lagen zwischen 1,6% (10 mg/Tag Blonanserin) und 6,7% (Haloperidol).
Alle aktiven Behandlungen waren nach 6 Wochen signifikant besser wirksam als Plazebo (p<0,001; Abb. 1): 10 mg/Tag Blonanserin bereits nach der ersten Behandlungswoche, 5 mg/Tag Blonanserin und 10 mg/Tag Haloperidol nach Woche 2 und 2,5 mg/Tag Blonanserin nach Woche 3. Die Reduktion des mittleren PANSS-Scores war nach Woche 6 unter 10 mg/Tag Blonanserin signifikant größer als unter 2,5 mg/Tag Blonanserin (p<0,001).
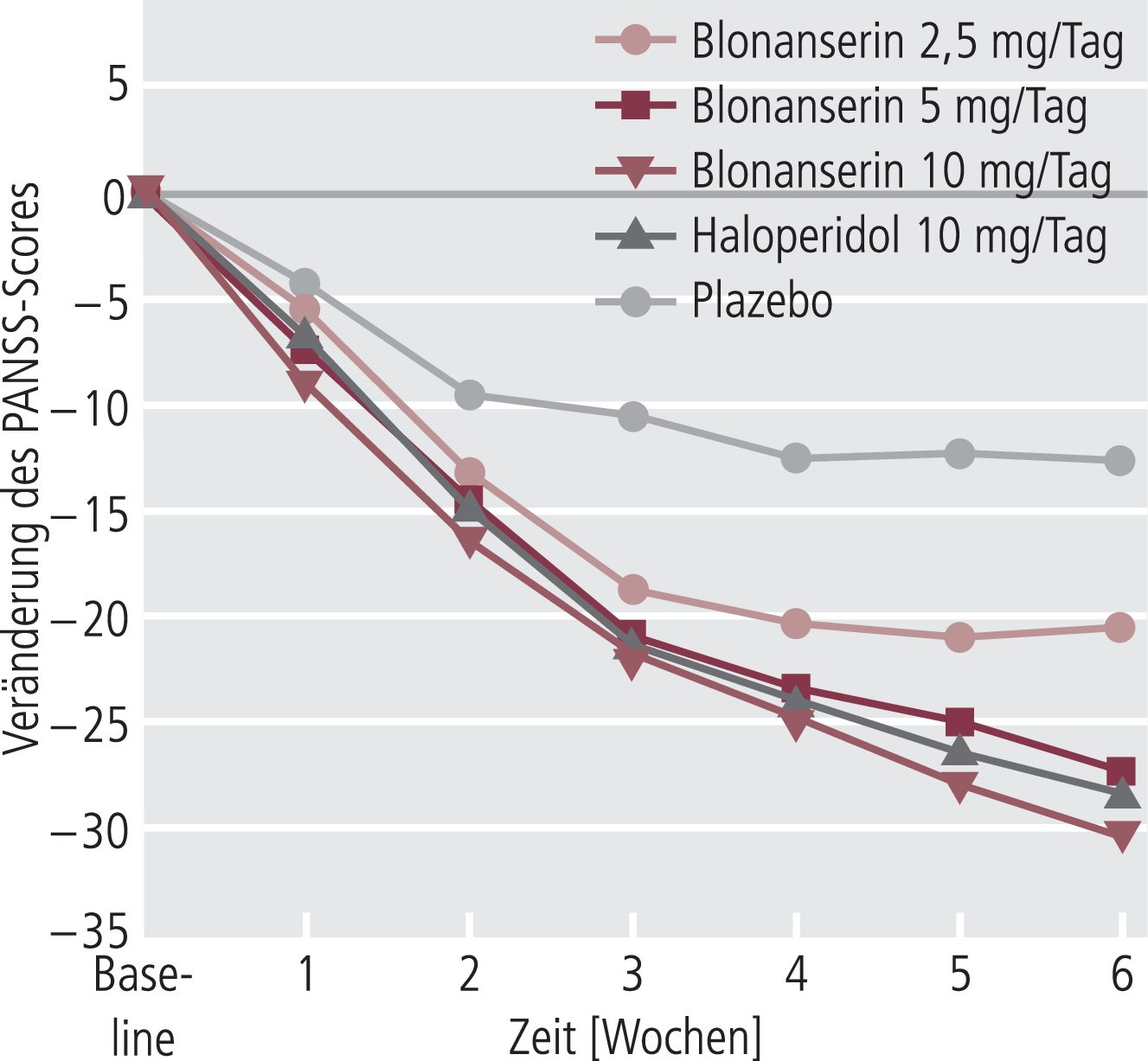
Abb. 1. Verlauf der mittleren PANSS-Gesamtscores über einen Zeitraum von 6 Wochen. Verglichen wurden drei verschiedene Dosierungen von Blonanserin mit Haloperidol und Plazebo bei Patienten mit akuter Schizophrenie [nach Garcia E et al. 2009].
Eine differenzierte Analyse der PANSS zeigte, dass im Vergleich zu Plazebo alle vier aktiven Therapien die Positivsymptomatik verbesserten (p<0,001), aber nur Blonanserin (5 und 10 mg/Tag) der Plazebo-Gabe in der Besserung der Negativsymptome signifikant überlegen war (p<0,001).
Der Anteil der Patienten mit einer Reduktion des PANSS-Scores um ≥20% war unter 5 und 10 mg/Tag Blonanserin sowie unter Haloperidol signifikant höher als unter Plazebo (p=0,0029; p=0,0017; p=0,0009). Der Anteil der Patienten mit einer Verbesserung von ≥40% unterschied sich nur mit 10 mg/Tag Blonanserin signifikant von Plazebo (p=0,0073).
Die mittlere Änderung des CGI-S-Scores war ab Woche 3 unter allen aktiven Behandlungen größer als unter Plazebo (p=<0,05).
Verträglichkeit
Insgesamt traten bei 52,4% der Patienten unerwünschte Ereignisse auf. Die Inzidenz war in der 10-mg/Tag-Blonanserin- und der Haloperidol-Gruppe (64% und 70%) höher als in den anderen Gruppen: in der 2,5-mg/Tag- und der 5-mg/Tag-Blonanserin-Gruppe berichteten 32,8% beziehungsweise 41,4% der Patienten unerwünschte Ereignisse, in der Plazebo-Gruppe waren es 51,3%. Von nur drei Patienten wurden schwerwiegende unerwünschte Ereignisse bekannt (unter Plazebo: Verschlimmerung eines Darmgeschwürs und Krampfanfälle; unter Haloperidol: Lungenentzündung).
Die häufigsten unerwünschten Ereignisse unter 10 mg/Tag Blonanserin waren Insomnie (9,4%) und Tremor (7,8%), während unter Haloperidol Tremor (23,3%), Agitation (10%) und Kopfschmerz (8,3%) am häufigsten auftraten.
Unberücksichtigt in dieser Aufzählung sind die extrapyramidal-motorischen Symptome (EPMS). Sie traten unter Haloperidol (53,3%) doppelt so häufig auf wie unter 10 mg/Tag Blonanserin (26,6%). In den beiden anderen Blonanserin-Gruppen (2,5 mg/Tag: 16,4%; 5 mg/Tag: 10,3%) lag die Inzidenz aller EPMS nahe am Plazebo-Niveau (9,4%). Die häufigsten Ereignisse unter Haloperidol waren Parkinsonismus (28,3%), Akathisie (21,7%) und erhöhter Muskeltonus (20%). Unter 10 mg/Tag Blonanserin traten Akathisie (17,2%) und Parkinsonismus (9,4%) am häufigsten auf.
Haloperidol verursachte ab Woche 2 durchgehend bis Woche 6 eine Erhöhung der Prolactinspiegel. Im Unterschied dazu waren die Plasmaprolactinspiegel unter Blonanserin nicht erhöht.
Die Zunahme des Körpergewichts war in allen Gruppen gering (0,08–0,57 kg).
Die Autoren schließen aus den Ergebnissen, dass Blonanserin aufgrund seiner guten Wirksamkeit und Verträglichkeit ein großes Potenzial als neues atypisches Antipsychotikum hat.
Kommentar
Die Ergebnisse dieses ersten international publizierten Vergleichs von Blonanserin mit Haloperidol fielen für die neue Substanz überzeugend aus. Vorteile von Blonanserin gegenüber Haloperidol zeigten die Daten zur Wirksamkeit gegen Negativsymptome (auch wenn sie bei einer Kurzzeitstudie vorsichtig bewertet werden müssen) und zur Verträglichkeit. Interessant ist auch die deutlich erkennbare Dosis-Wirkungs-Beziehung, wobei die Tagesdosis von 5 mg zwar etwas schwächer wirksam war, aber deutlich weniger Nebenwirkungen verursachte als die 10-mg-Dosis.
Weitergehende Bewertungen erscheinen allerdings zu diesem frühen Zeitpunkt der klinischen Entwicklung von Blonanserin nicht sinnvoll.
Quelle
Garcia E, et al. The efficacy and safety of blonanserin compared with haloperidol in acute-phase schizophrenia. A randomized, double-blind, placebo-controlled multicentre study. CNS Drugs 2009;23:615-25.
Psychopharmakotherapie 2010; 17(05)
