Detlef Degner, Göttingen, Eckart Rüther, Göttingen/München, Renate Grohmann und Alexander Becker, München
Dieser Fall wurde im Rahmen des AMSP-Programms (Arzneimittelsicherheit in der Psychiatrie) dokumentiert und bewertet. Er soll auf die klinische Bedeutung kardialer unerwünschter Arzneimittelwirkungen (UAW) sowohl unter Antidepressiva als auch Antipsychotika, speziell auch in Hinblick auf die zunehmende Anzahl von Kombinationsbehandlungen, aufmerksam machen und die Notwendigkeit einer intensiven interdisziplinären Zusammenarbeit (hier: Psychiatrie/Kardiologie) sowie eines konsequenten EKG-Monitorings unter einer psychopharmakologischen Medikation aufzeigen.
Fallbericht
Eine 41-jährige Patientin mit der Diagnose einer schizodepressiven Störung (F 25.1 nach ICD-10), Ersterkrankung 1990, kam zur insgesamt 7. stationären Aufnahme. Bei der Patientin bestanden eine Adipositas (BMI 28,4 kg/m2), eine medikamentös behandelte Fettstoffwechselstörung und eine nicht ausreichend substituierte Hypothyreose. Kardiale Vorerkrankungen lagen nicht vor.
Als Vormedikation hatte die Patientin seit mindestens drei Jahren Amitriptylin, in retardierter Form (100 mg/Tag), Carbamazepin, retardiert (450 mg/Tag), Inegy® (Ezetimib + Simvastatin) zur Cholesterolsenkung, Levothyroxin 100 µg, sowie seit einigen Monaten Lorazepam (1,5 mg/Tag).
Die Laborparameter lagen im Normbereich, einschließlich der Elektrolyte, das Plasma-Cholesterol war mit 288 mg/dl erhöht (Referenzwert <240 mg/dl als Entscheidungsgrenze), das Gesamt-T4 (TT4) und freies T4 (fT4) lagen im unteren Referenzbereich bei regelrechtem TSH basal.
Das EKG zeigte am Tag 1 nach der stationären Aufnahme einen Sinusrhythmus und eine QTc-Zeit von 433 ms ohne weitere Auffälligkeiten.
UAW-Verlauf (Tab. 1, Abb. 1)
Tab. 1. Medikation und EKG-Charakteristika der betrachteten Patientin im Verlauf
|
Substanz |
Tagesdosis/mg |
EKG |
|
|
Vormedikation |
Amitriptylin |
100 |
|
|
Tag 1 |
Amitriptylin |
150 |
QTc 433 ms |
|
Tag 8 |
Amitriptylin |
275 |
QTc 448 ms |
|
Tag 20 |
Amitriptylin |
275 |
|
|
Tag 31 |
Amitriptylin |
275 160 |
|
|
Tag 39 |
Amitriptylin |
275 |
QTc 516 ms |
|
Tag 41 |
Amitriptylin |
100 |
|
|
Tag 42 |
Amitriptylin > |
QTc 549 ms |
|
|
Tag 43 |
QTc 544 ms |
||
|
Tag 44 |
Paliperidon |
6 |
QTc 505 ms |
|
Tag 45 |
Paliperidon |
6 |
QTc 508 ms |
|
Tag 46 |
Paliperidon |
6 |
QTc 467 ms |
|
Tag 48 |
Paliperidon |
6 |
QTc 385 ms |
|
Tag 52 |
Paliperidon |
6 |
QTc 448 ms |
|
Tag 65 |
Paliperidon |
6 |
QTc 432 ms |
|
Tag 71 |
Paliperidon |
9 |
QTc 409 ms |
|
Tag 75 |
Entlassung |
SR: Sinusrhythmus; LSB: Linksschenkelblock; >: Wirkstoff abgesetzt
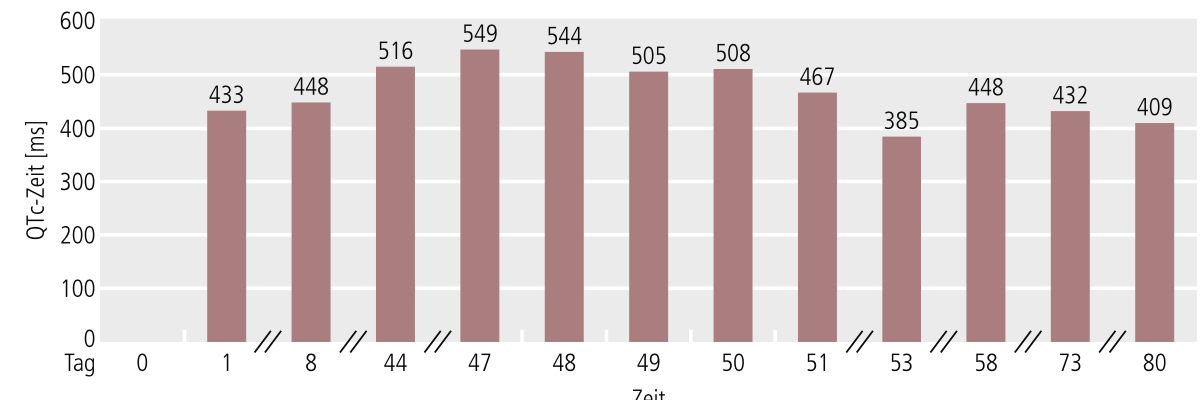
Abb. 1. QTc-Zeit im Verlauf
Bei einer Kontroll-EKG-Untersuchung 8 Tage nach stationärer Aufnahme zeigte sich bei einer Tagesdosis von 275 mg Amitriptylin eine Verlängerung der QTc-Zeit auf 448 ms, die Patientin zeigte keine klinisch auffällige Problematik. Im weiteren Verlauf zeigte sich bei der Kombinationstherapie mit zusätzlich Ziprasidon (max. 160 mg/Tag) am Tag 38 ein pathologisches EKG mit QTc 516 ms, Linksschenkelblock, AV-Block I°, T-Negativierungen (I, AVL, V5, V6).
Die QTc-Zeit stieg im weiteren Verlauf auf maximal 549 ms, eine klinische Symptomatik fand sich weiterhin nicht.
Die Patientin erhielt zum Beginn der UAW vorübergehend, auf Anraten der Internisten, für 5 Tage additiv Kalium (als Brausetablette) und Magnesium oral. Nach Absetzen von Amitriptylin und Ziprasidon waren die QTc-Zeiten rückläufig, bei weiteren Kontrollen unter dem neu angesetzten Paliperidon schließlich nicht mehr verlängert. Während des gesamten Behandlungszeitraums wurde die Vormedikation (Carbamazepin retard, Lorazepam, Levothyroxin) bis zum Zeitpunkt der Entlassung fortgeführt.
Der Carbamazepin-Spiegel im Serum zum Zeitpunkt des Beginns der UAW lag bei 20,9 µmol/l (Referenz-Bereich: 17–47 µmol/l), der Amitriptylin-Spiegel im Serum (36 Stunden nach Absetzen von 275 mg/Tag) bei 311 nmol/l (Referenz-Bereich: 180–720 nmol/l).
Die Laborwerte inklusive Kalium, Creatinkinase und Troponin-T nach UAW-Beginn waren regelrecht.
In der Vorgeschichte war es 2005 unter einer damaligen Kombination von Amitriptylin (125 mg/Tag), Risperidon und Carbamazepin zu einem Anstieg der QTc-Zeit auf maximal 458 ms gekommen (Vorwert 12 Tage zuvor unter 100 mg/Tag Amitriptylin: QTc 411 ms). Nach Absetzen von Amitriptylin normalisierten sich damals die QTc-Zeiten.
Weitere Diagnostik
Das Belastungs-EKG wurde wegen muskulärer Erschöpfung bei 75 Watt abgebrochen; es zeigte sich ein normaler Sinusrhythmus, keine Ischämiezeichen, keine Rhythmusstörungen.
Einschätzung des aktuellen Falls
Einer medikamentöse UAW-Ursache der EKG-Veränderungen wurde im AMSP-Programm in Bezug auf Amitriptylin als „sicher“ (nach Reexposition 2005) und zusätzlich (möglicherweise im Sinne eines additiven Effektes) in Bezug auf Ziprasidon als „wahrscheinlich“ (projekteigene Definitionen) eingeschätzt.
Bei Amitriptylin waren neben der früheren QTc-Verlängerung 2005 auch relativ hohe Serumkonzentrationen noch nach Absetzen der Substanz auffällig. Ob die Kombination mit Ziprasidon letzlich entscheidend für die EKG-Veränderungen war, bleibt unklar.
Relevant für die UAW waren daneben das weibliche Geschlecht sowie als Risikofaktoren eine Adipositas und eine vorbestehende Fettstoffwechselstörung (Hypercholesterolämie). Zusätzlich waren die Schilddrüsen-Hormonparameter trotz Substitution nicht optimal eingestellt, so dass möglicherweise bei niedrigen T4-Spiegeln ein retardierter Metabolismus vorlag.
Diskussion
Antidepressiva und Antipsychotika haben einen grundsätzlichen Einfluss auf die kardiale Hämodynamik mit einer potenziellen organischen Schädigung (der Myokardstruktur), die zum Teil irreversibel sein kann, sowie auf das kardiale Reizleitungssystem. Störungen dieses Herzreizleitungssystems sind gekennzeichnet durch ein akutes Auftreten mit einer potenziell vital bedrohlichen Gefährdung des Patienten, zeigen aber keine strukturelle Schädigungen und sind grundsätzlich reversibel. Neben bradykarden Rhythmusstörungen (z.B. AV-Block II oder Sick-Sinus-Syndrom) sind tachykarde Rhythmusstörungen und ventrikuläre Rhythmusstörungen wegen der vitalen Bedrohung besonders gefürchtet, beispielsweise als „Torsade-de-Pointes-Tachykardie“ („Spitzenumkehrtachykardie“) [2] bei QT-Zeit-Verlängerungen. Die QT-Zeit, definiert als Beginn der Q-Zacke bis zum Ende der T-Welle im Oberflächen-EKG, ist frequenzabhängig. Zur Beurteilung der QT-Dauer sollte daher die frequenzkorrigierte QTc-Zeit nach Bazett nach folgender Formel errechnet werden: QTc=QT/√RR. Als obere Grenze gelten für Männer bis 440 ms, für Frauen bis 460 ms. Eine QTc-Zeit, als Surrogatmarker der Kammervulnerabilität, gilt ab 500 ms oder einer Zunahme um 60 ms als gefährlich [8]. Einfluss haben unter anderem das weibliche Geschlecht, das Alter, vorbestehende Rhythmusstörungen, kardiale Vorschädigungen sowie Elektrolyt- (Hypokaliämie, Hypomagnesiämie) und Metabolisierungsstörungen (z.B. Hypothyreose).
Herzrhythmusstörungen sind schwere, potenziell lebensbedrohliche UAW zahlreicher Psychopharmaka. Neben einer unterschiedlichen Anzahl von Blockierungsbildern des Herzleitungssystems stellen Verlängerungen des QT-Intervalls ein besonderes Risiko in Form tachykarder Rhythmusstörungen (z.B. Torsade de Pointes [2] oder ventrikuläre Tachykardie) dar.
Goodnick et al. [6] stellen in einer Übersichtsarbeit von 2002 dar, dass es seit der Markteinführung von Psychopharmaka zwar umfangreiche Untersuchungen und Publikationen über die Hauptklassen (Antipsychotika, Antidepressiva, Lithium, Antikonvulsiva und Benzodiazepine) gegeben hätte, dass aber, nach Meinung der Autoren, Einzelmedikationen nicht gezielt untersucht worden und möglicherweise, durch den Einfluss der pharmazeutischen Industrie, Daten unveröffentlicht geblieben seien. Insgesamt gäbe es drei zeitlich unterschiedliche Phasen: als Sofortreaktion (in den ersten Minuten nach oraler oder parenteraler Applikation), nach kurzzeitigem (4 bis 12 Wochen) oder langzeitigem Einsatz (6 Monate). In der Literatur richte sich bei Sofortreaktionen die größte Aufmerksamkeit auf Haloperidol, Droperidol, Pimozid and Trazodon, bei kurzzeitigem Gebrauch auf Thioridazin, Pimozid, Sertindol, Nortriptylin, Clomipramin und Doxepin und bei langzeitigem Einsatz auf Clozapin, Olanzapin und Carbamazepin. Unter den Antidepressiva scheinen trizyklische Antidepressiva (TZA; Imipramin, Amitriptylin und Doxepin) mit QT-Dauer-Verlängerungen assoziiert zu sein.
Unter den sonstigen Antidepressiva gibt es Einzelberichte über Torsades de Pointes unter Mirtazapin, für selektive Serotonin-Wiederaufnahmehemmer (SSRI) fand sich in umfangreichen Untersuchungen kein Anhalt für einen Einfluss auf die QTc-Zeit. Desgleichen scheinen Lithium, Antikonvulsiva und Benzodiazepine sich nur sehr geringfügig auf QTc-Zeiten auszuwirken.
Schmid et al.[13] erfassten im Rahmen des AMSP-Projekts im Zeitraum 1993 bis 2000 insgesamt 122565 überwachte Patienten. Darunter kam es nur in 68 Fällen (0,055%) zu schweren kardialen UAW, unter Antidepressiva (ausschließlich unter TZA) bei 0,03%. Aktuelle AMSP-Daten aus den Jahren 2001 bis 2007 zeigten bei insgesamt 25917 überwachten Patienten insgesamt 19 UAW-Fälle mit einer pathologischen QTc-Zeit-Verlängerung (>500 ms). Ziprasidon wurde in zwei Fällen, Amitriptylin in einem Fall angeschuldigt.
In der vorliegenden Literatur gibt es umfangreiche Berichte über QTc-Zeit-Verlängerungen sowohl unter konventionellen Antipsychotika [4, 17] als auch unter atypischen Präparaten [5, 14]. Auch unter Antidepressiva ist ein solcher Effekt zu beobachten. In Rahmen einer aktuellen, naturalistischen Studie fanden Ramos-Rios et al. [12] bei insgesamt 6% aller stationären psychiatrischen Patienten (n=171) eine QTc-Strecken-Verlängerung.
Alvarez und Pahissa [1] gaben die Häufigkeit von QTc-Zeit-Verlängerungen (>456 ms) bei psychiatrischen Patienten mit 8% an. In ihrer aktuellen Übersichtsarbeit beschrieben sie als häufigste Risiko-Psychopharmaka TZA, Thioridazin, Droperidol und Olanzapin. Prädiktoren seien ein höheres Lebensalter (>65 Jahre) und die jeweilige Dosis des angeschuldigten Antipsychotikums. Torsades-de-Pointes-Fälle seien überwiegend unter Thioridazin, Haloperidol, Ziprasidon, Olanzapin und TZA beschrieben worden, das kardiale Risikoprofil von Ziprasidon und Olanzapin werde derzeit umfangreich evaluiert.
Van Noord und Mitarbeiter [15] ermittelten in einem Teilprojekt der sogenannten Rotterdam-Studie unter 3377 Männern und 4845 Frauen (>55 Jahre) insgesamt 813 Studienteilnehmer (9,9%) mit QTc-Verlängerungen bei einer Follow-up-EKG-Untersuchung, davon nahmen 492 (zu 74,4% Frauen) Psychopharmaka. Im Rahmen ihrer prospektiven Kohorten-Studie bestätigten sie QTc-Zeit-Verlängerungen als einen Klasseneffekt unter TZA.
Die Arbeitsgruppe von Harrigan [7] dagegen fand in einer prospektiven randomisierten Studie bei keinem der mit sechs unterschiedlichen Antipsychotika (Haloperidol, Thioridazin, Ziprasidon, Quetiapin, Olanzapin oder Risperidon) behandelten Patienten eine eindeutige Überschreitung der QTc-Zeit über 500 ms. Die stärksten QTc-Intervall-Verlängerungen wurden unter Thioridazin (300 mg/Tag, n=30) ermittelt.
Die Problematik der QTc-Zeit-Verlängerung war nach der Markteinführung von Sertindol evident und stand zumindest zeitweise im Fokus des Interesses. Inzwischen gibt es replizierte Daten mit eindeutiger Signifikanz mit einer umfangreichen Datenlage. Alvarez und Pahissa [1] stellten fest, dass die Ergebnisse bezüglich Sertindol und dem erhöhten Risiko einer QTc-Zeit-Verlängerung eindeutig und signifikant seien, allerdings im Gesamtkontext der anderen Antipsychotika betrachtet werden müssten. Komossa und Mitarbeiter [9] haben in einer Cochrane-Analyse Sertindol mit anderen Atypika bei schizophrenen Patienten verglichen. Insgesamt zeigten sich unter Sertindol weniger EPS, aber mehr kardiale UAW und sexuelle Funktionsstörungen.
Grundsätzlich gelten antipsychotische und antidepressive Substanzen als sichere Therapieoptionen [5, 10, 11]. Allerdings hat die Identifikation von Risikopatienten einen hohen Stellenwert [18]. Relevant sind internistische Vorerkrankungen, wie sie auch die hier vorgestellte Patientin aufwies. Zhang et al. [16] betonten die Bedeutung der Komorbidität besonders bei älteren Patienten.
Der vorliegende Fall unterstreicht die Notwendigkeit regelmäßiger EKG-Kontrollen bei Gabe von TZA und den meisten Antipsychotika, die Beobachtung eventueller (internistischer) Risikofaktoren und die sorgfältige Abwägung einer psychopharmakologischen Kombinationstherapie mit potenziellen pharmakodynamischen, aber auch pharmakokinetischen Risiken [10]. Darpö [3] betont zu Recht, dass die Arzneimittelüberwachung bezüglich potenzieller kardialer Risiken unzureichend ist („room for improvement“).
Literatur:
1. Alvarez PA, Pahissa J. QT alterations in psychopharmacology: proven candidates and suspects. Curr Drug Saf 2009: Epub ahead of print.
2. Aström-Lilja C, Odeberg JM, Ekman E, et al. Drug-induced torsades de pointes: a review of the Swedish pharmacovigilance database. Pharmacoepidemiol Drug Saf 2008;17:587–92.
3. Darpö B. Detection and reporting of drug-induced proarrhythmias: room for improvement. Eurospace 2007;9(Suppl 4):23–36.
4. Ginwalla M, Biblo LA, Paydak H. Torsades de pointes following intravenous haloperidol administration in a patient with complete heart block. WMJ 2009;108:48–50.
5. Glassman AH, Bigger JT jr. Antipsychotic drugs: prolonged QTc interval, torsades de pointes, and sudden death. Am J Psychiatry 2001;158:1774–82.
6. Goodnick PJ, Jerry J, Parra F. Psychotropic drugs and the ECG: focus on the QTc interval. Expert Opin Pharmacother 2002;3:478–98.
7. Harrigan P, Miceli JJ, Anziano R, et al. A randomized evaluation of the effects of six antipsychotic agents on QTc, in the absence and presence of metabolic inhibition. J Clin Psychopharmacol 2004;24:62–9.
8. Johnson JN, Ackerman MJ. QTc: how long is too long? Br J Sports Med 2009;43:657–62.
9. Komossa K, Rummel-Kluge C, Hunger H, Schwarz S, et al. Sertindole versus other atypical antipsychotics for schizophrenia. Cochrane Database Syst Rev 2009;2:CD006752.
10. Pacher P, Kecskemeti V. Cardiovascular side effects of new antidepressants and antipsychotics: new drugs, old concerns? Curr Pharm Des 2004;10:2463–75.
11. Pardo Cabello AJ, González Contreras LG, Manzano Gamero MV, et al. Prevalence of fatal adverse drug reactions in hospitalized patients. Int J Clin Pharmacol Ther 2009;47:596–602.
12. Ramos-Rios R, Arrojo-Romero M, Paz-Silva E, et al. QTc intervall in a sample of long-term schizophrenia inpatients. Schizoph Res 2009: Epub ahead of print.
13. Schmid C, Grohmann R, Engel RR, et al. Cardiac adverse effects associated with psychotropic drugs. Pharmacopsychiatry 2004;37(Suppl 1):S65–9.
14. Taylor D. Ziprasidone in the management of schizophrenia: the QT interval issue in context. CNS Drugs 2003;17:423–30.
15. Van Noord C, Strauss SM, Sturkenboom MC, et al. Psychotropic drugs associated with corrected QT intervall prolongation. J Clin Psychopharmacol 2009;29:9–15.
16. Zhang M, Holman CD, Price SD, et al. Comorbidity and repeat admission to hospital for adverse drug reactions in older adults: retrospective cohort study. BMJ 2009;338a:2752.
17. Zareba W, Lin DA. Antipsychotic drugs and QT interval prolongation. Psychiatr Q 2003;74:291–306.
18. Zopf Y, Rabe C, Neubert A, et al. Risk factors associated with adverse drug reactions following hospital admission: a prospective analyses of 907 patients in two Germany university hospitals. Drug Saf 2008;31:789–98.
Dr. Detlef Degner, Klinik für Psychiatrie und Psychotherapie der Universitätsmedizin Göttingen, Von-Siebold-Straße 5, 37075 Göttingen, E-Mail: ddegner@gwdg.de Prof. Dr. Eckart Rüther, Klinik für Psychiatrie und Psychotherapie der Universitätsmedizin Göttingen, Von-Siebold-Str. 5, 37075 Göttingen und Klinik für Psychiatrie und Psychotherapie der Ludwig-Maximilians-Universität München, Nussbaumstraße 7, 80336 München Dr. Renate Grohmann, Klinik für Psychiatrie und Psychotherapie der Ludwig-Maximilians-Universität München, Nussbaumstraße 7, 80336 München Dr. Alexander Becker, Medizinische Klinik und Poliklinik I der Ludwig-Maximilians-Universität, Klinikum Großhadern, Marchioninistraße 15, 81377 München
QTc interval prolongation associated with psychopharmacological treatment with amitriptyline and ziprasidone
Cardiac adverse events during psychopharmacological treatment are a strong risk factor for patients, especially alterations of QTc time which can lead to serious and life- threatening complications.
The authors report a case of a 41 years old woman suffering from a schizoaffective disorder. She had risk factors, e.g. obesity, hypothyroidism and increased cholesterine levels. During the treatment with amitriptyline in combination with ziprasidone we observed QTc interval prolongations without clinical signs. After discontinuation of both drugs the QTc time normalised. This case report demonstrates the clinical relevance of QTc interval alterations associated with drug therapy and shows specific risk factors.
Key words: Amitriptyline, ziprasidone, QTc, cardiac ADR
Psychopharmakotherapie 2010; 17(01)
