Wolf-Rüdiger Schäbitz, Münster
Cytidin-5’-Diphosphocholin (CDP-Cholin, engl. auch Citicoline, Ceraxon®) ist ein essenzieller Bestandteil bei der Biosynthese von Phospholipiden der Zellmembran. CDP-Cholin ist eine Nukleotid-Aminoalkoholverbindung und besteht aus einem Zucker (Ribose), einer Base (Cytosin), einer Phosphatgruppe (Pyrophosphat) und Cholin [1].
CDP-Cholin wird endogen synthetisiert und stellt den limitierenden Schritt der Phosphatidylcholin-Synthese dar, dem wichtigsten singulären Stoffwechselschritt zum Aufbau und zur Reparatur von Zellmembranen [2]. Aufgrund dieser Wirkungsweise wurde CDP-Cholin schon früh mit regenerativen Funktionen bei traumatischen und degenerativen Hirnerkrankungen in Zusammenhang gebracht. Besonders gut entschlüsselt sind die Wirkungen von CDP-Cholin nach einem Schlaganfall, wo es neben der membranregenerierenden Wirkung weitere wichtige Funktionen ausübt. Aufgrund einer Vielzahl experimenteller Untersuchungen bei zerebraler Ischämie sowie erster Hinweise aus klinischen Studien kann CDP-Cholin als vielversprechende, neue Möglichkeit der Schlaganfallbehandlung angesehen werden.
Pharmakokinetik und Metabolismus
CDP-Cholin ist wasserlöslich und besitzt eine sehr hohe Bioverfügbarkeit (>90%) [3]. Pharmakokinetische Studien mit gesunden Erwachsenen zeigten, dass oral appliziertes CDP-Cholin sehr schnell absorbiert und unter 1% enteral ausgeschieden wird. Die Plasmaspiegel steigen typischerweise biphasisch, das heißt eine Stunde nach Einnahme gefolgt von einem Anstieg nach 24 Stunden.
Exogen appliziertes CDP-Cholin wird in der Darmwand und in der Leber hydrolysiert und als Cholin und Cytidin absorbiert. Cholin und Cytidin werden dann weiter metabolisiert, passieren unter anderem die Blut-Hirn-Schranke, um im Gehirn in CDP-Cholin resynthetisiert zu werden [4]. Pharmakokinetische Studien zeigen, dass die Ausscheidung über die Lunge sowie über den Urin analog zur Plasmaverfügbarkeit biphasisch verläuft [5].
Endogen zugeführtes CDP-Cholin fungiert als Zwischenprodukt der Biosynthese von Phospholipiden wie Phosphatidylcholin, dem primären Phospholipid aller Zellmembranen (Abb. 1) [6]. Cytidin, ein Hauptbestandteil der RNS, wird im Zytoplasma in Cytidintriphosphat (CTP) umgewandelt. Cholin wird durch das Enzym Cholinkinase phosphoryliert. Das Produkt Cholinphosphat wird dann mit Cytidintriphosphat (CTP) zu CDP-Cholin metabolisiert [7]. CDP-Cholin reagiert mit 1,2-Diacylglycerol zu Phosphatidylcholin, katalysiert durch das Enzym CDP-Cholin-Diacylglycerol-Transferase [3].
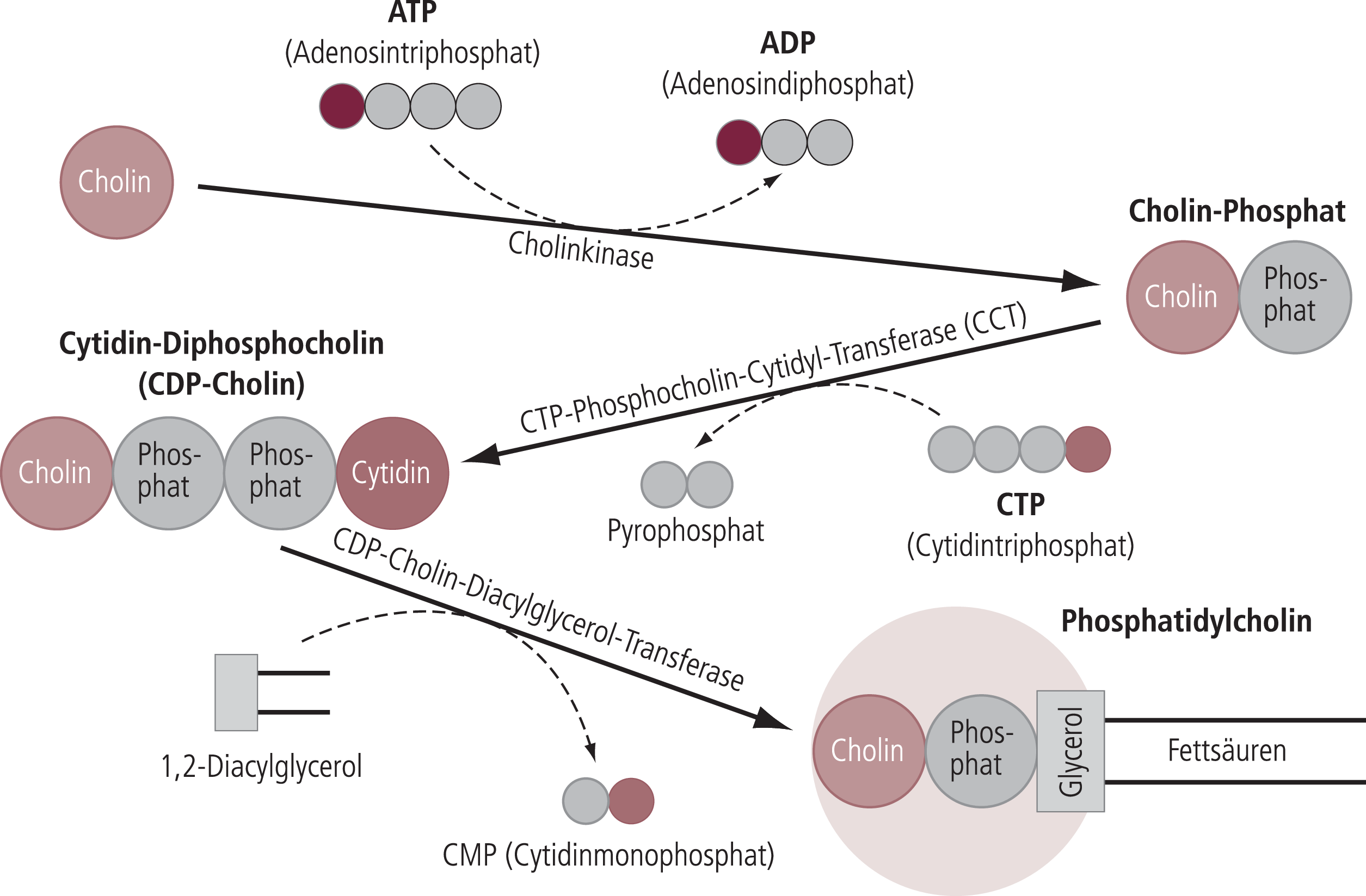
Abb. 1. Phosphatidylcholin-Synthese. CDP-Cholin stellt den limitierenden Schritt der Phosphatidylcholinsynthese dar, dem wichtigsten singulären Stoffwechselschritt zum Aufbau und zur Reparatur von Zellmembranen.
Die orale Gabe von CDP-Cholin erhöht die Plasmaspiegel von Cytidin und Cholin innerhalb von sechs bis acht Stunden. Eine prolongierte Verabreichung für 42 bis 90 Tage erhöht signifikant die Gehirnkonzentrationen von Phosphatidylcholin, Phosphatidylethanolamin, und Phosphatidylserin – den drei wesentlichen Phospholipiden aller Gehirn-Zellmembranen. Im Tierversuch zeigte sich nach einer Behandlung mit 500 mg/kg Körpergewicht (KG) pro Tag über 90 Tage ein Anstieg der Phosphatidylcholin-Spiegel um 25%, der Phosphatidylethanolamin-Spiegel um 17% und der Phosphatidylserin-Spiegel um 42% [8]. Cholin und Cytidin, die Hauptmetaboliten von CDP-Cholin, weisen bereits nach einmaliger oraler Gabe von CDP-Cholin signifikant erhöhte Plasmaspiegel bei jungen und älteren Patienten auf. Durch MR-spektroskopische Untersuchungen konnte gezeigt werden, dass nach einer CDP-Cholin-Behandlung für sechs Wochen bei älteren Menschen die Plasmaspiegel von Phosphodiestern, Nebenprodukten des Phospholipid-Stoffwechsels, im Gehirn signifikant stiegen. Eine CDP-Cholin-Behandlung erhöht somit die Phospholipidsynthese sowie den Turnover [9].
Nebenwirkungsprofil
Die LD50 nach einmaliger intravenöser Behandlung mit CDP-Cholin beträgt 4600 mg/kg Körpergewicht (KG) bei Mäusen und 4150 mg/kg KG bei Ratten. Die orale LD50 konnte nicht bestimmt werden, da keine Todesfälle, trotz maximaler oraler Dosierung, auftraten [10]. Keine toxischen Wirkungen wurden nach einer 30-tägigen Dauerbehandlung mit oralem CDP-Cholin in den Dosierungen von 100 mg/kg KG und 150 mg/kg KG im Tierversuch festgestellt [11]. Der Effekt einer chronischen oralen Behandlung mit CDP-Cholin bei Hunden (Dosierungen von 1,5 g/kg KG täglich über sechs Monate) zeigte weder toxische Wirkungen noch Veränderungen in den physiologischen, biochemischen, neurologischen oder morphologischen Untersuchungsparametern [12].
Auch beim Menschen weist CDP-Cholin ein äußerst geringes Toxizitätsprofil auf. Regelmäßige tägliche Dosierungen von 600 und 1000 mg bei gesunden Personen zeigten lediglich in einigen wenigen Fällen transiente moderate Kopfschmerzen. Keinerlei messbare Veränderungen ergaben die hämatologischen und biochemischen Bluttests sowie die neurologischen Untersuchungen [13].
Toxizitätsstudien zeigten, dass eine CDP-Cholin-Behandlung bei Ratten bis 2000 mg/kg KG über 14 Tage sehr sicher ist und keine Veränderungen des Körpergewichts, der Letalität, der klinischen Symptome oder der inneren Organe hervorrief. Bei 2817 Personen (60–80 Jahre), die überwiegend an vaskulären Erkrankungen litten, führte die Behandlung mit CDP-Cholin insgesamt zu 151 unerwünschten Ereignissen (5%). Die meisten davon waren transient und bedurften keiner spezifischen Behandlung: beispielsweise Magenschmerzen und Durchfall (insgesamt 102 Fälle), Hypotension, Tachykardie oder Bradykardie (insgesamt 16 Fälle) [14]. Aufgrund dieser günstigen Sicherheitsdaten sowie seiner endogenen Herkunft ist das kommerziell verfügbare CDP-Cholin (Ceraxon®) in Deutschland als diätetisches Lebensmittel für besondere medizinische Zwecke (ergänzende bilanzierte Diät) erhältlich.
Wirksamkeit nach zerebraler Ischämie
Präklinische Studien
Eine zerebrale Ischämie triggert eine Reihe nachfolgender Mechanismen, die insgesamt den postischämischen Verlauf bestimmen [15]. Hierzu gehört primär die durch die Ischämie induzierte Depolarisation präsynaptischer Neurone mit konsekutiver Glutamatfreisetzung. Durch Aktivierung postsynaptischer Glutamatrezeptoren kommt es zu einem intrazellulären Calciumionenanstieg. Hierdurch wird nachfolgend eine Überaktivierung von Lipasen, Proteasen und Endonukleasen sowie eine Funktionsstörung von Membranrezeptoren und -kanälen verursacht, die schließlich zu einer Zerstörung der Zellmembran und des Zytoskeletts führt. Eine Auslösung apoptotischer Mechanismen sowie Freisetzung toxischer Radikale, die eine entzündliche Reaktion unterhalten, sind weitere Folgen der postsynaptischen Glutamataktivierung. Neben den pathophysiologischen Veränderungen in der hyperakuten und subakuten Phase der zerebralen Ischämie hängt das funktionelle Langzeitergebnis entscheidend von der Fähigkeit des Gehirns zur Regeneration ab. Die Reorganisation der ischämischen und periischämischen Region wird durch molekulare neuronale Prozesse wie Neuro-, Axo- und Synaptogenese determiniert.
Die Wirksamkeit von CDP-Cholin nach einer zerebralen Ischämie konnte in verschiedenen experimentellen Studien gezeigt werden. Eine CDP-Cholin-Behandlung spontan hypertensiver Tiere besserte den neurologischen Schaden der Versuchstiere nach ischämischem Infarkt im Versorgungsgebiet der A. cerebri media [16]. Nach transienter fokaler zerebraler Ischämie (Fadenmodell) und nachfolgender CDP-Cholin-Behandlung mit 100 oder 500 mg/kg KG oder Plazebo über eine Woche zeigte sich ein signifikanter dosisabhängiger infarkt- und hirnödemreduzierender Effekt zugunsten der höchsten Dosis [17]. Diese Wirkung ließ sich dosisabhängig (500–2000 mg) bis zu einem Zeitfenster von vier Stunden auch nach permanenter Ischämie reproduzieren [18, 19].
Die Wirksamkeit von CDP-Cholin (250 mg/kg KG, 500 mg/kg KG) nach zerebraler Ischämie konnte auch im thrombembolischen Ischämiemodell, vor allem in Kombination mit einer Thrombolyse, gezeigt werden [20, 21]. Ein signifikanter infarktreduzierender Effekt zeigte sich bei den Versuchstieren, die CDP-Cholin und Alteplase (rt-PA, Actilyse®) bekamen. Diese Ergebnisse wurden in einer dritten Studie im thrombembolischen Infarktmodell bestätigt. Hier zeigte CDP-Cholin ebenfalls eine infarktreduzierende Wirkung, die durch eine Kombination mit Urokinase (z. B. Actosolv®) signifikant verstärkt wurde [22].
In einer Reihe von Studien wurde zudem untersucht, an welchen Schlüsselstellen CDP-Cholin in die Pathophysiologie der zerebralen Ischämie eingreift. Dabei wurden verschiedene Wirkansätze gefunden (Abb. 2):
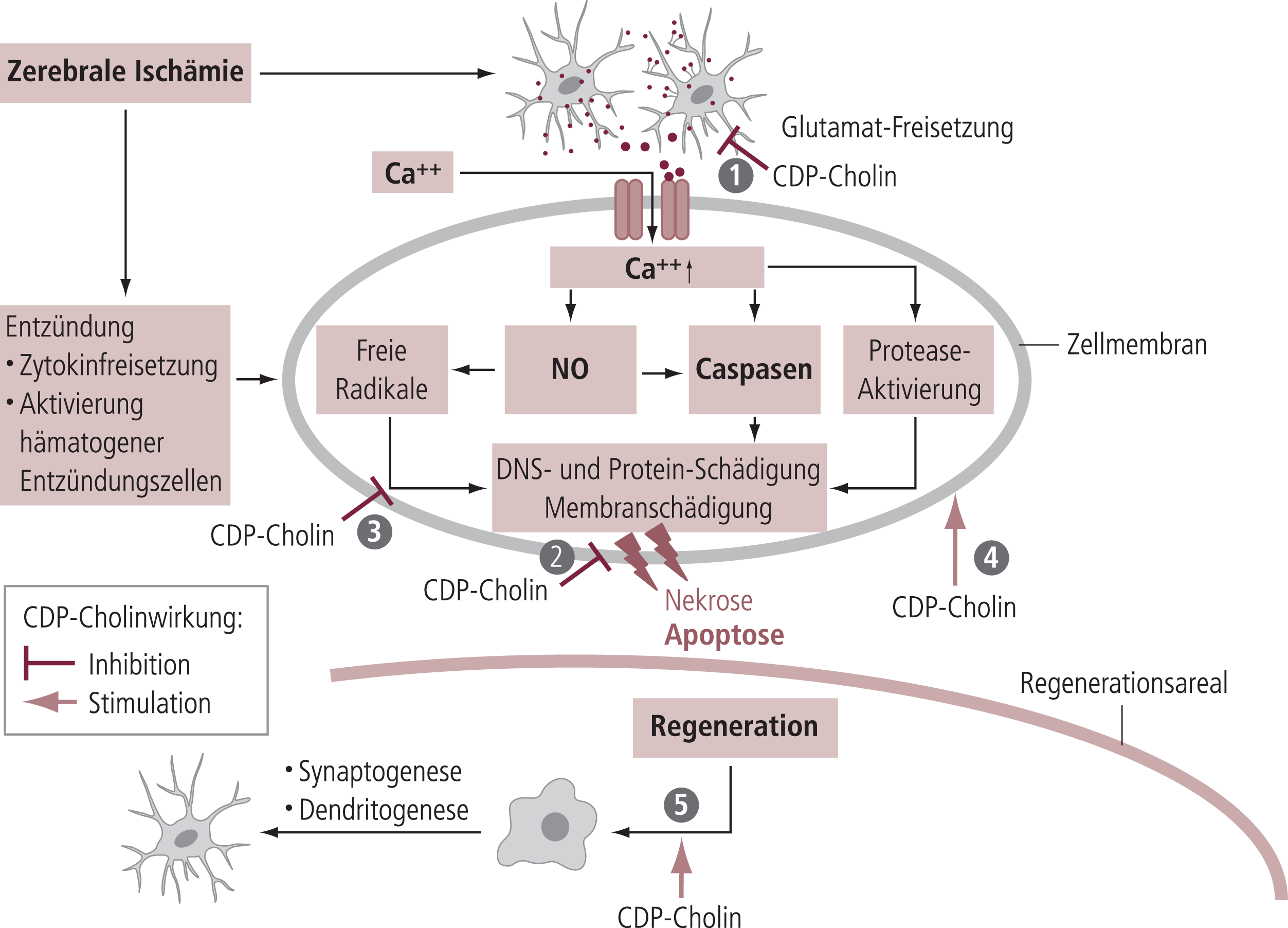
Abb. 2. Interaktion von CDP-Cholin mit Schlüsselmechanismen nach einer zerebralen Ischämie: (1) Antiexzitotoxische Wirkung; (2) antiapoptotische Wirkung; (3) antioxidative Wirkung; (4) Reparatur von Membranschäden neuronaler Zellen durch Synthese von Phosphatidylcholin; (5) neurotrophe Wirkung mit Induktion neuronaler Regenerationsprozesse
1. Aktuelle Studien zeigen, dass eine CDP-Cholin-Behandlung in vitro, aber auch in vivo zu einer Reduktion der extrazellullären Glutamat-Konzentration führt, vor allem im periischämischen Gewebe der sogenannten Penumbra. Dieser Befund wurde als antiexzitatorische Wirkungsweise der Substanz interpretiert [19].
2. Antiapoptotische Effekte wurden vor allem bei cholinergen Neuronen nachgewiesen: Durch exzessive neuronale Stimulation nach zerebraler Ischämie wird Acetylcholin freigesetzt und es entsteht konsekutiv ein Cholin-Mangel, der wiederum Apoptose induziert [23]. Die Ursache hierfür ist in der nach einer Ischämie auftretenden Störung der Cholin-Synthese zu suchen, bei der Membran-Phospholipide abgebaut werden, um Cholin für die Acetylcholin-Synthese bereitzustellen. Eine exogene CDP-Cholin-Behandlung stellt mehr Cholin für die Acetylcholin-Synthese zur Verfügung und verhindert über diesen Mechanismus den apoptotischen Zelltod cholinerger Neurone [24].
3. CDP-Cholin inhibiert über eine Reduktion der Phospholipase A2 die Freisetzung von Arachidonsäure und reduziert somit die Entstehung freier Sauerstoffradikale nach einer zerebralen Ischämie und Reperfusion [25]. Zusätzlich kann CDP-Cholin toxische Radikale neutralisieren und weist somit direkte antioxidative Effekte auf [26].
4. CDP-Cholin schützt vor postischämischer neuronaler Membranschädigung: ATP-Verbrauch führt zu einer Akkumulation von Cytidin-5’-Monophosphat in den Zellmembranen, die wiederum eine erhöhte Umwandlung von Phosphatidylcholin in Diacylglycerol und freie Fettsäuren bewirkt. Diese Stoffwechselprodukte weisen membrantoxische Eigenschaften auf, da sie zu einer exzessiven Bildung freier Radikale, Lipidperoxide und Arachidonsäure sowie ihrer Metaboliten (Leukotriene) führen können. CDP-Cholin reduziert die Freisetzung von Arachidonsäure. Daraus resultiert ein Schutz der Blut-Hirn-Schranke mit konsekutiver Reduktion des postischämischen Hirnödems und Protektion neuronaler Zellen in der ischämischen Penumbra [4].
CDP-Cholin besitzt neben membranprotektiven Wirkungen bedeutsame membranregenerierende Eigenschaften, da es ein wesentlicher Bestandteil der Phosphatidylcholin-Synthese ist. CDP-Cholin erhöht als Zwischenprodukt der Sphingomyelin-Synthese postischämisch die Plasmaspiegel des wichtigen Membran-Phospholipids Sphingomyelin [27]. CDP-Cholin führt auch zu einer Regeneration von Cardiolipin, dem wichtigsten Phospholipid der inneren Mitochondrien-Membran. Die Regeneration von Sphingomyelinspiegeln nach einer zerebralen Ischämie erfolgt wahrscheinblich über eine Inhibition der Phospholipase A2, was konsekutiv die enzymatische Hydrolyse von Cardiolipin bremst und die Sphingomyelinase inhibiert [4].
5. Synergistische neurotrophe Effekte ließen sich interessanterweise nach einer Kombinationsbehandlung mit dem Wachstumsfaktor bFGF (basic fibroblast growth factor) erzielen: CDP-Cholin (250 mg/kg KG) kombiniert mit bFGF (10 µg) führte zu einer signifikanten Infarktreduktion, während die jeweiligen Einzelbehandlungen wirkungslos blieben [28]. Echte neurotrophe Wirkungen zeigten sich in aktuellen Untersuchungen, in denen mit einer CDP-Cholin-Behandlung erst 24 Stunden nach einem Infarktereignis begonnen wurde: Verum-behandelte Tiere zeigten nicht nur eine signifikante Besserung funktionell-neurologischer Parameter, sondern wiesen auf zellulärer Ebene vermehrte Dendritenverzweigungen sowie eine höhere Synapsendichte als Hinweis für eine vermehrte Plastizität auf [18].
Insgesamt ist die präklinische Datenlage auch unter Berücksichtigung der STAIR(Stroke academic and industry round table)-Empfehlungen als aussagekräftig anzusehen. Somit zählt CDP-Cholin zu den experimentell am besten untersuchten aktuell verfügbaren Substanzen zur Behandlung des Schlaganfalls.
Klinische Studien
CDP-Cholin wurde insgesamt bei mehreren tausend Schlaganfallpatienten in kontrollierten klinischen Studien untersucht. In einer multizentrischen, doppelblinden, Plazebo-kontrollierten Studie wurde die Wirksamkeit von CDP-Cholin bei 272 Patienten mit mittleren bis schweren Schlaganfällen, die eine Bewusstseinstörung aufwiesen, untersucht [29]. 133 Patienten erhielten 1000 mg CDP-Cholin/Tag i. v. über 14 Tage und 139 Patienten erhielten Plazebo. Die CDP-Cholin-Behandlung führte zu einer signifikanten Besserung des Bewusstseinsstatus bei 54% im Vergleich mit 29%, die Plazebo erhielten. In weiteren Studien zeigten sich erste Hinweise, dass CDP-Cholin auch zu einer Verbesserung neurologischer Funktionen (z. B. Lähmungsgrad, Motilität ) oder einer Besserung kognitiver Defizite führt.
In einer multizentrischen, doppelblinden, kontrollierten Studie wurde von Clark et al. erstmals die Wirksamkeit einer oralen Behandlung mit CDP-Cholin bei 259 Schlaganfallpatienten untersucht [30]. Verglichen wurden CDP-Cholin-Dosierungen von 500 mg, 1000 mg, 2000 mg pro Tag und Plazebo über sechs Wochen mit Behandlungsbeginn innerhalb von 24 Stunden nach einem Schlaganfall. Der primäre klinische Endpunkt nach drei Monaten war die Verbesserung in den Alltagsfunktionen, bestimmt mit dem Barthel-Index. Bei Patienten, die mit 500 mg oder 2000 mg CDP-Cholin behandelt wurden, besserten sich die neurologischen Parameter doppelt so häufig wie bei Patienten der Plazebo-Gruppe. Interessanterweise zeigte sich kein Unterschied zwischen der mit 1000 mg CDP-Cholin behandelten Gruppe und der Plazebo-Gruppe. Möglicherweise war hierfür der Gewichtsunterschied zuungunsten der 1000-mg-Gruppe verantwortlich, der zu einer relativen Unterdosierung führte.
Aufgrund dieser positiven Daten führte die Citicoline (CDP-Cholin) Stroke Study Group eine zweite multizentrische Studie durch [31]. In dieser randomisierten Studie wurden 394 Patienten mit einem akuten Schlaganfall im Verhältnis 2:1 mit 500 mg CDP-Cholin oder Plazebo behandelt. Primäre Endpunkte waren eine Verbesserung des Barthel-Index und des neurologischen Defizits, bestimmt mit dem sogenannten NIH Stroke Scale Score (NIHSS). Es fand sich kein Unterschied zwischen den Behandlungsgruppen, vermutlich bedingt durch signifikant schwerere Infarkte in der Verum-Gruppe bei Studieneinschluss.
In einer weiteren multizentrischen Studie wurden 899 Patienten mit akutem Schlaganfall im Versorgungsgebiet der A. cerebri media untersucht und entweder mit CDP-Cholin (1000 mg zweimal täglich über sechs Wochen) oder Plazebo behandelt. Der primäre Endpunkt nach drei Monaten war die Verbesserung des neurologischen Defizits, definiert als eine Besserung um mindestens 7 Punkte auf der NIH Stroke Scale. Nach drei Monaten zeigte sich kein relevanter Unterschied zwischen den Behandlungsgruppen. Allerdings hatten nach der sechswöchigen Behandlungsphase signifikant mehr Patienten eine Besserung im Barthel-Index [32].
Eine MRT-basierte Studie belegte für Patienten mit einem Infarkt im Versorgungsgebiet der A. cerebri media eine dosisabhängige deutliche Reduktion des Infarktwachstums. Dieses Ergebnis korrelierte mit einer Verbesserung des klinisch-neurologischen Parameter der Patienten [33]. Die Patienten in dieser Studie erhielten sechs Wochen lang entweder 500 mg CDP-Cholin (n=41), 2000 mg CDP-Cholin (n=62) oder Plazebo (n=111).
Aufgrund dieser insgesamt vielversprechenden Ergebnisse wurden nach einer präspezifizierten Analyse die Daten dieser vier Studien gepoolt [34]. Dabei galten folgende Einschlusskriterien: Alter≥18 Jahre, therapeutisches Zeitfenster≤24Stunden, Baseline-NIHSS≥8, Baseline-mRS≤1, Hirninfarkt im Versorgungsgebiet der A. cerebri media. Primärer Endpunkt war die prozentuale Anteil der Patienten, der den präspezifizierten kombinierten Endpunkt NIHSS≤1, mRS≤1, Barthel-Index≥95 nach drei Monaten erreichte. Sekundäre Endpunkte waren die drei konstituierenden Einzelpunkte des primären kombinierten Endpunkts sowie Letalität und Sicherheit. Insgesamt wurden somit die Daten von 583 Patienten, die mit Plazebo behandelt wurden, und 782 Patienten, die mit CDP-Cholin behandelt wurden, ausgewertet. Den primären Endpunkt erreichten signifikant mehr Patienten der CDP-Cholin-Gruppe im Vergleich mit der Plazebo-Gruppe (Odds-Ratio [OR] 1,33; 95%-Konfidenzintervall [95%-KI] 1,10–1,62; p = 0,0034). Der größte Effekt wurde von der größten Patientengruppe, die eine CDP-Cholin-Dosis von 2000 mg erhielt, erreicht (OR 1,38; 95%-KI 1,10–1,72; p=0,0043). Für die sekundären Endpunkte, besonders den Barthel-Index und den NIH Stroke Scale Score, zeigten sich ebenfalls signifikante Verbesserungen zugunsten der CDP-Cholin-Behandlung. Die Rate der unerwünschten Arzenimittelwirkungen unterschied sich nicht zwischen der Verum- und Plazebo-Gruppe. Die Letalität war zwischen beiden Behandlungsgruppen identisch.
Aufgrund dieser positiven Daten wurde die ICTUS-Studie (International citicoline trial on acute stroke, ClinicalTrials.gov NCT00331890) initiiert, die nach den Einschlusskriterien der gepoolten Analyse sowie deren Endpunkte entwickelt wurde. In diese Studie, die bis zum Jahre 2011 abgeschlossen sein soll, sollen bis zu 2600 Patienten eingeschlossen werden.
Ausblick
Aufgrund der guten präklinischen Datenlage sowie erster Hinweise auf eine wirksame Verbesserung klinisch-neurologischer Symptome bei Schlaganfallpatienten stellt CDP-Cholin eine interessante und neue Behandlungsmöglichkeit des Schlaganfalls dar. Da es sehr gut verträglich ist, wird es bereits seit vielen Jahren in mehreren europäischen Ländern sowie Südamerika zur Schlaganfallbehandlung verwendet. In Deutschland erlangte CDP-Cholin kürzlich die Zulassung als ergänzend bilanzierte Diät (Ceraxon®). Nach strengen evidenzbasierten Kriterien fehlt bislang zwar ein Wirkungsnachweis aus einer multizentrischen Phase-III-Studie, dieser wird mit der aktuell laufenden ICTUS-Studie jedoch angestrebt. Nach Abwägung der positiven und plausiblen regenerativen Wirkungen nach einem Schlaganfall und der sehr guten Verträglichkeit könnte CDP-Cholin die Therapie des Schlaganfalls bereichern.
Literatur
1. Secades JJ, Frontera G. CDP-choline: pharmacological and clinical review. Methods Find Exp Clin Pharmacol 1995;17:1–54.
2. Weiss GB. Metabolism and actions of CDP-choline as an endogenous compound and administered exogenously as citicoline. Life Sci 1995;56:637–60.
3. D’Orlando KJ, Sandage BW Jr. Citicoline (CDP-choline): mechanisms of action and effects in ischemic brain injury. Neurol Res 1995;17:281–4.
4. Rao AM, Hatcher JF, Dempsey RJ. CDP-choline: neuroprotection in transient forebrain ischemia of gerbils. J Neurosci Res 1999;58:697–705.
5. Dinsdale JR, Griffiths GK, Rowlands C, et al. Pharmacokinetics of 14C CDP-choline. Arzneimittelforschung 1983;33:1066–70.
6. Agut J, Font E, Sacristan A, Ortiz JA. Radioactivity incorporation into different cerebral phospholipids after oral administration of 14C methyl CDP-choline. Arzneimittelforschung 1983;33:1048–50.
7. López G.-Coviella I, Wurtman RJ. Enhancement by cytidine of membrane phospholipid synthesis. J Neurochem 1992;59:338–43.
8. López G.-Coviella I, Agut J, Savci V, et al. Evidence that 5’-cytidinediphosphocholine can affect brain phospholipid composition by increasing choline and cytidine plasma levels. J Neurochem 1995;65:889–94.
9. Babb SM, Wald LL, Cohen BM, et al. Chronic citicoline increases phosphodiesters in the brains of healthy older subjects: an in vivo phosphorus magnetic resonance spectroscopy study. Psychopharmacology (Berl) 2002;161:248–54.
10. Grau T, Romero A, Sacristan A, Ortiz JA. CDP-choline: acute toxicity study. Arzneimittelforschung 1983;33:1033–4.
11. Romero A, Grau T, Sacristan A, Ortiz JA. Study of subacute toxicity of CDP-choline after 30 days of oral administration to rats. Arzneimittelforschung 1983;33:1035–8.
12. Romero A, Grau T, Sacristan A, Ortiz JA. CDP-choline: 6-month study on toxicity in dogs. Arzneimittelforschung 1983;33:1038–42.
13. Dinsdale JR, Griffiths GK, Castello J, et al. CDP-choline: repeated oral dose tolerance studies in adult healthy volunteers. Arzneimittelforschung 1983;33:1061–5.
14. Lozano Fernandez R. Efficacy and safety of oral CDP-choline. Drug surveillance study in 2817 cases. Arzneimittelforschung 1983;33:1073–80.
15. Schäbitz WR, Fisher M. Perspectives on neuroprotective stroke therapy. Biochem Soc Trans 2006;34:1271–6.
16. Aronowski J, Strong R, Grotta JC. Citicoline for treatment of experimental focal ischemia: histologic and behavioural outcome. Neurol Res 1996;18:570–4.
17. Schäbitz WR, Weber J, Takano K, et al. The effects of prolonged treatment with citicoline in temporary experimental focal ischemia. J Neurol Sci 1996;138:21–5.
18. Hurtado O, Cárdenas A, Pradillo JM, Morales JR, et al. A chronic treatment with CDP-choline improves functional recovery and increases neuronal plasticity after experimental stroke. Neurobiol Dis 2007;26:105–11.
19. Hurtado O, Moro MA, Cárdenas A, Sánchez V, et al. Neuroprotection afforded by prior citicoline administration in experimental brain ischemia: effects on glutamate transport. Neurobiol Dis 2005;18:336–45.
20. Andersen M, Overgaard K, Meden P, et al. Effects of citicoline combined with thrombolytic therapy in a rat embolic stroke model. Stroke 1999;30:1464–71.
21. Gutiérrez M, Díez Tejedor E, Alonso de Leciñana M, Fuentes B, et al. Thrombolysis and neuroprotection in cerebral ischemia. Cerebrovasc Dis 2006;21(Suppl 2): 118–26.
22. Shuaib A, Yang Y, Li Q. Evaluating the efficacy of citicoline in embolic ischemic stroke in rats: neuroprotective effects when used alone or in combination with urokinase. Exp Neurol 2000;161:733–9.
23. Yen CL, Mar MH, Zeisel SH. Choline deficiency- induced apoptosis in PC12 cells is associated with diminished membranephosphatidylcholine and sphingomyelin, accumulation of ceramide and diacylglycerol, and activation of a caspase. FASEB J 1999;13:135–42.
24. Adibhatla RM, Hatcher JF, Dempsey RJ. Citicoline: neuroprotective mechanisms in cerebral ischemia. J Neurochem 2002;80: 12–23.
25. Adibhatla RM, Hatcher JF. Citicoline mechanisms and clinical efficacy in cerebral ischemia. J Neurosci Res 2002;70:133–9.
26. Fresta M, Puglisi G, Di Giacomo C, Russo A. Liposomes as in vivo carriers for citicoline: effects on rat cerebral post-ischaemic reperfusion. J Pharm Pharmacol 1994;46:974–81.
27. Adibhatla RM, Hatcher JF. Citicoline decreases phospholipase A2 stimulation and hydroxyl radical generation in transient cerebral ischemia. J Neurosci Res 2003;73:308–15.
28. Schäbitz WR, Li F, Irie K, Sandage BW, et al. Synergistic effects of a combination of low-dose basic fibroblast growth factor and citicoline after temporary experimental focal ischemia. Stroke 1999;30:427–31.
29. Tazaki Y, Sakai F, Otomo E, et al. Treatment of acute cerebral infarction with a choline precursor in a multicenter double-blind placebo-controlled study. Stroke 1988;19:211–6.
30. Clark WM, Warach SJ, Pettigrew LC, et al.; Citicoline Stroke Study Group. A randomized dose-response trial of citicoline in acute ischemic stroke patients. Neurology 1997;49:671–8.
31. Clark WM, Williams BJ, Selzer KA, et al. A randomized efficacy trial of citicoline in patients with acute ischemic stroke. Stroke 1999;30:2592–7.
32. Clark WM, Wechsler LR, Sabounjian LA, Schwiderski UE; Citicoline Stroke Study Group. A phase III randomized efficacy trial of 2000 mg citicoline in acute ischemic stroke patients. Neurology 2001;57:1595–1602.
33. Warach S, Pettigrew LC, Dashe JF, Pullicino P, et al. Effect of citicoline on ischemic lesion volume as measured by diffusion MRI. International Stroke Conference, San Antonio, 2002, Feb 2–9 [Abstract].
34. Davalos A, Castillo J, Alvarez-Sabin J, et al. Oral citicoline in acute ischemic stroke: an individual patient data pooling analysis of clinical trials. Stroke 2002;33:2850–7.
Prof. Dr. Wolf-Rüdiger Schäbitz, Neurologische Klinik und Poliklinik, Westfälsche Wilhelms-Universität, Albert-Schweitzer-Str. 33, 48149 Münster, E-Mail: schabitz@uni-muenster.de
CDP-choline for the treatment of stroke
CDP-choline is an essential element of the cell membrane-phospholipid biosynthesis, and hereby important for membrane regeneration after stroke or other neurological diseases. Recent studies showed, that CDP-choline exerts additional multimodal mechanisms of action after stroke such as anti-excitotoxic, anti-apoptotic and antioxidant effects. CDP-choline improves the neurological deficits and decreases the infarct volume in a number of preclinical studies. Due to its very good tolerability CDP-choline has been used used for the treatment of stroke in Europe, Latin America and Asia for more than 30 years. Controlled clinical studies recently showed first signs of improvement of the neurological deficits of stroke patients after treatment with this substance. CDP-choline may therefore be an alternative for the treatment of stroke, especially when considering the very good benefit-risk ratio.
Keywords: CDP-Cholin, stroke, regeneration, neuroprotection
Psychopharmakotherapie 2009; 16(03)
