Michael Bauer, Dresden, Tom Bschor, Berlin, Andrea Pfennig, Dresden, Peter C. Whybrow, Los Angeles, Jules Angst, Zürich, Marcio Versiani, Rio de Janeiro, Hans-Jürgen Möller, München, und WFSBP Task Force on Unipolar Depressive Disorders*
Prof. Dr. med. Dr. rer. nat. Michael Bauer (Korrespondenzautor), Klinik und Poliklinik für Psychiatrie und Psychotherapie, Universitätsklinikum Carl Gustav Carus, Technische Universität Dresden, Fetscherstr. 74, 01307 Dresden, Deutschland, E-Mail: michael.bauer@uniklinikum-dresden.de
Dr. med. Andrea Pfennig, Universitätsklinikum Carl Gustav Carus, Klinik und Poliklinik für Psychiatrie und Psychotherapie, Technische Universität Dresden, Dresden, Deutschland Priv.-Doz. Dr. med. Tom Bschor, Jüdisches Krankenhaus Berlin, Klinik für Psychiatrie and Psychotherapie, Berlin, Deutschland Prof. Dr. Peter C. Whybrow, Semel Institute for Neuroscience and Human Behavior, Department of Psychiatry and Biobehavioral Sciences, University of California Los Angeles (UCLA), Los Angeles, CA, USA Prof. Dr. med. Jules Angst, Universitätsklinik Zürich, Klinik für Psychiatrie, Zürich, Schweiz Prof. Dr. Marcio Versiani, Federal University of Rio de Janeiro, Department of Psychiatry, Rio de Janeiro, Brasilien Prof. Dr. med. Hans-Jürgen Möller, Klinik und Poliklinik für Psychiatrie und Psychotherapie, Klinikum der Ludwig-Maximilians-Universität München, München, Deutschland * WFSBP Task Force on Unipolar Depressive Disorders: Michael Bauer, Deutschland (Vorsitzender); Jules Angst, Schweiz (Co-Vorsitzender); Marcio Versiani, Brasilien (Co-Vorsitzender); Andrea Pfennig, Deutschland (wissenschaftlicher Sekretär), Hans-Jürgen Möller, Deutschland (vorheriger WFSBP-Präsident), Siegfried Kasper, Österreich (WFSBP-Präsident) Hervé Allain, Frankreich Ian Anderson, Großbritannien José L. Ayuso-Gutierrez, Spanien David Baldwin, Großbritannien Per Bech, Dänemark Otto Benkert, Deutschland Michael Berk, Australien Istvan Bitter, Ungarn Marc L. Bourgeois, Frankreich Graham Burrows, Australien Giovanni Cassano, Italien Marcelo Cetkovich-Bakmas, Argentinien John C. Cookson, Großbritannien Delcir da Costa, Brasilien Mihai D. Gheorghe, Rumänien Gerardo Heinze, Mexiko Teruhiko Higuchi, Japan Robert M.A. Hirschfeld, USA Cyril Höschl, Tschechische Republik Edith Holsboer-Trachsler, Schweiz Rhee-Hun Kang, Korea Cornelius Katona, Großbritannien Martin B. Keller, USA E. Kostukova, Russland Parmanand Kulhara, Vereinte Arabische Emirate David J. Kupfer, USA Yves Lecrubier, Frankreich Brian Leonard, Irland Rasmus W. Licht, Dänemark Se-Won, Lim, Korea Odd Lingjaerde, Norwegen Henrik Lublin, Dänemark Julien Mendlewicz, Belgien Philip Mitchell, Australien Jong-Woo Paik, Korea Yong Chon Park, Korea Eugene S. Paykel, Großbritannien Stanislaw Puzynski, Polen A. John Rush, USA Janusz K. Rybakowski, Polen Isaac Schweitzer, Australien Andre Tylee, Großbritannien Jürgen Unützer, USA Per Vestergaard, Dänemark Eduard Vieta, Spanien Peter C. Whybrow, USA Kazuo Yamada, Japan
Die englische Originalfassung ist erschienen in World J Biol Psychiatry 2007;8:67–104.
Inhaltsverzeichnis
Zusammenfassung 239
Zusammenfassung der Empfehlungen 240
–Allgemeine Empfehlungen 240
–Spezifische Behandlungsempfehlungen 241
1 Unipolare depressive Störungen 241
1.1 Einführung 241
1.2 Ziel und Zielgruppe der WFSBP-Leitlinien 242
1.3 Methoden der Literatursuche und Datenauswertung 242
1.4 Evidenzbasierte Klassifikation der Empfehlungen 242
1.5 Epidemiologie und Verlauf der Major Depression 243
1.6 Indikationen und Ziele der Behandlung der Major
Depression 244
2 Akutbehandlung der Major Depression 245
2.1 Antidepressiva 246
2.2 Pflanzliche Wirkstoffe 253
2.3 Elektrokrampftherapie 254
2.4 Psychotherapie 254
2.5 Lichttherapie (Phototherapie) 254
2.6 Zusätzliche Therapie 255
2.7 Weitere Behandlungsmöglichkeiten 256
3 Erhaltungstherapie der Major Depression 256
4 Rezidivprophylaktische Behandlung der Major
Depression 256
4.1 Allgemeine Behandlungsprinzipien der Rezidiv-
prophylaxe 256
4.2 Pharmakotherapie der Rezidivprophylaxe 257
4.3 Dauer und Ende einer Rezidivprophylaxe 260
4.4 Konversion von einer unipolaren depressiven zu
einer bipolaren Störung 261
4.5 Psychotherapie 261
5 Behandlung chronischer depressiver Störungen 261
5.1 Dysthyme Störungen 261
5.2 Pharmakotherapie dysthymer Störungen 261
6 Behandlung in speziellen Situationen 262
6.1 Depression in Komorbidität mit anderen
psychiatrischen Erkrankungen 262
6.2 Depressionsbehandlung bei älteren Patienten 262
6.3 Behandlungsresistente Depression 263
6.4 Behandlung der Depression bei Kindern und
Jugendlichen 263
6.5 Depressionsbehandlung während Schwanger-
schaft und Stillzeit 264
7 Aktualisierung der Leitlinie 264
8 Referenzen (im Internet)
Zusammenfassung der Empfehlungen
Allgemeine Empfehlungen
Bei Patienten, welche die diagnostischen Kriterien für eine Major Depression (DSM-IV) oder eine unipolare depressive Episode (ICD-10) erfüllen, sollte im Allgemeinen eine biologische Behandlung (pharmakologische und nichtpharmakologische Ansätze) empfohlen werden. Vor Behandlungsbeginn sollte ein umfassender Behandlungsplan entwickelt werden, der auf der Anamnese und den Erfahrungen aus vorherigen Behandlungen, dem derzeitigen klinischen Subtyp, gegenwärtigen Untersuchungsbefunden, der Schwere der Erkrankung und dem Suizidrisiko basiert. Komorbide psychiatrische oder somatische Erkrankungen, nichtpsychotrope Medikation und psychosoziale Stressfaktoren sollten sorgfältig beachtet werden, da diese zu einem depressiven Syndrom beitragen oder mit der Behandlung interferieren können. Die Familienanamnese sollte auf das Vorliegen affektiver Störungen überprüft werden. Unabhängig von der Wahl der biologischen Behandlungsmethode sollte das klinische und psychiatrische Management begonnen und während der gesamten Behandlung beibehalten werden. Dieses beinhaltet das Festlegen des Behandlungsplans und -rahmens, den Aufbau und Erhalt einer therapeutischen Allianz, das Monitoring und Überprüfen des psychiatrischen Status einschließlich des Suizidrisikos, die Überprüfung der Richtigkeit der Diagnose und das Monitoring des Ansprechens des Patienten auf die Behandlung, eventuell auftretender Nebenwirkungen und des körperlichen Allgemeinzustands des Patienten sowie die Aufklärung des Patienten und dessen Angehörigen über die Wichtigkeit der Adhärenz für die Behandlung.
Das letztendliche Ziel der akuten Behandlungsphase ist das Erreichen einer Remission. Nach zwei- bis vierwöchiger Behandlung mit Antidepressiva sollte das Therapieansprechen evaluiert werden und im Falle eines unzureichenden Ansprechens sollten Strategien der Behandlungsoptimierung angewandt werden. Insgesamt können mindestens acht bis zehn Wochen notwendig sein, um das ganze Ausmaß der Symptomreduktion bestimmen zu können, welche vor Beginn der Erhaltungstherapie erreicht werden muss. Je schwerer die Depression ist, desto größer ist der potenzielle Nutzen einer adäquaten Behandlung.
Ziele der Erhaltungstherapie sind, einem frühen Rückfall vorzubeugen, alle Residualsymptome zu beseitigen und das psychosoziale und berufliche Funktionsniveau des Patienten wiederherzustellen.
Ziele der rezidivprophylaktischen Therapie (Langzeittherapie) sind die Verhinderung erneuter depressiver Episoden und von Suizid. Sie ist auf jeden Fall indiziert in Situationen mit einem hohen Rückfallrisiko, beispielsweise bei Patienten, die bereits drei oder mehr Episoden einer Major Depression oder eine hohe bisherige Rückfallfrequenz (z.B. zwei Episoden innerhalb von fünf Jahren) aufweisen. Die Rückfallprophylaxe kann über einen Zeitraum von drei Jahren bis lebenslang nötig sein. Im Allgemeinen sollte die Rückfallprophylaxe desto länger andauern, je schlechter die Prognose ist. Die erfolgreiche Behandlung depressiver Patienten mit Antidepressiva schließt die Aufklärung der Patienten und deren Angehörigen über die verfügbaren Behandlungsmöglichkeiten, die Dauer bis zu den ersten erkennbaren Anzeichen für ein Ansprechen auf die Behandlung, mögliche frühe Nebenwirkungen und den Umgang mit diesen sowie über den erwarteten Behandlungsverlauf ein.
Spezifische Behandlungs-empfehlungen
Antidepressiva sind die Behandlung der ersten Wahl für eine mittelschwere bis schwere depressive Episode. Abhängig von individuellen Charakteristika und/oder Wünschen des Patienten kann auch bei leichten depressiven Episoden eine Behandlung mit Antidepressiva indiziert sein, andernfalls können psycho- und soziotherapeutische Ansätze allein ausreichen.
Bei der Auswahl eines Antidepressivums sollten folgende Faktoren beachtet werden: Vorerfahrungen des Patienten mit dem Medikament (Response, Verträglichkeit, unerwünschte Wirkungen), gleichzeitig bestehende körperliche Erkrankungen und die Einnahme nichtpsychotroper Medikamente, kurz- und langfristige Nebenwirkungen des Medikaments, die Erfahrung des Arztes mit dem Medikament, die bisherige Adhärenz des Patienten für Medikamente, die Response von Erstgrad-Angehörigen des Patienten auf eine Medikation, die Patientenpräferenzen sowie die Kosten und die Verfügbarkeit spezifischer Antidepressiva.
Für keine Antidepressivaklasse wurde nachgewiesen, dass sie wirksamer wäre oder einen schnelleren Wirkungseintritt zeigen würde als eine andere, obwohl einige trizyklische Antidepressiva (TZA) (Amitriptylin und Clomipramin) sowie Venlafaxin bei schwer depressiven, hospitalisierten Patienten etwas wirksamer sind als selektive Serotonin-Wiederaufnahmehemmer (SSRI). Antidepressiva unterscheiden sich beträchtlich in ihren Nebenwirkungsprofilen, ihren potenziellen Wechselwirkungen mit anderen Medikamenten und ihrer Gefährlichkeit bei Überdosierung. Neuere Antidepressiva der zweiten Generation (z.B. Bupropion, Maprotilin, Mianserin, Trazodon) und der dritten Generation (z.B. SSRI, SNRI, Mirtazapin, Reboxetin) werden im Allgemeinen besser toleriert als die älteren Antidepressiva der ersten Generation, so dass die Patienten die Behandlung weniger häufig abbrechen.
Bei mindestens 30% der depressiven Episoden werden die Patienten, unabhängig von der Wahl des Antidepressivums, nicht genügend auf die adäquat durchgeführte antidepressive Behandlung der ersten Wahl ansprechen. In dieser Situation ist die sorgfältige Überprüfung der Diagnose, der richtigen Medikamentendosierung und der Compliance des Patienten nötig. Wenn die vorgenannten Gründe die fehlende Response nicht erklären, kommen folgende weitere Strategien in Frage:
1. Wechsel zu einem Antidepressivum aus einer anderen pharmakologischen Klasse,
2. Wechsel zu einem Antidepressivum aus derselben pharmakologischen Klasse,
3. Kombination zweier Antidepressiva aus unterschiedlichen pharmakologischen Klassen,
4. Augmentation des Antidepressivums mit anderen Wirkstoffen (z.B. einem Lithiumsalz [im Folgenden: Lithium], Schilddrüsenhormon, Pindolol, Estrogen, Buspiron, atypischen Antipsychotika), um die antidepressive Wirkung zu verstärken, und
5. Kombination des Antidepressivums mit einer psychotherapeutischen Intervention.
Von diesen Strategien ist die Augmentation mit Lithium die wichtigste und am besten dokumentierte Strategie.
Elektrokrampftherapie (EKT) sollte als Strategie der ersten Wahl nur in besonderen Situationen in Betracht gezogen werden, die eine schnelle Besserung der Depression verlangen (z.B. bei schwerer psychotischer Depression, schwerer Depression mit psychomotorischer Verlangsamung, „echter“ behandlungsresistenter Depression, anhaltender Verweigerung der Nahrungsaufnahme, schwerer Suizidalität) sowie bei Patienten mit positivem Ansprechen auf eine EKT-Behandlung in der Vergangenheit. Die Patienten sollten an einen Psychiater/Nervenarzt überwiesen werden.
Die Medikation der Wahl für die Rezidivprophylaxe einer Major Depression ist entweder das Antidepressivum, mit dem in der Akut- und Erhaltungsphase eine Remission erreicht wurde (in gleicher Dosierung), oder Lithium. Im letzteren Fall werden gewöhnlich Lithiumserumspiegel (gemessen 12 Stunden nach der letzten Lithiumgabe) von 0,5 bis 0,8 mmol/l (mEq/l) empfohlen, die regelmäßig kontrolliert werden sollten. Kein anderer Mood-Stabilizer, welcher zur Behandlung bipolarer Störungen verwendet wird (z.B. Valproat [Divalproex], Lamotrigin oder Gabapentin) ist bisher für die Rezidivprophylaxe einer Major Depression in randomisierten, kontrollierten Studien untersucht worden. Obwohl Daten aus kontrollierten Studien nur in begrenztem Umfang vorliegen, bestätigen die Ergebnisse die Wirksamkeit einer Reihe von Antidepressiva (TZA, SSRI, SNRI und anderer neuerer Antidepressiva) bei dysthymen Störungen.
1 Unipolare depressive Störungen
1.1 Einführung
Unipolare depressive Störungen sind ausschließlich durch depressive Symptome gekennzeichnet; aktuell und in der Vergangenheit lag keine manische/hypomane Symptomatik vor. Diese Charakterisierung unterscheidet sie von bipolaren affektiven Störungen. Die unipolaren depressiven Störungen lassen sich in drei diagnostische Hauptgruppen unterteilen (ICD-10 Diagnosen, World Health Organization 1992 [380]; die entsprechenden DSM-IV Diagnosen [12] befinden sich in Klammern):
- Depressive Episode oder rezidivierende depressive Störungen (DSM-IV: Major Depressive Disorder [MDD] – einzelne Episode oder rezidivierend)
- Dysthymie (DSM-IV: Dysthyme Störung und andere chronisch depressive Störungen [MDD in unvollständiger Remission und chronische MDD])
- Depressive Episode, unspezifiziert, rezidivierende kurze depressive Störung (DSM-IV: „unterschwellige Depressionen“)
Von diesen ist die Major Depression (MDD) die am besten untersuchte unipolare depressive Störung, auf die sich die hier gegebenen Empfehlungen zu Akuttherapie, Erhaltungstherapie und Rezidivprophylaxe fokussieren.
1.2 Ziel und Zielgruppe der WFSBP-Leitlinien
Diese WFSBP-Leitlinien bieten den aktuellsten Stand des derzeitigen Wissens zu unipolaren depressiven Störungen und auf Evidenz basierende Behandlungsempfehlungen. Sie wurden von den Autoren entwickelt und von der WFSBP Task Force für unipolare depressive Störungen, die aus 46 international renommierten Wissenschaftlern und Klinikern besteht, verabschiedet. Die klinischen Empfehlungen dieser Leitlinien basieren auf einer systematischen Übersicht der verfügbaren Evidenz bezüglich der Behandlung unipolarer depressiver Störungen und beinhalten weiterhin wichtige klinische und wissenschaftliche Neuerungen. Zudem werden die Meinungen zum State-of-the-Art der Behandlung unipolarer depressiver Störungen verschiedener wissenschaftlich anerkannter Experten und internationaler Vertreter zusammengefasst. Im Falle der wenigen Fragen, in denen kein Konsens erreicht werden konnte, wurde den Autoren die endgültige Entscheidung übertragen.
Die Leitlinien zur Behandlung unipolarer depressiver Störungen wurden erstmalig 2002 in zwei Teilen veröffentlicht [39, 40] und waren für den Gebrauch aller Ärzte, insbesondere Psychiater/Nervenärzte, bestimmt. Die vorliegende Version wurde vollständig überarbeitet. Sie ist an Hausärzte gerichtet, die Patienten mit depressiven Symptomen behandeln, und beschränkt sich im Wesentlichen auf die wichtigsten Fragen der hausärztlichen Versorgung und auf die in hausärztlichen Praxen möglichen Behandlungen. Die Ausführungen können ausschließlich als Leitlinien dienen, da die endgültige Entscheidung für ein Behandlungverfahren vom verantwortlichen behandelnden Arzt entsprechend dem klinischen Gesamtbild des Patienten und den verfügbaren Diagnose- und Behandlungsmöglichkeiten getroffen werden muss. Die vorliegenden Leitlinien beschäftigen sich primär mit den biologischen (somatischen) Behandlungsmöglichkeiten (z.B. der Behandlung mit Antidepressiva). Psychotherapeutische Behandlungsverfahren werden nur kurz behandelt. Die Leitlinien umfassen nicht jene depressiven Störungen, die im Rahmen bipolarer affektiver Störungen auftreten (diese werden in gesonderten WFSBP-Leitlinien abgehandelt [142–144]). Da die Verfügbarkeit von Medikamenten, Behandlungsformen und diagnostischen Verfahren zwischen einzelnen Ländern beträchtlich variieren kann, haben die Autoren mehrere unterschiedliche Behandlungsmöglichkeiten in die Leitlinien aufgenommen.
1.3 Methoden der Literatursuche und Datenauswertung
Die Daten, die für die Erstellung der Leitlinien verwendet wurden, stammen aus folgenden Quellen: Agency for Health Care Policy and Research (AHCPR) Depression Guidelines Panel [2]; AHCPR Evidence Report on Treatment of Depression: Newer Pharmacotherapies [3]; American Psychiatric Association (APA) Practice Guideline for the Treatment of Patients with Major Depressive Disorder, Revision [14]; British Association for Psychopharmacology Revised Guidelines for Treating Depressive Disorders [16]; Canadian Psychiatric Association and the Canadian Network for Mood and Anxiety Treatments, CANMAT, Clinical Guidelines for the Treatment of Depressive Disorders [71]; Canadian Consensus Guidelines for the Treatment of Seasonal Affective Disorder [200]; Deutsche Gesellschaft für Psychiatrie, Psychotherapie und Nervenheilkunde, DGPPN, Praxisleitlinien in Psychiatrie und Psychotherapie, affektive Erkrankungen [93]; The Cochrane Library; World Federation of Societies of Biological Psychiatry WFSBP Guidelines for biological treatment of unipolar depressive disorders [39, 40]; Metaanalysen über die Wirksamkeit antidepressiver Medikamente, die mit Hilfe einer MEDLINE-Recherche (bis zum 1. Februar 2005) gefunden wurden; relevante Übersichtsarbeiten, die bei der Suche in der MEDLINE-Datenbank und in Lehrbüchern gefunden wurden, sowie individuelle klinische Erfahrungen der Autoren und Mitglieder der WFSBP-Arbeitsgruppe für unipolare depressive Störungen. Beim Zitieren von Originaldaten wurden nur Artikel in englischer Sprache berücksichtigt, die in Fachzeitschriften mit „peer-review“-Verfahren vor Februar 2005 veröffentlicht wurden. Weitere wichtige Evidenz aus Artikeln, die nach diesem Zeitpunkt veröffentlicht wurden, ist durch Fußnoten gekennzeichnet.
1.4 Evidenzbasierte Klassifikation der Empfehlungen
Jede Behandlungsempfehlung wurde im Hinblick auf ihre Evidenzstärke für ihre Wirksamkeit, Sicherheit und Durchführbarkeit[1] bewertet. Tägliche Behandlungskosten wurden jedoch wegen weltweit unterschiedlicher Medikamentenkosten nicht in Betracht gezogen. Es wurden folgende vier Evidenz-Level genutzt:
Level A: Gute studienbasierte Evidenz, um die Empfehlung zu belegen. Dieser Level wird erreicht, wenn die Evidenz zur Wirksamkeit aus mindestens drei mittelgroßen randomisierten, kontrollierten (doppelblinden) Studien (randomized controlled trials, RCT) stammt, welche einen Vorteil der Intervention zeigten. Mindestens eine dieser drei Studien musste eine gut durchgeführte, Plazebo-kontrollierte Studie sein.
Level B: Mittelmäßige studienbasierte Evidenz, um die Empfehlung zu belegen. Die Wirksamkeit muss in mindestens zwei mittelgroßen randomisierten, doppelblinden Studien (dies können zwei oder mehr Vergleichsstudien gegen andere Substanzen oder eine Vergleichsstudie gegen eine andere Substanz und eine Plazebo-kontrollierte Studie sein) oder in einer mittelgroßen randomisierten, doppelblinden Studie (Plazebo-kontrolliert oder gegen eine andere Substanz) und in einer oder mehreren prospektiven, mittelgroßen (mit mindestens 50 Studienteilnehmern), offenen, naturalistischen Studien nachgewiesen sein.
Level C: Geringe studienbasierte Evidenz, um die Empfehlung zu belegen. Dieser Level wird erreicht, wenn eine randomisierte, doppelblinde Studie gegen eine andere Substanz und eine prospektive, offene Studie/Fallserie (mit mindestens 10 Studienteilnehmern) oder mindestens zwei prospektive, offene Studien/Fallserien (mit mindestens 10 Studienteilnehmern) eine Wirksamkeit zeigen.
Level D: Auf Expertenmeinung basierend (Autoren und Mitglieder der WFSBP Task Force für unipolare depressive Störungen) unterstützt von Evidenz aus mindestens einer prospektiven offenen Studie/Fallserie (mit mindestens 10 Studienteilnehmern).
Kein Evidenz-Level: Expertenmeinung zu allgemeinen Behandlungsverfahren und -prinzipien.
1.5 Epidemiologie und Verlauf der Major Depression
Die Major Depression (MDD) ist eine schwere affektive Störung, die mit signifikant erhöhter Morbidität und Mortalität assoziiert ist und die Personen jeden Alters und Herkunft betreffen kann. Die Global-Burden-of-Disease-(GBD-) Studie der Weltgesundheitsorganisation (WHO) hat gewisse Variationen zwischen Ländern und Regionen aufgezeigt, jedoch sind sich die Muster und Trends im Hinblick auf depressive Störungen weltweit bemerkenswert ähnlich [242, 243]. Die Major Depression ist durch eine einzelne oder rezidivierende depressive Episoden (MDEs) gekennzeichnet. Wesentliches Merkmal einer majoren depressiven Episode ist die mindestens zwei Wochen andauernde depressive Stimmungslage mit Beeinträchtigungen der neurovegetativen Funktionen (z.B. Appetit, Gewichtsverlust, Schlafstörungen), der psychomotorischen Aktivität (z.B. Antriebslosigkeit und Interessenverlust, Erregung oder Verlangsamung), der Kognition (z.B. Gefühle von Wert- und Hoffnungslosigkeit oder unangemessener Schuld) sowie mit Angst und Suizidgedanken (Tab. 1).
Tab. 1. Klassifikation und Kriterien einer Major Depression (DSM-IV) und einer depressiven Episode (ICD-10)
|
ICD-10a (Code) |
DSM-IVb (Code) |
|
A. Depressive Episode Leicht (F32.0): mindestens 2 Hauptsymptome, plus mindestens 2 Zusatzsymptome (kein Symptom besonders ausgeprägt) Mittelschwer (F32.1): mindestens 2 Hauptsymptome, plus mindestens 3 Zusatzsymptome Schwer (F32.2): alle 3 Hauptsymptome, plus mindestens 4 Zusatzsymptome B. Rezidivierende depressive Störung (F33): wiederholte depressive Episoden |
Major Depression Einzelne Episode (296.2x) Rezidivierend (296.3x) |
|
Kurzgefasste Kriterien der depressiven Episode: Mindestdauer der Episode: etwa 2 Wochen Hauptsymptome: 1. Depressive Stimmung 2. Verlust von Interesse und Freude 3. Antriebsmangel, erhöhte Ermüdbarkeit Zusatzsymptome: 1. Verminderte Konzentration und Aufmerksamkeit 2. Vermindertes Selbstwertgefühl und Selbstvertrauen 3. Gedanken der Schuld und Wertlosigkeit 4. Erregung oder Verlangsamung 5. Gedanken an Selbstverletzung oder Suizid bzw. entsprechende Handlungen 6. Schlafstörungen 7. Verminderter Appetit |
Kurzgefasste Kriterien der Major Depression: A Mindestens 5 der folgenden Symptome waren während der letzten 2 Wochen die meiste Zeit des Tages oder fast jeden Tag vorhanden (1. und 2. müssen eingeschlossen sein): 1. Depressive Stimmung 2. Verlust von Interesse und Freude an beinahe allen Aktivitäten 3. Signifikante Gewichtsab- oder -zunahme (mehr als 5% Änderung innerhalb 1 Monats) oder Abnahme oder Steigerung des Appetits an nahezu jedem Tag 4. Schlaflosigkeit oder vermehrter Schlaf 5. Psychomotorische Erregung oder Verlangsamung (durch andere beobachtbar) 6. Erschöpfung oder Antriebsverlust 7. Gefühl der Wertlosigkeit oder übermäßige und ungerechtfertigte Schuldgefühle (nicht nur Selbstvorwürfe, krank zu sein) 8. Verminderte Denk- und Konzentrationsfähigkeit oder Entschlusslosigkeit (entweder durch subjektive Einschätzung oder festgestellt durch andere Personen) 9. Wiederkehrende Gedanken an den Tod (nicht nur Angst zu sterben) oder wiederkehrende Suizidgedanken oder Suizidversuch oder einen spezifischen Suizidplan B Die Symptome verursachen klinisch signifikantes Leiden oder Einschränkungen in sozialen, beruflichen oder anderen wichtigen Funktionsbereichen. C Die Symptome sind nicht Folge einer direkten körperlichen Wirkung einer Substanz (z.B. Droge, Medikament) oder eines medizinischen Krankheitsfaktors (z.B. Hyperthyreose) oder einer Erkrankung. D Die Symptome lassen sich nicht besser durch eine einfache Trauerreaktion erklären (obwohl diese durch eine Major Depression verschlimmert werden kann). |
a10. Revision der Internation Classification of Diseases (World Health Organization 1992 [380]) b4. Revision des American Psychiatric Association’s Diagnostic and Statistics Manual (American Psychiatric Association 1994)
Die Major Depression hat eine mittlere Lebenszeitprävalenz von 16,1% (Spanne 4,4–18) [361, 378]. Die 12-Monats-Prävalenz beträgt zwischen 5% und 10%, wobei Frauen ein höheres Risiko aufweisen als Männer (das Verhältnis beträgt ca. 2:1) [159, 182, 267, 276].
Mindestens 10% aller Patienten, die sich in hausärztlichen Versorgungseinrichtungen vorstellen, leiden an Depressionen [29, 355]. Unter diesen Patienten zeigen etwa 50% hauptsächlich oder ausschließlich somatische Symptome [117]. Von allen Patienten, die sich in der hausärztlichen Versorgung mit einer depressiven Symptomatik vorstellen, leiden 25% an einer Major Depression, 30% an einer Minor Depression (2–4 depressive Symptome über mindestens 2Wochen) und bei 45% der Patienten handelt es sich um unspezifische depressive Symptome. Zusammen betrachtet könnten die beiden letzteren Gruppen als eine „unterschwellige“ Depression bezeichnet werden [29]. Sogar schwer depressive Patienten werden häufig in der hausärztlichen Versorgung gesehen, da diese Patienten aufgrund der Schwere der Symptome oft meinen, an einer somatischen Erkrankung zu leiden.
Die Major Depression kann in jedem Alter, sogar bereits in der Kindheit oder Adoleszenz beginnen, jedoch gibt es Erkrankungsgipfel im zweiten und vierten Lebensjahrzehnt [14, 22]. Das mittlere Alter bei erstmaligem Auftreten einer Major Depression wurde auf 30 Jahre geschätzt [378].
Eine unbehandelte depressive Episode hält rund sechs Monate oder auch länger an [14, 22, 320, 360]. Die moderne Pharmakotherapie kann die Beeinträchtigungen während der akuten Episoden lindern. Plazebo-kontrollierte Studien zeigen, dass unter psychopharmakologischer Behandlung Response und Remission deutlich schneller erreicht werden. Die Major Depression ist eine rezidivierende Erkrankung. Etwa 50% bis 85% der Patienten, die eine depressive Episode erlebten, werden von einer weiteren Episode betroffen sein [176, 236].
Die Prognose der einzelnen depressiven Episode ist günstig und die meisten Patienten erreichen nach dem Abklingen der Episode ihr normales Funktionsniveau wieder. Dennoch ist in 20% bis 30% der Fälle die Remission unvollständig und einige depressive Symptome bleiben chronisch bestehen [19, 40, 167, 176, 261, 309]. Die Major Depression ist mit einer beträchtlichen Morbidität und Mortalität assoziiert. Bei vielen Patienten entwickelt sich aus der ersten Episode heraus eine rezidivierende und/oder chronisch verlaufende Erkrankung mit signifikanten und andauernden Beeinträchtigungen im psychosozialen Funktionsniveau [61, 150, 168, 189, 225, 226, 259]. Studien zu den Auswirkungen einer Depression auf die gesundheitsbezogene Lebensqualität der Patienten zeigten Beeinträchtigungen, die denen von Patienten mit chronischen somatischen Erkrankungen (wie ischämischen Herzerkrankungen oder Diabetes mellitus) glichen oder diese gar noch übertrafen [3, 352, 364]. Bei depressiven Patienten mit komorbiden Erkrankungen bessern sich die depressiven Symptome tendenziell weniger und es besteht ein höheres Rückfallrisiko während der Behandlung [160].
Die schwerwiegendste Komplikation der Major Depression ist der Suizid. Eine Metaanalyse zeigte, dass die Lebenszeitprävalenz für Suizid bei Patienten mit affektiven Störungen von 2,2% (bei einer gemischten Population aus ambulant und stationär behandelten Patienten) bis 8,6% (bei aufgrund von Suizidalität hospitalisierten Patienten) reicht, während sie in der Allgemeinbevölkerung unter 0,5% liegt [60]. Eine depressive Erkrankung erhöht zudem wesentlich das Mortalitätsrisiko durch kardiovaskuläre Erkrankungen [385].
In der Global-Burden-of-Disease-Studie wurde geschätzt, dass unipolare Depressionen die vierthöchsten allgemeinen krankheitsbedingten Belastungen (vorzeitige Mortalität und Behinderung) verursachen. Zählt man die Suizide dazu, steigen die allgemeinen Belastungen durch unipolare Depressionen um nahezu 40% [242]. Im Jahre 2020 wird die Major Depression nach den Herz-Kreislauf-Erkrankungen an zweiter Stelle der Erkrankungen mit den höchsten allgemeinen Belastungen stehen [243].
Neben dem individuellen Leid für die Patienten und deren Familien verursachen depressive Erkrankungen zusätzlich signifikant erhöhte Kosten für die Gesellschaft [65, 110, 141, 224, 339], diese steigen bei inkorrekter Diagnose oder nicht ausreichender Behandlung sogar weiter an [353, 355, 363, 386].
1.6 Indikationen und Ziele der Behandlung der Major Depression
Eine spezifische Pharmakotherapie mit Antidepressiva sollte bei Patienten erwogen werden, welche die diagnostischen Kriterien für eine Major Depression (DSM-IV) oder eine depressive Episode (ICD-10) erfüllen (Tab. 1). Leitlinien unterscheiden sich jedoch in ihren Empfehlungen bezüglich der antidepressiven Behandlung bei leichter depressiver Episode sowie bei hausärztlich behandelten Depressionen (NICE 2004 [249], APA 2000 [14]). Abhängig von individuellen Charakteristika und/oder dem Wunsch des Patienten kann eine antidepressive Pharmakotherapie indiziert sein, andernfalls können psycho- und soziotherapeutische Maßnahmen ausreichen.
Die diagnostischen Kriterien beider Klassifizierungssysteme stellen einen klinischen und historischen Konsens zu den wichtigen Hauptsymptomen bzw. Anzeichen einer depressiven Erkrankung dar (Tab. 1).
Vor Behandlungsbeginn sollte der Hausarzt die Wünsche des Patienten sowie dessen Erfahrung mit vorherigen Behandlungen berücksichtigen. Vor allem, wenn ein Patient psychotische Symptome (z.B. Wahnvorstellungen) oder Suizidalität zeigt oder wenn die depressive Erkrankung im Rahmen einer bipolaren Störung auftritt, ist die Überweisung an einen Psychiater/Nervenarzt oder eine stationäre Behandlung angezeigt. Abbildung 1 zeigt das Stufenmodell der Behandlung. Das frühzeitige Erkennen einer bipolaren Störung ist von besonderer Bedeutung, da sich die Therapieansätze wesentlich von denen einer unipolaren Depression unterscheiden und sich die frühzeitige adäquate Behandlung positiv auf das Langzeitergebnis auswirkt. Unter den therapieresistenten Patienten finden sich überdurchschnittlich viele bipolar Erkrankte, bei denen fälschlicherweise eine unipolare Depression diagnostiziert wurde. Die alleinige Behandlung mit Antidepressiva hat bei diesen Patienten einen destabilisierenden Einfluss auf den Erkrankungsverlauf [133]. Neben einer genauen Befragung der Patienten und deren Familie nach manischen und hypomanischen Episoden können Screening-Instrumente (z.B. Mood Disorders Questionnaire, MDQ [151]; Hypomania Checklist [25, 26]) bei der Identifikation bipolar erkrankter Patienten helfen.
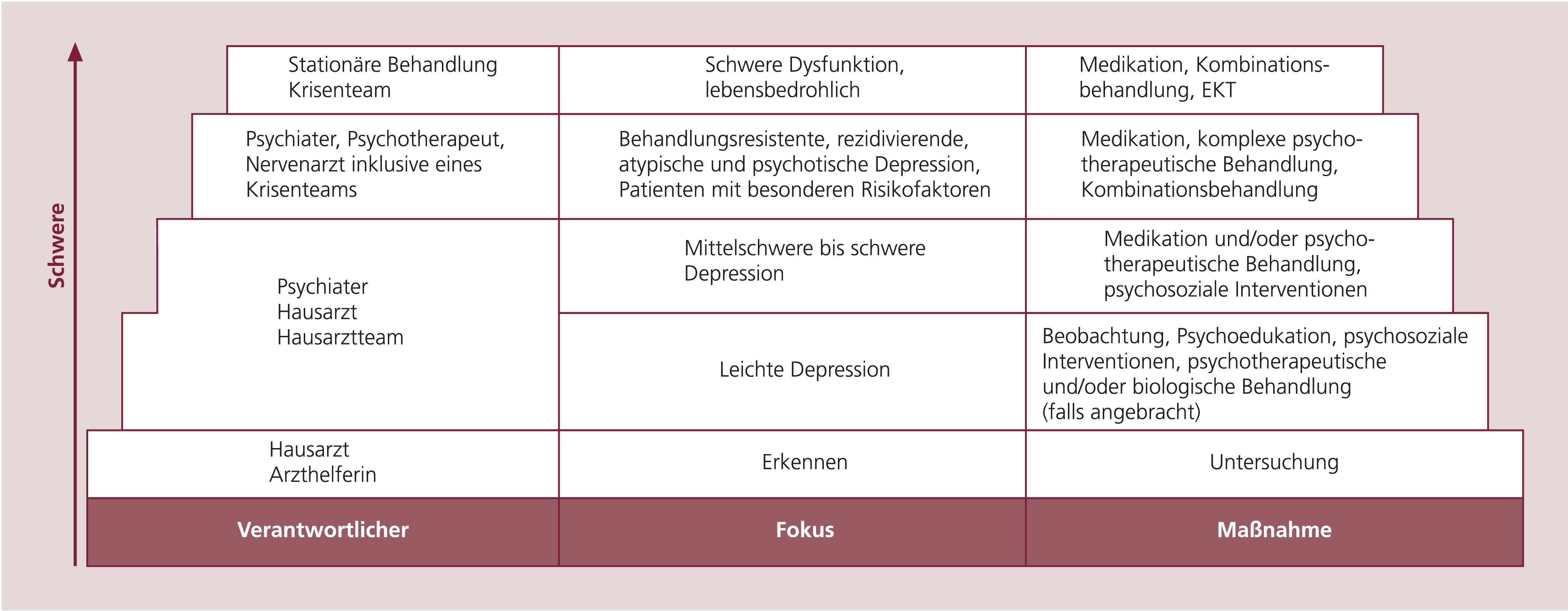
Abb. 1. Stufenmodell der Versorgung (adaptierte Version, Originalidee aus [249]); EKT: Elektrokrampftherapie
Bei der Behandlung depressiver Störungen gibt es akute, mittel- und langfristige Ziele. Kupfer et al. [195, 197] haben ein Modell für den typischen Verlauf einer depressiven Episode entwickelt, welches das Rückfallrisiko und ein entsprechend strukturiertes Behandlungskonzept einschließt. Die drei Phasen der Behandlung entsprechen in diesem Modell den drei Stadien der Erkrankung: 1. Akuttherapie, 2. Erhaltungstherapie und 3. Rezidivprophylaxe/Langzeittherapie (Abb. 2). Die Akutphase der Behandlung erstreckt sich von Beginn der Behandlung bis zur Remission. Remission ist das primäre Therapieziel [121, 197]. Die Erhaltungsphase folgt der Akutphase und dient dem Erhalt und der Festigung der erreichten Remission. In dieser Phase wird die Therapie unverändert weitergeführt, um einem Rückfall vorzubeugen. Wenn die depressiven Symptome während der Erhaltungstherapie wiederkehren, hat sich ein Rückfall ereignet. Von einer Gesundung spricht man, wenn der Patient für etwa sechs Monate asymptomatisch bleibt. Sie kann durch anhaltendes Fehlen depressiver Symptome nach Beendigung der Medikation bestätigt werden, wenn keine Langzeittherapie geplant ist. Gesundung bezieht sich ausschließlich auf die einzelne Erkrankungsepisode und bedeutet nicht, dass der Patient frei von späteren Rezidiven bleibt [37, 229]. Eine Langzeittherapie hat das Ziel, einer neuen depressiven Episode und einem Suizid vorzubeugen.
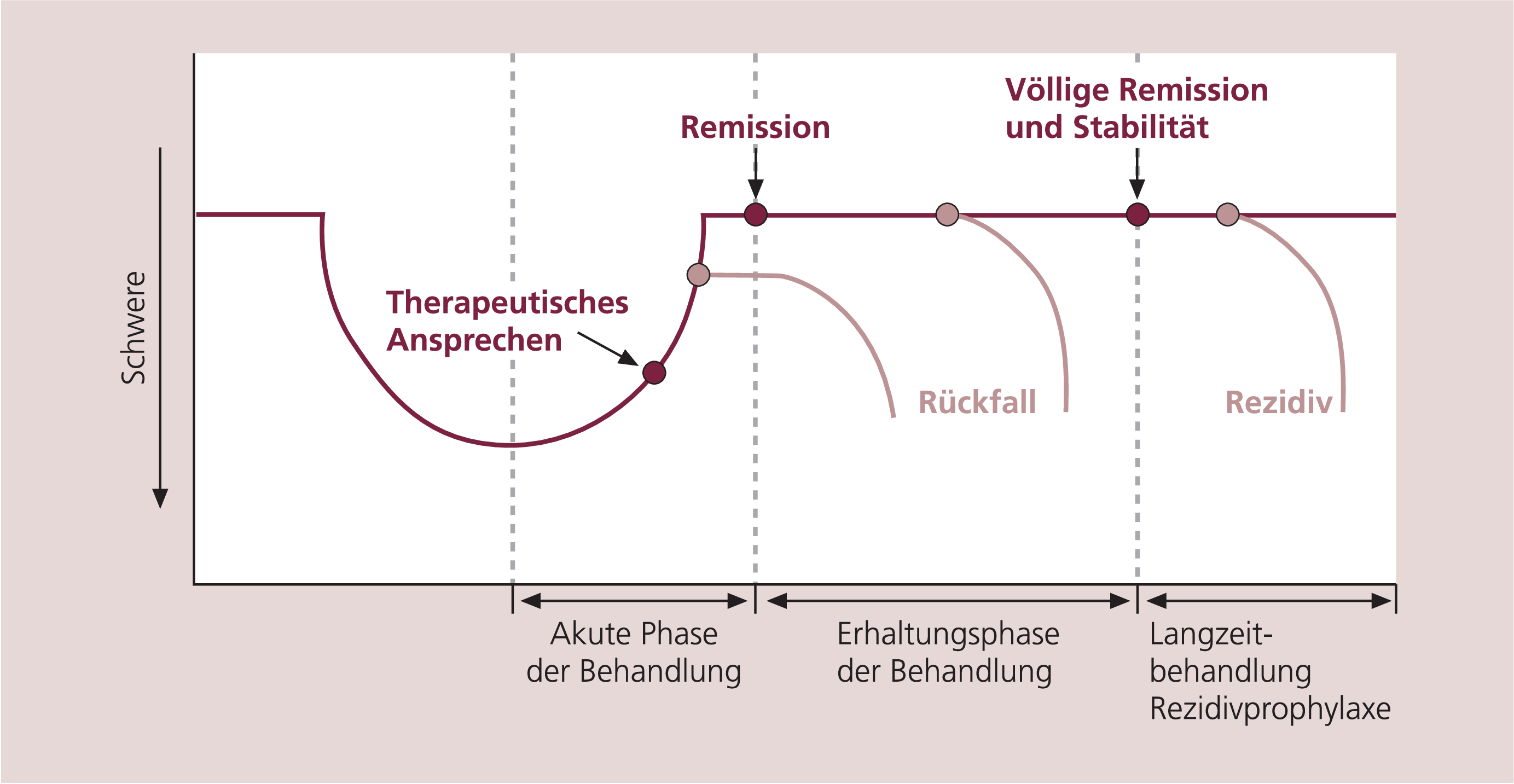
Abb. 2. Phasen der Erkrankung und Behandlung (adaptierte Version, Original von [195])
2 Akutbehandlung der Major Depression
Diese Leitlinien besitzen Gültigkeit, wenn
1. die Diagnose einer Major Depression durch einen Arzt anhand eines der zwei etablierten Klassifizierungssysteme, der International Classification of Disease (ICD-10, Weltgesundheitsorganisation 1992) oder des Diagnostic and Statistical Manual of Mental Disorders (DSM-IV) [12] (Tab. 1), gestellt wurde, wenn
2. andere psychiatrische Erkrankungen (bipolare Störung, schizoaffektive Störung, Alkohol- oder Substanzmissbrauch/-abhängigkeit, Angststörungen, Essstörungen, Persönlichkeitsstörungen) und somatische Erkrankungen (z.B. endokrinologische und neurologische Erkrankungen, Autoimmunkrankheiten, Infektionskrankheiten, Karzinome) ausgeschlossen wurden und
3. andere Faktoren (z.B. Medikamente oder psychosoziale Stressfaktoren), die ein depressives Syndrom hervorrufen oder die Behandlung beeinflussen können, diagnostisch abgeklärt wurden.
Es ist die Aufgabe des Arztes, die Erstbeurteilung der Depression einschließlich einer gründlichen körperlichen Untersuchung durchzuführen.
Im Folgenden wird eine Übersicht über die gebräuchlichsten Behandlungsmethoden für depressive Störungen mit Schwerpunkt auf biologische Behandlungsmethoden gegeben. Bestandteile des psychiatrischen Managements und allgemeine psychotherapeutische Unterstützung sollten erwogen und während der gesamten Behandlung fortgesetzt werden [14]. Diese Bestandteile beinhalten: Festlegen des Behandlungsplans und -rahmens, Aufbau und Erhalt einer therapeutischen Allianz, wiederholte Beobachtung und Neubeurteilung des psychiatrischen Status (einschließlich des Suizidrisikos des Patienten), Überprüfung der Richtigkeit der Diagnose und des Ansprechens auf die Behandlung, Monitoring des Patienten hinsichtlich Nebenwirkungen und allgemeinem körperlichem Zustand sowie Aufklärung des Patienten und dessen Familie über die Wichtigkeit der Adhärenz für den Behandlungserfolg [14]. Falls die Voraussetzungen gegeben sind, werden während der Akuttherapie Visiten im ein- oder zweiwöchigen Abstand empfohlen. Während der Erhaltungstherapie kann die Visitenhäufigkeit variieren, jedoch werden Visiten in ein- bis zweimonatigem Abstand empfohlen.
2.1 Antidepressiva
Eine der wichtigsten Errungenschaften bei der Behandlung der Major Depression war die Entwicklung antidepressiv wirkender Substanzen. Viele verschiedene Antidepressiva sind bisher als Erweiterung des pharmakotherapeutischen Repertoires hinzugekommen. Gegenwärtig sind mindestens 37 verschiedene Antidepressiva weltweit verfügbar (Tab. 2), jedoch variiert die Verfügbarkeit auf dem Markt der einzelnen Länder beträchtlich.
Tab. 2. Antidepressiva: Wirkungsmechanismen und Dosierungen
|
Generischer Namea (in alphabetischer Reihenfolge) |
Traditionelle strukturelle Klassifikationb |
Klassifikation gemäß neuro-chemischem Wirkungsmechanismusb |
Anfangsdosisc [mg/d] |
Standarddosisd [mg/d] |
Plasmaspiegele (therapeutischer Bereich) [ng/ml] |
|
Agomelatin |
MT-Agonist |
25 |
25–50 |
||
|
Amineptin |
100 |
200–300 |
|||
|
Amitriptylinf |
TZA |
25–50 |
100–300 |
80–200‡ |
|
|
Amoxapin |
TetraZA |
50 |
100–400 |
||
|
Bupropiong |
NDRI |
150 |
150–450¶ |
||
|
Citaloprami |
SSRI |
20 |
20–40 (60) |
||
|
Clomipraminh,i |
TZA |
25–50 |
100–250 |
175–450‡ |
|
|
Desipramin |
TZA |
25–50 |
100–300 |
100–300 |
|
|
Dibenzepin |
TZA |
120–180 |
240–720 |
||
|
Dosulepin |
TZA |
75 |
75–150 |
||
|
Doxepini |
TZA |
25–50 |
100–300 |
||
|
Duloxetink |
SNRI |
30–60 |
60–120 |
||
|
Escitaloprami |
SSRI |
10 |
10–20 |
||
|
Fluoxetinh |
SSRI |
20 |
20–60 |
||
|
Fluvoxaminh |
SSRI |
50 |
100–200 |
||
|
Imipramin |
TZA |
25–50 |
100–300 |
175–300‡ |
|
|
Isocarboxazidi |
20 |
20–60 |
|||
|
Lofepramin |
TZA |
70 |
140–210 |
||
|
Maprotilin |
TetraZA |
25–50 |
150–225 |
||
|
Mianserin |
TetraZA |
§ |
30 |
60–120 |
|
|
Milnacipran |
SNRI |
50–100 |
100–200 |
||
|
Mirtazapin |
$ |
15 |
15–45 |
||
|
Moclobemid |
RIMA |
150 |
300–600 |
||
|
Nefazodon |
100 |
300–600 |
|||
|
Nortriptylin |
TZA |
25–50 |
75–200 |
70–170 |
|
|
Paroxetinh,i,j |
SSRI |
20 |
20–40 (60) |
||
|
Phenelzini |
MAOI |
15 |
30–90 |
||
|
Protriptylin |
TZA |
10 |
20–60 |
||
|
Reboxetin |
NARI |
4–8 |
8–12 |
||
|
Sertralinh,i,j |
SSRI |
50 |
50–150 |
||
|
Setiptilin |
TetraZA |
3 |
3–6 |
||
|
Tianeptin |
# |
12,5 |
25–37,5 |
||
|
Tranylcypromini |
MAOI |
10 |
20–60 |
||
|
Trazodon |
50–100 |
200–600 |
|||
|
Trimipraminf,i |
TZA |
25–50 |
100–300 |
||
|
Venlafaxinj |
SNRI |
37,5–75 |
75–375 |
195–400‡ |
|
|
Viloxazin |
100 |
200–500 |
aErhältlichkeit auf dem Markt divergiert beträchtlich von Land zu Land
bAbkürzungen:
MAOI = irreversible Hemmung der Monoaminoxidase
MT-Agonist = Agonist des Melatonin-Rezeptors (MT1 und MT2)
NARI = Noradrenalin-Wiederaufnahmehemmung
NDRI = Noradrenalin- und Dopamin-Wiederaufnahmehemmung
RIMA = reversible Hemmung der Monoaminoxidase A
SNRI = selektive Serotonin- und Noradrenalin-Wiederaufnahmehemmer
SSRI = selektive Serotonin-Wiederaufnahmehemmer
TZA = trizyklische Antidepressiva
TetraZA = tetrazyklische Antidepressiva
§ = Noradrenalin-Wiederaufnahmehemmung plus präsynaptische Alpha2-Blockade
$ = Alpha2-Antagonist
# = Serotonin-(5-HT-)Wiederaufnahmeverstärker
cBei älteren Menschen (>60 Jahre) oder bei Patienten mit komorbiden körperlichen Erkrankungen (besonders kardiovaskuläre Erkrankungen; s. Text) können niedrigere Anfangsdosen nötig sein
dStandarddosierungen sind in Japan im Allgemeinen niedriger
eNur für Antidepressiva mit gut etabliertem therapeutischem Bereich angegeben [265a]
‡Der empfohlene therapeutische Bereich ist die Summe aus Arzneistoff und aktivem Metabolit
Andere Indikationen als Depression (bewährt in einigen Ländern) oder häufige Anwendungsgebiete:
fChronischer Schmerz
gNicotinentwöhnung; ¶nach europäischer Zulassung Tageshöchstdosis 300 mg
hZwangsstörungen (obsessive-compulsive disorder, OCD)
iAngststörungen (Panikstörungen, PTSD [post-traumatic stress disorder], soziale Phobie)
jGeneralisierte Angststörung
kDiabetischer und peripherer neuropathischer Schmerz, Stressinkontinenz
Die „neueren“ Antidepressiva wurden entwickelt, um die Nebenwirkungsrate zu verringern. Die zurzeit verfügbaren Klassen von Antidepressiva unterscheiden sich nur wenig in ihrer antidepressiven Wirksamkeit und zeigen Responseraten von 50% bis 75%. Letztendlich hängt die Wahl des Antidepressivums für den einzelnen Patienten von verschiedenen Faktoren ab (nach AHCPR 1993): von Vorerfahrungen mit Medikamenten (Therapieansprechen), von den Begleitumständen, die durch das ausgewählte Antidepressivum verschlechtert werden können (z.B. metabolisches Syndrom), von zusätzlicher Medikamenteneinnahme, die zu Wechselwirkungen zwischen den Substanzen führen kann (s. Tab. 5, Seite 258), von kurz- und langfristigen Nebenwirkungen des Medikaments (Nebenwirkungen, welche die Lebensqualität des Patienten einschränken, sind entscheidend für Zufriedenheit und Compliance des Patienten), von den Erfahrungen des Arztes mit dem Medikament, der Anamnese zur Regelmäßigkeit der Medikamenteneinnahme des Patienten und zum Ansprechen von Verwandten ersten Grades auf die Medikation, Patientenpräferenzen sowie den Kosten und der Verfügbarkeit eines spezifischen Antidepressivums.
2.1.1 Klassifikation und Wirksamkeit
Leider folgt die Klassifikation der Antidepressiva nicht immer einem systematischen Prinzip. Traditionell wurden Antidepressiva in folgende Hauptklassen unterteilt: trizyklische Antidepressiva (TZA), tetrazyklische Antidepressiva (beides sind nichtselektive Serotonin-Noradrenalin-Wiederaufnahmehemmer), selektive Serotonin-Wiederaufnahmehemmer (SSRI) und selektive Noradrenalin-Wiederaufnahmehemmer (NRI), selektive Serotonin-Noradrenalin-Wiederaufnahmehemmer (SNRI), Monoaminoxidase-Hemmer (MAOI) (einschließlich irreversibler MAO-I und reversibler Hemmer der Monoaminoxidase A [RIMA]) und andere Antidepressiva.[2]
Die Wirksamkeit der „älteren“ Antidepressiva (tri- und tetrazyklische Antidepressiva und irreversible MAO-Hemmer) wurde in zahlreichen Plazebo-kontrollierten Studien nachgewiesen (alle Klassen Level A) [115, 183, 330]. In gleicher Weise zeigen zahlreiche doppelblinde, kontrollierte Studien eine bessere Wirksamkeit von SSRI im Vergleich zu Plazebo (Level A) [3, 46, 183, 211]. Des Weiteren ist die Wirksamkeit von SNRI im Vergleich zu Plazebo in zahlreichen doppelblinden, kontrollierten Studien gezeigt worden (Level A) [107, 153]. Für Mirtazapin ist die Wirksamkeit im Vergleich zu Plazebo in klinischen Studien ebenso gut nachgewiesen worden (Level A) [47], desgleichen für Reboxetin [303a] und kürzlich für Agomelatin, ein melatonerges Antidepressivum [180a*].
Die „älteren“ (irreversiblen) MAO-Hemmer (z.B. Tranylcypromin und Phenelzin) sind nicht Therapie der ersten Wahl. Die Wirksamkeit ist mit der von trizyklischen Antidepressiva vergleichbar, jedoch bergen sie das Risiko einer potenziell tödlichen hypertensiven Krise oder eines Serotonin-Syndroms (s. Seite 249) bei Patienten, die tyraminhaltige Lebensmittel (z.B. gereiften Käse, geräuchertes, gepökeltes oder getrocknetes Fleisch; Sojasoße und Misopaste, gesalzenen Fisch und Rotwein, s. Packungsbeilagen des Herstellers) zu sich nehmen oder bestimmte Medikamente einnehmen (Level B) [14].
2.1.2 Wirksamkeit und Verträglichkeit im Vergleich
Die zahlreichen trizyklischen Antidepressiva sind in ihrer Wirksamkeit vergleichbar, unterscheiden sich jedoch in ihrem Nebenwirkungsprofil (Level A) (Tab. 3) [157]. Auch bei den SSRI ergab eine Metaanalyse keinen signifikanten Unterschied in der Wirksamkeit der einzelnen Substanzen (Level A) [102].
Tab. 3. Nebenwirkungsprofile der Antidepressivaa
|
Generischer Name (in alphabetischer Reihenfolge) |
Anticholinergb |
Übelkeit/ |
Sedierung |
Schlaflosigkeit/Erregung |
Sexuelle Dysfunktion |
Orthostatische Hypotension |
Gewichtszunahme |
Spezifische unerwünschte Nebenwirkungen |
Letalität bei Überdosierung |
|
Agomelatin |
– |
+ |
– |
– |
– |
– |
– |
Gering |
|
|
Amineptin |
– |
+ |
– |
++ |
+ |
+ |
+ |
Gefahr des Missbrauchs |
Gering |
|
Amitriptylin |
+++ |
– |
+++ |
– |
+ |
+++ |
+++ |
EKG-Veränderungenc; kann die Krampfschwelle herabsetzen |
Hoch |
|
Amoxapin |
+++ |
– |
+ |
++ |
+ |
+ |
+ |
Hyperprolaktinämie |
Hoch |
|
Bupropion |
+ |
+ |
– |
+ |
– |
– |
– |
Gering |
|
|
Citalopram |
– |
++ |
– |
++ |
++ |
– |
– |
Gering |
|
|
Clomipramin |
+++ |
+ |
+ |
+ |
++ |
++ |
++ |
EKG-Veränderungenc; kann die Krampfschwelle herabsetzen |
Mittel |
|
Desipramin |
+ |
– |
– |
++ |
+ |
+ |
+ |
Hoch |
|
|
Dibenzepin |
+ |
– |
+ |
– |
+ |
+ |
+ |
Mittel |
|
|
Dosulepin |
++ |
– |
++ |
– |
+ |
+ |
+ |
Hoch |
|
|
Doxepin |
+++ |
– |
+++ |
– |
++ |
+++ |
++ |
Hoch |
|
|
Duloxetin |
– |
++ |
– |
++ |
+ |
– |
– |
Gering |
|
|
Escitalopram |
– |
++ |
– |
++ |
++ |
– |
– |
Gering |
|
|
Fluoxetin |
++ |
+ |
Gering |
||||||
|
Fluvoxamin |
+ |
+++ |
+ |
+ |
Gering |
||||
|
Imipramin |
++ |
– |
+ |
++ |
+ |
++ |
++ |
EKG-Veränderungenc; kann die Krampfschwelle herabsetzen |
Hoch |
|
Isocarboxazid |
+ |
+ |
– |
++ |
+ |
++ |
+ |
Hypertensive Krisee; Gefahr eines Serotonin-Syndromsf |
Hoch |
|
Lofepramin |
+ |
– |
+ |
++ |
+ |
+ |
+ |
EKG-Veränderungenc; kann die Krampfschwelle herabsetzen |
Gering |
|
Maprotilin |
++ |
– |
++ |
– |
+ |
++ |
++ |
Erhöhtes Anfallsrisiko |
Hoch |
|
Mianserin |
+ |
– |
++ |
– |
– |
+ |
+ |
Blutdyskrasie (selten) |
Gering |
|
Milnacipran |
– |
++ |
– |
++ |
++ |
– |
– |
Gering |
|
|
Mirtazapin |
– |
– |
++ |
– |
– |
+ |
++ |
Gering |
|
|
Moclobemid |
+ |
+ |
– |
+ |
– |
– |
– |
Gering |
|
|
Nefazodon |
+ |
+ |
++ |
– |
– |
+ |
+ |
Inhibitorische Wirkungen auf CYP3A4d |
Gering |
|
Nortriptylin |
+ |
– |
+ |
+ |
+ |
+ |
+ |
EKG-Veränderungenc; kann die Krampfschwelle herabsetzen |
Hoch |
|
Paroxetin |
+ |
++ |
– |
++ |
++ |
– |
+ |
Inhibitorische Wirkungen auf CYP2D6d |
Gering |
|
Phenelzin |
+ |
+ |
+ |
++ |
++ |
++ |
+ |
Hypertensive Krisee; Gefahr eines Serotonin-Syndromsf |
Hoch |
|
Protriptylin |
+++ |
– |
+ |
++ |
+ |
++ |
+ |
EKG-Veränderungen; kann die Krampfschwelle herabsetzen |
Hoch |
|
Reboxetin |
– |
+ |
– |
++ |
+ |
++ |
– |
Gering |
|
|
Sertralin |
– |
++ |
– |
++ |
++ |
– |
– |
Gering |
|
|
Setiptilin |
+ |
– |
++ |
– |
+ |
+ |
+ |
Mittel |
|
|
Tianeptin |
+ |
+ |
– |
+ |
– |
– |
– |
EKG-Veränderungenc; kann die Krampfschwelle herabsetzen |
Gering |
|
Tranylcypromin |
– |
+ |
– |
++ |
+ |
++ |
– |
Hypertensive Krisee; Gefahr eines Serotonin-Syndromsf |
Hoch |
|
Trazodon |
– |
+ |
++ |
– |
++ |
+ |
+ |
Priapismus (selten) |
Gering |
|
Trimipramin |
++ |
– |
+++ |
– |
+ |
++ |
++ |
EKG-Veränderungenc; kann die Krampfschwelle herabsetzen |
Hoch |
|
Venlafaxin |
– |
++ |
– |
++ |
++ |
– |
– |
Hypertension |
Gering |
|
Viloxazin |
– |
+ |
– |
++ |
– |
– |
– |
Gering |
Zu Tabelle 3:
Kategorien der Stärke der Nebenwirkungen: +++ (hoch/stark), ++ (mittel), + (gering/schwach), – (sehr gering/keine)
aDie Nebenwirkungsprofile der Antidepressiva sind nicht vollständig und nur für einen ersten Vergleich geeignet. Details zu den verwendeten Medikamenten, wichtige Warnhinweise und Wechselwirkungen sollten in einem Lehrbuch oder in Reviews [z.B. 52, 53, 181], in der Originalliteratur, im Beipackzettel oder in der Roten Liste nachgelesen werden
bDiese beziehen sich auf Symptome, die gewöhnlich durch muskarinerge Rezeptorblockade ausgelöst werden, einschließlich Mundtrockenheit, Schwitzen, verschommenes Sehen, Obstipation und Urinretention
cReizleitungsstörungen
dEs werden nur die inhibitorischen Wirkungen auf die hepatischen CYP450-Enzyme gezeigt, die klinisch relevant sind; für mehr Details s. [62] und [181]
eErhöhtes Risiko in Kombination mit Nahrungsmitteln, die einen erhöhten Tyramingehalt haben, und mit Sympathomimetika
fIn Kombination mit serotonergen Medikamenten
Im Allgemeinen lassen sich keine klinisch signifikanten Unterschiede in der Wirksamkeit zwischen trizyklischen Antidepressiva (TZA) und SSRI nachweisen (Level A) [14, 16, 46, 126, 228]. Eine Metaanalyse mit 102 randomisierten kontrollierten Studien (RCT) zeigte, dass bei hospitalisierten und schwerkranken Patienten die TZA geringfügig wirksamer waren als SSRI (Level A) [14, 16, s. auch 83, 84]). Jedoch ergab eine weitere Metaanalyse mit einer kleineren Anzahl von RCT und unter Verwendung einer anderen Methodik keine statistisch signifikante Überlegenheit der TZA gegenüber den SSRI [126].
Die Verträglichkeit der SSRI ist gewöhnlich besser als die der TZA und die Behandlungsabbruchraten unter einer SSRI-Therapie sind deutlich geringer (Level A) [3, 16, 46, 265, 316; s. auch 357]. SSRI sind sicherer in ihrer Anwendung und haben ein besseres Verträglichkeitsprofil verglichen mit trizyklischen und tetrazyklischen Antidepressiva. Sie weisen weniger anticholinerge Nebenwirkungen und eine geringere kardiovaskuläre Toxizität auf (Level A) [211, 265, 275]. Daher sind SSRI und andere „neuere“ Antidepressiva bei leichten bis mittelschweren Depressionen Medikamente der ersten Wahl, besonders im Rahmen der ambulanten und hausärztlichen Versorgung sowie bei Patienten mit kardiovaskulären Begleiterkrankungen [11, 170, 303, 315].
Hinsichtlich der vergleichenden Wirksamkeit der „neueren“ Antidepressiva untereinander legen Metaanalysen eine etwas bessere Wirksamkeit von Venlafaxin im Vergleich zu SSRI [17, 103, 326, 340] und anderen Antidepressiva [318] nahe.
Zur Behandlung einer schweren Depression können TZA, SSRI und SNRI sowie, falls geeignet, eine EKT empfohlen werden (Level B) (s. Abschnitt 2.3).
Der NRI Reboxetin ist vergleichbar gut wirksam wie der SSRI Fluoxetin, wobei Reboxetin in klinischen Studien eine geringere Studienabbruchrate aufweist (Metaanalyse [73*]). Im Vergleich zum SSRI Citalopram zeigt Reboxetin ebenfalls eine ähnliche Wirksamkeit, führt jedoch zusätzlich weniger häufig zu sexuellen Dysfunktionen (beachte, dass hier die höhere Studienabbruchrate in der Reboxetin-Gruppe eintrat. Möglicherweise lag dies an der fehlenden Aufdosierung zu Behandlungsbeginn, [202*]).
Die Nebenwirkungsrate variiert zwischen den Antidepressivaklassen und in gewissem Ausmaß auch zwischen einzelnen Wirkstoffen (Tab. 3). Beim Vorhandensein von nichtpsychiatrischen Begleiterkrankungen werden einige Wirkstoffe aufgrund ihres Nebenwirkungsprofils bevorzugt, so dass beispielsweise bei Patienten mit koronarer Herzkrankheit Medikamente genutzt werden, die den Blutdruck nicht senken und nicht mit Veränderungen im Erregungsleitungssystem des Herzens einhergehen (z.B. Bupropion, SSRI, Mianserin). Unter den trizyklischen Antidepressiva zeigen die sekundären Amine (z.B. Desipramin, Nortriptylin) weniger Nebenwirkungen verglichen mit den tertiären Aminen (z.B. Amitriptylin, Imipramin).
Die häufigsten Nebenwirkungen von TZA und tetrazyklischen Antidepressiva sind: anticholinerge/antimuskarinerge Nebenwirkungen (z.B. Mundtrockenheit, Obstipation, verschwommenes Sehen, Harnverhalt und Tachykardie), kardiovaskuläre Nebenwirkungen (z.B. a-adrenerge Blockade, orthostatische Hypotension, Bradyarrhythmien, Tachykardie), antihistaminerge Nebenwirkungen (z.B. Sedierung und Gewichtszunahme) und neurologische Nebenwirkungen (z.B. schwacher Myoklonus, epileptische Anfälle bei Überdosierung, Delirium bei älteren Patienten) (Tab. 3). Deshalb sollten TZA und tetrazyklische Antidepressiva nicht bei Patienten mit mittelschweren bis schweren kardiovaskulären Erkrankungen [315], Engwinkelglaukom, Prostatahypertrophie, kognitiven Einschränkungen, epileptischen Anfällen und im Delirium angewandt werden.
Die häufigsten unerwünschten Wirkungen von SSRI sind: gastrointestinale Nebenwirkungen (z.B. Übelkeit, Erbrechen und Diarrhö); Ruhelosigkeit (z.B. Zunahme der Unruhe, Agitation, Schlafstörungen), sexuelle Dysfunktion (z.B. Verminderung der Erektions- und Ejakulationsfähigkeit bei Männern, Libidoverminderung und Anorgasmie bei beiden Geschlechtern) und neurologische Nebenwirkungen (z.B. Zunahme von Migräne- und Spannungskopfschmerzen) (Tab. 3). Kontraindiziert ist die Anwendung von SSRI in Kombination mit MAO-Hemmern sowie kurz vor oder nach einer Behandlung mit MAO-Hemmern aufgrund des Risikos eines auftretenden Serotonin-Syndroms. Typische klinische Symptome eines Serotonin-Syndroms sind Veränderungen im mentalen Status, Ruhelosigkeit, Myoklonus, Hyperreflexie, Zittern, abdominale Schmerzen, Diarrhö und Tremor [116, 329]. Es resultiert häufig aus Wechselwirkungen zwischen irrever-siblen MAO-Hemmern und SSRI, es kann aber auch bei der gleichzeitigen Einnahme serotonerg wirksamer Substanzen auftreten (z.B. Clomipramin, L-Tryptophan, Fenfluramin, Buspiron, Venlafaxin, Milnacipran, Nefadozon und Trazodon).
Die Nebenwirkungen der SNRI (Venlafaxin, Milnacipran and Duloxetin) ähneln denen der SSRI, vor allem der Blutdruck sollte auf einen möglichen Anstieg hin überwacht werden. Mirtazapin kann zu einer Gewichtszunahme führen.
Antidepressiva unterschieden sich in ihrem Einfluss auf die sexuelle Funktionsfähigkeit [82, 114, 232, 235]. TZA, SSRI und Venlafaxin führen mit höherer Wahrscheinlichkeit zu sexuellen Dysfunktionen als Duloxetin und Reboxetin [366*]. Zum Umgang mit sexuellen Dysfunktionen nach Gabe von Antidepressiva siehe Zajecka 2001 [387], Worthington und Peters 2003 [382].
Der gewonnene Nutzen durch eine adäquate Behandlung scheint mit der Schwere der Depression proportional zu steigen [21]. Bei leichten depressiven Episoden ist der Nutzen einer Behandlung mit Antidepressiva unklar. Aufklärung, Unterstützung und die Vermittlung von Bewältigungsstrategien stellen Alternativen zur Behandlung einer leichten depressiven Episode dar (Level B) [16, 249].
2.1.3 Suizidalität
Suizid ist die schwerwiegendste Komplikation bei Patienten mit einer Major Depression. Das Suizidrisiko muss am Anfang und regelmäßig während der Behandlung beurteilt werden. Folgende Faktoren können den Hausarzt auf ein hohes Suizidrisiko hinweisen: affektive Störung, schlechte Impulskontrolle, Alter und Geschlecht (Männer zwischen dem 20. und 30. Lebensjahr und ab dem 50. Lebensjahr [und insbesondere sehr alte Männer] und Frauen zwischen dem 40. und 60. Lebensjahr), in der Anamnese beschriebener früherer Suizidversuch (Faktor mit der höchsten Relevanz), suizidales Verhalten in der Familienanamnese, positive Familienanamnese für eine frühzeitig beginnende affektive Störung (early-onset), Substanzmissbrauch (insbesondere Alkoholmissbrauch), Familienstand (ledig, geschieden oder verwitwet), plötzliche Veränderung des sozioökonomischen Status (Arbeitsplatzverlust, finanzielle Probleme, ungewollte Pensionierung) und fehlende soziale Unterstützung [24, 27, 57, 60, 230, 252, 253]. Wenn der Patient suizidale Gedanken oder eine Suizidabsicht äußert, sind eine engmaschige Überwachung und eine psychiatrische Behandlung notwendig, die Aufnahme in eine psychiatrische Abteilung wird empfohlen (Abb. 1). Eine Einweisung auf eine geschützte Station ohne die Einwilligung des Patienten kann notwendig werden. Eine intensive Behandlung sollte umgehend begonnen werden und eine Pharmakotherapie sowie eine Psychotherapie zur Ansprache psychosozialer Faktoren einschließen. Ein spezifisches, akut „antisuizidal“ wirkendes Medikament gibt es nicht.
Viele Ärzte behandeln suizidale Patienten erfolgreich mit einem Antipsychotikum oder mit Benzodiazepinen zusätzlich zum Behandlungsregime [124]. (Für Informationen zu Behandlungsempfehlungen bei Major Depression mit psychotischen Merkmalen [wahnhafte Depression] s. Abschnitt 2.6.1 [Antipsychotika].) Es wird empfohlen, den Patienten mit einem Risiko für beabsichtigte Überdosierung jeweils nur den Vorrat für eine Woche an potenziell suizidgeeigneten Antidepressiva (z.B. TZA oder irreversible MAO-Hemmer) zu verschreiben. Es sollte ein Antidepressivum ausgewählt werden, das bei Überdosierung relativ sicher ist (Tab. 3) [2].
Epidemiologische Studien zeigten in den letzten Jahrzehnten eine Verringerung der Suizidhäufigkeit und eine Erhöhung der Verschreibungshäufigkeit von Antidepressiva. Demgegenüber steht die Debatte, ob bestimmte Antidepressiva oder Antidepressiva im Allgemeinen das Risiko für suizidales Verhalten potenziell erhöhen. In diesem Zusammenhang könnten klinische Faktoren wie komorbide Persönlichkeitsstörungen und die inadäquate Behandlung einer bipolaren Depression von Bedeutung sein. Einige Daten lassen vermuten, dass die Behandlung mit SSRI, und potenziell auch mit anderen Antidepressivaklassen, die Suizidalität (vor allem Suizidversuche) bei einigen Patienten erhöhen könnte [231*]. Dieses Risiko scheint in der initialen Behandlungsphase am stärksten ausgeprägt zu sein [164]. Simon und Kollegen zeigten, dass das Suizidrisiko im Monat vor Behandlungbeginn mit Antidepressiva am höchsten ist, in der ersten Woche der Behandlung sehr viel niedriger ist, danach weiter sinkt und schließlich auf ein nochmals niedrigeres, stabiles Risiko abnimmt (Ergebnisse aus Krankenakten von 65000 Patienten mit Depression [317*]). Khan et al. verglichen die Inzidenz von Suizid und Suizidversuchen bei Behandlung mit verschiedenen „neueren“ Antidepressiva im Vergleich zu Plazebo und fanden keine statistisch signifikanten Unterschiede [183]. Die U.S. Food and Drug Administration [354] hat eine offizielle Warnung ausgesprochen, und zwar für den Fachbereich der Kinder- und Jugendpsychiatrie, da für Kinder und Jugendliche die Wirksamkeit der meisten Antidepressiva noch nicht gezeigt werden konnte, und für junge Erwachsene bis 24 Jahre.
Bei der ärztlichen Entscheidung sollte das potenzielle Risiko sorgfältig mit dem Nutzen einer Behandlung mit Antidepressiva abgewogen werden. Die Beachtung der individuellen Krankeitsgeschichte, inklusive der Risikofaktoren für suizidales Verhalten, und ein enges Monitoring des Patienten (z.B. wöchentliche Visiten in den ersten Wochen der Behandlung) werden zu Beginn einer Behandlung mit Antidepressiva empfohlen.
2.1.4 Beurteilung der Wirksamkeit der initialen Behandlung
Um die Wirksamkeit der initialen Behandlung beurteilen zu können, sollte der Hausarzt das Antidepressivum über einen definierten Zeitraum verabreichen und dann das Ansprechen des Patienten auf das Antidepressivum angemessen beurteilen. Dabei sollten (neben der Erhebung des gesundheitlichen Allgemeinzustands [CGI]) folgende spezifische Beurteilungsskalen genutzt werden: Selbstbeurteilungsskalen für Patienten (z.B. Beck Depression Inventory, [BDI; 48], das 9-Fragen-Modul des Patient Health Questionnaire, [PHQ-9; 323]) und/oder spezifische Beurteilungsskalen für Untersucher (z.B. Hamilton Rating Scale for Depression [HRSD; 146] oder Montgomery-Åsberg Depression Rating Scale [MADRS; 233]) [298].
Um den Begriff Response (Ansprechen auf die Behandlung) klar zu definieren, werden folgende Kriterien vorgeschlagen:
- Keine Response: ≤25% Abnahme der Schwere der Symptomatik im Vergleich zum Zustand vor der Behandlung
- Teil-(Partial-)Response: 26% bis 49% Abnahme der Schwere im Vergleich zur Anfangssymptomatik
- Response: ≥50% Abnahme der Schwere im Vergleich zur Anfangssymptomatik
- Response mit Restsymptomen (Residualsymptomen): Ansprechen mit teilweiser Remission
- Remission: Fehlen von Symptomen, definiert durch einen absoluten Skalenwert (abhängig von der jeweiligen Skala, z.B. HRSD-Score von ≤7) (auch als vollständige Response oder Remission bezeichnet).
Nach einer zwei- bis vierwöchigen antidepressiven Behandlung sollte das Ansprechen des Patienten erfasst werden. Bei unzureichendem Ansprechen auf die antidepressive Behandlung sollten Strategien zur Behandlungsoptimierung durchgeführt werden. Eine Behandlungsdauer von mindestens acht bis zehn Wochen ist notwendig, um die volle Abnahme der Symptomschwere zu erfassen [298]. Wenn die initiale Behandlungsstrategie aufgrund von nicht zu tolerierenden Nebenwirkungen abgebrochen werden muss, ist ein Wechsel zu einer anderen Behandlungsmethode gefordert (für zusätzliche Behandlungsmethoden, s.u.).
2.1.5 Wann liegt Therapieversagen vor?
Wann die Behandlung mit einem Antidepressivum abgebrochen wird, sollte vom Arzt in enger Zusammenarbeit mit dem Patienten entschieden werden, da der Zeitpunkt für den Wechsel im Behandlungsplan äußerst wichtig ist. Wird die Behandlungsstrategie zu früh geändert, könnte der Patient den Schluss ziehen, dass die Medikation unwirksam war, und damit entmutigt werden. Im Gegensatz dazu kann ein Festhalten an einer bestimmten Medikation über einen zu langen Zeitraum ohne Response zu unnötiger Verlängerung des Leidens und der Dauer der Episode führen. Zeigt ein Patient nach zwei- bis vierwöchiger antidepressiver Behandlung im oberen Bereich der Standarddosis (Tab. 2) keine Response, sinkt die Wahrscheinlichkeit eines späteren Ansprechens auf das jeweilige Medikament. Zeigt der Patient nach vier bis sechs Wochen eine Teilresponse, steigt die Wahrscheinlichkeit für ein Ansprechen nach acht bis zwölf Wochen der Therapie an [327, 332]. Es gibt einige Hinweise darauf, dass ältere Menschen erst nach einem Behandlungszeitraum von bis zu zwölf Wochen ansprechen, insbesondere auf „ältere“ Antidepressiva [172]. Neuere Studien mit SSRI legen jedoch nahe, dass ältere Patienten nicht grundsätzlich eine spätere Response zeigen müssen [302*].
2.1.6 Diagnostische Beurteilung und Optimierung der antidepressiven Behandlung
Bevor ein Wechsel in der Behandlungsstrategie in Erwägung gezogen wird, sollte im ersten Schritt die Diagnose überprüft werden. Die Erfassung von pharmakokinetischen Faktoren, die den Plasmaspiegel der Antidepressiva beeinflussen könnten, sollte ebenfalls in Erwägung gezogen werden. Falls verfügbar, können Plasmaspiegel von trizyklischen Antidepressiva zur Überprüfung der adäquaten Dosis und zur Dosisanpassung hilfreich sein (s. Abschnitt 2.1.7 und Tab. 2). Eine Neubewertung der Befunde aus körperlicher Untersuchung und Laborparametern ist ratsam, um ein Übersehen gleichzeitig bestehender Allgemeinerkrankungen, ungenügend kontrollierter Schmerzsymptome, nichtpsychiatrischer Medikamente und verborgenem Substanzmissbrauch, die alle der depressiven Episode zugrunde liegen oder mit ihr in Verbindung gebracht werden können, zu vermeiden. Anhaltende psychosoziale Stressoren sollten als möglicher Grund für eine Nonresponse in Betracht gezogen werden. Eine Neubewertung der Angemessenheit der verwendeten Medikation ist ebenfalls ratsam. Eine Optimierung der Behandlung kann oft durch eine Dosiserhöhung des Antidepressivums erreicht werden (Abb. 3). Dies trifft insbesondere bei Patienten zu, die mit TZA behandelt werden. Jedoch gibt es nur wenige Hinweise darauf, dass diese Strategie bei Patienten, die eine Behandlung mit SSRI erhalten, wirksam ist [30]. Licht und Qvitzau fanden sogar ein geringeres Ansprechen bei den Patienten, die eine substanzielle Dosiserhöhung von Sertralin erhielten, im Vergleich zu denen, die mit einer gleichbleibenden mittleren Dosis über fünf weitere Wochen behandelt wurden [207], (s. Review [1*]).
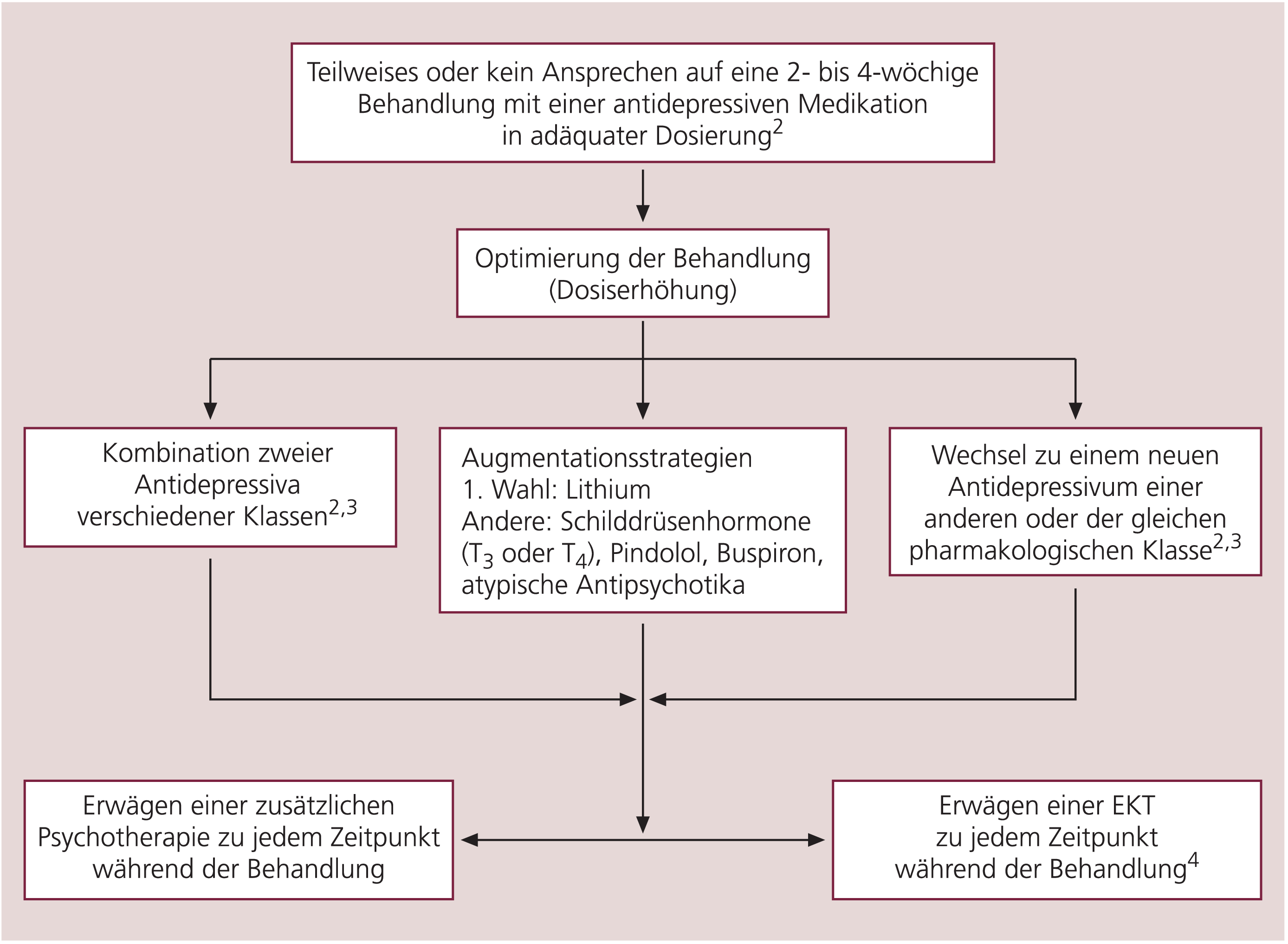
Abb. 3. Flussdiagramm – Therapeutische Möglichkeiten bei teilweisem oder keinem Ansprechen1 auf die anfängliche Behandlung mit einem Antidepressivum bei Major Depression
1Teilweises Ansprechen (Partial-Response): 26%–49% Abnahme der Schwere der depressiven Grundsymptomatik; kein Ansprechen: ≤25% Abnahme der Schwere der depressiven Grund- symptomatik.
2S. Tabelle 2
3Vorsicht bei der Kombination mit irreversiblen MAO-Hemmern (s. Kapitel 2.1.8.2)
4Für Indikationen s. Kapitel 2.3
2.1.7 Therapeutisches Drug-Monitoring
Therapeutisches Drug-Monitoring (TDM) dient der Ermittlung der Plasmakonzentration eines Medikaments, das heißt, es wird geprüft, ob die Konzentration über, unter oder innerhalb des optimalen therapeutischen Fensters liegt. Weiterhin kann mittels TDM die Absorption des Medikaments bestimmt und die Compliance der Medikamenteneinnahme überprüft werden. Im Gegensatz zur Situation bei TZA gibt es bei den SSRI weder eine klare Beziehung zwischen klinischer Wirksamkeit und Plasmakonzentration noch eine Schwelle, die eine toxische Konzentration definiert. Deshalb kann eine routinemäßige Überwachung der Plasmaspiegel bei SSRI nicht empfohlen werden [1*]. Darüber hinaus variieren die Plasmakonzentrationen der Antidepressiva erheblich bei Patienten, die mit ähnlichen Dosen behandelt werden [149, 181].
2.1.8 Behandlungsoptionen bei Teil- und Nonresponse
Unabhängig von der anfänglichen Wahl des Antidepressivums zeigt sich bei mindestens 30% der Depressionen eine ungenügende Response auf die Behandlung [246, 335, 348]. Es werden verschiedene Behandlungsstrategien für Depressionen, die keine oder nur eine Teilresponse zeigen, vorgeschlagen [15, 215, 251, 270, 313]. Die wichtigsten Strategien, welche nach erneuter Überprüfung der richtigen Diagnose, adäquater Medikamentendosis und gesicherter Compliance des Patienten angewandt werden, sind:
1. Wechsel zu einem anderen Antidepressivum aus einer anderen pharmakologischen Klasse (z.B. von einem SSRI zu einem dual wirkendem AD),
2. Wechsel zu einem anderen Antidepressivum innerhalb der gleichen Klasse (z.B. von einem SSRI zu einem anderen SSRI),
3. Kombination zweier Antidepressiva verschiedender Klassen (z.B. eine Kombination eines TZA mit einem SSRI),
4. Augmentation eines Antidepressivums mit einem anderen Wirkstoff (z.B. Lithium oder Schilddrüsenhormon), um die antidepressive Wirkung zu erhöhen, und
5. Kombination eines Antidepressivums mit einer psychotherapeutischen Behandlung (s. 2.4).
Diese Strategien wurden mit verschiedenen Wirkstoffen und Wirkstoffkombinationen untersucht, jedoch sind die meisten dieser Studien methodisch nicht hochwertig und umfassen nur eine geringe Fallzahl.
Gegenwärtig gibt es keine einheitliche Meinung, welche Strategie bei nichtrespondierenden Patienten bevorzugt werden sollte, da aktuell noch keine randomisierte, doppelblinde klinische Studie vorliegt, welche die Fragestellung ausreichend sicher beantwortet [80, 201]. Einige Autoren argumentieren zugunsten der Augmentationsstrategien, beispielsweise mit Lithium. Zur Augmentation mit Lithium liegen bereits Plazebo-kontrollierte klinische Studien vor.
2.1.8.1 Strategie 1:
Wechsel zu einem Antidepressivum aus einer anderen Klasse
Der Vorteil dieser Strategie liegt darin, dass die Polypharmazie minimiert wird. Dies hilft, toxische Wirkungen zu verhindern und unerwünschten Wechselwirkungen zwischen Medikamenten vorzubeugen. Die Strategie des Medikamentenwechsels zwischen zwei Klassen kann zu weniger oder zu besser tolerierten Nebenwirkungen führen und darüber hinaus die regelmäßige Medikamenteneinnahme des Patienten positiv beeinflussen [111, 280, 342].
Der Wechsel von einem SSRI beispielsweise zu den neuartigen dual wirkenden Antidepressiva, einem selektiven Noradrenalin-Wiederaufnahmehemmer oder noradrenergen/dopaminergen Wirkstoffen, trizyklischen Antidepressiva oder Mianserin scheint berechtigt zu sein [293*, systematischer Review]. Einer der möglichen Nachteile ist der Verlust der partiellen Wirksamkeit beim Medikamentenwechsel sowie die relativ lange Zeitspanne bis zum Eintritt der antidepressiven Wirksamkeit der neuen Substanz (späterer Wirkungseintritt im Vergleich zu Dosiserhöhung oder Kombination).
Bei längerer Einnahme der meisten Antidepressiva wird ein Ausschleichen der Medikation über ein bis zwei Wochen empfohlen, da ein abruptes Absetzen zu Entzugserscheinungen führen kann. Beim Wechsel von oder zu einem irreversiblen MAO-Hemmer ist Vorsicht geboten, eine zweiwöchige Auswaschperiode zwischen den Medikamenten (beim Wechsel von Fluoxetin sogar eine fünfwöchige Auswaschperiode) sollte eingehalten werden (Level B).
2.1.8.2 Strategie 2:
Wechsel zu einem Antidepressivum aus der gleichen Klasse
Patienten, die nicht auf einen SSRI ansprechen, haben eine 40- bis 70%ige Chance, auf einen anderen SSRI anzusprechen (Level C) [336]. Dies wurde in einer Reihe von offenen Studien herausgefunden. Eine andere Studie zeigte beim Wechsel zu einem neuen Antidepressivum aus der gleichen Klasse Responseraten von 50% bis 60% [158].
2.1.8.3 Strategie 3:
Kombination zweier Antidepressiva unterschiedlicher Klassen
Gründe, die für eine Kombinationsbehandlung sprechen, sind die Aufrechterhaltung der Teilresponse aus der Monotherapie und das Vermeiden der Gefahr einer Verschlechterung depressiver Symptome durch Absetzen der teilweise wirksamen Medikation. Nachteile dieser Strategie sind das erhöhte Risiko von Wechselwirkungen zwischen Medikamenten, eine mögliche Potenzierung von Nebenwirkungen und die höheren Medikamentenkosten. Obwohl diese Strategie oft in der klinischen Praxis angewandt wird, gibt es nur wenig kontrollierte Daten zugunsten des Nutzens dieser Strategie (Level C, trifft auf alle Kombinationen zu; [87, 207]). Die Kombination aus irreversiblem MAO-Hemmer und SSRI oder einem anderen Antidepressivum, welches das serotonerge System beeinflusst (z.B. Clomipramin, Venlafaxin), muss aufgrund potenziell tödlicher Wechselwirkungen vermieden werden (Serotonin-Syndrom). Aus demselben Grund darf ein SSRI nicht mit L-Tryptophan kombiniert werden (s. dazu der systematische Review [98]).
In der STAR*D-Studie zeigte bei Patienten, die auf den SSRI Citalopram allein nicht ausreichend ansprachen, die Kombination von Citalopram mit dem Antidepressivum der zweiten Generation Bupropion oder mit dem Anxiolytikum Buspiron Remissionsraten von etwa 30% in jeder Gruppe [349*] (für mehr Informationen über das Studiendesign dieser multizentrisch angelegten, prospektiven und sequenziell randomisierten klinischen Studie bei ambulant betreuten depressiven Patienten s. [299]).
2.1.8.4 Strategie 4: Augmentation eines Antidepressivums
Unter Augmentationstherapie versteht man das Hinzufügen eines zweiten Wirkstoffs, der nicht in die Gruppe der Antidepressiva gehört, mit dem Ziel, bei Teil- oder Nonresponse die Behandlung zu optimieren. Augmentationstherapien bieten den Vorteil, dass die Übergangszeit zwischen dem Wirkungseintritt des einen zum anderen Antidepressivum entfällt und die Möglichkeit besteht, auf der partiellen Response des ersten Antidepressivums aufzubauen. Folglich können Augmentationsstrategien einen schnellen Wirkungeintrittt zeigen.
Für die Anwendung bei behandlungsresistenten Depressionen wurden zahlreiche Augmentationsstrategien beschrieben. Unter diesen ist die Lithium-Augmentation als wichtigste und am besten dokumentierte Strategie zu nennen (über 27 offene und 10 Plazebo-kontrollierte Studien zur Akutbehandlung der uni- und bipolaren Depression; Level A, Review [43*, 113]). Folglich wird die Gabe von Lithium zusätzlich zur bestehenden Antidepressivabehandlung als Augmentationsstrategie der ersten Wahl empfohlen [35]. Es wurde nachgewiesen, dass Lithium die therapeutischen Wirkungen einer großen Bandbreite von Antidepressiva, einschließlich TZA [166, 173] und SSRI [44, 173, 389], verstärkt. Eine Metaanalyse, die zehn prospektive Studien einschloss, zeigte, dass die Augmentation mit Lithium der Augmentation mit Plazebo bei unipolaren Depressionen überlegen ist, wobei Ansprechraten von durchschnittlich 41,2% in der Lithium-Gruppe und 14,4% in der Plazebo-Gruppe erreicht wurden [81]. Die Lithium-Augmentation sollte für zwei bis vier Wochen verabreicht werden, um das Ansprechen des Patienten beurteilen zu können. Bei den empfohlenen Lithiumdosierungen (etwa 20 bis 30 mmol/d) erreichen die Patienten üblicherweise einen Serum-Lithium-Spiegel von 0,6 bis 0,8 mmol/l [67]. Im Falle des Ansprechens auf die Behandlung sollte die Lithium-Augmentation für mindestens zwölf Monate fortgesetzt werden [37, 66].
Studien zur Wirkung von Schilddrüsenhormonen bei behandlungsresistenten Depressionen wurden überwiegend mit Triiodthyronin (Liothyronin, T3) durchgeführt. Zahlreiche Fallberichte und mindestens 13 prospektive Studien (neun offene und vier doppelblinde, kontrollierte Studien) beurteilen die Wirksamkeit einer T3-Augmentation, wobei in den meisten Studien 25 bis 37,5 µg/d verwendet wurden, um die Responseraten auf trizyklische Antidepressiva bei Nonresponse zu erhöhen (Level B) [10, 38, 166]. Jedoch zeigten nicht alle doppelblinden, kontrollierten Studien signifikante Ergebnisse zugunsten von T3. Eine später veröffentlichte Metaanalyse fand keine einheitlichen Ergebnisse hinsichtlich einer T3-Augmentation [28]. Eine kleine Anzahl offener Studien ergab Responseraten von rund 50% bei behandlungsresistenten depressiven Patienten, bei denen höhere, supraphysiologische Dosen von Levothyroxin (T4) angewandt wurden (Level D) [34, 41]. Schilddrüsenhormone sollten aufgrund ihrer potenziell unerwünschten Nebenwirkungen mit besonderer Vorsicht verabreicht werden.
Eine weitere neuere Strategie ist die Kombination von Antidepressiva mit atypischen Antipsychotika. Hauptsächlich offene Studien und Fallberichte zeigen positive Ergebnisse für eine Kombination oder eine Augmentation mit atypischen Antipsychotika [33, 257, 383]. Jedoch gibt es aktuell nur eine doppelblinde kontrollierte Studie über acht Wochen, die einen signifikanten Vorteil einer Kombination von Olanzapin und Fluoxetin gegenüber Olanzapin oder Fluoxetin allein zeigt [312] (für weitere doppelblinde RCTs [78*, 314*]).
2.2 Pflanzliche Wirkstoffe
Für Patienten, die keine traditionellen Antidepressiva einnehmen möchten, stellen pflanzliche Wirkstoffe eine mögliche Alternative dar. Es gibt Evidenz aus einer Anzahl kontrollierter Studien dafür, dass Auszüge der Pflanze Hypericum perforatum (im Volksmund Johanniskraut genannt) im Rahmen einer Kurzzeitbehandlung von leichten bis mittelschweren depressiven Störungen wirksamer sind als Plazebo (Level A) [208, 209*]. Verglichen mit trizyklischen Antidepressiva und SSRI scheint es keinen signifikanten Unterschied beim Ansprechen auf die Behandlung zu geben [209]. In einer kürzlich veröffentlichten Plazebo-kontrollierten, multizentrischen Studie zeigten sich jedoch keine Vorteile von Johanniskraut im Vergleich zur Plazebo-Behandlung bei Patienten mit mittelschwerer bis schwerer Depression [311]. Aufgrund der vorhandenen Daten kann Johanniskraut nicht für die Behandlung von schweren Depressionen empfohlen werden [365].
Die Standarddosierung von Hypericum perforatum (Johanniskraut) liegt bei 600 bis 900 mg/d. Es gibt bis jetzt wenige Informationen zur mittel- bis langfristigen Wirksamkeit und zu den Nebenwirkungen des Pflanzenextrakts [3, 208]. Unerwünschte Nebenwirkungen treten bei Johanniskraut im Vergleich mit trizyklischen Antidepressiva seltener auf [184]. Bei gleichzeitiger Gabe von Johanniskraut und einer Anzahl rezeptpflichtiger Arzneimittel können Wechselwirkungen auftreten (z.B. Senkung der TZA-Spiegel im Blut sowie der Blutspiegel anti-retroviraler Medikamente, die zur Behandlung von HIV-Infektionen verwendet werden [161]). Zusätzlich gibt es Bedenken hinsichtlich der Reinheit sowie der variierenden Potenz der pflanzlichen Arzneimittel.
2.3 Elektrokrampftherapie
Elektrokrampftherapie (EKT) als Therapie der ersten Wahl ist indiziert bei: schwerer Major Depression mit psychotischen Symptomen oder mit psychomotorischer Verlangsamung, „echter“ behandlungsresistenter Major Depression (s. Abschnitt 6.3), Verweigerung der Nahrungsaufnahme oder anderen besonderen Situationen, die eine rasche Besserung der Depression verlangen (z.B. bei schwerer Suizidalität oder in der Schwangerschaft) [14]. In diesen Fällen sollte eine Überweisung an einen Psychiater/Nervenarzt sowie gegebenenfalls eine stationäre Behandlung erfolgen. Eine randomisierte, kontrollierte Studie ergab für die EKT zur Behandlung der behandlungsresistenten Depression eine signifikant stärkere Reduktion der Symptomschwere verglichen mit dem SSRI Paroxetin [119]. Eine Metaanalyse konnte die bessere Wirksamkeit der EKT im Vergleich zu einer Antidepressivatherapie mit TZA und MAO-Hemmern nachweisen [258]. Im Allgemeinen wird eine Erhaltungstherapie benötigt, entweder in Form einer Psychopharmakotherapie oder mit EKT.
2.4 Psychotherapie
Obwohl die Psychotherapie nicht im Fokus dieser Leitlinien steht, spielt sie eine wichtige Rolle in der Behandlung von depressiven Patienten in der hausärztlichen Versorgung. Sie sollte als eine initiale Behandlungsform bei Patienten mit leichter Depression erwogen werden. Darüber hinaus wird eine Psychotherapie als Kombinationstherapie mit Antidepressiva für Patienten mit mittelschwerer bis schwerer Depression, Patienten mit nur teilweiser Response auf eine antidepressive Medikation oder Patienten mit Schwierigkeiten mit der regelmäßigen Einnahme von Antidepressiva empfohlen [296].
Für die kurzen strukturierten Psychotherapien konnte gezeigt werden, dass sie in der Akutphase der Behandlung einer Major Depression wirksam sind [123] und einem Rückfall in der Erhaltungsphase der Therapie vorbeugen können [163]. Zu den am besten untersuchten Psychotherapien, die bei einer Depression wirksam sind, gehören kognitive Verhaltenstherapie (KVT, cognitive behavioural therapy, CBT) [49, 56, 92, 97, 125, 136, 155, 266, 295], die Verhaltenstherapie (VT, behavioural therapy, BT) [2, 50, 162, 205, 248, 277], die interpersonelle Therapie (interpersonal therapy, IPT) [104, 188, 217, 308] und das kognitive Verhaltensanalysesystem (cognitive behavioural analysis system of psychotherapy, CBAS) [221, 222]. Einige dieser Psychotherapieformen sind ebenso bei älteren depressiven Patienten wirksam ([147], systematischer Review [156]*). Es gibt weniger empirische Belege für die Wirksamkeit anderer Arten von Psychotherapie (z.B. der psychodynamischen Psychotherapie), was jedoch nicht bedeutet, dass diese Behandlungen nicht potenziell wirksam sind.
Die Kombination von Antidepressiva mit einer Psychotherapie ist wirksamer als die alleinige Verordnung einer Pharmakotherapie [69, 90, 165]; (s. auch [178] für die Wirksamkeit bei chronischer Depression). Jedoch konnte in einer klinischen Studie kein Vorteil einer Kombination aus Antidepressiva und Psychotherapie gegenüber Psychotherapie allein nachgewiesen werden [91].
In einer randomisierten kontrollierten Studie wurde gezeigt, dass ein Problemlösetraining (problem solving treatment, PST) eine wirksame Behandlungsmöglichkeit für depressive Störungen in der hausärztlichen Versorgung ist [244]. Um depressive Symptome bei älteren Menschen zu verringern, stellt PST ebenso eine wirksame Behandlungsform dar [7]. PST kann auch von fachfremden Therapeuten (Nichtspezialisten) nach einem entsprechenden Training durchgeführt werden und ist deshalb eine kostengünstige Alternative zu formalen Psychotherapien, die in der hausärztlichen Versorgung vieler Länder am Anfang nur selten oder überhaupt nicht verfügbar sind.
Bei der Auswertung von Studiendaten, die psychotherapeutische und pharmakologische Behandlungen miteinander vergleichen, sollte eine potenzielle Verzerrung der Ergebnisse aufgrund der Erwartungshaltung der Patienten, ineffizienter Studienverblindung und unzureichender Fallzahl der Studie berücksichtigt werden.
2.5 Lichttherapie (Phototherapie)
Die saisonale depressive Störung (seasonal affective disorder, SAD) stellt einen speziellen Subtyp der rezidivierenden Major Depression dar, die in einem saisonalen Muster auftritt [12, 290]. Es wird geschätzt, dass etwa 5% bis 10% der Allgemeinbevölkerung, insbesondere Frauen, betroffen sind [169, 288]. Die „Winter”-Depression ist die verbreitetste Art der SAD, bei der die Patienten Symptome speziell im Herbst und Winter zeigen und eine vollständige Remission im Frühling und Sommer erleben.
Lichttherapie (Phototherapie) ist die Behandlung der ersten Wahl bei SAD, wenn die Anwendung möglich und die Compliance des Patienten gesichert ist (Level A). SSRI scheinen eine ähnlich gute Wirksamkeit wie die Lichttherapie zu haben, jedoch benötigen sie mehr Zeit bis zur Symptombesserung und führen zu mehr Nebenwirkungen [199, 204, 294, 343]. Für weitere Details s. Reviews [137]* und [268]*.
Das bevorzugte Gerät für die Anwendung der Lichttherapie ist eine Lichtquelle, die weißes, fluoreszierendes Licht abgibt (bei dem der UV-Anteil herausgefiltert wird) und welche Lichtintensitäten größer als 2500 Lux erzeugt. Die anfängliche Dosis von 10000 Lux wird für 30 bis 40 Minuten pro Tag jeden Morgen über zwei bis vier Wochen verabreicht. Alternativ können Lichtquellen mit einer Intensität von 2500 Lux verwendet werden, bei denen die Patienten zwei Stunden Lichttherapie pro Tag erhalten [200]. Die richtige Platzierung vor der Lichtquelle (ausreichend nah, d.h. nicht weiter als 50 bis 80 cm entfernt, und mit offenen Augen) ist während der Therapie von Bedeutung. Patienten zeigen in der Regel innerhalb einer Woche eine Besserung, jedoch kann es bis zu vier Wochen dauern, bis eine vollständige Response erreicht wird. Falls eine künstliche Lichtquelle nicht zur Verfügung steht, kann bei Patienten mit SAD eine Behandlung mit natürlichem Licht in Form eines täglichen einstündigen Morgenspaziergangs im Freien für zwei oder mehr Wochen verordnet werden [206, 373].
Es gibt keine absoluten Kontraindikationen für eine Lichttherapie und keine Evidenz dafür, dass sie mit Augen- oder Retinaschäden assoziiert ist. Jedoch sollten Patienten mit Risikofaktoren im Bereich der Augen vor der Behandlung einen Ophthalmologen aufsuchen. Die häufigsten Nebenwirkungen der Lichttherapie, die von Patienten in klinischen Studien berichtet wurden, beinhalten Augenbelastungen, Sehstörungen, Kopfschmerzen, Erregung, Übelkeit, Sedierung und sehr selten hypomanische oder manische Symptome. Die Nebenwirkungen sind meist vorübergehend und nur leicht ausgeprägt. Sie nehmen mit der Zeit ab oder können über eine Lichtdosisreduktion verringert werden [200].
Eine Metaanalyse mit Studien zur Wirksamkeit der Lichttherapie bei nicht saisonalen depressiven Störungen fand insgesamt keinen statistisch signifikanten Unterschied der Response im Vergleich zur Kontrollgruppe. Jedoch zeigte sich in Studien von hoher methodischer Qualität und in denen, welche die morgendliche Anwendung der Lichtquelle untersuchten, ein Vorteil zugunsten der Therapie mit einer hellen Lichtquelle (Cochrane-Review [350]).
2.6 Zusätzliche Therapie
Für die Behandlung der Major Depression wurden pharmakologische wie auch nichtpharmakologische Zusatzbehandlungen untersucht [214]. Im Folgenden werden Zusatztherapien mit Antipsychotika, Tranquilizern/Anxiolytika, Schlafentzug und körperlichem Training betrachtet. Zusatzbehandlungen können helfen, Angstzustände und Schlafstörungen sowie psychotische Symptome zu verringern, bis eine vollständige Gesundung erreicht wird.
2.6.1 Antipsychotika
Eine Major Depression kann mit Wahnsymptomen und/oder Halluzinationen assoziiert sein [14]. Patienten mit psychotischen Symptomen im Rahmen einer depressiven Störung zeigen deutlich höhere Ansprechraten auf die Kombination eines Antidepressivums mit einem Antipsychotikum als unter einer Monotherapie der einzelnen Substanzen (Level A) [186, 291, 292, 313, 322, 341]. Daher wird bei diesen Patienten empfohlen, zu Beginn der Behandlung ein Antidepressivum und ein Antipsychotikum zu kombinieren (Level A). Eine kürzlich veröffentlichte Metaanalyse mit zwei Studien zeigte für die Kombinationsbehandlung aus trizyklischem Antidepressivum und klassischem Antipsychotikum eine bessere Wirksamkeit als unter Antidepressiva allein, jedoch waren die Unterschiede nicht statistisch signifikant [369*]. Die neueren atypischen Antipsychotika (z.B. Amisulprid, Aripiprazol, Olanzapin, Quetiapin, Risperidon, Ziprasidon) sollten aufgrund ihres geringeren Risikos für extrapyramidale Symptome den klassischen Antipsychotika (z.B. Chlorpromazin, Fluphenazin, Haloperidol) oder dem älteren atypischen Antipsychotikum Clozapin vorgezogen werden [33, 77, 220, 257]. Jedoch muss das höhere Risiko der atypischen Antipsychotika, ein metabolisches Syndrom hervorzurufen, berücksichtigt werden.
Es gibt keine kontrollierten Daten, welche die Wirksamkeit der neueren mit den älteren Antipsychotika bei psychotischen Depressionen vergleichen. Die Dosierungen der Antipsychotika bei wahnhaft depressiven Patienten liegen in der Regel niedriger als bei schizophrenen Patienten.
2.6.2 Tranquilizer/Anxiolytika
Obwohl Tranquilizer (besonders Benzodiazepine) in der klinischen Praxis weltweit häufig als Zusatzmedikation eingesetzt werden, glauben viele Experten, dass Benzodiazepine den Stimmungsstatus nicht beeinflussen. Eine kürzlich veröffentlichte Übersicht zeigt, dass in den meisten Ländern zwischen 30% und 60% der depressiven Patienten einen Tranquilizer als Komedikation neben dem Antidepressivum erhalten [124, 356]. Gründe für den weitverbreiteten Gebrauch von Benzodiazepinen ist der schnelle Wirkungseintritt, mit dem Angst, Erregung und Schlaflosigkeit vermindert werden, und die hohe Rate der Komorbitität mit Angststörungen unter Patienten mit Major Depression (zwischen 33% und 85% im Studienquerschnitt). Eine systematische Übersichtsarbeit von Furukawa et al. konnte nachweisen, dass Patienten, die eine Kombinationsbehandlung aus Antidepressiva und Anxiolytika erhielten, nach ein bis vier Wochen häufiger eine Response zeigten als Patienten, die mit einer Antidepressivamedikation allein behandelt wurden (jedoch war dieser Unterschied bereits nach 6 bis 8 Wochen nicht mehr statistisch signifikant [124]). Der Nutzen einer Zusatztherapie mit Anxiolytika muss sorgfältig gegen das mögliche Risiko einer Abhängigkeit und der Neigung zu Stürzen/Unfällen abgewogen werden.
Insgesamt muss bei jedem einzelnen Patienten der potenzielle Nutzen einer Zusatzbehandlung mit Benzodiazepinen sorgfältig gegen den möglichen Schaden (wie Sedierung, psychomotorische und kognitive Beeinträchtigungen, Gedächtnisverlust, Potenzierung anderer zentral wirksamer sedierender Wirkstoffe und durch die Behandlung verursachte Depression, Entwicklung von Abhängigkeit und Absetzsyndrom) abgewogen werden. Prädisponierte Personen haben ein größeres Risiko, eine Medikamentenabhängigkeit zu entwickeln. Daher sollten Benzodiazepine nicht an Patienten mit bestehendem Alkohol- oder Drogenmissbrauch/-abhängigkeit in der Anamnese verabreicht werden. Die Dauer der Benzodiazepingabe bei depressiven Patienten sollte vier Wochen nicht überschreiten.
2.6.3 Schlafentzug
Teilweiser (partieller) oder vollständiger Schlafentzug ist die einzige antidepressive Intervention mit positiven Wirkungen noch am gleichen Tag, indem sie zu einer vorübergehenden Besserung der Depression bei rund 60% der Patienten führt (Level A) [135, 193, 374]. Schlafentzug ist aufgrund der schnellen Wirkung, der Nichtinvasivität und der geringen Kosten eine günstige Zusatzbehandlung bei Major Depression und wird von der Mehrheit der Patienten gut vertragen. Jedoch erleiden die meisten Patienten einen Rückfall nach nur einer Nacht normalen Schlafs [134, 384]. Die antidepressive Wirkung kann in der Regel durch wiederholten vollständigen Schlafentzug (Level B) [368] oder durch eine Kombination aus Schlafentzug und anschließender Schlafphasenverschiebung (Level D) [283] repliziert werden. Lichttherapie kann die antidepressive Wirkung einer partiellen Schlafentzugstherapie weiter unterstützen [247].
2.6.4 Körperliches Training
Studien mit gesunden jungen Menschen haben gezeigt, dass körperliche Aktivität eine positive Wirkung auf die Stimmung haben kann. Offene Studien über kurzfristige Wirkungen eines täglichen Programms mit Aerobic-Übungen legen nahe, dass Stimmungsverbesserungen bei Patienten mit einer Major Depression relativ schnell (nach 14 Tagen) erzielt werden können [96]. Für eine kritische Diskussion des potenziellen Wirkungsmechanismus siehe die Übersichtsarbeit [63]. Die Wirksamkeit dieser Behandlungsstrategie konnte in einer Metaanalyse aufgrund des Mangels an qualitativ hochwertigen Forschungsergebnissen nicht untersucht werden [203]. Kürzlich wurde jedoch in einer randomisierten, kontrollierten Studie mit 38 ausgewerteten depressiven Patienten gezeigt werden, dass Walking eine antidepressive Wirkung hat [191].
2.7 Weitere Behandlungsmöglichkeiten
Die repetitive transkranielle Magnetstimulation (rTMS) ist eine neue Technologie, die nichtinvasiv kortikale Neurone durch magnetische Induktion stimuliert. Dabei wird ein elektromagnetisches Feld in Kopfhautnähe aufgebaut. Studien zur Wirksamkeit von rTMS unterschieden sich hinsichtlich Häufigkeit und Applikationsort der elektromagnetischen Stimulation und zeigten inkonsistente Ergebnisse. In einer kürzlich veröffentlichten Metaanalyse ergab sich für die Behandlung mit rTMS ein geringer Vorteil gegenüber der Scheinbehandlung bereits nach zwei Wochen [218].
Die Vagusnerv-Stimulation (VNS) ist eine neue Technologie zur indirekten Gehirnstimulation über den Vagusnerv (X. Hirnnerv). Ein Schrittmacher in Größe einer Taschenuhr wird subkutan in die linke Brustwand implantiert. Seine zwei Elektroden stehen im Bereich des Halses mit dem linken Vagusnerv in Verbindung. Die Aktivierung des Vagusnervs könnte zu einer Stimmungsverbesserung führen, da seine absteigenden Nervenfasern mit der Amygdala und anderen limbischen Strukturen in Verbindung stehen, welche wiederum Emotion und Stimmung beeinflussen [129]. Zwei kleine, offene Studien berichten Responseraten von etwa 30% [216, 301]. Daten aus zwei Studien mit scheinstimulierter Kontrollgruppe, die erst nach beendeter Literaturrecherche dieser Leitlinie veröffentlicht wurden, fanden im Wesentlichen keinen Unterschied in der Response nach zehn Wochen, jedoch stiegen die Responseraten bei einer Behandlung mit VNS im Laufe des Jahres an [130, 300].
3 Erhaltungstherapie der Major Depression
Ziel der Erhaltungstherapie ist es, die Wahrscheinlichkeit eines Rückfalls in der vulnerablen Periode, welche auf die symptomatische Remission folgt, zu verringern (d.h. dem Rückfall in die überwundene Depressionsepisode vorzubeugen) [2] (Abb. 2). Die Erhaltungstherapie wird in der Regel für sechs Monate nach Remission durchgeführt. Einige Autoren empfehlen jedoch eine Erhaltungstherapie von bis zu neun Monaten [152, 278, 298]. Besonders Patienten mit langer Episodendauer in der Anamnese sollten eine Erhaltungstherapie erhalten, die länger als neun Monate dauert [298]. Da Residualsymptome Prädiktoren für ein hohes Rückfallrisiko sind, wird empfohlen, die Behandlung so lange fortzusetzen, bis diese Symptome abgeklungen sind [262].
In Plazebo-kontrollierten Erhaltungstherapie-Studien liegen die Rückfallraten in der Plazebo-Gruppe zwischen 31% und 80%, verglichen mit 0% bis 31% in der Gruppe mit trizyklischen Antidepressiva [127, 271, 272]. Es wird empfohlen, die Behandlung mit dem Antidepressivum gleicher Dosierung fortzuführen, auf das der Patient in der Akutphase angesprochen hat (Level A) [298, 338]. Bei Patienten ohne Rückfall in der Erhaltungsphase wird ein langsames Ausschleichen der antidepressiven Medikation empfohlen [289]. Man sollte die Patienten während und direkt nach der Ausschleichphase sorgfältig beobachten, um eine Stabilität der Remission zu gewährleisten [14]. Falls sich eine Symptomverschlechterung andeutet, sollte die Behandlung in der ursprünglichen Dosierung für mindestens sechs weitere Monate fortgesetzt werden, bevor man einen weiteren Absetzversuch unternimmt. Nach einer erfolgreichen Lithium-Augmentation in der Akutphase ist die weitere kombinierte Behandlung eines Antidepressivums mit Lithium in der Erhaltungstherapie wirksamer als die Kombination eines Antidepressivums mit Plazebo [36, 66].
4 Rezidivprophylaktische Behandlung der Major Depression
4.1 Allgemeine Behandlungsprinzipien der Rezidivprophylaxe
4.1.1 Ziele und Indikationen
Die Hauptziele der Rezidivprophylaxe bestehen darin, einem Rezidiv, einem möglichen Suizid und einer Chronifizierung der Erkrankung vorzubeugen. Ein Rezidiv ist das Auftreten neuer depressiver Symptome nach einer vollständig symptomfreien Periode (Remission) über einen Zeitraum von mindestens sechs Monaten (Gesundung) [121, 180, 197] (Abb. 2). Für die Behandlungsstrategie in der Rezidivprophylaxe müssen der Krankheitsverlauf des Patienten und seine Anamnese beachtet werden. Obwohl keine präzisen Empfehlungen gegeben werden können, wann mit einer medikamentösen Prophylaxetherapie begonnen werden sollte, ist sie in Situationen mit einem hohen Rezidivrisiko definitiv indiziert [23, 65, 86, 152, 264] (Tab. 4). Zusätzlich zu den in Tabelle 4 genannten Risikofaktoren spielen Patientenwünsche, der Schweregrad der funktionellen Einschränkungen sowie Nebenwirkungen, die in der Erhaltungstherapie auftraten, eine Rolle bei der Entscheidung über den Zeitpunkt des Beginns einer Rezidivprophylaxe [2, 14].
Tab. 4. Faktoren, die mit einem erhöhten Rückfallrisiko der Major Depression assoziiert sind
|
Drei oder mehr Episoden einer Major Depression |
|
Vorausgehende hohe Rückfallhäufigkeit |
|
Vorausgehende Episode im letzten Jahr |
|
Residualsymptome während der Erhaltungstherapie |
|
Subsyndromale Residualsymptome bei Remission |
|
Zusätzliche dysthyme Störung |
|
Schwere der Episoden (einschließlich Suizidalität und psychotische Symptome) |
|
Vorausgehende Episoden von langer Dauer |
|
Rückfall nach fehlender Einnahme der Medikamente |
|
Zusätzlich bestehender Substanzmissbrauch |
|
Zusätzlich bestehende Angststörung |
|
Major Depression bei Verwandten ersten Grades |
|
Beginn der Erkrankung vor dem 30. Lebensjahr |
|
Alter von 60 bis 65 Jahren und älter |
4.1.2 Durchführung der Rezidivprophylaxe
Schlüsselelemente einer Langzeitbehandlung von rezidivierenden depressiven Störungen sind: 1. Psychoedukation, 2. Pharmakotherapie und 3. Monitoring der regelmäßigen Medikamenteneinnahme. Da die Rezidivprophylaxe eine Compliance für die Pharmakotherapie voraussetzt, sind Aufklärung und ein enges therapeutisches Bündnis mit dem Patienten und seinen Angehörigen von großer Bedeutung [197]. Strategien, die Patienten und ihre Angehörigen auf eine Rezidivprophylaxe/Langzeitbehandlung vorbereiten, sollten folgende Themen beinhalten: typischer Verlauf der Erkrankung, Behandlungsmöglichkeiten, Wirksamkeit der Medikamente und unerwünschte Nebenwirkungen, (täglicher) Gebrauch von Selbstbeurteilungsinstrumenten der Stimmung, um Frühwarnzeichen für einen drohenden Rückfall oder ein Rezidiv zu erkennen, die Langzeitprognose sowie das voraussichtliche Behandlungsende. Es ist wichtig, den Patienten darüber aufzuklären, dass eventuell mehrere Behandlungsvarianten ausprobiert werden müssen, bevor die individuell beste Behandlungsform gefunden wird.
Die Häufigkeit der Arztbesuche zur (kurzen) psychiatrischen Beurteilung und dem Monitoring der Medikation (z.B. Beurteilung von Nebenwirkungen, Medikamentenblutspiegel) kann bei stabilen Patienten von monatlichen Konsultationen bis zu Terminen alle drei bis sechs Monate variieren. Bei instabilen Patienten sind häufigere Termine notwendig. Falls der Patient während der Langzeitbehandlung eine körperliche Erkrankung entwickelt, sollten mögliche Wechselwirkungen zwischen Medikamenten bedacht werden (Tab. 5). Patienten und Angehörige sollten aufgeklärt werden, ihren behandelnden Arzt zu informieren, sobald erste Zeichen einer erneut beginnenden Depression auftreten.
Tab. 5. Mögliche Wechselwirkungen der Antidepressiva mit anderer Komedikation
|
Komedikation |
Wechselwirkung |
|
TZA |
|
|
Alpha1-Adrenorezeptor-Antagonisten (Prazosin) |
Erhöhter Blutdruckabfall |
|
Anästhetika/Muskelrelaxanzien (Halothan, Pancuronium, Gallamin) |
Erhöhte Gefahr von Arrhythmien |
|
Antazida, Adsorbenzien |
Möglicherweise niedrigere Antidepressiva-Blutspiegel |
|
Antiarrhythmika (Chinin, Lidocain, Disopyramid, Procainamid, Propafenon) |
Verlängerte intrakardiale Reizleitung, erniedrigte myokardiale Kontraktion bis hin zur Herzinsuffizienz |
|
Antikoagulanzien (Warfarin, möglicherweise |
Erhöhte Wirkung auf die Antikoagulation mit verlängerter Blutungszeit |
|
Antikonzeptiva |
Mehr Nebenwirkungen der TZA, niedrigere Plasmaspiegel an TZA wurden beobachtet, daher geringere antidepressive Wirkung |
|
Antidiabetika, oral |
Höhere Plasmaspiegel mit erhöhter Senkung des Blutzuckers |
|
Antimykotika (Fluconazol, Ketoconazol) |
Höhere Plasmaspiegel an TZA mit mehr Nebenwirkungen |
|
Betablocker |
Erhöhter Blutdruckabfall, erniedrigte Plasmaspiegel an Propranolol und TZA, daher mehr Nebenwirkungen; mit Propranolol mögliche Verschlechterung oder Induktion einer Depression |
|
Calciumkanalblocker (Diltiazem, Verapamil) |
Höhere Plasmaspiegel von z.B. Imipramin, daher mehr Nebenwirkungen |
|
Carbamazepin |
Gefahr niedrigerer Plasmaspiegel von TZA aufgrund der Enzyminduktion (CYP) |
|
Cimetidin |
Höhere Plasmaspiegel mit mehr Nebenwirkungen |
|
Cisaprid |
Höhere Plasmaspiegel von Antidepressiva mit erhöhtem Risiko für Nebenwirkungen |
|
Diuretika |
Erhöhter Blutdruckabfall |
|
Insulin |
Möglicherweise Erhöhung der blutzuckersenkenden Wirkung |
|
Nicotin, Rauchen |
Niedrigere Blutspiegel von TZA möglich |
|
Omeprazol |
Möglicherweise höhere Plasmaspiegel von TZA mit mehr Nebenwirkungen |
|
Rifampicin |
Niedrigere Plasmaspiegel von TZA, daher geringere antidepressive Wirkung möglich |
|
SSRI |
Gefahr der höheren Plasmaspiegel von TZA aufgrund der Enzyminhibition (CYP) |
|
SSRI |
|
|
Antiarrhythmika (Propafenon, Flecainid) |
Inhibition der Metabolisierung mit eventuell höheren Plasmaspiegeln von Antiarrhythmika |
|
Antikoagulanzien (Phenprocoumon, Warfarin) |
Fluvoxamin könnte den Warfarin-Spiegel erhöhen. Erhöhte Blutungsneigung könnte daraus resultieren. |
|
Antidiabetika, oral |
Eventuell erhöhte blutzuckersenkende Wirkung der Antidiabetika |
|
Antihistaminika (Terfenadin, Astemizol) |
Verlängerte intrakardiale Reizleitung und Arrhythmien |
|
Betablocker |
Inhibition der Metabolisierung von Paroxetin, daher eventuell höhere Plasmaspiegel mit erhöhtem Risiko für Nebenwirkungen |
|
Carbamazepin |
Risiko für höhere Plasmaspiegel von Carbamazepin |
|
Cimetidin |
Inhibition der Metabolisierung von Paroxetin, daher eventuell höhere Plasmaspiegel mit erhöhtem Risiko für Nebenwirkungen |
|
Cisaprid |
Höhere Plasmaspeigel von Antidepressiva mit erhöhtem Risiko für Nebenwirkungen |
|
Digitoxin |
Eventuell niedrigere Plasmaspiegel von Digitoxin mit geringerer Wirksamkeit |
|
Immunsuppressiva |
Höhere Plasmaspiegel an Immunsuppressiva in Verbindung mit Fluoxetin und Fluvoxamin |
|
Theophyllin, Coffein |
Inhibition der Metabolisierung von Theophyllin in Verbindung mit Fluvoxamin, daher höheres Risiko für Theophyllin-Nebenwirkungen |
|
Tramadol |
Risiko eines zentralen Serotonin-Syndroms |
|
Venlafaxin |
|
|
Betablocker |
Inhibition der Metabolisierung, daher eventuell höhere Plasmaspiegel mit höherem Risiko für Nebenwirkungen |
|
Carbamazepin |
Risiko für niedrigere Plasmaspiegel von Venlafaxin aufgrund der Enzyminduktion (CYP) |
|
SSRI |
Risiko für höhere Plasmaspeigel von Venlafaxin aufgrund der langsameren Metabolisierung |
|
Tramadol |
Risiko eines zentralen Serotonin-Syndroms |
|
MAO-Hemmer |
|
|
Serotonerge Medikamente (besonders SSRI) |
Potenzierung der Effekte und des Risikos eines zentralen serotonergen Syndroms |
|
Sympathomimetika (Epinephrin und andere Katecholamine, Ephedrin) |
Risiko für hypertensive Krisen |
4.2 Pharmakotherapie der Rezidivprophylaxe
4.2.1 Evidenz der Wirksamkeit
Die Pharmakotherapie, insbesondere mit Antidepressiva und Lithium, ist die am besten untersuchte Behandlungsform in der langfristigen Therapie von rezidivierenden unipolaren Depressionen. Die Mehrzahl der kontrollierten Studien, die den Einsatz dieser Medikamente in der Rezidivprophylaxe untersucht haben, zeigten eine prophylaktische Wirksamkeit gegen Rezidive [2, 3, 85, 152, 319].
Medikamente erster Wahl zur Rezidivprophylaxe von unipolaren Depressionen sind entweder das Antidepressivum, mit dem in der Akut- und Erhaltungstherapie eine Remission erreicht wurde, oder Lithium [2, 14, 250, 264, 273]. Gründe für eine bevorzugte Gabe von Antidepressiva gegenüber Lithium sind, dass Patienten während der Akut- und Erhaltungstherapie in der Regel mit Antidepressiva behandelt werden und dass Patienten Medikamente bevorzugen, die keine regelmäßigen Laboruntersuchungen verlangen. Die endgültige Wahl des Medikaments zur Rezidivprophylaxe muss davon abhängen, wie der einzelne Patient auf die Behandlung mit Antidepressiva oder Lithium anspricht und wie er die Therapie verträgt [305]. Patientenwünsche und eigene Erfahrungen der Patienten oder Erfahrungen der Angehörigen mit einer Rezidivprophylaxe sollten bei der Wahl des Medikaments berücksichtigt werden.
4.2.1.1 Antidepressiva
Die meisten Patienten erhalten während der Akut- und Erhaltungstherapie Antidepressiva. Die beste Möglichkeit, einem Rezidiv vorzubeugen, ist, die antidepressive Medikation, die erfolgreich in der Akut- und Erhaltungstherapie eingesetzt wurde, mit derselben Dosierung in der Rezidivprophylaxe fortzuführen (Level B) ([120, 122], systematischer Review mit Metaanalyse [127]).
Bereits schwache oder moderate Nebenwirkungen während einer Langzeittherapie können zu unregelmäßigen Medikamenteneinnahmen vonseiten des Patienten führen, was wiederum zu einer Symptomverschlechterung und einem erhöhten Rezidivrisiko führt. Daher kann der Gebrauch von Medikamenten mit einem günstigeren Nebenwirkungsprofil als jenem der trizyklischen Antidepressiva (TZA) die Patientencompliance erhöhen. Neuere Antidepressiva sind mit weniger langfristigen Nebenwirkungen assoziiert als ältere trizyklische oder tetrazyklische Antidepressiva [2, 3, 14, 219, 265].
4.2.1.2 Lithium
Die Anwendung von Lithium in der Langzeittherapie unipolarer rezidivierender Depressionen ist gut belegt (Level A) [76, 100, 113, 139, 264, 305]. Zwei Metaanalysen gaben Hinweise, dass Lithium zur Verhinderung von Rezidiven bei unipolar rezidivierender Depression wirksamer ist als Plazebo [68, 321]. Jedoch waren die Unterschiede nur in einer der Metaanalysen statistisch signifikant [321]. Im letzten Jahrzehnt wurden Daten aus retrospektiven und prospektiven Studien gewonnen, die zeigen, dass eine langfristige Lithiumprophylaxe das Suizidrisiko senken und sogar die hohe Mortalitätsrate normalisieren kann (Level C) [75, 79, 140, 237, 238, 307, 346, 347].
Zur Rezidivprophylaxe werden Lithiumspiegel im Bereich von 0,5 bis 0,8 mmol/l (mEq/l), zwölf Stunden nach der letzten Lithiumeinnahme gemessen, empfohlen [304]. Bei Patienten bis 60 Jahre werden die empfohlenen Lithiumspiegel normalerweise mit einer täglichen Dosis von 12 bis 30 mmol (ca. 10 bis 20 mmol für Patienten asiatischer Herkunft) und bei älteren Patienten mit einer täglichen Dosis von etwa 6 bis 12 mmol erreicht (s. auch [54]). Die ein- oder zweimalige Gabe von Lithium pro Tag führt zu keinen Unterschieden in der Wirksamkeit. Einige Patienten finden, dass eine Einmalgabe ihnen die Compliance in der langfristigen Behandlung erleichtert und Nebenwirkungen seltener auftreten. Im Allgemeinen sind die Retardformen von Lithium besser verträglich.
Ein Vorteil einer Rezidivprophylaxe mit Lithium ist die lange und weltweite Erfahrung mit diesem Wirkstoff. Spezialisierte Lithiumkliniken, die auf eine prophylaktische Langzeitbehandlung mit Lithium bei Patienten mit affektiven Störungen spezialisiert sind, wurden in den letzten 30 Jahren in vielen Ländern eingerichtet und liefern Informationen über die Langzeitnebenwirkungen einer Lithiumbehandlung [305]. Nebenwirkungen von Lithium sind in der Regel dosisabhängig und können oft schon durch eine moderate Dosisreduktion verhindert oder gebessert werden [13]. Die wichtigsten Nebenwirkungen von Lithium sind Tremor der Hände (mögliche Gegenmaßnahme: Gabe eines Betablockers), Struma und Hypothyreose (durch eine zusätzliche Gabe von Levothyroxin [T4] kann die Struma verkleinert und ein euthyreoider Zustand erreicht werden), vermindertes Konzentrierungsvermögen der Niere, Polyurie und/oder Polydipsie (Patienten vor einer Dehydrierung warnen, mögliche Dosisverringerung), Gewichtszunahme (Anraten einer leichten Diät und körperlichem Training), gastrointestinale Nebenwirkungen wie beispielsweise Übelkeit, Dyspepsie, weicher Stuhl (kann durch eine Lithiumgabe zu den Mahlzeiten oder Wechsel zu einem anderen Lithiumpräparat oder eine Dosisverringerung beherrscht werden) und in wenigen Fällen Gedächtnisbeeinträchtigungen und mentale Verlangsamung (durch eine Dosisreduktion beherrschbar) [13, 54]. Ein geringer Prozentsatz der Patienten, die mit Lithium behandelt werden, entwickelt nach zehn- oder mehrjähriger Behandlung steigende Creatininwerte. Jedoch scheint bei Patienten, die mehr als 15 Jahre mit Lithium behandelt werden, die Beeinträchtigung der glomerulären und tubulären Funktion verbreitet zu sein [51].
Während der Langzeitanwendung von Lithium werden regelmäßige Bestimmungen der Lithiumspiegel empfohlen (drei- bis viermal pro Jahr oder häufiger, falls klinisch notwendig, z.B. am Anfang der Behandlung, bei älteren Patienten oder nachdem klinische Veränderungen der Schilddrüsenfunktion [z.B. TSH-Spiegel] oder der Nierenfunktion [Creatinin, ein oder zweimal pro Jahr] offensichtlich werden) [13, 54, 187, 305]. Ziel der Lithiumspiegelmessungen ist es, sicherzustellen, dass zu hohe Lithiumspiegel rechtzeitig entdeckt und verringert werden können, und zu gewährleisten, dass Schritte eingeleitet werden, um einem Rezidiv aufgrund zu niedriger Lithiumspiegel vorzubeugen. Außerdem ist es besonders wichtig, die Patienten und ihre Angehörigen über die Warnzeichen einer Lithiumintoxikation aufzuklären.
Eine relativ geringe Anzahl von Studien hat verschiedene Medikationen zur Langzeitbehandlung bei rezidivierender unipolarer Depression direkt verglichen [319]. Eine Metaanalyse aus Studien, welche Lithium im Vergleich zu Antidepressiva untersuchten, konnte keinen überzeugenden Vorteil für Lithium in der Rezidivprophylaxe einer unipolaren Erkrankung [321] finden. Obwohl die Daten zur prophylaktischen Wirksamkeit von Carbamazepin zur Behandlung einer unipolaren Depression begrenzt sind, lassen die Ergebnisse der Studien vermuten, dass Carbamazepin eine Alternative für Patienten sein könnte, die eine Rezidivprophylaxe mit Lithium oder mit Antidepressiva nicht vertragen oder auf diese nicht ansprechen (Level C) (Abb. 4).
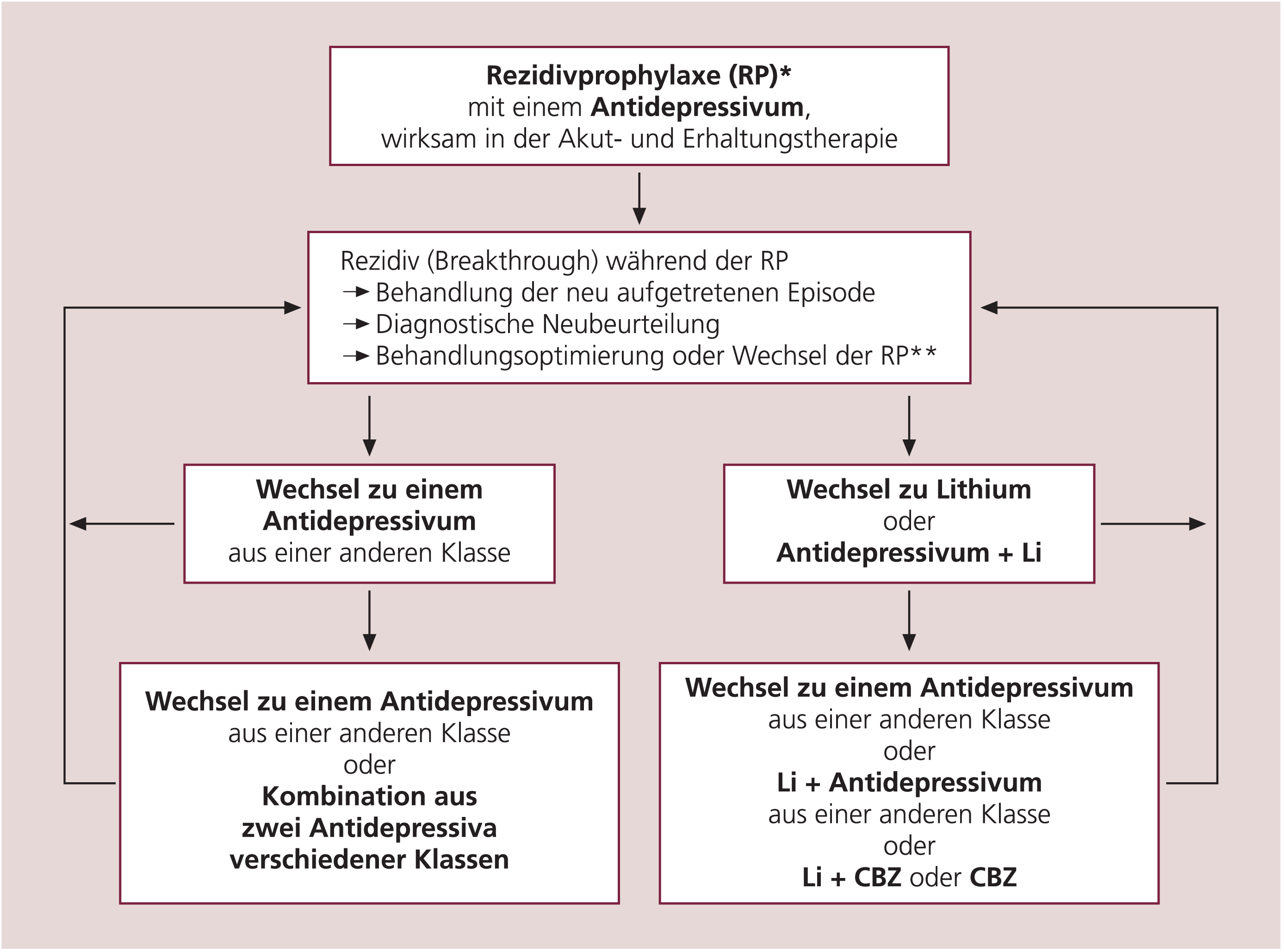
Abb. 4. Flussdiagramm – Therapeutische Möglichkeiten für die Rezidivprophylaxe einer Major Depression
RP: Rezidivprophylaxe, Li: Lithium, CBZ: Carbamazepin
*Elektrokrampftherapie (EKT) ist eine Behandlungsmöglichkeit für Patienten, die in der akuten Phase der Behandlung auf EKT angesprochen haben oder bei denen zwei oder mehr rezidivprophylaktische Therapieversuche fehlgeschlagen sind.
**Eine Kombination mit Psychotherapie sollte in Erwägung gezogen werden.
4.2.2 Behandlung bei Symptomverschlechterung und Rezidiv
Kurze, leichte depressive Symptome (sogenannte „blips“) treten im Rahmen der Rezidivprophylaxe recht häufig auf. Sie sind gewöhnlich selbstlimitierend und verlangen in der Regel im Gegensatz zu Rezidiven (wiederauftretende Episoden) keine spezifische Behandlung oder eine Änderung des Behandlungsregimes im Rahmen der Rezidivprophylaxe. Ein psychiatrisches Management (z.B. Dosisanpassung, Beruhigung des Patienten) und eine kurzfristige Behandlung mit Benzodiazepinen oder anderen sedierenden Medikamenten zur Behandlung von Schlaflosigkeit und/oder Angstzuständen oder eine zusätzliche psychotherapeutische Intervention, die auf spezifische psychosoziale Stressoren fokussiert ist, können hilfreich sein [297].
Viele Patienten zeigen in der Prodromalphase zum vollausgeprägten Rezidiv ein vorhersagbares Symptommuster. Wenn ein Patient trotz gegenwärtiger Rezidivprophylaxe („breakthrough episode“) ein Rezidiv einer depressiven Episode erleidet, stehen die behandelnden Ärzte vor einer großen Herausforderung. Eine frühzeitige Intervention kann die Episodenlänge verkürzen [194]. Zur differenzialdiagnostischen Abklärung eines Rezidivs sollten ein verborgener Substanzmissbrauch, eine nicht diagnostizierte somatische Erkrankung (z.B. Schilddrüsendysfunktion), eine unzureichende Compliance und die Möglichkeit von negativen Lebensereignissen in Betracht gezogen werden [297]. Patienten, die eine erneute depressive Episode erleben, während sie stimmungsstabilisierende Medikamente oder Antidepressiva einnehmen, können aus einer Behandlungsoptimierung möglicherweise einen Nutzen ziehen (z.B. Erhöhung des Serumspiegels in den oberen Bereich des therapeutischen Fensters, „Add-on“-Therapie von Schilddrüsenhormonen, falls die Schilddrüsenfunktion erniedrigt ist – besonders bei mit Lithium behandelten Patienten –, zusätzliche psychotherapeutische Interventionen und Arztbesuche). Falls der Patient trotz Behandlungsoptimierung keine Besserung zeigt, sollte eine erneute Akutbehandlung mit anschließender Erhaltungstherapie begonnen werden (s. oben).
4.2.3 Möglichkeiten in der Rezidivprophylaxe behandlungsresistenter Depressionen
Es gibt ein wachsendes Bewusstsein dafür, dass bei einem großen Teil der Patienten die Prophylaxebehandlung affektiver Störungen nicht adäquat durchgeführt wird. Die Rezidivprophylaxe depressiver Patienten, die ein Rezidiv unter prophylaktischer Therapie mit Standardmedikamenten, wie beispielsweise Lithium oder Antidepressiva, erleiden, ist eine der größten Herausforderungen in der Behandlung dieses Krankheitsbilds. Jedoch stehen nur wenige Daten aus kontrollierten Studien zur Verfügung, um Ärzte bei der Rezidivprophylaxe von Patienten zu leiten [37]. Ein Algorithmus, der Möglichkeiten für die Rezidivprophylaxe von Patienten mit einer Major Depression beinhaltet, ist in Abbildung 4 dargestellt. Die Behandlungsmöglichkeiten umfassen die Kombination eines Antidepressivums mit Lithium, die Kombination von Lithium mit Carbamazepin, die Kombination zweier Antidepressiva verschiedener Klassen und die Elektrokrampftherapie (EKT).
4.3 Dauer und Ende einer Rezidivprophylaxe
Der optimale Zeitpunkt, eine Langzeitmedikation abzusetzen, ist schwierig vorherzusagen. Eine kontrollierte Studie über fünf Jahre lieferte gute Hinweise dafür, dass die Patienten, die den größten Nutzen aus einer langfristigen Prophylaxe zogen, diejenigen waren, welche die volle Medikamentendosis über mindestens fünf Jahre erhielten (Level B) [196]. Eine Rezidivprophylaxe ist daher bei einigen Patienten für sehr lange Zeit (z.B. zehn Jahre) und für andere auf unbestimmte Zeit notwendig [298]. Eine dreijährige Rezidivprophylaxe sollte routinemäßig durchgeführt werden, besonders dann, wenn der aktuellen Episode in den letzten fünf Jahren eine andere Episode voranging oder wenn eine Remission nur schwer zu erreichen war. Für Patienten mit einem größeren Risiko wird eine fünfjährige oder auf unbestimmte Zeit geplante Rezidivprophylaxe empfohlen, besonders wenn zwei oder drei Absetzversuche eine weitere Episode innerhalb eines Jahres zur Folge hatten. In der klinischen Praxis sollten Antidepressiva nach einer Rezidivprophylaxe immer langsam über vier bis sechs Monate ausgeschlichen werden, um ein frühzeitiges Erkennen erneut auftretender Symptome zu ermöglichen und um das Risiko von Absetzsyndromen zu minimieren. Absetzsymptome nach einem abrupten Stop der antidepressiven Medikation wurden für alle Antidepressivaklassen berichtet. Sie sind üblicherweise leicht und von kurzer Dauer, dennoch können sie für den Patienten stressreich sein. Sie beinhalten neben einem erhöhten Risiko für ein frühzeitiges Rezidiv [358], beispielsweise bei einer Behandlung mit SSRI und SNRI, Schwindel, Ataxie, gastrointestinale und grippeähnliche Symptome sowie Schlafstörungen. Bei einer Behandlung mit Lithium scheint ein erhöhtes Rezidivrisiko hauptsächlich durch das abrupte Absetzen der Medikation beeinflusst zu werden. Nach Einstellung der Lithiumbehandlung ist das Risiko für unmittelbar auftretende, neue manische oder depressive Episoden erhöht [72]. Jedoch wird diskutiert, ob dies auch für unipolar depressive Patienten zutrifft und ob der Abbruch zu einem Wirksungsverlust führen kann [212]. Ein spezifisches Absetzsyndrom konnte nicht eindeutig nachgewiesen werden [306].
Während der Absetzperiode sollte der Patient engmaschiger beobachtet werden. Um Patienten zu identifizieren, bei denen ein hohes Rückfallrisiko besteht, sollte das Monitoring während der nächsten Monate fortgeführt werden (z.B. insbesondere während der nächsten sechs Monate, die ein hohes Rezidivrisiko bergen [298]). Falls während oder nach dem Absetzen eine vollständig neue depressive Episode auftritt, sollte erneut die volle therapeutische Dosis des Medikaments gegeben werden [2]. Ungeachtet der Gründe sollte, wenn die Langzeitpharmakotherapie unterbrochen wird, der Patient über die Risiken und frühen Warnzeichen eines Rezidivs aufgeklärt werden.
4.4 Konversion von einer unipolaren depressiven zu einer bipolaren Störung
Eine Diagnoseänderung von einer unipolaren Depression zu einer bipolaren Störung wurde bei etwa 10% bis 20% der Patienten beschrieben [5, 18, 320]. Antidepressiva, besonders trizyklische Antidepressiva, können zudem bei einigen Patienten eine Manie induzieren [8, 260]. Falls ein Switch in die Manie auftritt, sind eine rasche Dosisreduktion des Antidepressivums und eine gleichzeitige Behandlung der manischen Episode einzuleiten (für mehr Informationen zur Behandlung der Manie siehe WFSBP-Leitlinien für die Behandlung von bipolaren Störungen).
4.5 Psychotherapie
Diese Leitlinie konzentriert sich auf biologische Behandlungsformen. Deshalb werden psychotherapeutische Behandlungsmethoden allein oder in Kombination mit Pharmakotherapie nur kurz erwähnt und keine Evidenzlevel angegeben (stattdessen wird weiterführende Literatur zu diesem Thema aufgeführt).
Obwohl Psychotherapie als alleinige Behandlung zur Rezidivprophylaxe nur selten untersucht wurde und an dieser Stelle nicht als Behandlung erster Wahl empfohlen wird (Ausnahmen: der Patient möchte oder kann aus bestimmten Gründen, z.B. Schwangerschaft, keine Medikamente einnehmen [2]), stellt sie eine Behandlungsmöglichkeit für einige Patienten dar. Vorläufige Daten zeigen, dass kognitive Verhaltenstherapie (KVT) eine wirksame Behandlungsform sein kann, um Rezidiven bei Patienten mit Major Depression vorzubeugen [334, 359], einschließlich der Patienten, die erfolgreich mit Antidepressiva behandelt wurden [109]. Es gibt Evidenz, dass Patienten mit Residualsymptomen von einer KVT profitieren, um einem Rezidiv vorzubeugen [109, 263]. Auch die als Erhaltungstherapie durchgeführte interpersonelle Psychotherapie (maintenance interpersonal psychotherapy, IPT-M) wurde untersucht [64, 123]. Zusätzlich könnte bei chronischer Depression das kognitive Verhaltensanalysesystem als Langzeittherapie eingesetzt werden [186].
5 Behandlung chronischer depressiver Störungen
Chronische depressive Störungen sind durch eine unzureichende Behandlung und psychosoziale Einschränkungen gekennzeichnet. Patienten mit chronischer Depression werden oft nicht oder nur inadäquat behandelt [177].
5.1 Dysthyme Störungen
Die ICD-10 definiert die Dysthymie als eine chronische Verstimmung, die gegenwärtig nicht die Kriterien für eine rezidivierende depressive Störung hinsichtlich der Schwere oder der Dauer einer einzelnen Episode erfüllt (WHO 1991). Ähnlich charakterisiert das DSM-IV dysthyme Störungen als chronisches, leichtes depressives Syndrom, das mindestens zwei Jahre oder länger besteht [12]. Patienten mit Dysthymie zeigen oft eine komorbide Major Depression („Doppeldepression“/„double depression“). Diese Patienten haben eine geringere Aussicht auf eine vollständige Gesundung als Patienten mit einer depressiven Störung ohne Dysthymie [14]. Jedoch profitieren Patienten mit einer „Doppeldepression“, die im Rahmen der depressiven Episode behandelt werden, auch hinsichtlich ihrer Dysthymie [4, 192].
Die Dysthymie ist mit einer mittleren Punktprävalenz von etwa 2,1% weltweit eine relativ häufige Störung [361, 378]. Die Lebenszeitprävalenz wurde auf 3,1% [362] bis 6,4% [182] geschätzt. Es gibt epidemiologische Daten für eine hohe Komorbidität (bis zu 75%) mit anderen psychiatrischen Störungen, hauptsächlich mit der Major Depression, Angststörungen und Substanzmissbrauch [185]. Die Dysthymie (und die unterschwellige sowie die Minor Depression) ist zudem häufig bei älteren Menschen anzutreffen [245].
5.2 Pharmakotherapie dysthymer Störungen
Obwohl die Daten aus kontrollierten Studien noch begrenzt sind, bestätigte eine umfassende Übersichtsarbeit die Wirksamkeit von verschiedenen Anti-depressiva bei dysthymen Störungen (Level A) [381]. Eine Metaanalyse mit 15 randomisierten kontrollierten Studien, die verschiedene Medikamente (meist Antidepressiva, v.a. TZA, SSRI und MAO-Hemmer) mit Plazebo verglichen, zeigte, dass die medikamentöse Therapie wirksamer ist als Plazebo. Dabei gab es keine Unterschiede zwischen den verschiedenen Antidepressiva-Klassen und Substanzen [88, 89].
Obwohl die optimale Dauer einer Pharmakotherapie bei Dysthymie nicht unter kontrollierten Bedingungen untersucht wurde, wird die antidepressive Behandlung für mindestens zwei bis drei Jahre empfohlen, ähnlich wie bei der Major Depression. Durch die bessere Verträglichkeit und das günstigere Nebenwirkungsprofil sind SSRI und andere neuere Antidepressiva verglichen mit älteren Antidepressiva (z.B. TZA) Medikamente der ersten Wahl in der Rezidivprophylaxe der Dysthymie (Level A). Amisulprid, ein Antipsychotikum der zweiten Generation, zeigt eine vergleichbare Wirksamkeit wie der SSRI Paroxetin [284] und eine bessere Wirksamkeit als der SSRI Sertralin [234]. Die Dosisempfehlungen bei Dysthymie gleichen denen, die bei der Akuttherapie einer depressiven Episode empfohlen werden.
Es gibt wenig Evidenz zur Wirksamkeit von Antidepressiva bei der Dysthymie bei älteren Patienten. Eine kürzlich veröffentlichte Studie lässt vermuten, dass Fluoxetin nur eine begrenzt bessere Wirksamkeit im Vergleich zu Plazebo aufweist und dass weitere Untersuchungen notwendig sind, um Vorhersagen über das Ansprechen bei älteren dysthymen Patienten treffen zu können [95]. Eine offene Studie gab Hinweise auf eine hohe Responserate bei dysthymen Patienten, die mit Venlafaxin behandelt wurden. Jedoch vollendeten nur 18 Patienten von 23 die geplante Studiendauer von zwölf Wochen [94].
6 Behandlung in speziellen Situationen
In speziellen Situationen muss die Therapie einer Major Depression entsprechend modifiziert werden. Zu diesen Situationen zählen Depressionen, die gemeinsam mit anderen psychiatrischen Erkrankungen auftreten (z.B. Angststörungen, Substanzmissbrauch/-abhängigkeit), Depressionen bei Kindern und Jugendlichen sowie bei älteren Menschen, somatische Erkrankungen als Ursache für eine Depression oder Depressionen bei schwangeren oder stillenden Frauen. In diesen Fällen wird empfohlen, einen Psychiater/Nervenarzt bei der Behandlung hinzuzuziehen (s. WFSBP Guidelines [39]).
6.1 Depression in Komorbidität mit anderen psychiatrischen Erkrankungen
6.1.1 Komorbide Angststörungen
Bis zu 30% der unipolar depressiven Patienten leiden zusätzlich unter Angststörungen, einschließlich Panikattacken und posttraumatischen Belastungsstörungen (posttraumatic stress disorder, PTSD) [377]. SSRI und duale Antidepressiva [112, 279], aber auch TZA und MAO-Hemmer, können wirksam zur Behandlung eingesetzt werden. Die initiale Dosis sollte niedrig angesetzt sein (z.B. mit 5 mg Fluoxetin oder 10 mg Paroxetin) und die Dosis bis zur therapeutischen Dosis gesteigert werden. Die Dosis sollte entsprechend gegebenenfalls auftretenden Nebenwirkungen angepasst werden. Die kognitive Verhaltenstherapie (KVT) kann ebenfalls wirksam zur Behandlung von Angststörungen, die neben einer Depression auftreten, eingesetzt werden. Anxiolytika sollten nur in den ersten Tagen eingesetzt werden, falls schwere Angstzustände vorliegen.
6.1.2 Substanzmissbrauch und Abhängigkeit
Komorbider Substanzmissbrauch bzw. -abhängigkeit treten bei Depression mit einer hohen Prävalenz auf (bei 30% bis 60% der Patienten mit Substanzmissbrauch/-abhängigkeit treten zusätzlich affektive und Angststörungen auf und ungefähr ein Drittel der Patienten mit affektiven Störungen geben Episoden eines Substanzmissbrauchs oder einer -abhängigkeit in der Anamnese an) [276, 310]. Es ist besonders wichtig, beide Störungen, das heißt sowohl die depressive Störung als auch den Substanzmissbrauch bzw. die -abhängigkeit, zu behandeln, da ein bestehender Substanzmissbrauch die Effektivität der antidepressiven Behandlung und die Compliance des Patienten beeinträchtigen kann. In einigen Fällen sollte der Substanzmissbrauch zuerst behandelt werden, da dies bereits zu einer Abnahme der depressiven Symptomatik führt. Mögliche pharmakokinetische Wechselwirkungen müssen bei gleichzeitiger Behandlung mit beispielsweise Methadon und Antidepressiva beachtet werden, da diese zu Atemdepression und Sedierung führen können.
Substanzinduzierte affektive Störungen treten nur während Intoxikations- oder Entzugsstadien auf, während primäre Depressionen dem Substanzmissbrach vorausgehen oder während der Zeit anhaltender Abstinenz auftreten können [13]. In diesem Fall sollten Antidepressiva wegen des höheren Risikos unerwünschter Ereignisse mit Vorsicht eingesetzt werden. Eine auf den Patienten zugeschnittene kognitive Psychotherapie hat sich als wirksam erwiesen [310].
6.2 Depressionsbehandlung bei älteren Patienten
Eine Major Depression im höheren Lebensalter tritt viel häufiger auf als bisher angenommen. Sie wird häufig nicht diagnostiziert, insuffizient behandelt und die generelle Prognose bei diesen Patienten ist eher schlecht [74, 175, 328, 367]. Es stellt eine besondere Herausforderung dar, ältere Patienten mit einer Major Depression wirksam und sicher zu behandeln. Altersbedingte physiologische Veränderungen führen zu klinisch signifikanten Unterschieden in der Metabolisierung und Pharmakokinetik der Medikamente [274]. Ältere Patienten erhalten aufgrund von Multimorbidität oft mehrere Medikamente, was das Risiko für schwerwiegende pharmakokinetische und pharmakodynamische Wechselwirkungen zwischen den Medikamenten erhöht [101, 269].
Es gibt nur wenige Daten zur Anwendung von Antidepressiva bei älteren Patienten, speziell bei den über 75-Jährigen und denjenigen mit ausgeprägter Komorbidität, Demenz oder neurologischen Ausfällen [118, 285, 287]. Im Vergleich zu Plazebo konnte eine Übersichtsarbeit die bessere Wirksamkeit von TZA, SSRI und Mirtazapin bei Patienten über 55 Jahren belegen [333]. Vergleichende Metaanalysen zu verschiedenen Antidepressivaklassen ergaben keine signifikanten Unterschiede bezüglich ihrer Wirksamkeit und Verträglichkeit bei älteren (>55 bzw. >60 Jahre) depressiven Patienten [132, 223, 227]. Das trizyklische Antidepressivum Nortriptylin ist das am besten untersuchte Medikament bei älteren Patienten (Level A) [118, 282, 285].
Die Wirksamkeit und Verträglichkeit der SSRI bei älteren depressiven Patienten wurde in einer Reihe von klinischen Studien mit Sertralin, Paroxetin und Fluoxetin untersucht (Level A) [59, 99, 240, 241, 285, 345]. Für Venlafaxin und Reboxetin konnte die Wirksamkeit in doppelblinden Vergleichsstudien gezeigt werden [174, 325] (Level B). Eine Metaanalyse zum RIMA Moclobemid unterstreicht dessen Wirksamkeit bei geriatrischen Patienten (Level A) [20].
Im Vergleich zu jungen Erwachsenen kann die Response auf die antidepressive Therapie bei älteren Patienten verzögert sein, obwohl dies nur für die Behandlung mit älteren Antidepressiva nachgewiesen werden konnte [172], während eine Behandlung mit SSRI nicht regelmäßig zu einer verzögerten Response bei älteren Patienten führt [302]. Ältere Patienten zeigen vermutlich eine höhere Rückfallrate während der Phase der Erhaltungstherapie [281]. Es gibt Evidenz, dass ältere Patienten von einer aktiven Behandlung in der Erhaltungsphase weiter profitieren können. Eine Plazebo-kontrollierte Studie hat dies für den SSRI Citalopram untersucht [190] (Level D).
Für die Rezidivprophylaxe gibt es Evidenz, dass folgende Substanzen im Vergleich zu Plazebo Rückfälle wirksam verhindern können: Dosulepin (Dothiepin) [256], Phenelzin [131], Citalopram [190] und Lithium, das zusätzlich zu einem Antidepressivum gegeben wird [371] (Level B).
Kardiovaskuläre Nebenwirkungen sind bei älteren Patienten besonders problematisch. Eine Vergleichsstudie von Paroxetin und Nortriptylin zur Behandlung depressiver Patienten mit Angina pectoris (mit einem großen Anteil von Patienten über 60 Jahren) zeigte für beide Substanzen eine vergleichbare Wirksamkeit. Jedoch wiesen die mit Nortriptylin behandelten Patienten eine signifikant höhere Rate schwerwiegender unerwünschter kardialer Nebenwirkungen auf [286]. Unerwünschte anticholinerge Nebenwirkungen (kognitive Beeinträchtigung, Obstipation, Harnverhalt) stellen ein besonderes Problem dar (Tab. 3).
Aufgrund der vergleichbaren Wirksamkeit der verschiedenen Antidepressivaklassen wird die Medikamentenwahl durch die Nebenwirkungsprofile der jeweiligen Substanzen bestimmt. Da ältere Patienten häufiger zu orthostatischer Hypotension neigen und vulnerabler für andere kardiovaskuläre und anticholinerge Nebenwirkungen sind, werden bei dieser Patientengruppe SSRI und die anderen neueren Antidepressiva den TZA vorgezogen (Level A) [175, 372].
Ältere Patienten benötigen üblicherweise geringere orale Dosen als jüngere Patienten, um die gleiche Wirksamkeit zu erreichen. Jedoch finden sich bei älteren Patienten bei gleicher Dosis häufig höhere Plasmakonzentrationen des Medikaments im Vergleich zu jüngeren Patienten [14, 16]. Besonders bei Patienten mit Nieren- oder Lebererkrankungen sollte die Dosis der Medikamente speziell angepasst werden.
Für Empfehlungen zur Behandlung einer Depression im hohen Alter im Rahmen der hausärztlichen Versorgung siehe die Leitlinie des Royal College of Psychiatrists [32]. Zur Behandlung der Dysthymie bei älteren Patienten siehe Abschnitt 5.2.
6.3 Behandlungsresistente Depression
Es gibt keine allgemein akzeptierte Definition der Behandlungsresistenz. Jedoch ist sie wahrscheinlich, wenn der Patient auf mindestens zwei Behandlungszyklen mit unterschiedlichen Medikamentenklassen (gegeben in einer Dosis, die 150 mg eines TZA entspricht, und über einen Zeitraum von vier bis sechs Wochen) nicht gemäß validierten psychometrischen Skalen respondiert. Da eine Behandlungsresistenz den Patienten schwer beeinträchtigt, wird die Überweisung an einen Psychiater/Nervenarzt empfohlen (s. Abschnitt 2.1.8 zu Möglichkeiten der Therapieoptimierung, wie zusätzlicher Psychotherapie oder in schweren Fällen EKT).
6.3.1 Behandlungsresistente Depression bei älteren Patienten
Eine behandlungsresistente Major Depression ist ein weitverbreitetes klinisches Problem bei älteren depressiven Patienten. Sie betrifft bis zu einem Drittel dieser Patientengruppe. Nicht diagnostizierte somatische oder psychiatrische Begleiterkrankungen sowie Fehldiagnosen tragen häufig zu Behandlungsresistenz bei. Atypische depressive Symptome, wie somatische und kognitive Symptome, und komorbide somatische Begleiterkrankungen, die selbst depressive Symptome hervorrufen können, erschweren in dieser Altersgruppe eine adäquate Beurteilung der antidepressiven Wirksamkeit [175, 241]. Für das Management behandlungsresistenter Depression bei älteren Patienten sollte die Diagnose überprüft werden und eine Optimierung der Behandlung und die Anwendung einer alternativen therapeutischen Methode in Erwägung gezogen werden, einschließlich des Wechsels zu einem anderen Wirkstoff, einer Kombinationstherapie und EKT.
Obwohl es im Vergleich zu jüngeren Patienten weniger Daten gibt, welche die Wirksamkeit einer Augmentation mit Lithium belegen, scheint Lithium als Augmentationssubstanz zur Depressionsbehandlung bei älteren Patienten geeignet zu sein (Level C) [171, 198, 351, 388]. Jedoch ist die Anwendung von Lithium bei älteren Patienten aufgrund einer weniger effektiven Clearance und wegen möglicher Wechselwirkungen mit Begleitmedikationen nicht unproblematisch [324]. Regelmäßige klinische Untersuchungen und die Kontrolle des Lithiumplasmaspiegels (Richtwert zwischen 0,4 und 0,8 mmol/l), ermöglicht eine sichere Lithiumbehandlung, auch bei älteren Patienten [171].
6.4 Behandlung der Depression bei Kindern und Jugendlichen
Ein Teil der Patienten erlebt die erste Episode der Major Depression in früher Kindheit, vor der Pubertät oder Adoleszenz [55]. Die früh auftretende Major Depression ähnelt der von Erwachsenen, jedoch ist sie aufgrund hoher Rückfallraten während dieser kritischen Entwicklungsperiode der jungen Patienten eine besonders schwere Form der affektiven Störungen. Obwohl in diesen Fällen eine Überweisung an einen Kinder- und Jugendpsychiater empfohlen wird, soll im Folgenden ein kurzer Überblick über die Behandlungsmöglichkeiten gegeben werden.
Antidepressiva können sich in einigen Fällen als nützlich erweisen und werden insbesondere bei Patienten mit einer schweren Depression und psychotischen Symptomen empfohlen [55]. Fast keine doppelblinde kontrollierte Studie konnte einen signifikanten Unterschied in der Wirksamkeit zwischen TZA und Plazebo zeigen. Daher sollte der therapeutische Nutzen der TZA (besonders Desipramin und Imipramin) bei Kindern und Jugendlichen sorgfältig gegen die potenziell letalen Folgen einer Überdosis, die Möglichkeit eines plötzlichen Herztodes (möglicherweise in Zusammenhang mit kardialen Reizleitungsstörungen; [370]) und die Verfügbarkeit von Medikamenten, deren Anwendung sicherer zu überwachen ist [128], abgewogen werden.
SSRI scheinen bei Kindern und Jugendlichen in ihrer Wirksamkeit Plazebo überlegen zu sein (Level B) (für Fluoxetin s. [106] und für Paroxetin s. [179]). Die anderen neueren Antidepressiva wurden noch nicht systematisch in randomisierten kontrollierten Studien untersucht, jedoch zeigten zwei kleinere offene Studien mit Venlafaxin [213] und Nefazodon [138] vielversprechende erste Ergebnisse (Level D).
EKT sollte nur bei akut suizidalen, psychotischen oder behandlungsresistenten Patienten in Erwägung gezogen werden [344].
Wie oben erwähnt, gibt es eine aktuelle Diskussion darüber, ob die SSRI (insbesondere Paroxetin, diskrepante Ergebnisse gibt es für Citalopram und Sertralin) und die neueren Antidepressiva (z.B. Venlafaxin) das Risiko für suizidales Verhalten (einschließlich Suizidgedanken und -versuchen) bei Kindern erhöhen, was zu offiziellen Stellungnahmen der U.S. amerikanischen Food and Drug Administration (FDA) [354] und der European Medicines Agency (EMEA) [105] geführt hat. Daher sollten sowohl die Patienten als auch deren Eltern/Betreuer über dieses Risiko ausführlich aufgeklärt werden. Wird der Patient erfolgreich mit SSRI behandelt, sollte ein sorgfältiges Monitoring erfolgen. Im Falle einer Partial- oder Nonresponse kann das Medikament schrittweise unter engmaschigen Kontrollen ausgeschlichen werden. Ein abruptes Absetzen der Medikation sollte unbedingt vermieden werden. Aufgrund hoher Rückfallraten bei Kindern und Jugendlichen wird empfohlen, dass die Erhaltungstherapie mindestens sechs Monate andauern sollte. Ebenso wie bei Erwachsenen sollte die Antidepressivatherapie in der gleichen Dosierung fortgeführt werden, die notwendig war, um die Remission in der Akutphase zu erreichen. Am Ende der Erhaltungstherapie sollte die Medikation allmählich über mindestens sechs Wochen ausgeschlichen werden.
6.5 Depressionsbehandlung während Schwangerschaft und Stillzeit
Depressive Störungen während der Schwangerschaft stellen ein großes therapeutisches Problem dar [14]. Im Gegensatz zu Mood-Stabilizern (Lithium, Carbamazepin und Valproinsäure), die eine Teratogenität aufweisen, scheinen Antidepressiva (TZA, SSRI) kein erhöhtes Risiko für eine Organfehlentwicklung zu besitzen [9, 10]. TZA und SSRI zeigen kein erhöhtes Risiko für intrauterinen Fruchttod oder größere Geburtsschäden [376]. Die Entwicklung von Kindern, deren Mütter während der Schwangerschaft TZA oder Fluoxetin einnahmen, unterschied sich nicht von der der Kontrollen [254, 255]. Bei einigen Kindern, deren Mütter kurz vor Geburtstermin mit Antidepressiva behandelt wurden, traten direkte Medikamenteneffekte und vorübergehende Entzugserscheinungen (z.B. Zittern, Tachypnoe) auf [376]. Für die neueren Antidepressiva liegen aktuell nur wenige Daten vor. MAO-Hemmer sind während der Schwangerschaft aufgrund möglicher hypertensiver Krisen kontraindiziert. Die Anwendung von Antidepressiva während der Schwangerschaft ist in vielen klinischen Situationen angebracht und sollte unter sorgfältiger Risikoabwägung der pränatalen Exposition versus eines depressiven Rückfalls der Mutter durchgeführt werden (Risiko-Nutzen-Bewertung in der Entscheidungsfindung). Als Behandlungsalternativen sollten Psychotherapie und EKT in Betracht gezogen werden. Für Patientinnen mit identifizierten Risiken (z.B. ungenügende Gewichtszunahme) wird ein engmaschiges Monitoring und gegebenenfalls eine Intervention empfohlen [376].
Nach der Geburt haben viele Frauen ein besonders hohes Risiko für den Beginn oder das Wiederauftreten affektiver Störungen. Das vorübergehende, sieben bis zehn Tage andauernde depressive Syndrom nach der Geburt, auch als „Postpartum Blues“ bekannt, erfüllt die typischen Kriterien für eine depressive Störung nicht und erfordert daher auch in der Regel keine medikamentöse Intervention [14]. Der Begriff postpartale Depression bezieht sich auf eine depressive Episode, die innerhalb von vier Wochen nach der Geburt auftritt. Studien zeigten eine gleichbleibende Inzidenz von etwa 10% bis 15% der Mütter in den ersten Wochen nach der Geburt [154]. Frauen mit einer Major Depression in ihrer Anamnese haben ein etwa 25- bis 50%iges Risiko für eine depressive Episode nach der Geburt eines Kindes.
Viele Frauen, die eine antidepressive Behandlung benötigen, möchten ihre Kinder stillen. Einige neue Studien haben Antidepressiva identifiziert, die während der Stillzeit sicher angewandt werden können (Level C) [70, 154, 375]. Die am besten untersuchten Substanzen bei stillenden Müttern sind Paroxetin, Sertralin, Fluoxetin, Clomipramin und Nortriptylin [148, 331]. Wird eine psychotrope Medikation verabreicht, sollte das Kind von der Mutter täglich auf Veränderungen des Schlafens, der Nahrungsaufnahme und des Verhaltens hin überwacht werden. Gründe zur Besorgnis sollten dem behandelnden Arzt mitgeteilt werden.
7 Aktualisierung der Leitlinie
Die klinischen Empfehlungen dieser Leitlinie werden 2010 aktualisiert. Dabei wird die Evidenz aus aktuell laufenden klinischen Studien aufgenommen.
Disclosure statement
Die Erstellung dieser WFSBP-Leitlinien wurde von keiner kommerziellen Organisation finanziell unterstützt.
Danksagung
Die Autoren danken der Firma Lilly Deutschland, die für die Kosten der Übersetzung der Originalversion ins Deutsche aufgekommen ist. Unser Dank gilt weiterhin Frau Beate Weikert für Ihre Hilfe bei der Übersetzung.
Literatur
Das Literaturverzeichnis finden Sie auf unserer Website (www.ppt-online.de) beim Inhaltsverzeichnis des aktuellen Hefts.
[1]Anmerkung: Es wird betont, dass eine abgestufte Wirksamkeitsevaluation Limitationen besitzt. Die Stärke einer Empfehlung reflektiert die wissenschaftliche Evidenz, auf welcher sie basiert, und nicht notwendigerweise ihre Bedeutung. Die Ebenen der Empfehlung beziehen sich nur auf die Behandlung, nicht auf andere Aspekte.
[2]Anm.: Die gebräuchlichen Abkürzungen der Antidepressivaklassen unterscheiden sich in der Literatur. Zum Beispiel werden selektive Noradrenalin-Wiederaufnahmehemmer sowohl mit NRI als auch SNRI abgekürzt. Für selektive Serotonin- und Noradrenalin-Wiederaufnahmehemmer sind die Abkürzungen SNRI oder SSNRI geläufig.
*(hier und an allen folgenden Stellen mit dieser Markierung:) Veröffentlicht nach Abschluss der systematischen Literaturrecherche
Psychopharmakotherapie 2008; 15(06)
