Priv.-Doz. Dr. Dieter Angersbach, Wolfratshausen
Desvenlafaxin (O-Desmethylvenlafaxin) ist der Hauptmetabolit von Venlafaxin. Ebenso wie Venlafaxin ist Desvenlafaxin ein Serotonin-Noradrenalin-Wiederaufnahmehemmer und hat nur eine geringe Affinität zu cholinergen, histaminergen oder alpha-adrenergen Rezeptoren.
Von den drei publizierten 8-wöchigen Phase-III-Studien wurden in zweien feste Dosen von Desvenlafaxin gegeben. In der dritten Studie konnte die Dosis verändert werden.
● In einer 3-armigen Studie wurden die Patienten randomisiert einer Behandlung mit Plazebo, 200 mg/d oder 400 mg/d Desvenlafaxin zugeteilt [1].
● In einer 4-armigen Studie wurden die Patienten mit Plazebo oder mit 100 mg/d, 200 mg/d oder 400 mg/d Desvenlafaxin behandelt [2].
● In einer multizentrischen 2-armigen Studie war die Dosis veränderbar [3]. In den ersten 14 Tagen erhielten die Patienten Plazebo oder 100 mg/d Desvenlafaxin. Die Dosis konnte danach auf 200 mg/d gesteigert, jedoch bei Unverträglichkeit später wieder auf 100 mg/d reduziert werden. Die mittlere Dosis variierte nach Woche 2 zwischen 179 und 195,3 mg/d.
In allen Studien wurde Desvenlafaxin in retardierter Formulierung als Einmaldosis verabreicht.
Die Ein- und Ausschlusskriterien waren in allen Studien vergleichbar. Eingeschlossen wurden ambulante Patienten im Alter von 18 bis 75 Jahren mit der Diagnose einer Major Depression nach Kriterien des DSM-IV und einer depressiven Episode ohne psychotische Merkmale, die ≥30 Tage vor dem Screening-Besuch begonnen hatte. Vorausgesetzt wurde ein Gesamtscore auf der Hamilton-Depressionsskala, 17-Item-Version, (HAMD-17) von ≥20 und ein Score ≥4 (mäßig krank) auf der Clinical Global Impression Scale, Teil: Schweregrad der Erkrankung (CGI-S). Ausgeschlossen wurden Patienten mit einer Vorbehandlung mit Desvenlafaxin oder (in den letzten 90 Tagen) mit Venlafaxin, Patienten mit Substanz-/Alkoholabhängigkeit, Angsterkrankungen und klinisch bedeutenden anderen Erkrankungen, Engwinkelglaukom oder/und deutlichen Anomalien im EKG und den Laborwerten
Studienziele
Primäres Studienziel aller drei Studien war der Vergleich der Wirksamkeit und Verträglichkeit von Desvenlafaxin und Plazebo.
Der primäre Wirksamkeitsparameter war die Abnahme des mittleren HAMD-17-Gesamtscores vom Einschluss bis zum Endpunkt (nach Woche 8 bzw. bis zum Abbruch).
Sekundäre Parameter waren unter anderen:
● Abnahme des mittleren Scores auf der Montgomery Åsberg Depression Rating Scale (MADRS)
● Änderung im CGI-I-Score (CGI, Teil: Besserung der Erkrankung) und CGI-S-Score
● Anteil der Responder (≥50% Reduktion des HAMD-17-Gesamtscores)
● Anteil der wiederhergestellten Patienten (HAMD-17-Score von ≤7)
● Änderungen auf der Visual Analog Scale-Pain Intensity (VAS-PI)
Die mittleren HAMD-Scores bei Einschluss waren vergleichbar: 24,8 bis 25,3 [1], 22,9 bis 23,2 [2] bzw. 23,7 [3]. Ebenso vergleichbar war die Stärke der Behandlungsarme: in die insgesamt neun Behandlungsarme wurden jeweils 120 bis 125 Patienten eingeschlossen.
Ergebnisse: Wirksamkeit
Die Flexible-Dosis-Studie [3] verfehlte das Studienziel. Sie konnte mit dem primären Wirksamkeitsparameter keine größere Wirksamkeit im Vergleich zu Plazebo zeigen. Eine deutliche Überlegenheit von Desvenlafaxin zeigte jedoch die analoge Schmerz-Skala (VAS-PI) insgesamt und in mehreren Schmerzzonen, wie Rücken, Arme, Beine und Gelenke.
Erfolgreicher war die Behandlung mit Desvenlafaxin in den beiden Studien mit fester Dosis [1, 2].
In der 3-armigen Studie [1] nahm der HAMD-17-Score sowohl unter 200 mg/d (–12,6) als auch unter 400 mg/d Desvenlafaxin (–12,1) signifikant stärker ab als unter der Plazebo-Behandlung (–9,3; Abb. 1).
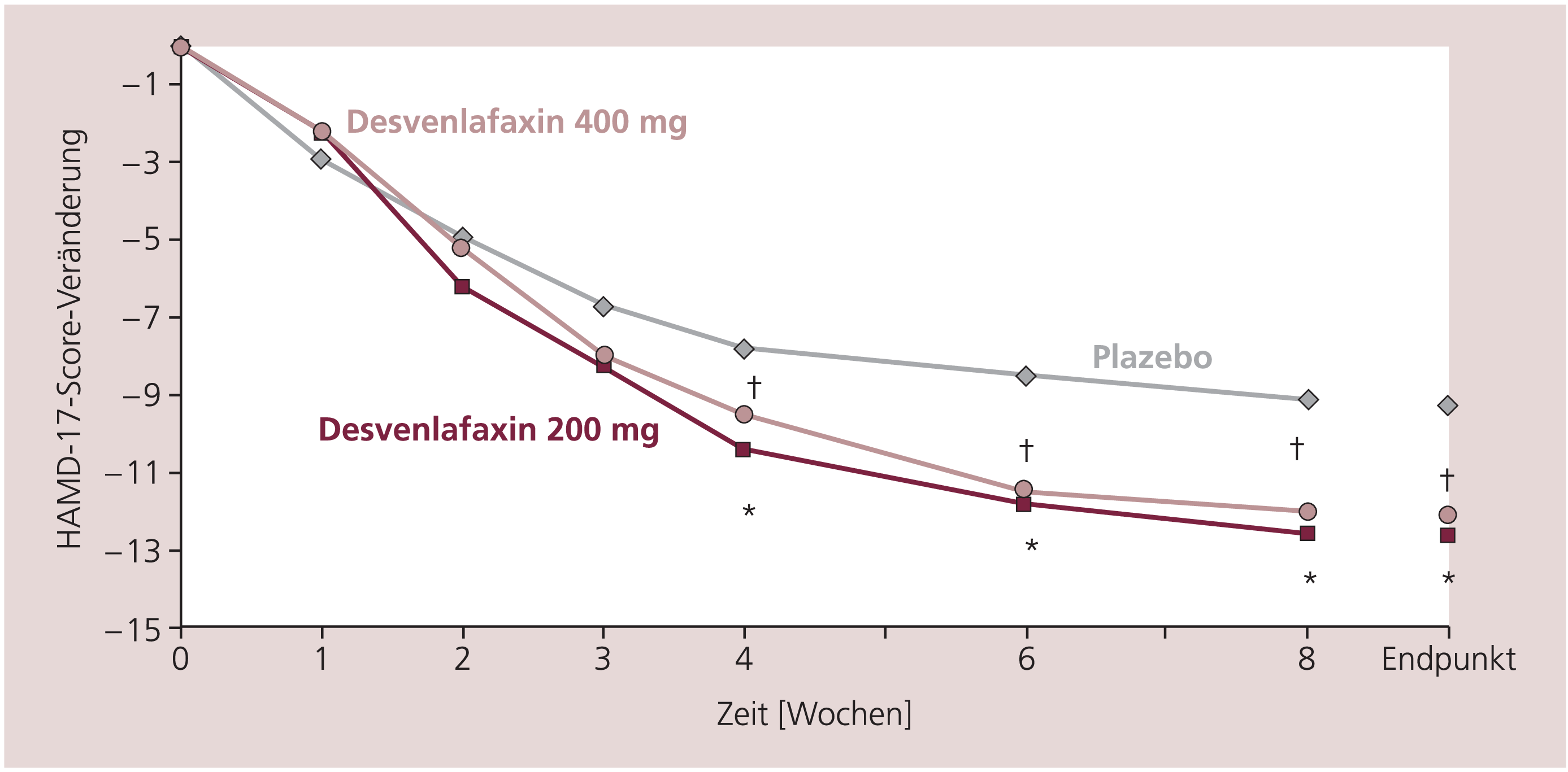
Abb. 1. Abnahme der mittleren HAMD-17-Scores nach Einschluss bis zum Ende der Therapie bzw. Woche 8 unter Plazebo und Desvenlafaxin; * p≤0,05 Desvenlafaxin 200 mg vs. Plazebo, † p≤0,05 Desvenlafaxin 400 mg vs. Plazebo [nach 1]
Beide Desvenlafaxin-Dosen waren ab Woche 4 der Plazebo-Behandlung überlegen.
Auch bei den meisten sekundären Wirkparametern (VAS-PI Schmerzen insgesamt, CGI-I, MADRS, Responserate) waren beide Desvenlafaxin-Dosen signifikant wirksamer als Plazebo.
Die Responseraten lagen bei 60% (200 mg/d), 56% (400 mg/d) und 38% (Plazebo). Die Remissionsraten waren nur unter 200 mg/d signifikant höher (37%) als unter Plazebo (23%).
Die Ergebnisse der 4-armigen Studie [2] waren unterschiedlich. Auf der HAMD-Skala waren nur 100 mg/d (–10,6) und 400 mg/d Desvenlafaxin (–10,74) wirksamer als Plazebo (–7,65).
Unter den sekundären Wirkparametern nahm der CGI-S-Score ebenfalls nur unter 100 und 400 mg/d Desvenlafaxin ab, während die Abnahme des MADRS-Scores unter allen drei Dosen der Prüfsubstanz signifikant größer war als unter Plazebo. Die Schmerzen insgesamt wurden unter der 100-mg-Dosis geringer.
Sicherheit
Unerwünschte Wirkungen traten meist dosisabhängig und insbesondere in der ersten Behandlungswoche auf. Die häufigsten waren Übelkeit (30–50%), Insomnie (17–30%), Schwitzen (7–29%), Mundtrockenheit (17–26%), Somnolenz (6–25%), Schwindel (14–19%), und Anorexie (10–14%). Unter der 400-mg-Dosis traten vermehrt sexuelle Störungen auf.
Von allen drei Studienteams wurde die Verträglichkeit als gut bezeichnet.
Kommentar
Von den Ergebnissen der vorliegenden Studien könnte man zunächst enttäuscht sein: die Verbesserungen im HAMD-Score erscheinen im Vergleich zu Plazebo nicht besonders groß.
Das britische National Institute for Health and Clinical Excellence (NICE) sieht eine Differenz zwischen Plazebo und Prüfsubstanz von wenigstens 3 HAMD-17-Punkten als klinisch relevanten Unterschied, ohne jedoch diese Zahl zu begründen. Andere Autoren meinen, dass eine Differenz von 3 HAMD-Punkten hinsichtlich ihrer klinischen Signifikanz relativ klein ist [4]. Diese Differenz wurde in den positiven Studien nur knapp erreicht. Weiterhin setzte die Wirksamkeit erst in der Woche 4 bis 6, also relativ spät, ein. Zudem war der Ausgang einer der Studien negativ.
Ein Vergleich mit anderen in der Entwicklung befindlichen oder neu zugelassenen Substanzen zeigt jedoch, dass die vorliegenden Ergebnisse aus Plazebo-kontrollierten Studien in dem zu erwartenden Rahmen liegen und dass sich in solchen Studien Antidepressiva in ihrer Wirksamkeit häufig nicht von Plazebo unterscheiden. Einer der Gründe dafür könnte darin liegen, dass in Studien, die einen Plazebo-Arm enthalten, ungern schwerer erkrankte Patienten eingeschlossen werden. Niedrige HAMD-Eingangswerte, wie die in den vorliegenden Studien, sind möglicherweise mit einer geringeren Effektstärke der Behandlung verbunden und eine Trennung vom Plazebo-Effekt ist schwierig. Insbesondere bei weniger schwer depressiven Patienten ist die Plazebo-Wirkung wegen der intensiven Betreuung in solchen Studien ohnehin sehr hoch. Desvenlafaxin dürfte also in seiner Wirksamkeit mit anderen Antidepressiva vergleichbar sein.
Interessant ist diese Substanz nach Ansicht der Studienautoren wegen ihrer pharmakokinetischen Eigenschaften: die Steady-State-Plasmakonzentration ist bereits nach 3 bis 4 Tagen erreicht. Weiterhin wird Desvenlafaxin nicht über CYP450 metabolisiert und hemmt die P450-Enzyme nur minimal. Da außerdem die Plasmaproteinbindung gering ist, wird das Interaktionspotenzial dieser Substanz als gering eingeschätzt.
Desvenlafaxin wurde im Februar 2008 in den USA zur Behandlung von Depressionen zugelassen (Pristiq™).
Quellen
1. Septien-Velez L, et al. A randomized, double-blind, placebo-controlled trial of desvenlafaxine succinate in the treatment of major depressive disorder. Int Clin Psychopharmacol 2007;22:338–47.
2. DeMartinis NA, et al. A double-blind, placebo-controlled study of the efficacy and safety of desvenlafaxine succinate in the treatment of major depressive disorder. J Clin Psychiatry 2007;68:677–88.
3. Liebowitz MR, et al. A randomized, double-blind, placebo-controlled trial of desvenlafaxine succinate in adult outpatients with major depressive disorder. J Clin Psychiatry 2007;68:1663–72.
4. Kirsch I, Moncrieff J. Clinical trials and the response rate illusion. Contemp Clin Trials 2007;28:348–51.
Psychopharmakotherapie 2008; 15(05)
