Jens Westheide, Bonn, Wolfgang Weig, Osnabrück, Jürgen Köhler, Wedel, und Kai-Uwe Kühn, Bonn
Sexuelle Dysfunktion ist eine häufige Nebenwirkung von Neuroleptika [1, 2, 15, 21, 23], wobei die Angaben zur Prävalenz erheblich schwanken [11]. Problematisch bei der Bestimmung der Prävalenz von Pharmaka-induzierten sexuellen Dysfunktionen ist die Tatsache, dass sexuelle Dysfunktionen durch die psychiatrische Erkrankung selbst ausgelöst werden können [8, 13, 17]. Dossenbach und Kollegen [9] zeigten in einer internationalen prospektiven Studie, dass rund die Hälfte aller 7655 befragten schizophrenen Patienten während der Behandlung mit Neuroleptika unter sexuellen Funktionsstörungen litten. Ähnlich berichten Smith und Kollegen [19], dass 45% ihrer mit konventionellen Neuroleptika behandelten Patienten sexuelle Nebenwirkungen hatten. Dabei ändert sich die Bewertung der subjektiven medikamentösen Nebenwirkungen im Laufe der Therapie. Leiden beispielsweise schizophrene Patienten in der Akutphase der Therapie am meisten unter Akathesie und Akinese, fühlen sie sich in der Remissionsphase an erster Stelle durch die sexuellen Dysfunktionen in ihrer Lebensqualität eingeschränkt [18]. Entsprechend zeigten Hellewell et al. [12] in ihrer Untersuchung, dass 74% der Patienten die neuroleptische Medikation aufgrund sexueller Nebenwirkungen absetzten, aber nur 34% wegen der extrapyramidalen Nebenwirkungen.
Bobes und Kollegen [3] verglichen die Häufigkeiten sexueller Dysfunktionen unter typischer und atypischer Neuroleptika-Therapie mit dem Ergebnis, dass unter Quetiapin deutlich weniger Patienten sexuelle Funktionsstörungen aufwiesen (18%) im Vergleich zu mit Risperidon (43%), Olanzapin (35%) oder Haloperidol (38%) behandelten Patienten. Auch Knegtering und Kollegen [16] konnten zeigen, dass die Behandlung mit Quetiapin lediglich bei 16% der Patienten zu sexuellen Dysfunktionen führte, Risperidon hingegen bei der Hälfte der Patienten. Zuletzt fanden Byerly et al. [5] bei 238 ambulanten schizophrenen Patienten, dass Quetiapin deutlich seltener zu sexuellen Dysfunktionen führte als Olanzapin oder Risperidon. Obwohl die Autoren eine große Stichprobe untersuchten, berichten sie nichts über mögliche Geschlechterunterschiede beim Auftreten sexueller Funktionsstörungen. Bobes et al. [3] und Knegtering et al. [16] beschreiben zwar einige Geschlechtseffekte, jedoch nur zwischen den verschiedenen medizierten Gruppen. Bisher existiert keine Studie, in der speziell die sexuellen Nebenwirkungen von Quetiapin bei Männern und Frauen verglichen wurden.
Dementsprechend war das Ziel der vorliegenden Anwendungsbeobachtung, die sexuellen Nebenwirkungen von Quetiapin bei ambulanten männlichen und weiblichen schizophrenen Patienten über einen längeren Zeitraum zu untersuchen. Da nur eine Minderheit Schizophrener in einer stabilen Partnerschaft oder sexuellen Beziehung leben [14, 22], wurde ein Sexualitätsfragebogen eingesetzt, der nicht auf der realen Durchführung von Geschlechtsverkehr beruht, sondern auch autoerotisches Verhalten mit einschließt [6, 7, 21].
Methodik
In der Zeit von August 2004 bis Oktober 2006 nahmen 17 Männer und 23 Frauen mit Schizophrenie in psychiatrischen Praxen in und im Umkreis von Osnabrück an der AWB teil. Die Patienten waren teilweise schon auf Quetiapin eingestellt oder wurden aufgrund von Nebenwirkungen oder mangelnder Wirksamkeit der vorangegangen Medikation auf Quetiapin umgestellt. Der Beobachtungszeitraum betrug 12 Wochen. Einschlusskriterium war neben der Diagnose Schizophrenie ein Alter zwischen 18 und 65 Jahren. Als Ausschlusskriterien wurden Suizidalität, Demenz, schwere somatische Erkrankungen (die mit sexuellen Funktionsstörungen einhergehen) und Substanzabhängigkeit festgelegt.
Neben demographischen Daten wurde der Schweregrad der Erkrankung mit Hilfe der Clinical Global Impression-Severity of Illness Scale (CGI) [10] bestimmt.
Sexuelle Dysfunktionen wurden anhand des „Essener Fragenbogens zur Sexualität“ [6, 7, 21] gemessen, der vom Patienten selbst ausgefüllt wird. Der Fragebogen besteht aus sieben Abschnitten, die neben der Zeit seit dem Auftreten der Symptomatik Libidoverlust, Orgasmusstörung etc. erfassen. Die Ausprägung der sexuellen Nebenwirkungen wird auf einer 7-stufigen Likert-Skala (0 = „gar nicht“ bis 6 = „sehr ausgeprägt“) erfasst. Es gibt eine Version für Männer und eine Version für Frauen.
Statistische Analyse
Alle statistischen Berechnungen wurden mit SPSS 14.0 durchgeführt. Zuerst wurden alle erhobenen intervallskalierten Variablen auf Normalverteilung anhand des Shapiro-Wilks-Tests überprüft, wobei sich zeigte, dass alle untersuchten Variablen diese Voraussetzung erfüllten. Anschließend wurden die intervallskalierten Variablen anhand von t-Tests verglichen. Gruppenvergleiche ordinalskalierter Variablen wurden mithilfe des Mann-Whitney-Tests berechnet, Häufigkeitsdaten mit χ2-Tests analysiert. Veränderungen des Schweregrads der Erkrankung und der sexuellen Funktionsstörungen während der Beobachtungsdauer wurden mit dem Friedman-Test für jede Gruppe getrennt untersucht. Zuletzt wurden potenzielle Gewichtszu- oder -abnahmen getrennt für Männer und Frauen mithilfe von Varianzanalysen mit Messwiederholung mit Gewicht als dreistufigem Faktor getestet.
Ergebnisse
Die Patienten und Patientinnen unterschieden sich nicht hinsichtlich demographischer Merkmale (Tab. 1). Das Durchschnittsalter lag bei knapp 37 bzw. 38 Jahren. Ein Drittel der Patienten war zum ersten Mal erkrankt, die durchschnittliche Episodenanzahl lag bei 5,6 bzw. 4,1 Episoden. Nach 12 Wochen lag die Drop-out-Rate bei den Männern bei 12%, bei den Frauen bei 9%.
Tab. 1. Demographische Charakteristika der Patienten
|
Männer |
Frauen |
Statistik |
Resultat |
|
|
N |
17 |
23 |
||
|
Alter [Jahre] |
36,7 |
37,9 |
t(35)=–0,3 |
p=0,745 |
|
Erstmanifestation |
31% |
29% |
χ2(1)=0,3 |
p=0,860 |
|
Alter bei Ersterkrankung [Jahre] |
27,3 |
27,0 |
t(36)=0,1 |
p=0,922 |
|
Episoden [n] |
5,6 |
4,1 |
t(33)=1,0 |
p=0,320 |
|
Krankenhausaufenthalte [n] |
3,2 |
2,4 |
t(33)=1,0 |
p=0,319 |
|
Vorzeitiger Abbruch |
12% |
9% |
χ2(1)=1,0 |
p=0,749 |
Die psychiatrische Komedikation wurde im Laufe der Anwendungsbeobachtung bei den meisten Patienten zuerst reduziert und dann abgesetzt (Tab. 2). Dabei erhielten Männer wie Frauen gleichermaßen zusätzliche Medikation mit Ausnahme in der ersten Woche, in der männliche Patienten signifikant häufiger mit Antidepressiva behandelt wurden (χ2(1)=4,8; p=0,028).
Tab. 2. Komedikation der Patienten
|
Männer |
Frauen |
Statistik |
Resultat |
|
|
Neuroleptika |
||||
|
Woche 1 |
23% |
22% |
χ2(1)=0,2 |
p=0,893 |
|
Woche 4 |
0% |
17% |
χ2(1)=3,3 |
p=0,070 |
|
Woche 12 |
0% |
4% |
χ2(1)=0,8 |
p=0,384 |
|
Antidepressiva |
||||
|
Woche 1 |
29% |
4% |
χ2(1)=4,8 |
p=0,028* |
|
Woche 4 |
6% |
4% |
χ2(1)=0,5 |
p=0,826 |
|
Woche 12 |
6% |
0% |
χ2(1)=1,4 |
p=0,239 |
|
Anxiolytika |
||||
|
Woche 1 |
12% |
4% |
χ2(1)=0,8 |
p=0,379 |
|
Woche 4 |
6% |
0% |
χ2(1)=1,4 |
p=0,239 |
|
Woche 12 |
6% |
0% |
χ2(1)=1,4 |
p=0,239 |
|
Phasenprophylaktika |
||||
|
Woche 1 |
6% |
0% |
χ2(1)=1,4 |
p=0,239 |
|
Woche 4 |
0% |
0% |
– |
– |
|
Woche 12 |
0% |
0% |
– |
– |
Zu Beginn der Behandlung mit Quetiapin zeigten sich keine Gruppenunterschiede hinsichtlich des Schweregrads der Erkrankung (Tab. 3). Nach 12 Wochen hatten die Patientinnen jedoch einen signifikant niedrigeren CGI-Wert als die Männer (U=85,5; p=0,013), was darauf hindeutet, dass sie etwas besser auf die Therapie angesprochen hatten. In beiden Gruppen nahm der Schweregrad der Erkrankung innerhalb der drei Monate signifikant ab (χ2Männer(2)=9,9; p=0,007; χ2Frauen(2)=29,6; p<0,001). Auch die sexuellen Funktionsstörungen verbesserten sich in beiden Gruppen deutlich (Tab. 4): Der Libidoverlust nahm ab (χ2Männer(2)=11,7; p=0,003; χ2Frauen(2)=19,9; p<0,001), ebenso wie die Orgasmusstörung (χ2Männer(2)=7,5; p=0,023; χ2Frauen(2) =27,0; p<0,001) und die Befriedigungsstörung (χ2Männer(2)=6,4; p=0,040; χ2Frauen(2)=30,4; p<0,001). Lediglich die Abnahme der Erregungsstörung war bei den Männern nicht signifikant (χ2Männer(2)=5,1; p=0,078) im Gegensatz zu den Frauen (χ2Frauen(2)=18,7; p<0,001), was sich aber dadurch erklärt, dass die Patientinnen grundsätzlich in der ersten Woche quantitativ etwas höhere Ausprägungen bei sexuellen Dysfunktionen aufwiesen. Da zwischen den beiden Gruppen keine signifikanten Unterschiede bestanden (Tab. 4), ist von einer vergleichbar positiven Beeinflussung sexueller Dysfunktionen bei Männern und bei Frauen in der Behandlung mit Quetiapin auszugehen. Grundsätzlich ist die Ausprägung sexueller Beeinträchtigungen in beiden Gruppen nach 12 Wochen gering. In Abbildung 1 ist die Abnahme der sexuellen Dysfunktionen bei den Patienten graphisch dargestellt.
Tab. 3. Schweregrad der Erkrankung (CGI) der Patienten an den 3 Messzeitpunkten
|
Männer |
Frauen |
Teststatistik |
Ergebnis |
|
|
Woche 1 |
4,9 (1,1) |
4,8 (1,1) |
U=193,5 |
p=0,957 |
|
Woche 4 |
4,2 (1,3) |
4,0 (1,2) |
U=160,5 |
p=0,723 |
|
Woche 12 |
4,1 (1,4) |
3,1 (0,9) |
U=85,5 |
p=0,013* |
Tab. 4. Sexuelle Dysfunktion der Patienten gemäß Essener Fragebogen (Likert-Skala) an den 3 Messzeitpunkten (Mittelwerte und Standardabweichung)
|
Männer |
Frauen |
Teststatistik |
Ergebnis |
|
|
Libidoverlust |
||||
|
Woche 1 |
3,4 (2,7) |
3,8 (2,1) |
U=158,0 |
p=0,843 |
|
Woche 4 |
1,8 (2,2) |
2,7 (2,5) |
U=120,5 |
p=0,344 |
|
Woche 12 |
1,4 (1,9) |
1,3 (1,9) |
U=153,5 |
p=0,987 |
|
Erregungsstörung |
||||
|
Woche 1 |
3,3 (2,3) |
3,9 (2,2) |
U=149,0 |
p=0,497 |
|
Woche 4 |
2,4 (2,2) |
3,1 (2,3) |
U=117,0 |
p=0,389 |
|
Woche 12 |
1,7 (2,0) |
1,7 (1,8) |
U=160,5 |
p=0,891 |
|
Orgasmusstörung |
||||
|
Woche 1 |
3,4 (2,6) |
4,1 (2,2) |
U=153,0 |
p=0,575 |
|
Woche 4 |
2,6 (2,3) |
3,1 (2,5) |
U=136,5 |
p=0,448 |
|
Woche 12 |
2,0 (2,0) |
1,8 (1,8) |
U=138,5 |
p=0,778 |
|
Befriedigungsstörung |
||||
|
Woche 1 |
3,3 (2,7) |
4,5 (2,1) |
U=137,0 |
p=0,300 |
|
Woche 4 |
2,3 (2,4) |
3,5 (2,3) |
U=112,0 |
p=0,180 |
|
Woche 12 |
2,1 (1,9) |
2,1 (1,7) |
U=141,0 |
p=0,960 |
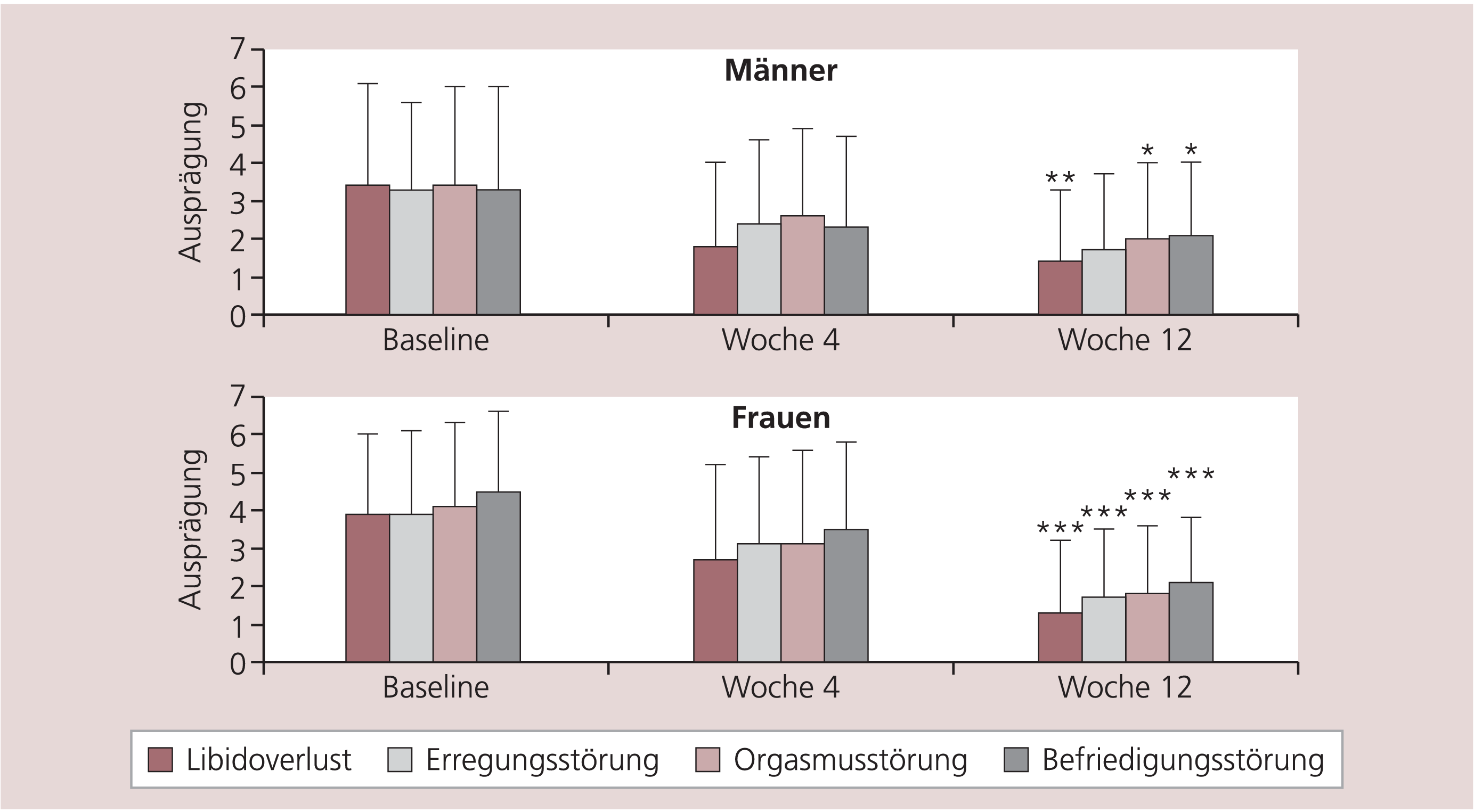
Abb. 1. Sexuelle Dysfunktion bei männlichen und weiblichen Patienten;
* p<0,05, ** p<0,01, *** p<0,001 vs. Baseline
Schwere unerwünschte Nebenwirkungen traten nicht auf. Bei den männlichen Patienten war eine Tendenz (p<0,1) zur Gewichtszunahme (ca. 3 kg) zu beobachten (F(1,10)=5,2; p=0,078).
Diskussion
Die vorliegende Anwendungsbeobachtung zeigt, dass in der neuroleptischen Therapie mit Quetiapin bei männlichen und weiblichen ambulanten schizophrenen Patienten nur geringe sexuelle Funktionsstörungen auftreten. Dabei waren keine geschlechtsspezifischen Unterschiede messbar. Innerhalb der dreimonatigen Beobachtungsphase nahmen die sexuellen Funktionsstörungen bei allen Patienten kontinuierlich ab. Das Ergebnis entspricht der großen Mehrheit klinischer Studien, die ebenfalls nur sehr schwache oder leichte sexuelle Funktionsstörungen bei schizophrenen Patienten in der Behandlung mit Quetiapin feststellen konnten [3–5, 16]. Zusätzlich ist die geringe Drop-out-Rate ein Hinweis darauf, dass die Therapie mit Quetiapin von (ambulanten) schizophrenen Patienten gut akzeptiert wird und nur sehr wenige Patienten die Behandlung aufgrund von Nebenwirkungen oder mangelnder Wirksamkeit abbrechen. Der Schweregrad der Erkrankung nahm in beiden Gruppen signifikant während der 12 Wochen ab, wobei die weiblichen Patienten am Ende einen geringeren CGI-Wert aufwiesen als die Männer. Da es sich um eine nichtrandomisierte, unverblindete AWB handelte, ist der Hinweis auf eine erhöhte Wirksamkeit von Quetiapin bei den schizophrenen Frauen nicht generalisierbar und wurde im Übrigen bisher auch nicht berichtet. Ausdrücklich zu warnen ist vor monokausalen Erklärungsversuchen:
Zwar ist es richtig, dass der Prolactinspiegel unter Quetiapin-Therapie im Unterschied zu anderen Präparaten nur geringfügig steigt, hieraus aber zu schließen, dies sei der Grund für die vergleichsweise geringe Häufigkeit von sexueller Dysfunktion, greift viel zu kurz [20]. Die Patienten dieser Untersuchung hatten insgesamt am Ende der Beobachtungsperiode ein außerordentlich hohes Funktionsniveau, erfreuten sich aus Sicht der behandelnden Psychiater einer weitgehend wiederhergestellten psychischen Gesundheit und hatten keine wesentlichen somatischen Komplikationen. Die Patienten waren schon zu Beginn der Untersuchung einwilligungsfähig und verbesserten sich im Verlauf auch kognitiv. Der ansonsten bei Schizophrenen häufig vorkommende Substanzmissbrauch war in dieser Untersuchung ein Ausschlusskriterium. Insofern ist diese Untersuchung im Einklang mit anderen Studien, die zeigen, dass Veränderungen des Prolactins nur maximal 25% der Varianz von sexuellen Dysfunktionen unter antipsychotischer Therapie erklären, jedoch Schweregrad der Erkrankung, Affektivität, körperliche Begleiterkrankungen, Antriebsmangel/Sedation und Substanzmissbrauch 75% der Varianz erklären [16, 21].
Literatur
1. Aizenberg D, Zemishlany Z, Dorfman-Etrog P, Weizman A. Sexual dysfunction in male schizophrenic patients. J Clin Psychiatry 1995; 56:137–41.
2. Baldwin DS, Mayers A. Sexual side-effects of antidepressant and antipsychotic drugs. Adv Psychiatr Treat 2003;9:202–10.
3. Bobes J, Garc A, Portilla MP, Rejas J, et al. Frequency of sexual dysfunction and other reproductive side-effects in patients with schizophrenia treated with risperidone, olanzapine, quetiapine, or haloperidol: the results of the EIRE study. J Sex Marital Ther 2003;29: 125–47.
4. Byerly MJ, Lescouflair E, Weber MT, Bugno RM, et al. An open-label trial of quetiapine for antipsychotic-induced sexual dysfunction. J Sex Marital Ther 2004;30:325–32.
5. Byerly MJ, Nakonezny PA, Bettcher BM, Carmody T, et al. Sexual dysfunction associated with second-generation antipsychotics in outpatients with schizophrenia or schizoaffective disorder: an empirical evaluation of olanzapine, risperidone, and quetiapine. Schizophr Res 2006;86:244–50.
6. Cohen S, Huber TJ. Stichtagserhebung zu Störungen der Sexualität bei stationär behandelten, psychisch kranken Menschen. Nervenarzt 2006;77:S326.
7. Cohen S, Kuhn KU, Bender S, Erfurth A, et al. Sexual impairment in psychiatric inpatients: focus on depression. Pharmacopsychiatry 2007;40:58–63.
8. Cutler AJ. Sexual dysfunction and antipsychotic treatment. Psychoneuroendocrinology 2003;28(Suppl 1):69–82.
9. Dossenbach M, Hodge A, Anders M, Molnar B, et al. Prevalence of sexual dysfunction in patients with schizophrenia: international variation and underestimation. Int J Neuropsychopharmacol 2005;8:195–201.
10. Guy W. 028 CGI. Clinical global impressions. In: ECDEU Assessment Manual for Psychopharmacology. Revised edition. Rockville, MD: National Institute of Mental Health (NIMH), 1976:218–22.
11. Hartmann U, Rüffer-Hesse C. Sexualität und Pharmakotherapie. Arzneimittelinduzierte sexuelle Funktionsstörungen und medikamentöse Optionen zur Behandlung sexueller Dysfunktionen. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz 2007;50:19–32.
12. Hellewell JS. Treatment-resistant schizophrenia: reviewing the options and identifying the way forward. J Clin Psychiatry 1999;60(Suppl 23):14–9.
13. Hummer M, Huber J. Hyperprolactinaemia and antipsychotic therapy in schizophrenia. Curr Med Res Opin 2004;20:189–97.
14. Kelly DL, Conley RR. A randomized double-blind 12-week study of quetiapine, risperidone or fluphenazine on sexual functioning in people with schizophrenia. Psychoneuroendocrinology 2006;31:340–6.
15. Knegtering H, Boks M, Blijd C, Castelein S, et al. A randomized open-label comparison of the impact of olanzapine versus risperidone on sexual functioning. J Sex Marital Ther 2006;32:315–26.
16. Knegtering R, Castelein S, Bous H, Van Der Linde J, et al. A randomized open-label study of the impact of quetiapine versus risperidone on sexual functioning. J Clin Psychopharmacol 2004;24:56–61.
17. Kockott G, Pfeiffer W. Sexual disorders in non-acute psychiatric outpatients. Compr Psychiatry 1996;37:56–61.
18. Naber D. Atypische Neuroleptika in der Behandlung schizophrener Patienten. 2. Aufl. Bremen: Uni-Med, 2000.
19. Smith S, O’Keane V, Murray R. Sexual dysfunction in patients taking conventional antipsychotic medication. Br J Psychiatry 2002;181:49–55.
20. Tenback DE, van Harten PN, Slooff CJ, van Os J. Tardive dyskinesia in schizophrenia is associated with prolactin-related sexual disturbances. Neuropsychopharmacology 2006;31:1832–7.
21. Westheide J, Cohen S, Bender S, Cooper-Mahkorn D, et al. Sexual dysfunction in psychiatric inpatients. The role of antipsychotic medication. Pharmacopsychiatry 2007; 40:140–5.
22. Westheide J, Helmstaedter C, Cooper-Mahkorn D, Strater B, et al. Sexuality in male psychiatric inpatients. A descriptive comparison of psychiatric patients, patients with epilepsy and healthy volunteers. Pharmacopsychiatry 2007;40:183–90.
23. Wirshing DA, Pierre JM, Marder SR, Saunders CS, et al. Sexual side effects of novel antipsychotic medications. Schizophr Res 2002;56:25–30.
Priv.-Doz. Dr. med. Kai-Uwe Kühn, Dr. phil. Jens Westheide, Klinik und Poliklinik für Psychiatrie und Psychotherapie der Universität Bonn, Sigmund-Freud-Str. 25, 53105 Bonn, E-Mail: kai-uwe.k%C3%BChn@ukb.uni-bonn.de
Prof. Dr. Wolfgang Weig, Niedersächsisches Landeskrankenhaus Osnabrück Dr. Jürgen Köhler, AstraZeneca GmbH, Tinsdaler Weg 183, 22876 Wedel
Sexual functioning in the treatment with quetiapine
Sexual dysfunction is a frequent side-effect of antipsychotic medication. Many patients become non-compliant, once ascribing their sexual impairment to their psychotropic medication. Quetiapine has been associated with only minor sexual side-effects compared with other atypical neuroleptics. It has not been examined yet whether quetiapine is equally advantageous for male and female schizophrenic patients with regard to sexual impairment.
In a non-randomized open label observational study 17 male and 23 female schizophrenic patients treated with quetiapine were examined for 12 weeks. Apart from demographic data severity of illness was assessed by means of the Clinical Global Impression-Severity of Illness Scale (CGI). The patients completed a self-rating questionnaire focussing on sexual dysfunction (“Essener Fragebogen zur Sexualität”).
Severity of illness significantly improved after 12 weeks treatment of quetiapine. Furthermore, sexual dysfunction decreased in males and females. There was no effect of gender.
In accordance with other authors the present study demonstrates that quetiapine is associated with minor sexual impairment only. Male and female patients equally benefit from this advantageous side-effect profile.
Keywords: Sexual dysfunction, neuroleptics, quetiapine, gender
Psychopharmakotherapie 2008; 15(04)
