Randi D. von Wrede, Bonn
Epilepsien als chronische Erkrankungen bedürfen einer individuellen und langfristig ausgelegten Pharmakotherapie. Neben der Wirksamkeit sind klar definierte Nebenwirkungsprofile und Langzeiterfahrungen notwendig, um für den einzelnen Patienten ein individuell zugeschnittenes Therapieregime zu entwickeln.
Zur Zusatzbehandlung erwachsener Patienten mit fokalen und sekundär generalisierten Anfällen steht in Europa seit März 2005 Zonisamid als neues Antikonvulsivum zur Verfügung. Der Wirkstoff, der 1974 in Japan synthetisiert wurde, ist bereits seit 1989 in Japan und seit 2000 in den USA zur Epilepsiebehandlung zugelassen.
Grundlagen
Zonisamid (Abb. 1) ist ein Benzisoxazol mit einer Sulfonamid-Gruppe und unterscheidet sich damit chemisch von den anderen zugelassenen Antikonvulsiva. In komplexen Untersuchungen konnten verschiedene Wirkungsmechanismen der Substanz nachgewiesen werden, hierzu zählen neben der Blockade spannungsabhängiger Ionenkanäle (Natrium, Calcium) auch die Abschwächung der Glutamatwirkung und Verstärkung der GABA-Wirkung. Zusätzlich beschleunigt Zonisamid den Acetylcholin-Abbau, wirkt als Radikalfänger für Hydroxyl- und Stickoxyd-Radikale, hebt den striatalen und hippocampalen Dopamin- und Serotonin-Level und hemmt die Carboanhydrase. Der letztendlich für die antikonvulsive Potenz verantwortliche Mechanismus ist noch unklar. Die antikonvulsive Potenz konnte sowohl in In-vitro-Versuchen als auch in verschiedenen tierexperimentellen Epilepsiemodellen gezeigt werden [Übersicht bei 3].
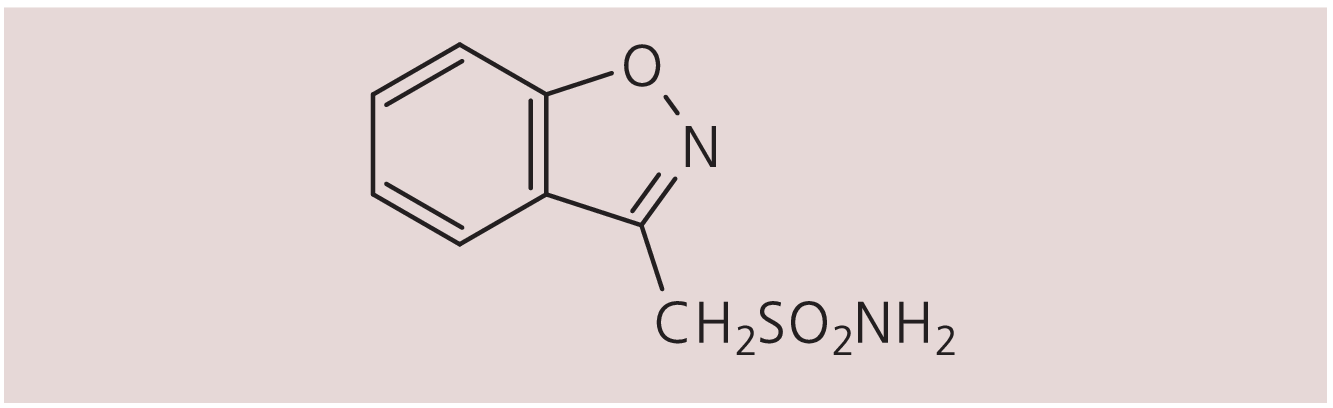
Abb. 1. Zonisamid
Wie bei der Behandlung mit anderen Antikonvulsiva ist die Kenntnis der pharmakokinetischen Daten Voraussetzung, um einen sinnvollen sicheren Einsatz der Substanz zu gewährleisten (Tab. 1).
Tab. 1. Pharmakokinetik von Zonisamid
|
Tmax |
2–5 h |
|
|
Bioverfügbarkeit |
Ca. 100% |
|
|
Eiweißbindung |
40–50% |
|
|
Elimination |
Renal (97%) |
|
|
Metaboliten |
Im Plasma nicht nachweisbar, keine antikonvulsive Potenz |
|
|
Therapeutischer Bereich |
10–40 µg/ml |
|
|
Halbwertszeit |
60 h |
|
|
Mit Phenytoin |
27 h |
|
|
Mit Carbamazepin oder Phenobarbital |
38 h |
|
|
Mit Valproinsäure |
46 h |
|
Vorteilhaft ist, dass Zonisamid keinen Effekt auf die Cytochrom-P450-Isoenzyme, und damit auch keine Autoinduktion, zeigt und weder mit oralen Kontrazeptiva noch mit anderen Antikonvulsiva interagiert. Bei Komedikation mit CYP3A4-Induktoren und -Inhibitoren kann jedoch der Zonisamid-Metabolismus verändert werden.
Studienlage
Nach umfangreichen Phase-II- und -III-Studien sowie drei Plazebo-kontrollierten Studien [8, 17, 18] erfolgte die Zulassung von Zonisamid in Japan (Exegran®, 1989) und den USA (Zonegran®, 2000), da bei guter Wirksamkeit keine Sicherheitsbedenken bestanden. Die Zulassung von Zonisamid in Europa beruht zusätzlich auf einer weiteren Plazebo-kontrollierten doppelblinden Studie (Studie 302), in der insgesamt 351 Patienten mit refraktären fokalen Anfällen eingeschlossen wurden [4]. Hier erfolgte eine Beurteilung unter den Parametern Anfallsreduktion, Responderrate (Anteil der Patienten mit einer Reduktion der Anfallsfrequenz um >50%), sowie die Definition der wirksamen Dosis (eingesetzt wurden Tagesdosen von 100, 300 und 500 mg).
Wirksamkeit
In der letztendlich ausschlaggebenden Multicenterstudie 302 konnte eine gute Wirksamkeit für Zonisamid belegt werden. Die Gabe von 500 mg/d Zonisamid führte zu Ansprechraten von über 50% für alle untersuchten Gruppen (komplex partielle Anfälle, einfach und komplex partielle Anfälle, alle partiellen Anfälle inklusive sekundär generalisierte Anfälle) und erreichte somit statistische Signifikanz im Vergleich zur Plazebo-Gabe. Die Reduktion der Anfallsfrequenz war in diesem Studienarm (500 mg/d) ebenfalls für alle untersuchten Gruppen statistisch signifikant. Für die 300-mg-Gruppe konnte eine statistisch signifikante Anfallsreduktion sowohl für die Untergruppe der fokalen Anfälle als auch für alle Anfälle inklusive der sekundär generalisierten gezeigt werden; für komplex partielle Anfälle und für die Ansprechraten ließ sich zwar keine statistische Signifikanz erreichen, jedoch deutliche Trends. Anfallsfreiheit konnte bei 6 von 101 (6%) mit 500 mg/d Zonisamid behandelten Patienten erreicht werden [4].
In einer Subgruppenanalyse von Patienten, die lediglich ein weiteres Antikonvulsivum einnahmen und damit einer eher weniger refraktären Patientengruppe entsprechen sollten, zeigten sich dosisabhängige Ansprechraten bis über 60%, wobei bereits 100 mg als überlegen galten. Die Autoren kamen zu dem Schluss, dass ein frühzeitiger Einsatz aufgrund der Wirksamkeit und guten Verträglichkeit zu wünschen ist.
Das Odds-Ratio dieser Studie zeigt, dass Patienten in der 500-mg-Gruppe eine viermal so große Wahrscheinlichkeit haben anzusprechen wie Patienten der Plazebo-Gruppe. Die Ergebnisse der Studie 302 reproduzieren und vertiefen im Wesentlichen die Vorläuferstudien 922 (USA), 912 (USA) und 912 (EU).
Die US-Studie aus der Mitte der 90er Jahre erbrachte statistische Signifikanz hinsichtlich der Reduktion der Anfallsfrequenz als auch der Responderrate für die Tagesdosis von 400 mg Zonisamid versus Plazebo; sowohl 100 mg als auch 200 mg/d Zonisamid erbrachten eine Verbesserung der Anfallskontrolle, wobei die Responderraten von 25% jedoch keine statistische Signifikanz erreichten [8].
Umfangreiche Daten aus randomisierten kontrollierten und offenen Studien in Japan liegen vor, die nicht nur die Wirksamkeit bei fokalen Anfällen, sondern auch bei anderen Anfallsarten (generalisiert tonisch-klonische Anfälle, atonische Anfälle, myoklonische Anfälle, Absencen) sowie anderen Epilepsie-Syndromen (idiopathisch generalisierte Epilepsie, Lennox-Gastaut-Syndrom, West-Syndrom, andere symptomatische generalisierte Epilepsien, progressive Myoklonusepilepsie ) zeigen [19, 23].
Postmarketing-Erfahrungen in Japan belegen die Effektivität von Zonisamid als Monotherapie in neu diagnostizierten Epilepsien, hier konnten Responderraten von über 80% für fokale Anfälle gezeigt werden [23]. Tosches und Mitarbeiter konnten in ihrer Untersuchung mit einer Zonisamid-Monotherapie eine Anfallsfreiheit bei 55,6% der Patienten erreichen bei zusätzlichen 20% Respondern [20]. Ebenso konnte Wirksamkeit in der Behandlung von kindlichen Epilepsien belegt werden, wobei insbesondere Epilepsie-Patienten ohne Intelligenzminderung deutlich von Zonisamid profitierten (Responderrate 78% versus 43%) [11].
Langzeitwirksamkeit
Da Epilepsien als chronische Erkrankung einer langfristigen, häufig lebenslangen antikonvulsiven Medikation bedürfen, sind Langzeituntersuchungen zu Wirksamkeit und Sicherheit der eingesetzten Antikonvulsiva von grundlegender Bedeutung, um den Platz des jeweiligen Wirkstoffs in der Gruppe der Antikonvulsiva festzulegen. Umfangreiche Prä-und Postmarketing-Daten im Rahmen einer 17-jährigen Anwendung sowie die daraus resultierenden Erfahrungen aus über zwei Millionen Patientenjahren liefern eine umfangreiche Datenlage zu Zonisamid.
Durch die Möglichkeit offener Verlängerungsstudien konnte die Wirksamkeit von Zonisamid über größere Zeitspannen verfolgt werden. In einer Metaanalyse an 1207 Patienten, die bis zu neun Jahre nachbeobachtet wurden, konnte gezeigt werden, dass es zu keiner Tachyphylaxie kam und sich keine Hinweise auf eine pharmakologische Toleranzentwicklung abbildeten [14]; Zwischenanalysen legen sogar eine progressive Abnahme der Anfallshäufigkeit nahe [22].
Nebenwirkungen
Insgesamt wurde Zonisamid bei über 1200 Patienten in klinischen Studien untersucht.
Das Studiendesign der europäischen Zulassungsstudie 302 ermöglichte die Beurteilung von unerwünschten Wirkungen (UAW) sowohl in der Titrationsphase (6 Wochen) als auch in der Steady-State-Phase (18 Wochen). Der Großteil der Nebenwirkungen war leicht oder mäßig; Nebenwirkungen mit einer Inzidenz von mehr als 10% waren Schläfrigkeit, Schwindel, Kopfschmerz und Übelkeit in der Titrationsphase; Kopfschmerz und Pharyngitis in der Steady-State-Phase, wobei Kopfschmerzen in der Plazebo-Gruppe häufiger als in den Zonisamid-Gruppen auftraten (12,5% versus 10,7%/100 mg; 10,1%/300 mg, 4,2%/500 mg). Ein Gewichtsverlust trat bei 6,8% der Patienten in der 500-mg-Zonisamid-Gruppe auf. Die Ergebnisse sprechen dafür, dass es sich bei einem Teil der Nebenwirkungen um Titrationsphänomene handelt und sich eine Toleranz gegenüber den unerwünschten Wirkungen entwickeln kann.
Die Studienabbrüche waren in der 300-mg- und 500-mg-Zonisamid-Gruppe größer als in der Plazebo-Gruppe (s. Tab. 2). Zusammengefasst wurden die Nebenwirkungen jedoch zum Großteil als transient eingestuft [4].
Tab. 2. Häufigkeit von unerwünschten Arzneimittelwirkungen (UAW) in Studie 302 [nach 4]
|
Plazebo |
Zonisamid |
Zonisamid |
Zonisamid |
|
|
UAW |
82 (68,3%) |
38 (67,9%) |
39 (70,9%) |
96 (81,4%) |
|
Titrationsphase |
60 (50%) |
32 (57,1%) |
34 (61,8%) |
73 (61,9%) |
|
Steady-State-Phase |
58 (48,3%) |
29 (51,8%) |
23 (41,8%) |
59 (50%) |
|
Studienabbruch bei UAW |
12 (10%) |
1 (1,8%) |
10 (18,2%) |
32 (27,1%) |
|
Schwerwiegende UAW |
10 (8,3%) |
0 |
5 (9,1%) |
9 (7,6%) |
|
Todesfälle |
2 (1,7%) |
0 |
0 |
0 |
Aus den vier Plazebo-kontrollierten Studien aus Europa und den USA liegen gepoolte Sicherheitsdaten von 848 Patienten vor. Unerwünschte behandlungsbezogene Nebenwirkungen fanden sich bei 61% der Zonisamid-Patienten (versus 48,6% der Plazebo-Gruppe), wobei die meisten nur leicht bis mäßiggradig eingestuft wurden. Im Vordergrund stehen ZNS-assoziierte Nebenwirkungen wie Schläfrigkeit (15,3% versus 7,7%), Schwindel (13,3% versus 7,7%) und Appetitverlust (9,6% versus 3,7%). Zu einem Studienabbruch führten diese Nebenwirkungen bei 19,3% der mit Zonisamid behandelten Patienten (versus 8,6% der Plazebo-Gruppe). Schwerwiegende Ereignisse waren bei Zonisamid und Plazebo gleich häufig (4,8% versus 4,6%) [5].
In einer groß angelegten Postmarketing-Untersuchung aus Japan konnte an insgesamt 1512 Patienten eine Inzidenz von 31,6% für Nebenwirkungen bestimmt werden. Hier konnte belegt werden, dass die Inzidenz bei Kindern deutlich niedriger ist als bei Erwachsenen (26,2% versus 40,1%) und dass unerwünschte Wirkungen bei Patienten, die eine Monotherapie erhielten, statistisch signifikant seltener auftraten als bei polytherapeutisch behandelten Patienten (21% versus 35,8%) [16].
Langzeitsicherheit
Umfangreiche Postmarketing-Erfahrungen aus Japan (Exegran®-Zulassung 1989) und den USA (Zonegran®-Zulassung 2000) bei über zwei Millionen Patientenjahren liegen vor, so dass dem Behandler ein gut dokumentiertes Profil der Nebenwirkungen zur Verfügung steht.
Die gepoolten Daten aus 12 verschiedenen Studien, bei denen insgesamt 1207 Patienten bis zu fünf Jahre nachuntersucht wurden, erlauben ein Follow-up-Profil von bis zu neun Jahren anzulegen. Es zeigte sich eine Häufigkeit von 80,8% behandlungsbezogener Nebenwirkungen, die meist leicht bis mäßig ausgeprägt waren. Lediglich 19% waren schwerwiegend, ein Studienabbruch aufgrund von Nebenwirkungen erfolgte bei 21,8%. Mit einer Häufigkeit von größer als 10% traten vorwiegend ZNS-assoziierte Nebenwirkungen auf, unter anderem Schläfrigkeit/Müdigkeit, Schwindel, Anorexie, Übelkeit, Kopfschmerzen, Verwirrtheit, mentale Verlangsamung, Agitiertheit/Reizbarkeit [14].
In der bereits oben skizzierten Zwischenanalyse der europäischen langfristigen Verlängerungsstudie 353 wurde die Sicherheit von Zonisamid im Wesentlichen bestätigt. Unerwünschte Nebenwirkungen traten bei 66% der Zonisamid-Patienten auf und lediglich 11,5% brachen die Studie aufgrund von Nebenwirkungen ab [22].
Hautallergien
Unerwünschte Wirkungen im Sinne von Hautallergien sind eine bekannte Nebenwirkung von Sulfonamiden. Bei Zonisamid handelt es sich um ein Benzisoxazol mit einer Sulfonamidgruppe ohne aromatischen Substituenten (sog. Nicht-Arylamin-Sulfonamid-Seitenkette) und daher einer niedrigeren Allergierate.
In den gepoolten Sicherheitsdaten von 1207 Patienten wurden drei Fälle mit Hautausschlag berichtet. Aus den Postmarketing-Informationen aus den USA und Japan liegen Berichte über 47 Fälle pro 1 Mio. Patientenjahre vor [14]. In einer umfangreichen Vergleichsstudie zum Auftreten von Hautausschlag unter verschiedenen Antikonvulsiva traten solche bei Zonisamid in etwa 4,6% der Fälle auf, was zwar häufiger als der Durchschnitt war (2,8%), jedoch keine statistische Signifikanz erlangte [1].
Gewichtsverlust
Ergebnisse der Initialstudien verweisen auf eine Appetitabnahme und Gewichtsverlust unter Zonisamid. Eine Anorexie wurde in der gepoolten Sicherheitsanalyse aus allen vier europäischen und US-amerikanischen Studien mit insgesamt 848 Patienten bei 9,6% der Patienten beobachtet (versus 3,7% in der Plazebo-Gruppe), in der laufenden Verlängerungsstudie 353 zeigte sich bei 7,8% der Patienten ein Gewichtsverlust [5, 14]. Hierbei scheint der mittlere Gewichtsverlust <1,7 kg zu sein und nicht progressiv zu verlaufen [14, 21]. Dieser Gewichtsverlust wird von einem Teil der Patienten als positiv empfunden, insbesondere von solchen, die unter anderen Medikamenten eine deutliche Gewichtszunahme erfahren haben.
Nierensteine
Das Auftreten von Nierensteinen wurde während der Entwicklung von Zonisamid verzeichnet, es kam jedoch in keiner Plazebo-kontrollierten Studie zu Nierensteinen. Aus gepoolten Sicherheitsdaten konnte die Rate für das Auftreten von Nierensteinen mit 18 pro 1000 Patientenjahre angenommen werden, das relative Risiko wird mit 5- bis 9fach höher als für die Normalbevölkerung bezeichnet. Eine eindeutige Korrelation zur Zonisamid-Dosis oder Therapielänge konnte nicht belegt werden. Da die beobachteten Nierensteine meist mit anderen Nierenereignissen einhergehen, sind prädisponierende Risikofaktoren zu vermuten und vor der Eindosierung von Zonisamid zu erheben.
Obwohl die Ursache für das vermehrte Auftreten von Nierensteinen nicht geklärt ist, kann ein Zusammenhang mit der leichten Carboanhydrase-Hemmung vermutet werden [14].
Teratogenität
Daten zur Teratogenität liegen nur unzureichend vor. In Tierversuchen wurde eine Reproduktionstoxizität beobachtet. In einer japanischen prospektiven Untersuchung konnten 26 Schwangerschaften unter Zonisamid (4 Monotherapie, 22 Polytherapie) erfasst werden, hierbei zeigten sich zwei Missbildungen (Anenzephalie, Vorhofseptumdefekt) in der Polytherapie-Gruppe [12]. Teratogenitätsdaten werden prospektiv gesammelt. Eine ausreichende Empfängnisverhütung wird empfohlen.
Erweitertes Wirkungsspektrum
Für einen Teil der gängigen Antikonvulsiva liegen weitere Zulassungen vor. Zwar ist Zonisamid in Deutschland lediglich zur Zusatzbehandlung partieller Epilepsien zugelassen, Ergebnisse aus verschiedenen Untersuchungen legen jedoch eine Wirksamkeit auch bei anderen Erkrankungen nahe. Untersuchungen bei Patienten mit neuropathischen Schmerzen konnten eine Wirksamkeit von Zonisamid in der Schmerzreduktion zeigen [2, 10, 13]. Hinweise auf eine Wirksamkeit bei der Migräne-Prophylaxe liegen vor [7].
Wie in klinischen Studien beobachtet, kann Zonisamid zur Gewichtsabnahme führen, ein Zusammenhang mit der Carboanhydraseinhibition kann vermutet werden [6]; Untersuchungen an übergewichtigen Patienten ohne Epilepsie bestätigen den Effekt des Gewichtsverlustes [9].
Nach ersten Hinweisen auf die Wirksamkeit von Zonisamid bei Parkinson-Patienten konnte in einer doppelblinden Plazebo-kontrollierten Untersuchung an 347 Patienten gezeigt werden, dass sich die motorischen Funktionen unter Zonisamid deutlich verbesserten, wobei schon Dosen von 50 mg effektiv waren. Nebenwirkungen traten vermehrt in der 100-mg-Gruppe auf (Plazebo 65,1%, 25 mg/70,9%, 50 mg/72,9%, 100 mg/79,5%) und entsprachen im Wesentlichen denen, die bei Epilepsie-Patienten berichtet wurden [15].
Praktische Anwendung
Die empfohlene Startdosis beträgt 50 mg in zwei Einzelgaben, welche nach einer Woche auf 100 mg Tagesdosis erhöht wird. Im Verlauf sind wöchentliche Erhöhungen um 100 mg möglich, wobei eine erste Zieldosis bei 300 mg/d angestrebt werden sollte. Weitere Erhöhungen bis 500 mg/d können sinnvoll sein. Bei nieren- und/oder leberinsuffizienten Patienten empfiehlt sich eine langsamere Steigerung (14-tägiger Abstand zwischen den Erhöhungen).
Ausblick
Mit Zonisamid steht ein modernes Antikonvulsivum zur Zusatztherapie erwachsener Patienten mit fokalen Anfällen mit und ohne sekundäre Generalisierung zur Verfügung, für das aufgrund umfangreicher Prä- und Postmarketing-Erfahrungen in Japan, den USA und Europa ein klar definiertes Profil von Wirksamkeit und Sicherheit, auch in Langzeiterfahrungen, vorliegt. Responderraten von bis zu 50% bei schwer behandelbaren Epilepsien konnten belegt werden. Hinweise auf eine Tachyphylaxie im Langzeitverlauf fanden sich nicht. Die Nebenwirkungen sind meist ZNS-assoziiert und werden zum Großteil als leicht bis mäßig ausgeprägt klassifiziert. In Untersuchungen zur Monotherapie und bei Kindern konnte eine noch höhere Wirksamkeit und Verträglichkeit gezeigt werden, so dass zu hoffen bleibt, dass sich in Zukunft diese Möglichkeiten durch Erweiterung der Zulassungsindikation auch dem deutschen Behandler eröffnen.
Literatur
1. Arif H, Buchsbaum R, Weintraub D, Koyfman S, et al. Neurology 2007;68:1701–9.
2. Atli A, Dogra S. Pain Med 2005;6:225–34.
3. Baulac M. Epilepsy Res 2006;68(Suppl):S3–9.
4. Brodie MJ, Duncan R, Vespignani H, Solyom A, et al. Epilepsia 2005;46:31–41.
5. Brodie MJ. Epilepsy Res 2006;68(Suppl):S11–6.
6. DeSimone G, Supran CT. Curr Top Med Chem 2007;7:879–84.
7. Drake ME, Greathouse NI, Renner JKB, Armentbright AD. Clin Neuropharmacol 2004;27:278–80.
8. Faught E, Ayaka R, Montouris GG, Leppik I, and the Zonisamide 922 Trial Group. Neurology 2001;57:1774–9.
9. Gadde KM, Franciscy DM, Wagner HR, Krishan KR. JAMA 2003;289:1820–5.
10. Hasegawa H. Curr Med Res Opin 2004;20:577–80.
11. Iinuma K, Haginoya K. Seizure 2004;13(Suppl): S34–9.
12. Kondo T, Kaneko S, Amano Y, Egawa I. Epilepsia 1996;37:1242–4.
13. Krusz JC. Pain Pract 2003;3:317–20.
14. Leppik IE. Epilepsy Res 2006;68(Suppl):S17–24.
15. Murata M, Hasegawa K, Kanazawa I, The Japan Zonisamide on PD Study Group. Neurology 2007;68:45–50.
16. Ohtahara S. Epilepsy Res 2006;68(Suppl):S25–33.
17. Sackellares JC, Ramsay RE, Wilder BJ, Browne TR, et al. Epilepsia 2004;45:610–7.
18. Schmidt D, Jacob R, Loiseau P, Deisenhammer E. Epilepsy Res 1993;15:67–73.
19. Seino M. Seizure 2004;13(Suppl):S2–4.
20. Tosches WA, Tisdell J. Epilepsy Behav 2006;8: 522–6.
21. Welty TE, Kuzniecky RI, Limdi N, Faught E. Epilepsia 2001;42(Suppl 7):262.
22. Wroe S, Brodie MJ. 26th International Epilepsy Congress, August 28 – September 1, 2005, Paris, France [Poster].
23. Yagi, K. Seizure 2004;13(Suppl):S11–5.
Das ausführliche Literaturverzeichnis finden Sie auf unserer Website beim Inhaltsverzeichnis des aktuellen Hefts:
www.ppt-online.de > Inhalt > Heft 1
Dr. med. Randi D. von Wrede, Klinik für Epileptologie, Universität Bonn, Sigmund-Freud-Str. 25, 53105 Bonn, E-Mail: Randi.von.Wrede@ukb.uni-bonn.de
Zonisamide – a modern anticonvulsant. Review on efficacy and safety
Zonisamide is a modern antiepileptic drug for the add-on treatment of adults with partial epilepsy with or without secondary generalization, for which good efficacy and safety could be shown. Side effects are mostly CNS-associated and rated as mild or modest. Loss of weight sometimes is a side effect which is appreciated by patients and should be considerated in the decision of therapy. The pharmacologic profile (lack of liver enzyme alteration, high bioavailability and renal elimination) allows an uncomplicated use of zonisamide, even in the elderly or patients with co-medication.
Keywords: Epilepsy, long-term experience, side effects, responder, zonisamide
Psychopharmakotherapie 2008; 15(01)
