Hans-Jürgen Möller, Michael Riedel, München, Irini Karapanagiotou-Schenkel, Heidelberg, und Werner Kadus, Karlsruhe
Ziprasidon gehört zur Gruppe der Antipsychotika der 2. Generation. Es zeigt in Phase-III-Studien eine gute Wirksamkeit auf Positiv- und Negativsymptomatik schizophrener Psychosen [4, 6, 7, 13, 17, 20] sowie unter Verträglichkeitsaspekten den Vorteil der Gewichtsneutralität.
In Zeiten der Evidenz-basierten Medizin wird den Ergebnissen aus randomisierten kontrollierten klinischen Prüfungen der Phase III, unter anderem Prüfungen gegen Plazebo, der höchste Evidenzwert zugesprochen. Wegen der fehlenden Generalisierbarkeit solcher Ergebnisse, die aus Stichproben extrem selektierter Patienten abgeleitet werden, ist es nötig, in der Phase IV des Evaluationsprozesses Erfahrungen in der breiten und unselektierten Anwendung eines bisher nur in Phase III geprüften Medikaments zu sammeln, um zu überprüfen, ob die Ergebnisse der Phase III auch unter den „real world“-Bedingungen Gültigkeit behalten. Die nicht in die Versorgungsgegebenheiten eingreifende prospektive Beobachtungsstudie mit großer Fallzahl und standardisierter Erfassung von Wirksamkeit und unerwünschten Begleitwirkungen ist neben der randomisierten „effectiveness“-Studie der dafür bevorzugte Untersuchungsansatz.
Das Ziel der nachfolgend beschriebenen Ziprasidon-Studie war, an einer großen Stichprobe von etwa 3000 schizophrenen Patienten Möglichkeiten und Grenzen von Ziprasidon unter den Bedingungen der alltäglichen ambulanten Versorgung zu evaluieren. Neben Wirksamkeitsaspekten sollte dabei hinsichtlich Verträglichkeit vor allem die in der Phase III beschriebene Gewichtsneutralität überprüft werden, während zur Erfassung von QT-Veränderungen eine diesbezüglich speziell geplante offene klinische Studie durchgeführt wurde [9].
Patienten und Methoden
Die Zepko-Studie (Zeldox prospektive Kohortenstudie) wurde von Mai 2002 bis April 2004 als prospektive, nicht interventionelle Beobachtungsstudie an 848 Zentren in Deutschland durchgeführt. Die überwiegende Mehrzahl der teilnehmenden Zentren waren psychiatrische und nervenärztliche Praxen (743) sowie 79 psychiatrischen Kliniken. Die restlichen 26 Zentren gehörten den Fachrichtungen Innere Medizin, Geriatrie und Allgemeinmedizin an. Es konnten sowohl Patienten mit neu diagnostizierter als auch mit schon länger bekannter Schizophrenie eingeschlossen werden. Die Diagnostik erfolgte nach den Kriterien der ICD-10. Ziprasidon kam im Rahmen der praxisüblichen Therapie zum Einsatz; die Therapieentscheidung wurde vom behandelnden Arzt auf Grundlage des Krankheitsbilds in Absprache mit dem Patienten getroffen. Darüber hinaus waren keine weiteren Kriterien zum Studieneinschluss vorgegeben, da diese Studie den routinemäßigen Einsatz von Ziprasidon in der täglichen Praxis widerspiegeln sollte.
Bei Studieneinschluss wurden Angaben über Demographie und Anamnese mit Schwerpunkt psychiatrische Anamnese erfasst. Klassifikation und vorherrschende Symptomatik der Schizophrenie wurden dokumentiert. Ziprasidon wurde entsprechend der Herstellerempfehlung verordnet. Die Dosis konnte vom behandelnden Arzt bedarfsorientiert adaptiert werden. Die Anfangsdosierung und alle Dosisänderungen wurden fortlaufend dokumentiert. Die individuelle Beobachtungsdauer betrug 12 Wochen.
Die Psychopathologie wurde mit der Brief Psychiatric Rating Scale (BPRS) [18] und der Scale for the Assessment of Negative Symptoms (SANS) [3] erfasst, wobei im Rahmen der SANS nur die Globalbeurteilung der Hauptmerkmale der Negativsymptomatik erhoben wurde. Die Beurteilung der Positivsymptomatik erfolgte anhand der vier Kernsymptome der BPRS: Zerfall der Denkprozesse, Halluzinationen, Misstrauen, ungewöhnliche Denkinhalte. Die Veränderung des psychopathologischen Zustandsbilds unter Behandlung wurde mittels Globalbeurteilung (Clinical Global Impression of Change, CGI-C) [16] erhoben. Zur Quantifizierung extrapyramidaler Störungen wurde eine modifizierte Extrapyramidal-Symptom-Skala (EPS) [21] herangezogen. Diese modifizierte EPS besteht aus den Items Gang, Rigidität, Glabellareflex, Tremor und Speichelsekretion. Zur Erfassung möglicher Akathisien wurde das Item 4 der Barnes Akathisia Rating Scale (BARS) [5] eingesetzt: die globale klinische Beurteilung der Akathisie. Der BARS-Score beschreibt im Folgenden immer die Bewertung dieses Items 4. Bis auf den CGI-C, der am Studienende durchgeführt wurde, wurden die psychometrischen Tests zu Studienbeginn und nach zwölf Wochen beziehungsweise bei vorzeitigem Abbruch am individuellen Studienende durchgeführt. Unerwünschte Ereignisse (UE) wurden fortlaufend dokumentiert.
Statistik
Alle Patienten, die zumindest einmal Ziprasidon eingenommen hatten, wurden in die Auswertung zu Sicherheit und Verträglichkeit eingeschlossen (n=3121). Eine Intention-to-treat(ITT)-Auswertung wurde durchgeführt. Für die Wirksamkeitsanalyse schloss sie alle Patienten der Verträglichkeitsauswertung ein, für die mindestens ein Wirksamkeitsparameter unter Therapie bestimmt war (n=3 087).
Die Auswertung erfolgte deskriptiv und explorativ. Für die psychometrischen Tests wurden Summenscores gebildet, wobei die Beurteilung der BPRS-Kernsymptome in dieser Studie von 0 (nicht vorhanden) bis 6 beziffert wurde (im Folgenden BPRS-Score benannt). Für den EPS-Score wurde der Gesamtwert gebildet, indem die einzelnen Itembewertungen aufaddiert und durch die Anzahl der bewerteten Items dividiert wurden. In der Auswertung des CGI-C wurden die Wertungen „sehr viel besser“ und „viel besser“ als „Ansprechen auf die Behandlung“ zusammengefasst. Für die Veränderung der Wirksamkeitsparameter sowie der Inzidenzraten von unerwünschten Ereignissen (UE) wurden exakte 95%-Konfidenzintervalle (95%-KI) angegeben.
Zur Charakterisierung von Einflussgrößen und Risikofaktoren wurden Subgruppen gebildet und stratifizierte Analysen explorativ durchgeführt. Prognostische Faktoren für Ansprechen auf die Behandlung und vorzeitigen Studienabbruch wurden durch schrittweise logistische Regression ermittelt. In das Modell gingen Alter, Gewicht, Geschlecht, Klassifikation der Schizophrenie und die Werte der psychometrischen Skalen (BPRS, SANS, EPS und BARS) in der Eingangsuntersuchung als unabhängige Variablen ein. Durch eine schrittweise Rückwertseliminierung wurden die Variablen aus dem Modell entfernt, die einen p-Wert >0,05 hatten. Die verbleibenden unabhängigen Variablen bildeten die prognostischen Faktoren (prädiktive Faktoren) auf das Ansprechen beziehungsweise den vorzeitigen Studienabbruch. Die Analyse der Zeit bis zum Auftreten eines UE erfolgte mit dem Kaplan-Meier-Schätzer. Es erfolgte eine Schätzung der Hazard-Rate und eine graphische Darstellung (Kaplan-Meier-Plot).
Ergebnisse
Studienpopulation
3142 Patienten wurden in die Studie eingeschlossen, wobei 21 Patienten keine Studienmedikation erhielten und deshalb nicht in die Auswertung eingingen, so dass die Stichprobe dadurch auf 3121 Patienten reduziert wurde. 531 Patienten (17%) brachen die Studie vorzeitig ab. Dies geschah bei 231 Patienten aus Gründen der Verträglichkeit und in 74 Fällen wegen ungenügender Wirksamkeit der Studienmedikation. Alle anderen vorzeitigen Studienabbrüche hatten Ursachen unabhängig von der Studienmedikation. Bei 34 Patienten lag keine Erhebung zur Wirksamkeit unter Therapie vor. Nach Ausschluss dieser Patienten wurden 3087 in die ITT-Auswertung eingeschlossen.
Die meisten Patienten (66%) waren zwischen 18 und 44 Jahre alt. Etwas mehr als die Hälfte waren Frauen. Weitere Basisdaten der ITT-Studienpopulation sind in Tabelle 1 aufgeführt. Die Mehrheit der Patienten (65%) litt unter paranoider Schizophrenie, bei 11% bestand ein schizophrenes Residuum. Mit deutlich geringerer Inzidenz wurden hebephrene Schizophrenie (6%), Schizophrenia simplex (3%) und katatone Schizophrenie (2%) diagnostiziert.
Tab. 1. Demographische Daten der Studienpopulation nach Geschlecht
|
Männlich |
Weiblich |
Gesamt* |
|
|
Anzahl (%) Patienten |
1376 (44,0) |
1726 (55,3) |
3121 (100) |
|
Alter [Jahre] |
|
|
|
|
Mittelwert (SD**) |
37,5 (12,5) |
42,6 (13,9) |
40,3 (13,5) |
|
Gewicht [kg] |
|
|
|
|
Größe [cm] |
|
|
|
* Bei 19 Patienten ist keine Angabe zum Geschlecht verfügbar
** Standardabweichung
Die Verteilung von Stadium und vorherrschender Symptomatik der Erkrankung in der Studienpopulation ist in Tabelle 2 dargestellt, bezogen auf die 2328 Patienten, für die entsprechende Informationen vorlagen. In den letzten drei Monaten vor Einschluss in die Studie waren 76% der Patienten mit Neuroleptika behandelt worden, die meisten mit atypischen (46%), 20% mit typischen und 11% hatten sowohl typische als auch atypische Neuroleptika erhalten. Hauptsächliche Gründe für die Umstellung auf Ziprasidon waren ungenügende Wirksamkeit (58%), Gewichtszunahme unter der Vormedikation (50%) und Wunsch des Patienten (36%) (Mehrfachnennungen waren bei dieser Fragestellung möglich). 250 Patienten wurden zu Studienbeginn stationär behandelt. Bei 312 Patienten wurde mindestens eine stationäre Behandlung der Schizophrenie in der Anamnese dokumentiert. Detaillierte Angaben zum Ausmaß der Positivsymptomatik im Sinne der BPRS-Kernsymptome finden sich in Tabelle 3, bezogen auf einzelne Subgruppen. Analoge Informationen zur Negativsymptomatik, gemessen mit der SANS, gibt Tabelle 4.
Tab. 2. Stadium und vorherrschende Symptomatik der Schizophrenie bei Studienbeginn
|
Stadium |
Vorherrschende Symptomatik |
||||
|
Positivsymptomatik |
Negativsymptomatik |
Depressive |
Keine vorherrschende Symptomatik |
Gesamt |
|
|
Erstmanifestation einer Schizophrenie |
213 (9,2%) |
82 (3,5%) |
49 (2,1%) |
48 (2,1%) |
392 (16,8%) |
|
Akute Exazerbation einer Schizophrenie |
464 (19,9%) |
123 (5,3%) |
83 (3,6%) |
61 (2,6%) |
731 (31,4%) |
|
Chronisch stabile Schizophrenie |
95 (4,1%) |
450 (19,3%) |
115 (4,9%) |
137 (5,9%) |
797 (34,2%) |
|
Therapieresistente Schizophrenie |
156 (6,7%) |
145 (6,2%) |
55 (2,4%) |
52 (2,2%) |
408 (17,5%) |
|
Gesamt |
928 (39,9%) |
800 (34,4%) |
302 (13,0%) |
298 (12,8%) |
2328 (100%) |
Patienten, für die keine Angabe zum Stadium der Schizophrenie oder zur vorherrschenden Symptomatik vorlag, sind hier nicht berücksichtigt.
Tab. 3. Ausprägung der Positivsymptomatik zu Studienbeginn (BPRS-Score*)
|
Population |
N |
BPRS-Score |
BPRS-Score |
|
|
Klassifikation der Schizophrenie |
Paranoide Schizophrenie |
1906 |
10,3 (5,4) |
11 (1; 19) |
|
Stadium der Erkrankung |
Erstmanifestation |
508 |
11,3 (5,2) |
12 (3;19) |
|
Vorbehandlung |
Vorbehandelt |
2307 |
9,2 (5,4) |
9 (1; 18) |
|
Gesamt |
2931 |
9,9 (5,4) |
10 (1; 18) |
|
*Kernsymptome, **Standardabweichung, *** 5%-Perzentile; 95%-Perzentile
Tab. 4. Ausprägung der Negativsymptomatik zu Studienbeginn (SANS-Score)
|
Population |
N |
SANS-Score |
SANS-Score |
|
|
Klassifikation der Schizophrenie |
Paranoide Schizophrenie |
1898 |
8,7 (4,2) |
9 (2; 15) |
|
Stadium der Erkrankung |
Erstmanifestation |
507 |
8,6 (4,3) |
8,8 (2; 16) |
|
Vorbehandlung |
Vorbehandelt |
2298 |
9,0 (4,3) |
9 (2; 16) |
|
Gesamt |
2922 |
9,0 (4,2) |
9 (2; 16) |
|
*Standardabweichung, ** 5%-Perzentile; 95%-Perzentile
Medikation
Bei der überwiegenden Mehrzahl der Patienten der ITT-Stichprobe (98,5%) erfolgte die Therapie im Rahmen der Studie von Anfang an oral. Nur 40 Patienten erhielten initial Ziprasidon intramuskulär. Die Dauer der Therapie betrug im Median 92 Tage. Die Mehrzahl der Patienten (55%) erhielt Ziprasidon im Rahmen der Studie 91 Tage oder länger, ein Viertel 61 bis 90 Tage und 11% 29 bis 60 Tage. Bei 82% der Patienten, die die Studie bis zum Ende durchführten, wurde die Therapie nach Studienabschluss fortgesetzt. Die Therapie wurde bei oraler Gabe mehrheitlich (63%) mit 80 mg pro Tag initiiert. 17% der Patienten brachen die Studie vorzeitig ab.
Betrachtet man die Patienten, die die Studie vorzeitig abbrachen, fällt eine Tendenz zu niedrigeren Anfangsdosierungen auf im Vergleich zu denen, die die Studie regelrecht abschlossen hatten (Abb. 1). Diese Tendenz lässt sich analog für die Enddosis nach Titration beobachten. Die häufigsten Enddosierungen waren 80 mg (33%) und 120 mg (31%). 20% erhielten als letzte Dosis 160 mg. Insgesamt betrachtet betrug die mittlere tägliche Dosis 101,3 mg (± 36,1), die mittlere Maximaldosis 128,7 mg (± 60,9). Auch hier liegen die Dosierungen bei Studienabbrechern niedriger als bei Patienten, die die Studie durchliefen: Studienabbrecher erhielten im Mittel eine Tagesdosis von 94,4 mg (± 35,8), was deutlich unter der mittleren täglichen Dosis von 102,7 mg (± 36,1) lag, die Patienten mit regelrechtem Studienabschluss im Verlauf der Studie erhalten hatten. Die mittlere Maximaldosis betrug bei Abbrechern 120,3 mg (± 58,0) im Vergleich zu 130,3 mg (± 61,3) bei Patienten, die die Studie komplett durchlaufen hatten.
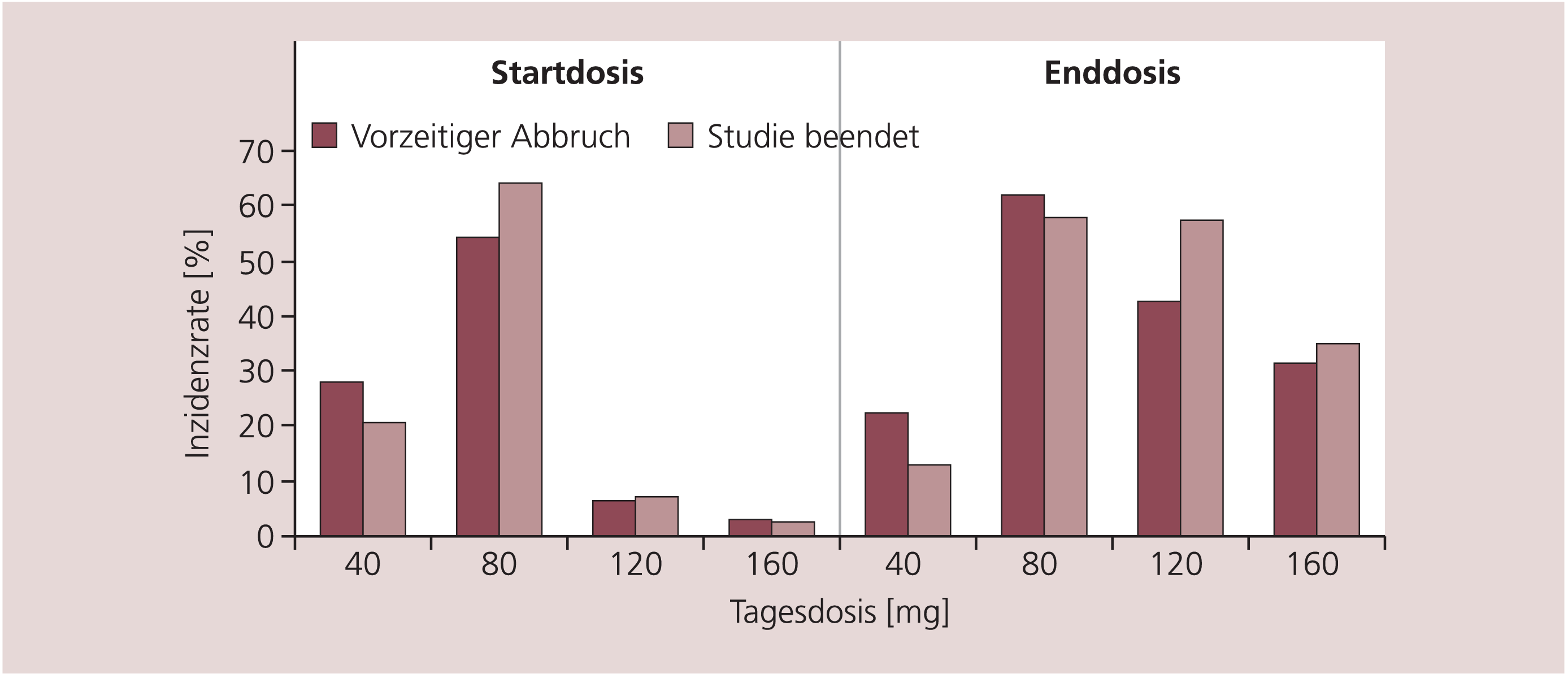
Abb. 1. Dosierungsverhalten bei Studienabbrechern im Vergleich zu Patienten mit regelrechtem Studienabschluss
52% der Patienten erhielten begleitend andere Antipsychotika. 22% wurden während der Studie mit Antidepressiva behandelt und 12% nahmen parallel Sedativa, Hypnotika oder Anxiolytika ein.
Klinische Wirkung
Positivsymptomatik
Der mittlere BPRS-Score (Kernsymptome) zu Studienbeginn betrug 9,9. Bei Stratifizierung nach der Klassifikation der Schizophrenie befinden sich die Subgruppen mit paranoider, hebephrener und katatoner Schizophrenie auf einem Niveau, bei Patienten mit schizophrenem Residuum, Schizophrenia simplex oder anderen Formen der Schizophrenie war die Positivsymptomatik deutlich geringer ausgeprägt (Tab. 3). Legt man eine stadienbezogene klinische Charakteristisierung der Erkrankung zugrunde, so findet sich bei Patienten mit chronisch stabiler Schizophrenie ein wesentlich niedriger BPRS-Score als in anderen Stadien. Patienten, die innerhalb der letzten drei Monate eine medikamentöse antipsychotische Behandlung erhalten hatten, zeigten im BPRS-Score eine deutlich geringere Positivsymptomatik als Unvorbehandelte.
In der Gesamtpopulation verbesserte sich der BPRS-Score bis zum Studienende im Mittel um –4,9 (95%-KI –5,1; –4,7). Eine deutlich geringere mittlere Abnahme des BPRS-Scores zeigten Patienten mit schizophrenem Residuum (–2,9) und Schizophrenia simplex (–3,7). Bei Erstmanifestation oder Exazerbation der Schizophrenie nahm der BPRS-Score in vergleichbarem Umfang ab, während Patienten mit therapieresistenter oder chronisch stabiler Schizophrenie eine deutlich geringere Verbesserung aufwiesen (Abb. 2). Die mittlere Abnahme des BPRS war bei nicht Vorbehandelten mit –7,6 deutlich höher als bei Vorbehandelten (–4,2).
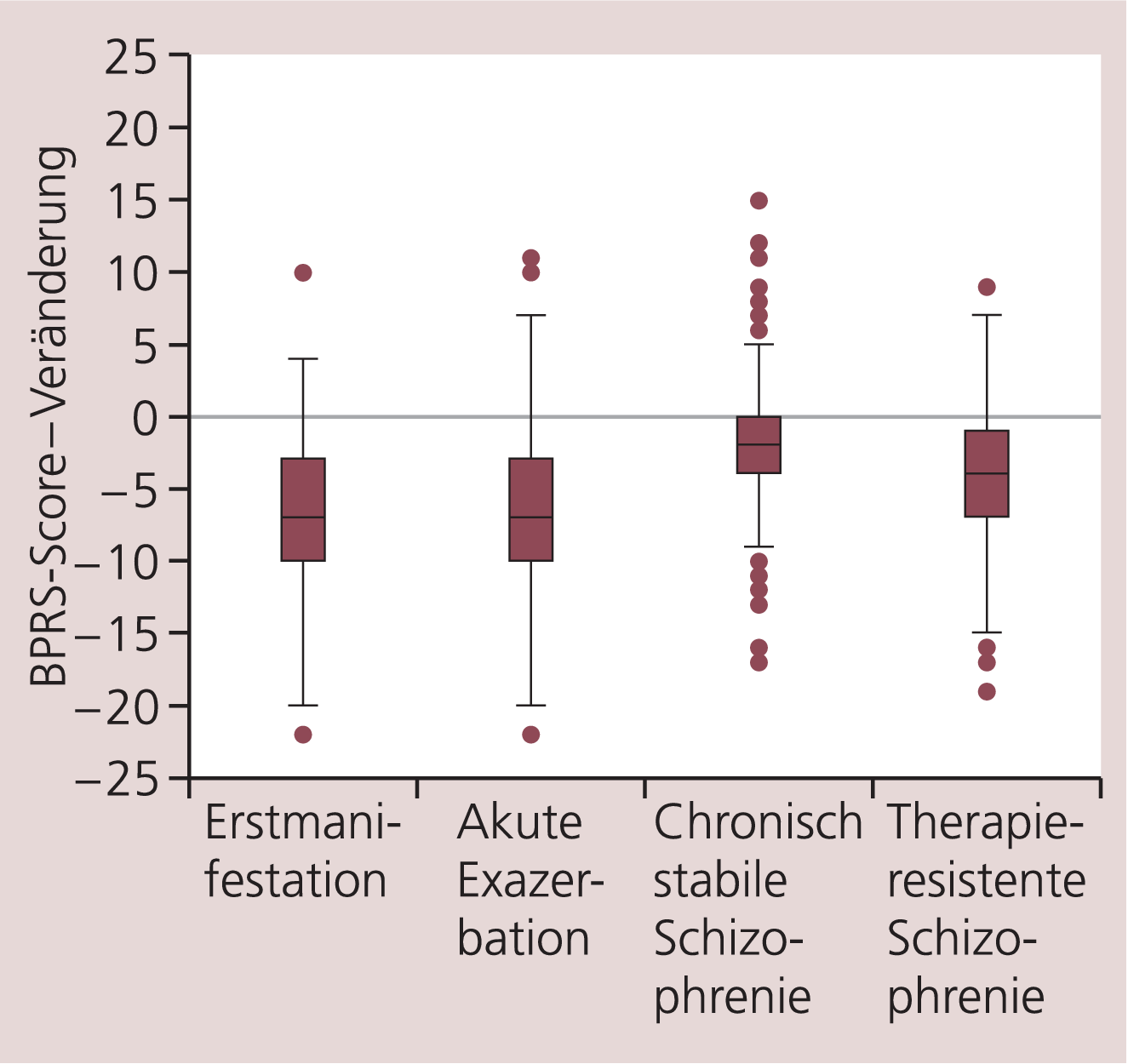
Abb. 2. Abnahme der Positivsymptomatik bei unterschiedlichen Stadien der Erkrankung. Reduktion des BPRS-Scores während der Studie
Negativsymptomatik
Der mittlere SANS-Score zu Studienbeginn betrug 9,0. Bei Stratifizierung nach der Klassifikation der Schizophrenie lag der Ausgangswert für fast alle Subgruppen auf ähnlichem Niveau (8,7 bis 10,5) bis auf die Populationen mit anderen Formen der Schizophrenie (7,6) (Tab. 4). Betrachtet man das Stadium der Erkrankung, bewegt sich der mittlere SANS-Score zu Studienbeginn im Bereich von 8,4 bis 10,2. Das Ausgangsniveau des SANS-Scores war nicht beeinflusst durch eine Vorbehandlung der Schizophrenie.
Unter Therapie nahm der SANS-Score von 9,0 (± 4,2) auf 5,6 (± 3,8) am Studienende ab. Die mittlere Differenz betrug –3,4 (95%-KI –3,6; –3,3). Die Abnahme des SANS war in den Gruppen mit paranoider und hebephrener Schizophrenie sowie mit schizophrenem Residuum vergleichbar mit Werten von –3,3 bis –3,7. Bei katatoner Schizophrenie wurde eine etwas größere Verbesserung beobachtet (–4,3). Schizophrenia simplex und andere Formen der Schizophrenie besserten sich deutlich weniger (–2,8 und –3,0). Stratifiziert man nach Erkrankungsstadium, ging die Negativsymptomatik bei Patienten mit Erstmanifestation am meisten zurück, bei Patienten mit therapieresistenter oder chronisch stabiler Schizophrenie am wenigsten (Abb. 3). Die mittlere Abnahme des SANS-Scores war bei nicht Vorbehandelten mit –4,3 höher als bei Vorbehandelten (–3,2).
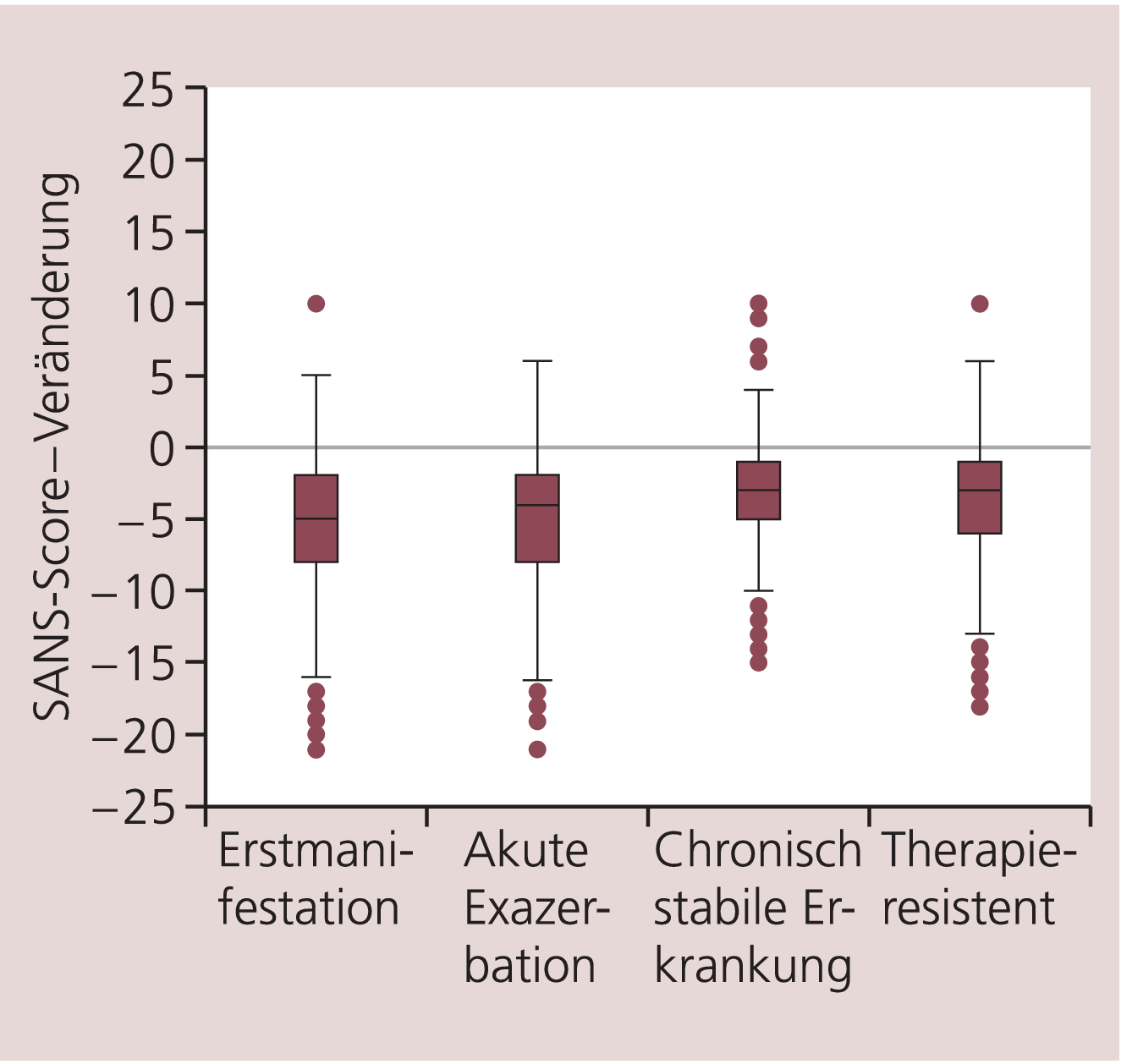
Abb. 3. Abnahme der Negativsymptomatik bei unterschiedlichen Stadien der Erkrankung. Reduktion des SANS-Scores während der Studie
Klinische Gesamtbeurteilung (CGI-C)
Basierend auf dem klinischen Gesamteindruck wurden am Studienende 16,4% der Patienten als sehr viel besser und 45,6% als viel besser beurteilt (Abb. 4). „Ansprechen auf die Behandlung“ war als CGI-Score „sehr viel besser“ oder „viel besser“ definiert. Die Gesamtpopulation zeigte eine Ansprechrate von 62,0% (95%-KI: 60,2%; 63,8%). Ähnliche Ansprechraten wurden bei paranoider, katatoner und hebephrener Schizophrenie beobachtet (64,6%–60,4%), wobei der Anteil „sehr viel besser“ in der Gruppe mit paranoider Schizophrenie am höchsten war (Tab. 5). Schizophrenes Residuum und Schizophrenia simplex zeigten mit 53,8% und 52,3% niedrigere Ansprechraten. Unterschiedliche Ansprechraten wurden auch für die unterschiedlichen Krankheitsstadien berichtet: Bei Erstmanifestation und akuter Exazerbation lagen die Ansprechraten auf demselben Niveau (74,7%, 73,4%), wogegen Patienten mit chronisch stabiler Schizophrenie deutlich seltener ansprachen (52,5%). Am schlechtesten war die Ansprechrate bei therapieresistenter Schizophrenie (46,5%).
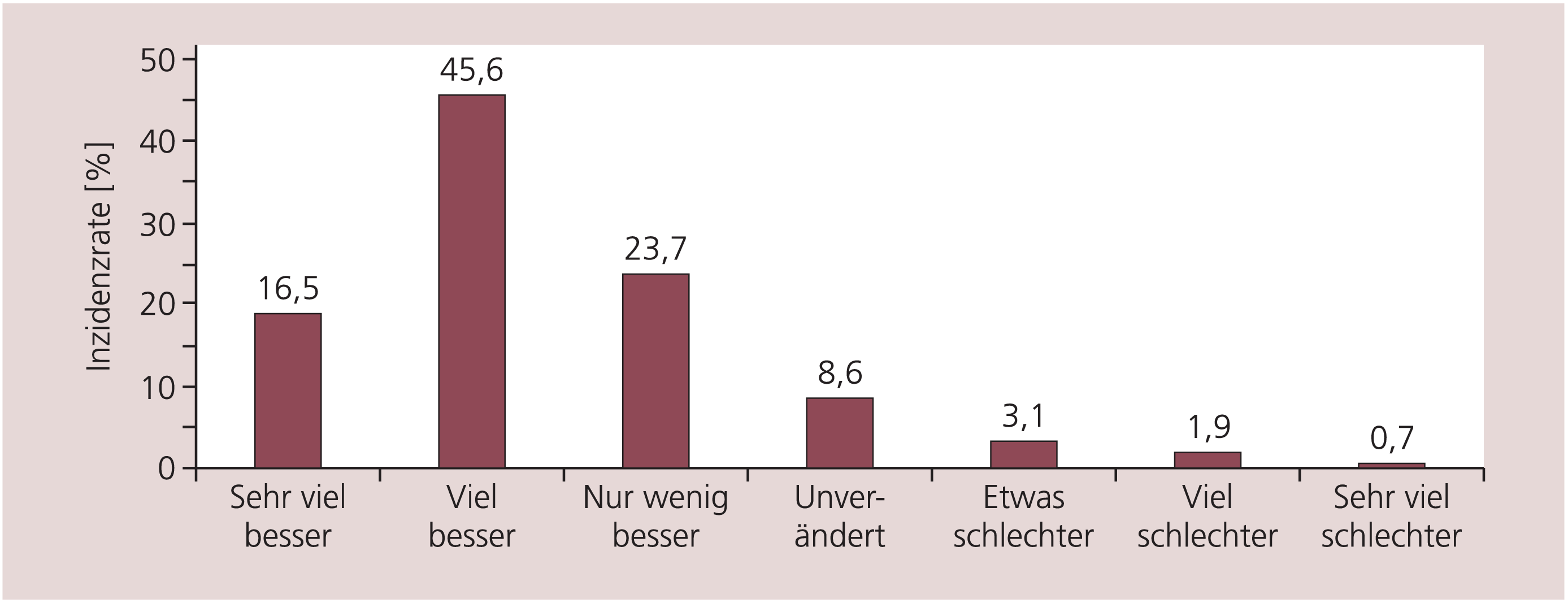
Abb. 4. Gesamtbeurteilung der klinischen Wirkung – CGI-C bei Studienende
Tab. 5. Verbesserung der klinischen Symptomatik – CGI-C am Studienende
|
Population |
Sehr viel besser |
Viel besser |
Nur wenig besser |
|
|
n (%) |
n (%) |
n (%) |
||
|
Klassifikation der Schizophrenie |
Paranoide Schizophrenie |
342 (18,3) |
863 (46,3) |
408 (21,9) |
|
Stadium der Erkrankung |
Erstmanifestation |
138 (27,5) |
237 (47,2) |
67 (13,3) |
|
Vorherrschende Symptomatik |
Positivsymptomatik |
207 (23,6) |
397 (45,3) |
162 (18,5) |
|
Vorbehandlung |
Vorbehandelt |
301 (13,4) |
1006 (44,8) |
584 (26,0) |
Betrachtet man die Stratifizierung nach vorherrschender Symptomatik, hatten Patienten mit vorwiegend Positiv- oder depressiver Symptomatik eine vergleichbare Ansprechrate (68,9% und 61,9%). Patienten mit vorwiegend Negativsymptomatik oder keiner vorherrschenden Symptomatik sprachen mit 55,7% und 53,5% schlechter an. Der CGI-Score „viel besser“ war bei allen vier Gruppen ähnlich häufig vertreten; die Unterschiede in der Ansprechrate sind durch eine unterschiedliche Häufigkeit in der Beurteilung „sehr viel besser“ bedingt.
Patienten ohne Vorbehandlung innerhalb der letzten drei Monate zeigten mit 76,0% ein wesentlich besseres Ansprechen als vorbehandelte (58,2%). Bei den Vorbehandelten hatten Patienten, die nur typische Neuroleptika erhalten hatten, die beste Ansprechrate (64,7%), gefolgt von dem Kollektiv, das mit typischen und atypischen Neuroleptika behandelt worden war (58,5%). Mit 55,0% war die Ansprechrate am niedrigsten in der Gruppe, die nur mit atypischen Neuroleptika vorbehandelt war.
Die logistische Regressionsanalyse zeigte, dass Patienten mit höheren BPRS- und EPS-Scores zu Studienbeginn eine höhere Wahrscheinlichkeit eines Ansprechens auf die Behandlung hatten, desgleichen Patienten mit paranoider und hebephrener Schizophrenie (Tab. 6). Für Patienten mit Schizophrenia simplex, einem schizophrenen Residuum oder katatoner Schizophrenie bestand ein Trend zu niedrigeren Ansprechraten.
Tab. 6. Prädiktive Faktoren (logistische Regression). Adjustierte Odds-Ratios and 95%-Konfidenzintervalle für das Ansprechen auf die Behandlung (CGI-C „sehr viel besser“ oder „viel besser“)
|
Variable |
Odds-Ratio |
95%-KI |
|
BPRS |
1,062 |
1,044–1,080 |
|
EPS |
1,064 |
1,029–1,100 |
|
Diagnose der Schizophrenie |
||
|
–Paranoide |
1,181 |
0,871–1,602 |
|
–Hebephrene |
1,145 |
0,736–1,783 |
|
–Katatone |
0,969 |
0,471–1,997 |
|
–Schizophrenes Residuum vs. andere |
0,798 |
0,546–1,165 |
|
–Schizophrenia simplex vs. andere |
0,697 |
0,401–1,211 |
Die Variablen BPRS (p<0,001), EPS (p=0,003) und Diagnose der Schizophrenie (p=0,0357), die in das Modell als unabhängige Variablen gingen, wurden als prädiktive Faktoren identifiziert. Die restlichen unabhängigen Variablen Alter (p=0,60), SANS (p=0,26), Körpergewicht (p=0,24), Akathisia (p=0,20), und Geschlecht (p=0,06) hatten keinen prädiktiven Effekt auf die Ansprechrate.
Verträglichkeit und Sicherheit
Unerwünschte Ereignisse
Insgesamt wurden 599 unerwünschte Ereignisse (UE) bei 452 Patienten unter Ziprasidon berichtet. Die Inzidenz der UE ist in Tabelle 7 dargestellt. Bei 461 UE wurde der Zusammenhang mit der Medikation als „ja“ oder „unbekannt“ vom jeweiligen Prüfarzt beurteilt. Diese wurden hier insgesamt als mit der Medikation in Zusammenhang stehend aufgeführt. Bei 231 Patienten aus der Gesamtzahl der 281, die vorzeitig wegen UE abgebrochen hatten, wurde das zum Abbruch führende UE vom Prüfer als in Zusammenhang mit der Medikation stehend beurteilt. Hierzu zählen 40 Fälle von schizophrener oder psychotischer Exazerbation sowie eine paranoide Reaktion. Ein Todesfall unbekannter Ursache wurde gemeldet. Ein Patient mit vorbestehender KHK verstarb an Herzinfarkt. Zwei Suizide ereigneten sich während der Studie, die von den Prüfern jeweils auf die schizophrene Grunderkrankung zurückgeführt wurden. Die meisten UE entstammten dem psychiatrischen Bereich. Die häufigsten UE sind in Tabelle 8 dargestellt. Auch bei den schwerwiegenden UE war die Gruppe der psychiatrischen Erkrankungen mit 2,3% am häufigsten vertreten. Alle anderen lagen weit unter 0,5%. Innerhalb der ersten Behandlungswoche war das Risiko, ein UE zu erfahren, am höchsten (Abb. 5). In Woche zwei und drei nahm das Risiko steil ab; danach ging es stetig weiter zurück. Insgesamt entsprach das Sicherheitsprofil von Ziprasidon den aus anderen Studien bekannten Ergebnissen.
Tab. 7. Inzidenz unerwünschter Ereignisse (UE)*
|
Sicherheitspopulation |
Alle UE |
In Zusammenhang mit der Medikation |
|
Anzahl UE (gesamt) |
599 |
461 |
|
Patienten mit UE |
452 (14,5) |
349 (11,2) |
|
Patienten mit SUE# |
93 (3,0) |
30 (1,0) |
|
Studienabbruch wegen UE |
281 (9,0) |
231 (7,4) |
* Erfasst sind Ereignisse bis sechs Tage nach letzter Medikationseinnahme im Rahmen der Studie
# SUE=schwerwiegendes UE
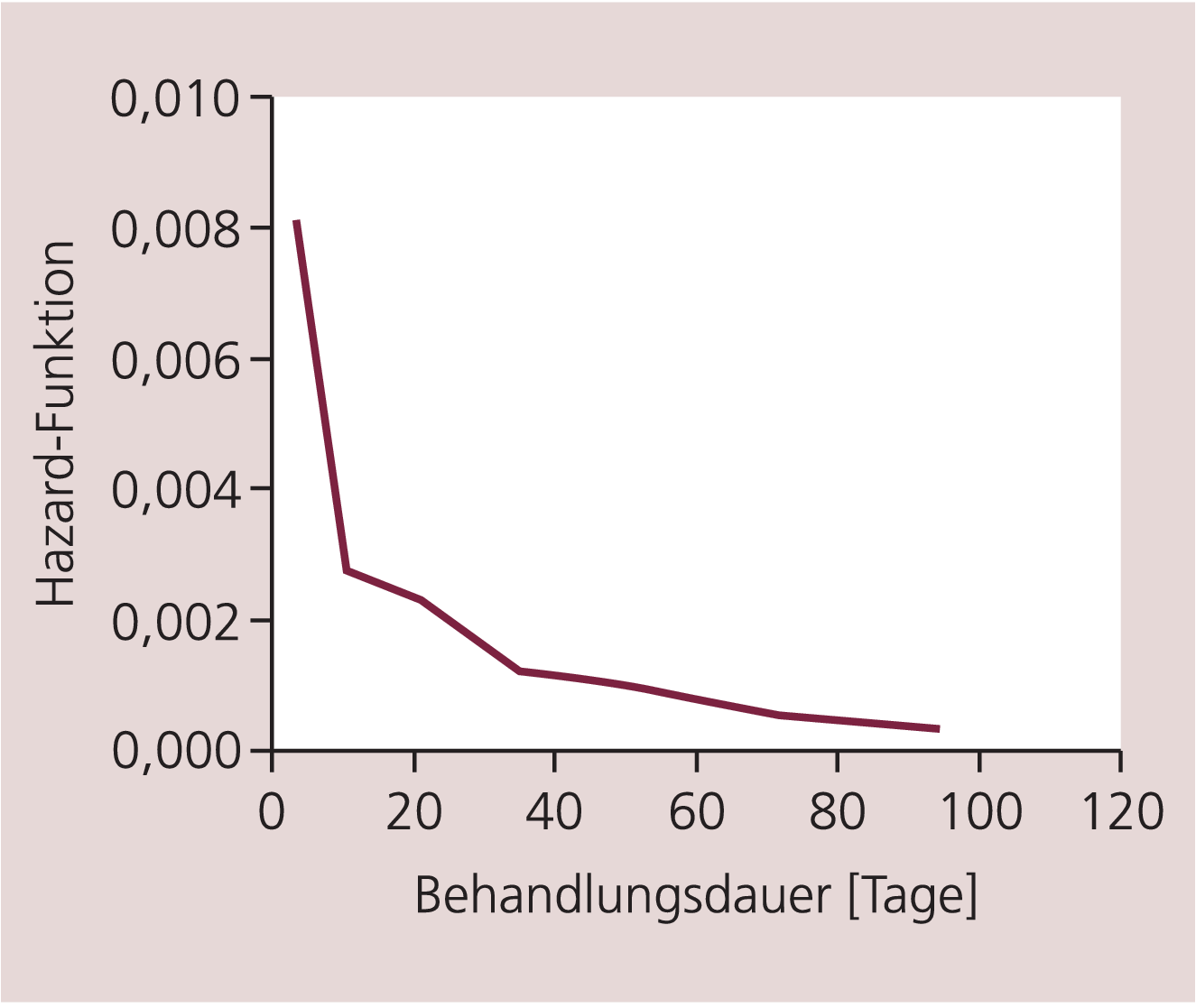
Abb. 5. Risiko, ein unerwünschtes Ereignis im Verlauf der Studie zu erleiden: Hazard-Rate
Tab. 8. Häufigste (≥0,5%) unerwünschte Ereignisse (UE)
|
Alle UE |
In Zusammenhang mit der Medikation |
|
|
Psychiatrische Ereignisse |
188 (6,0) |
115 (3,7) |
|
Allgemeine Ereignisse |
161 (5,2) |
144 (4,6) |
|
ZNS Ereignisse |
84 (2,7) |
79 (2,5) |
|
Kardiovaskuläre Ereignisse |
27 (0,9) |
20 (0,6) |
|
Magen-Darm-Ereignisse |
27 (0,9) |
20 (0,6) |
Sonstige Verträglichkeitsparameter
Extrapyramidale Symptomatik. Der mittlere EPS-Score nahm von 0,55 (± 0,70) im Verlaufe der Studie auf 0,30 (± 0,48) ab. Dies entspricht einer mittleren Reduktion von –0,26 (95%-KI: –0,28; –0,24). Bei Patienten mit einer Erstmanifestation lag der EPS-Score zu Studienbeginn mit 0,36 niedriger als bei Patienten mit einer akuten Exazerbation (0,55), einer chronisch stabilen Schizophrenie (0,58) oder einer therapieresistenten Schizophrenie (0,71). Entsprechend war die Abnahme in der Gruppe mit Erstmanifestation am niedrigsten (–0,17) im Vergleich mit den drei anderen Gruppen (–0,27 bis –0,30) (Abb. 6). Bei nicht vorbehandelten Patienten lag der Ausgangs-EPS-Score mit 0,30 um die Hälfte niedriger als bei vorbehandelten (0,61), wobei er bei beiden Gruppen während des Studienverlaufs abnahm (Unvorbehandelte –0,1; Vorbehandelte –0,31). Die Tatsache, dass auch nicht mit Neuroleptika vorbehandelte Patienten einen gewissen EPS-Score zeigten, kann darauf hinweisen, dass EPS-Skalen eine gewisse Unspezifität haben, mag aber auch durch Validitätsprobleme bei der Erhebung bedingt sein. Den höchsten mittleren EPS-Score zu Studienbeginn wiesen die mit typischen Neuroleptika Vorbehandelten auf (0,94) gegenüber den Subgruppen mit atypischen Neuroleptika in der Vorbehandlung (0,47) oder mit beiden (0,67). Die Abnahme in diesen drei Gruppen stand im selben Verhältnis wie die Ausgangswerte (–0,51; –0,22; –0,29) (Abb. 7). Bei der Analyse nach Altersklassen fiel eine Zunahme der Anfangsscores mit zunehmendem Alter auf: bei Patienten mit 20 Jahren oder darunter 0,42, zwischen 20 und 65 Jahren 0,53 und mit 65 Jahren oder älter 0,97. In allen Altersklassen nahm der mittlere EPS-Score während der Studie ab – im selben Verhältnis wie die Ausgangswerte: –0,20; –0,26; –0,38.
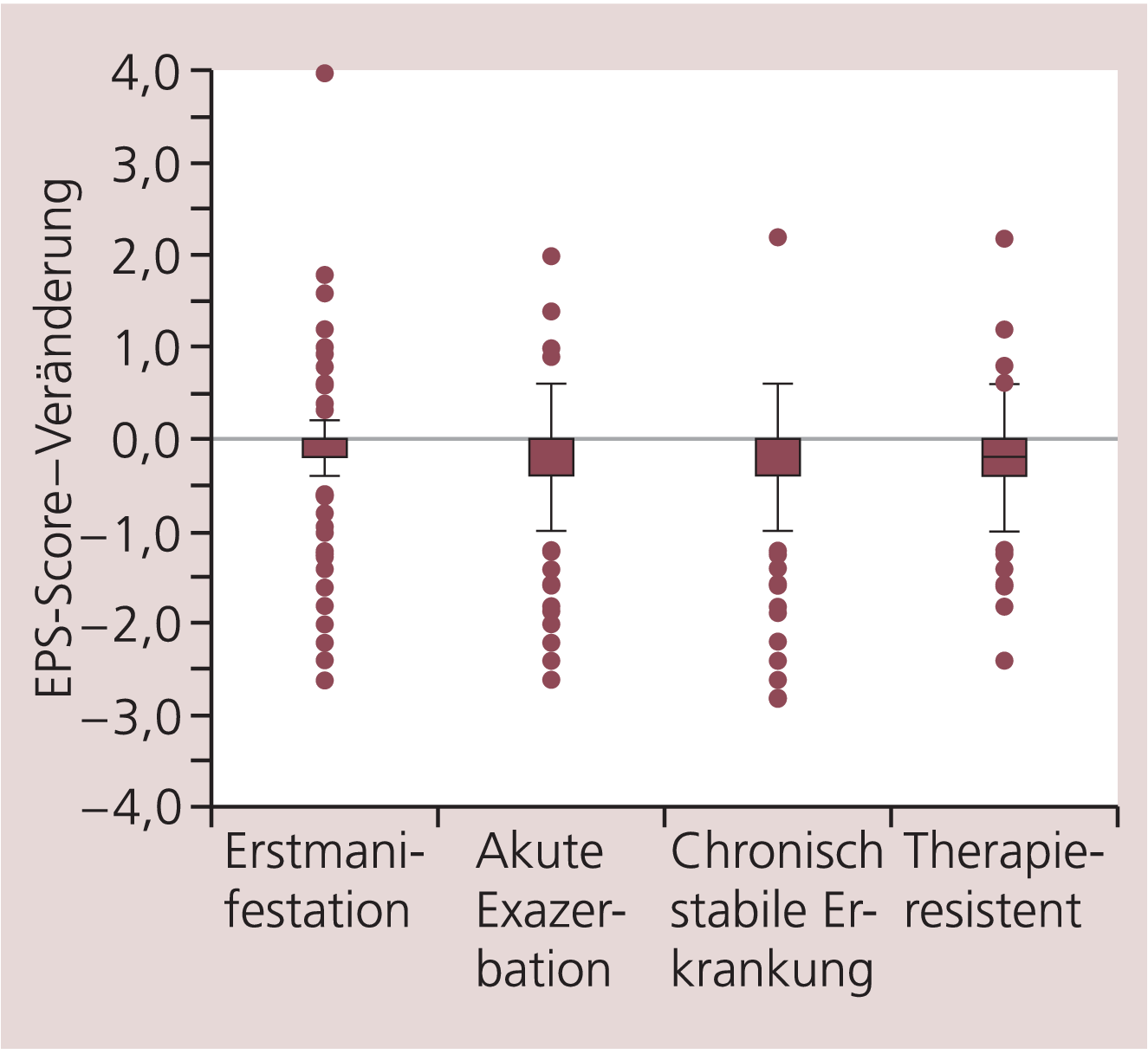
Abb. 6. Abnahme der extrapyramidalen Symptomatik bei unterschiedlichen Stadien der Erkrankung. Reduktion des EPS-Scores während der Studie
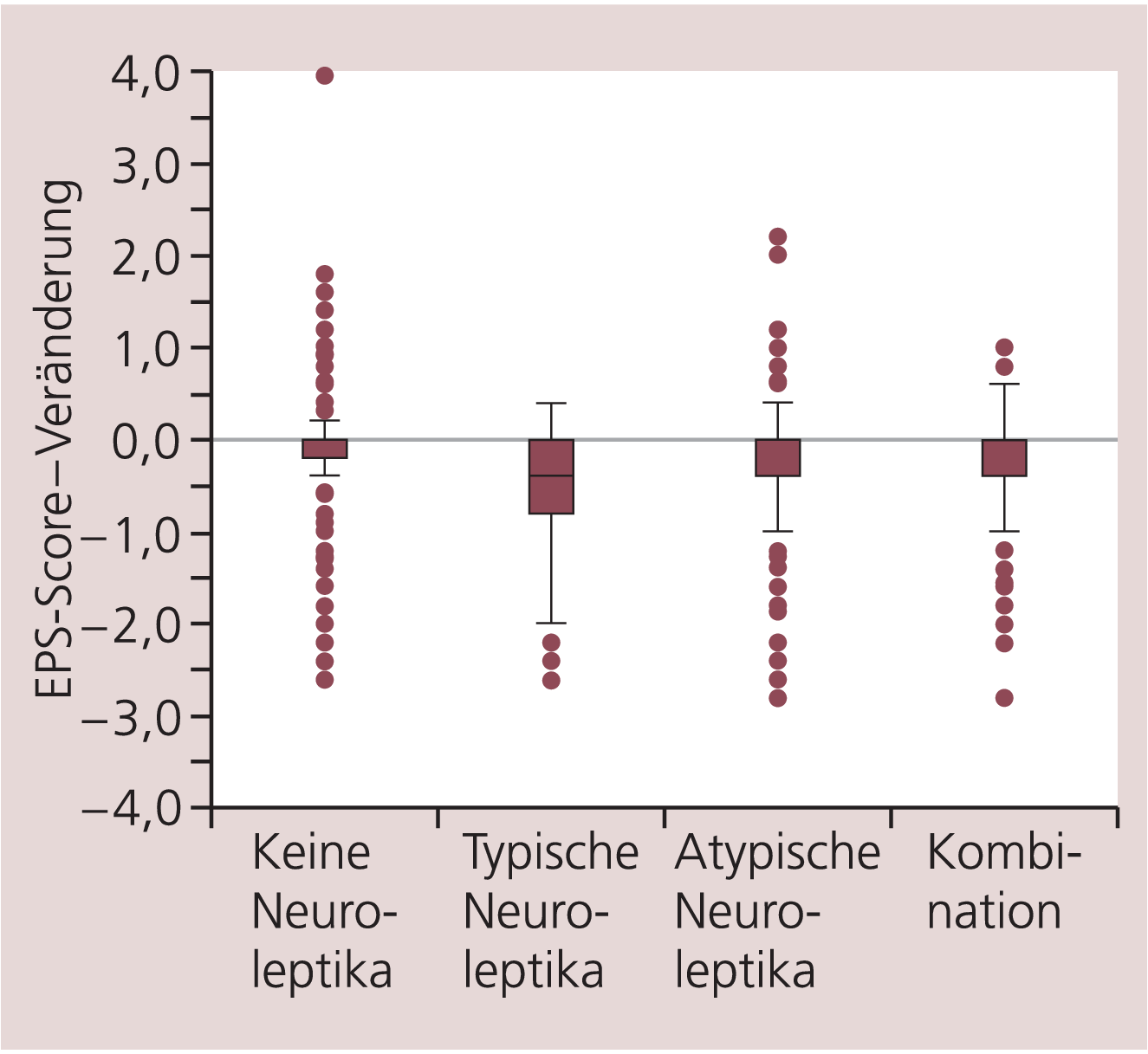
Abb. 7. Abnahme der extrapyramidalen Symptomatik bei unterschiedlicher Vorbehandlung. Reduktion des EPS-Scores während der Studie
Akathisie. Für die Gesamtpopulation wurde eine Abnahme des mittleren BARS-Scores von 0,81 (± 1,13) auf 0,43 (± 0,82) beobachtet. Der niedrigste Ausgangswert fand sich bei Patienten mit Erstmanifestation (0,53), der höchste bei therapieresistenter Schizophrenie (1,08). Bei allen Stadien der Schizophrenie nahm der BARS-Score unter Ziprasidon ab; bei Erstmanifestation um 0,26 im Durchschnitt, bei allen anderen zwischen 0,39 und 0,47. Bei unvorbehandelten Patienten lag der BARS-Score zu Anfang bei 0,48, bei vorbehandelten bei 0,89. Dass nicht mit Neuroleptika vorbehandelte Patienten einen Score in einer Akathisie-Skala zeigen, kann einerseits auf gewisse Unspezifitäten solcher Skalen hinweisen, hängt aber wahrscheinlich auch mit Validitätsaspekten bei der Erhebung zusammen. Vorbehandelte Patienten zeigten mit –0,45 die größere Reduktion im Studienverlauf gegenüber –0,17 bei den unvorbehandelten. Anfangswert und auch die Reduktion während der Studie waren in der Gruppe, die mit atypischen Neuroleptika vorbehandelt war, am niedrigsten (0,71, Reduktion um 0,33) gegenüber der Population mit typischen Neuroleptika oder mit beiden (1,28; Reduktion um 0,75 bzw. 0,99, Reduktion um 0,45).
Wie bei der extrapyramidalen Symptomatik bestand eine Abhängigkeit vom Alter. Den höchsten BARS-Score wiesen die 65-Jährigen und Älteren auf (1,30), gefolgt von den 20- bis 65-Jährigen mit 0,79. Der niedrigste Ausgangswert (0,56) wurde bei 20-Jährigen oder Jüngeren beobachtet. In allen Altersklassen nahm der mittlere BARS-Score während der Studie ab – im selben Verhältnis wie die Ausgangswerte: –0,54; –0,39; –0,21.
Körpergewicht. Betrachtet man die Verträglichkeitsstichprobe, nahm das mittlere Körpergewicht während der Studie leicht um 1,4 kg (± 4,0) von 80,4 kg auf 79,1 kg ab. Insgesamt verloren 55% im Studienverlauf Gewicht (mittlere Abnahme 3,8 kg). 9,8% konnten ihr Körpergewicht um mehr als 7% reduzieren. Bei den meisten Patienten (87,6%) bewegte sich die Reduktion unterhalb von 7% des anfänglichen Körpergewichts. Nur 2,6% nahmen um mehr als 7% zu. Analysiert man die Gruppe, die aufgrund vorhergehender Gewichtszunahme auf Ziprasidon umgestellt worden war, reduzierten deutlich mehr ihr Gewicht um mehr als 7% (21%). Nur 1% nahm über 7% des Ausgangsgewichts zu.
Wie bei der extrapyramidalen Symptomatik bestand eine Abhängigkeit vom Alter. Den höchsten BARS-Score wiesen die 65-Jährigen und Älteren auf (1,30), gefolgt von den 20- bis 65-Jährigen mit 0,79. Der niedrigste Ausgangswert (0,56) wurde bei 20-Jährigen oder Jüngeren beobachtet. In allen Altersklassen nahm der mittlere BARS-Score während der Studie ab – im selben Verhältnis wie die Ausgangswerte: –0,54; –0,39; –0,21.
Patienten mit einer Erstmanifestation der Schizophrenie hatten mit 74,4 kg im Mittel ein erheblich niedrigeres Ausgangsgewicht als Patienten mit chronisch stabiler (84,4 kg) oder therapieresistenter Schizophrenie (82,1 kg). In der Gruppe mit Erstmanifestation blieb das Körpergewicht praktisch stabil: die mittlere Abnahme betrug 0,24 kg. Patienten mit chronisch stabiler Schizophrenie verloren im Mittel 2,4 kg, mit therapieresistenter Schizophrenie 1,5 kg. Ähnliche Unterschiede finden sich, wenn man Patienten mit antipsychotischer Vorbehandlung in den letzten drei Monaten mit Unvorbehandelten vergleicht. Die Unvorbehandelten waren zu Studienbeginn mit durchschnittlich 74,3 kg deutlich leichter als Vorbehandelte (82,0 kg), wobei die Unvorbehandelten ihr Gewicht beibehielten (mittlere Änderung +0,18 kg) und die Vorbehandelten es um 1,87 kg im Mittel reduzierten. Berücksichtigt man die Art der Vorbehandlung, hatten die Patienten bei Therapie mit typischen Neuroleptika, atypischen oder beiden ein vergleichbares mittleres Ausgangsgewicht (81,5–82,9 kg). Die lediglich mit atypischen Neuroleptika Vorbehandelten zeigten allerdings die ausgeprägteste mittlere Gewichtsreduktion (–2,2 kg) gegenüber der mit typischen Neuroleptika oder beiden vorbehandelten Gruppe (–1,2 kg bzw. –1,8 kg) (Abb. 8).
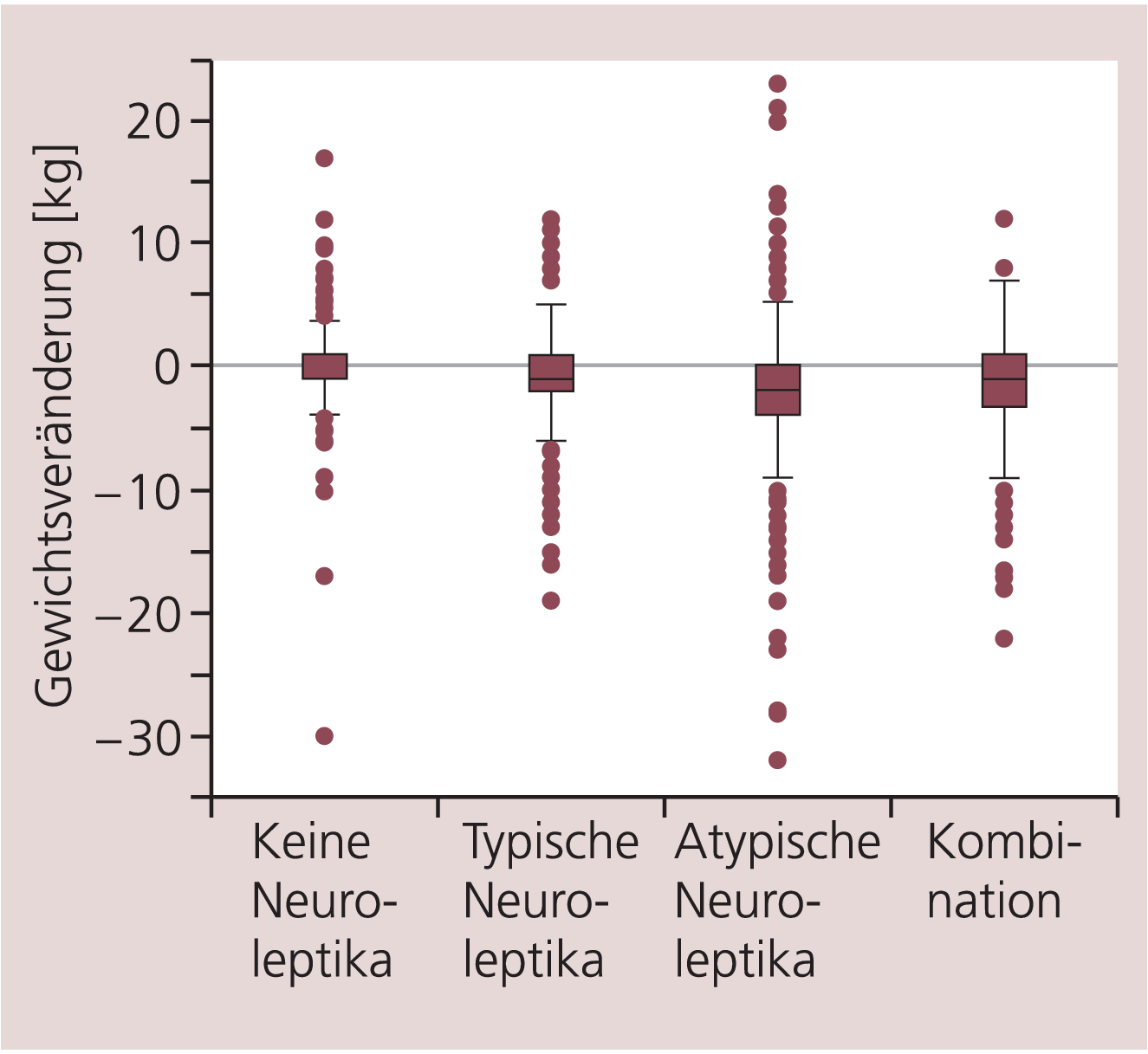
Abb. 8. Mittlere Gewichtsveränderung in Abhängigkeit von der Vorbehandlung
Am deutlichsten waren die Unterschiede im Vergleich der Patientengruppe, die wegen Gewichtszunahme unter der Vormedikation auf Ziprasidon umgestellt worden war, mit den anderen Patienten (Abb. 9). Die aus Gewichtsgründen Umgestellten wogen zu Studienbeginn im Mittel 87,3 kg und erreichten eine Reduktion um 3,6 kg unter Ziprasidon. Die Gruppe der anderen Patienten behielt dagegen ihr Anfangsgewicht von 76,3 kg im Studienverlauf bei (mittlere Differenz –0,03 kg).
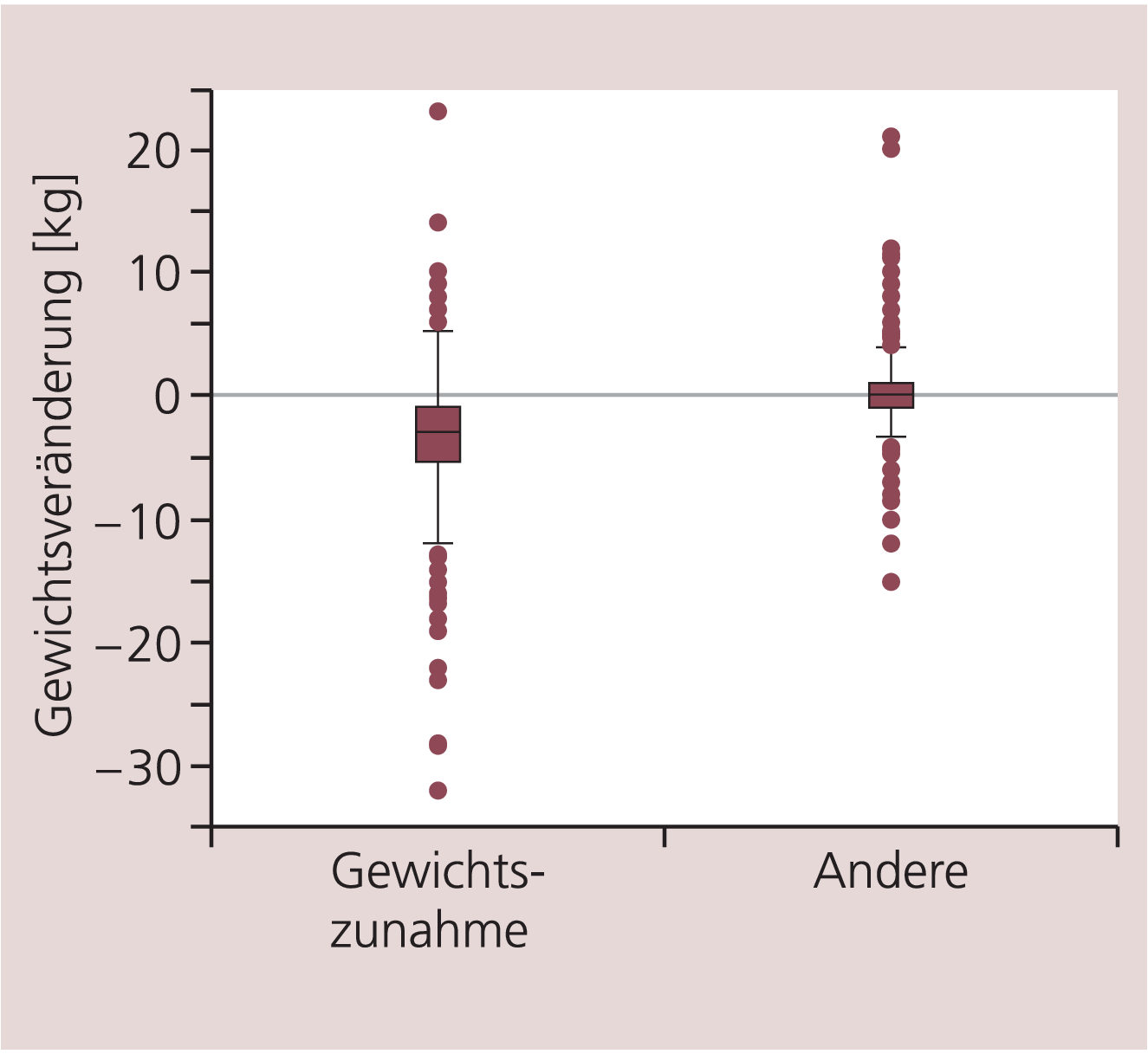
Abb. 9. Mittlere Gewichtsveränderung bei vorbehandelten Patienten in Abhängigkeit vom Umstellungsgrund
Diskussion
In der großen Anwendungsbeobachtung zu Ziprasidon wurde eine Fülle deskriptiver Daten erhoben, die unter verschiedenen Detailgesichtspunkten von Interesse sind. Die Diskussion fokussiert auf einige wenige klinisch relevante Hauptergebnisse.
In der gegenwärtigen Situation, induziert durch die CATIE-Studie [11], wird den „effectiveness“-Studien eine besondere Bedeutung als komplementärer Ansatz zu den eigentlichen „efficacy“-Studien beigemessen und gleichzeitig, wie in der CATIE-Studie praktiziert, die „non-discontinuation“-Quote (Nicht-Abbruch-Quote) als zentrales Maß der „effectiveness“ propagiert. Es ist bemerkenswert, dass im Gegensatz zu der höheren Drop-out-Quote der CATIE-Studie (ca. 30% der Patienten schieden nach drei Monaten aus der ersten Studienphase aus) nur 17% der unter den Bedingungen der ambulanten Versorgung in psychiatrischen und nervenärztlichen Praxen in Deutschland mit Ziprasidon behandelten schizophrenen Patienten die 12-wöchige Studie vorzeitig beendet haben. Das kann einerseits hinweisen auf die hohe allgemeine Akzeptanz von Ziprasidon sowohl aus der Sicht der Patienten wie aus der Sicht ihrer behandelnden Ärzte. Das Ergebnis könnte gleichzeitig dafür sprechen, dass die Gesamtsituation der alltäglichen ambulanten psychiatrischen Versorgung in Deutschland geeignet ist, eine große Zahl von Patienten, zumindest in den ersten 12 Wochen, in ausreichendem Maße zur Compliance anzuhalten. Allerdings müssen solche Unterschiede in der Patientenselektion und in der Behandlung mit größter Vorsicht interpretiert werden, da nicht nur Unterschiede bei den Patienten, sondern auch Unterschiede im Design (bei der CATIE-Studie handelt es sich um eine randomisierte Kontrollgruppenuntersuchung mit der Möglichkeit des Übergangs in eine andere Behandlungsoption) zu solchen Unterschieden führen können. Zur Illustration der Varianzbreite mögen deshalb noch weitere Studienergebnisse dienen: In der großen randomisierten, in Europa durchgeführten Anwendungsbeobachtung zu Olanzapin und anderen atypischen Neuroleptika bei schizophrenen Patienten (der sog. SOHO-Studie, [10]) ergab sich eine Drop-out-Quote von 9% (für alle Neuroleptika) nach drei Monaten und 12,5% nach sechs Monaten. Für die analoge Studie zu Aripiprazol und anderen atypischen Neuroleptika lag die 26-Wochen-Absetzquote insgesamt bei 40,5% [22]. Leider fehlen in der sehr pragmatisch auf Durchführbarkeit zugeschnittenen Zepko-Studie detailliertere Angaben zur Krankheitsvorgeschichte, die über mögliche Unterschiede der Stichproben Auskunft geben könnte.
Drop-out-Gründe waren in der Zepko-Studie zu einem größeren Teil Verträglichkeitsgründe, in geringerem Ausmaß ungenügende Wirksamkeit. Als Hauptgründe für den vorzeitigen Therapieabbruch wurden unerwünschte Ereignisse (9,0%), ungenügende Wirksamkeit (2,4%) und andere Gründe (5,5%) angegeben.
Die Mehrzahl der Patienten (63%) wurde zu Beginn mit einer Tagesdosis von 80 mg oral behandelt, die häufigsten Enddosierungen waren 80 mg (33%) und 120 mg (31%), während 160 mg nur bei 20% der Patienten als Enddosierung gegeben wurde. Die mittlere Maximaldosis betrug 128,7 mg (±60,9). Insgesamt zeigen diese Daten einen sinnvollen Dosierungsrahmen, der eher im mittleren und oberen Bereich der empfohlenen Tagesdosis ist; dies wird auch aus der mittleren Maximaldosis von rund 130 mg deutlich. Aus einer weiter differenzierenden Analyse ergeben sich Hinweise, dass tendenziell Patienten mit einer niederen durchschnittlichen Dosis eher das Risiko eines Studienabbruchs zeigten als die mit einer höheren Dosierung. Die Erfahrungen mit der breiten Anwendung von Ziprasidon haben gezeigt, dass im klinischen Alltag eher der höhere Dosisbereich von 120 bis 160 mg/d anzustreben ist und dass die anfangs vorgeschlagenen niedrigeren Dosierungen im Hinblick auf eine gute Wirksamkeit problematisch sind und bei vielen Patienten nicht ausreichen [8, 12, 15].
Insgesamt liegt die globale Wirksamkeit, gemessen mit den CGI-C-Kategorien „sehr viel besser“/„viel besser“, hoch. In dieser Kategorisierung ergab sich für die Gesamtgruppe eine Ansprechrate von 62%. Einige Subgruppen wie schizophrenes Residuum, therapieresistente Schizophrenie und Patienten mit vorwiegender Negativsymptomatik hatten im Vergleich dazu ungünstigere Ansprechraten, in der Größenordnung um 50% oder bei therapieresistenter Schizophrenie sogar bei 46%. Patienten ohne Vorbehandlung innerhalb der letzten drei Monate zeigten hingegen mit 76% die beste Ansprechquote, im Vergleich dazu die Vorbehandelten nur 58%. Interessant ist auch, dass Patienten, die nur mit typischen Neuroleptika vorbehandelt waren, eine bessere Ansprechquote hatten (64,7%) im Vergleich zu denen, die bereits mit atypischen Neuroleptika vorbehandelt waren (55%). All diese Differenzierungen der Anspruchquote sind per se klinisch plausibel und bedürfen keiner weiteren Erläuterung. Es soll deshalb nur angemerkt werden, dass bei schon als therapierefraktär bezeichneten Patienten eine Ansprechquote von 46,4% nach Umsetzen auf Ziprasidon als ein gutes Resultat zu bewerten ist. Dass Patienten mit vorwiegender Negativsymptomatik insgesamt nicht so gut auf Neuroleptika ansprechen wie Patienten mit vorherrschender Positivsymptomatik, ist ein klinisch bekanntes Faktum. Auch neue Antipsychotika können die Negativsymptomatik nur in begrenztem Maße beeinflussen, obwohl, wie aus vielen doppelblinden Studien bekannt ist, sie diesbezüglich besser wirken als klassische Neuroleptika [14].
Bezieht man die Ergebnisse der standardisierten Beurteilungsskalen mit ein, so zeigt sich eine klinisch relevante und statistisch signifikante Besserung der Scores der ausgewählten Kernsymptome für Positivsymptomatik, der sich in einem Mittelwert von 9,9 zu Beginn um 4,9 verringert. Hinsichtlich der verschiedenen Subgruppen ergeben sich ähnliche Differenzierungen wie bereits mit der CGI-C gemessene Verbesserungen, so ist beispielsweise die mittlere Abnahme dieses Scores bei nicht Vorbehandelten mit –7,6 deutlich höher als bei Vorbehandelten (–4,2). Auch die Negativsymptomatik nahm deutlich und signifikant ab. Die Negativsymptomatik wurde mit einer vereinfachten Form der SANS-Skala beurteilt. Der Mittelwert dieser modifizierten SANS lag zu Beginn bei 9,0, unter Therapie nahm der Score signifikant um einen mittleren Differenzwert von 3,4 auf 5,6 ab. Auch hier ließen sich Differenzierungen hinsichtlich der einzelnen Subgruppen finden.
Insgesamt war die Verträglichkeit von Ziprasidon gut. Bei 452 Patienten wurden Nebenwirkungen irgendwelcher Art berichtet, insgesamt 599 UE. Der größte Teil der unerwünschten Ereignisse betraf psychiatrische Symptomatik, die (wie z.B. psychotische Reaktion bzw. schizophrene Reaktion) als unzureichende Wirksamkeit der antipsychotischen Medikation interpretiert werden können. Dazu gehört auch Agitation, die als Ausdruck unzureichender Sedierung durch Ziprasidon aufgefasst werden kann.
Extrapyramidal-motorische Störungen wurden mit 0,7% sehr selten als unerwünschtes Ereignis gemeldet. Dazu passen auch die günstigen Skalenwerte mit einer Kurzform der Simpson-Angus-Skala und einer Kurzform der Akathisie-Skala. Sowohl die mittleren Werte der Kurzform der Simpson-Angus-Skala wie auch der Akathisie-Skala nahmen im Verlauf der Studie deutlich ab. Die günstigen Werte im Hinblick auf extrapyramidal-motorische Nebenwirkungen belegen die auch von klinischen Prüfungen bekannten diesbezüglichen Befunde und unterstreichen, aus der breiten klinischen Anwendung, die für atypische Neuroleptika wie Ziprasidon bekannten extrapyramidal-motorischen Verträglichkeitsvorteile [13]. Kardiovaskuläre Ereignisse wurden in 0,9% der Fälle angegeben. Sie beziehen sich im Wesentlichen auf orthostatische Störungen. Ein Patient mit vorbestehender chronischer Herzkrankheit verstarb an Herzinfarkt. Ein Todesfall unbekannter Ursache wurde gemeldet. In der schon erwähnten deutschen Ziprasidon-Studie mit 276 schizophrenen Patienten und einem Fokus auf kardiale Verträglichkeitsparameter war keine klinisch relevante QTc-Verlängerung im Prae-post-Mittelwertsvergleich und kein Fall einer QTc-Verlängerung über den kritischen Wert von ≥500 ms zu beobachten [9].
In den letzten Jahren ist zunehmend die Problematik der Gewichtszunahme und des damit assoziierten metabolischen Syndroms als ein Problem einiger atypischer Neuroleptika beschrieben worden, eine Problematik, die nicht nur die atypischen Neuroleptika betrifft, sondern auch von einigen der klassischen Neuroleptika wie beispielsweise Chlorpromazin und Thioridazin bekannt ist [1, 2]. Ziprasidon ist aus allen bisherigen Untersuchungen als gewichtsneutral bekannt. Das wird auch in den Ergebnissen der hier vorgelegten Anwendungsbeobachtung unterstrichen. Es zeigte sich eine durchschnittliche Gewichtsabnahme von 1,3 kg, von 80,4 kg auf 79,1 kg. Die Patienten, die bereits vorbehandelt waren, zeigten eine stärkere Gewichtsabnahme, insbesondere die, die mit atypischen Neuroleptika vorbehandelt waren. Sie hatten eine mittlere Gewichtsreduktion von 2,2 kg. Am deutlichsten war die Gewichtsabnahme bei den Patienten, die wegen einer Gewichtszunahme unter der Vormedikation auf Ziprasidon umgestellt worden waren: sie erreichten eine Reduktion um 3,6 kg unter Ziprasidon. Insgesamt verloren 44% der Patienten im Studienverlauf Gewicht mit einer mittleren Abnahme von 3,8 kg. Gerade diese Vorteile hinsichtlich des Gewichtsverhaltens, die sich unter anderem auch in der randomisierten 6-Monats-Vergleichsstudie Ziprasidon vs. Olanzapin zeigte [21], gibt Ziprasidon einen besonderen Platz in der Gruppe der atypischen Neuroleptika.
Literatur
1. Allison DB, Mentore JL, Heo M, Chandler LP, et al. Antipsychotic-induced weight gain: a comprehensive research synthesis. Am J Psychiatry 2001;158:501–2.
2. American Diabetes Association, American Psychiatric Association, American Association of Clinical Endocrinologists, North American Association for the Study of Obesity. Consensus development conference on antipsychotic drugs and obesity and diabetes. Diabetes Care 2004;27:596–601.
3. Andreasen NC. Negative symptoms in schizophrenia. Arch Gen Psychiatry 1982;39:784-8.
4. Arato M, O’Connor R, Meltzer HY; ZEUS Study Group. A 1-year, double-blind, placebo-controlled trial of ziprasidone 40, 80 and 160 mg/day in chronic schizophrenia: the ziprasidone extended use in schizophrenia (ZEUS) study. Int Clin Psychopharmacol 2002;17:207–15.
5. Barnes TRE. A rating scale for drug-induced akathisia. Br J Psychiatry 1989;154:672-6.
6. Brook S, Walden J, Benattia I, Siu CO, et al. Ziprasidone and haloperidol in the treatment of acute exacerbation of schizophrenia and schizoaffective disorder: comparison of intramuscular and oral formulations in a 6-week, randomized, blinded-assessment study. Psychopharmacology 2005;178:514–23.
7. Harvey PD, Bowie CR. Ziprasidone: efficacy, tolerability, and emerging data on wide-ranging effectiveness. Expert Opin Pharmacother 2005;6:337–46.
8. Joyce AT, Harrison DJ, Loebel AD, Carter CT, et al. Effect of initial ziprasidone dose on length of therapy in schizophrenia. Schizophr Res 2006;83:285–92.
9. Kudla D, Lambert M, Domin S, Kasper S, et al. Effectiveness, tolerability, and safety of ziprasidone in patients with schizophrenia or schizoaffective disorder: results of a multi-centre observational trial, Eur Psychiatry 2007;22:195–202.
10. Lambert M, Haro JM, Novick D, Edgell ET, et al. Olanzapine vs. other antipsychotics in actual out-patient settings: six month tolerability results from the European schizophrenia out-patient health outcomes study. Acta Psychiatr Scan 2005;111:232–43.
11. Lieberman A, et al. Effectiveness of antipsychotic drugs in patients with chronic schizophrenia. N Engl J Med 2005;353:12.
12. Mamo D, Kapur S, Shammi CM, Papatheodorou G, et al. A PET study of dopamine D2 and serotonin 5-HT2 receptor occupancy in patients with schizophrenia treated with therapeutic doses of ziprasidone. Am J Psychiatry 2004;161:818–25.
13. Möller HJ. Definition, psychopharmacological basis and clinical evaluation of novel/atypical neuroleptics: methodological issues and clinical consequences. World J Biol Psychiatry 2000;1:75–91.
14. Möller HJ. Management of the negative symptoms of schizophrenia. New treatment options. CNS Drugs 2003;17:793–823.
15. Mullins CD, Shaya FT, Zito JM, Obeidat N, et al. Effect of initial ziprasidone dose on treatment persistence in schizophrenia. Schizophr Res 2006;83:277–84.
16. National CGI: Clinical Global Impressions. In: Guy W, Bonato RR (eds.). Manual for the ECDEU Assessment Battery. 2nd rev. ed. Chevy chase, Md: National Institute of Mental Health, 1970:12.1–12.6.
17. Olie JP, Spina E, Murray S, Yang R. Ziprasidone and amisulpride effectively treat negative symptoms of schizophrenia: results of a 12-week, double-blind study. Int Clin Psychopharmacol 2006;21:143–51.
18. Overall JE, Gorham DR. The Brief Psychiatric Rating Scale. Psychol Rep 1962;10:799–812.
19. Simpson GM, Angus JWS. Drug-induced extrapyramidal disorders. Acta Psychiatr Scand Suppl 1970;212:11–9.
20. Simpson GM, Glick ID, Weiden PJ, Romano SJ, et al. Randomized, controlled, double-blind multicenter comparison of the efficacy and tolerability of ziprasidone and olanzapine in acutely ill inpatients with schizophrenia or schizoaffective disorder. Am J Psychiatry 2004;161:1837–47.
21. Simpson GM, et al. Six-month, blinded, multicenter continuation study of ziprasidone versus olanzapine in schizophrenia. Am J Psychiatry 2005;162:1535–8.
22. Kerwin R, Millet B, Herman E, et al. A multicenter, randomized, naturalistic, open-label study between aripiprazole and standard of care in the management of community-treated schizophrenic patients. Schizophrenia Trial of Aripiprazol: (STAR) study. Eur Psychiatry 2007;22:433–43.
Prof. Dr. med. Hans-Jürgen Möller, Dr. med. Michael Riedel, Psychiatrische Klinik der Ludwig-Maximilians-Universität, Nussbaumstr. 7, 80336 München, E-Mail: hans-juergen.moeller@med.uni-muenchen.de Dipl. Volksw. Irini Karapanagiotou-Schenkel, Nationales Zentrum für Tumorerkrankungen, 69120 Heidelberg, vorher: Pfizer Pharma GmbH, 76139 Karlsruhe Dr. med. Werner Kadus, Pfizer Pharma GmbH, 76139 Karlsruhe
Results of a large post-marketing observational study on ziprasidone
Ziprasidone was evaluated in the treatment of 3,142 schizophrenic outpatients in a 12-week, post-marketing observational study. No changes of the usual treatment procedures were permitted, apart from the application of standardised methods of evaluation to record efficacy and adverse events. The results demonstrate a high degree of acceptance of ziprasidone (drop-out rate 17%), good efficacy (62% achieved the CGI category “very much improved”/“much improved”) and tolerability when used under the conditions of routine clinical care. Reports of extrapyramidal-motor side effects were rare (0.7%), as were cardiovascular events (0.9%). The average weight loss was 1.3 kg, i.e. from 80.4 kg to 79.1 kg. The average weight loss in patients who were changed over to ziprasidone for weight-related reasons was 3.6 kg. Results of randomised clinical studies and large post-marketing observational studies show that besides good efficacy in treating the symptoms of schizophrenic disorders, whereby positive and negative symptoms in particular were investigated, the special advantages of the atypical antipsychotic ziprasidone are its weight neutrality and the positive effects on neuroleptic-related excess weight.
Keywords: Treatment of schizophrenia, atypical neuroleptics, ziprasidone
Psychopharmakotherapie 2008; 15(01)
