Pasquale Calabrese, Bochum, Ute Essner, Hamburg, und Hans Förstl, München
Die Alzheimer-Demenz ist eine neurodegenerative, progredient verlaufende Erkrankung. Nach Schätzungen gibt es in Deutschland 900000 Patienten mit einer Demenz, davon leiden etwa 650000 an einer Alzheimer-Demenz. Jährlich kommen 200000 Neuerkrankungen hinzu; bei etwa 120000 handelt es sich um eine Alzheimer-Demenz. Das Alter gilt noch immer als der größte Risikofaktor, so dass mit zunehmender Überalterung die Zahl der Demenzerkrankungen weiter steigen wird [1].
Neben dem cholinergen Defizit bei der Alzheimer-Demenz [4] kommt es auch zu Störungen im glutamatergen System. Glutamat ist der wichtigste exzitatorische Neurotransmitter: Etwa 70% der Neuronen sind glutamaterg [11]. Obwohl man bislang nicht alle am Pathomechanismus beteiligten Prozesse kennt, gibt es zahlreiche gesicherte Erkenntnisse über die Entstehung der gestörten Neurotransmission und des neuronalen Zelluntergangs sowie über die Rolle des Glutamats. Bei der Alzheimer-Demenz kommt es zu einer Konzentrationserhöhung von Glutamat im synaptischen Spalt, entweder durch vermehrte Ausschüttung in den oder durch reduzierte Wiederaufnahme aus dem synaptischen Spalt. Dieser Anstieg von Glutamat führt einerseits dazu, dass die Signalweiterleitung gestört wird, und sie bewirkt zum anderen einen exzitotoxischen Effekt [2, 3, 10].
Zur Behandlung der Alzheimer-Demenz gibt es derzeit zwei zugelassene Therapieoptionen: Cholinesterase-Hemmer, die dem cholinergen Defizit entgegenwirken [5, 6], und Memantin, einen nicht-kompetitiven NMDA-Antagonisten, der die neuronale Signalweiterleitung verbessert und neuroprotektive Eigenschaften aufweist [2, 10]. Während die Cholinesterase-Hemmer zur Behandlung der leichten bis mittelschweren Alzheimer-Demenz zugelassen sind, steht mit Memantin seit 2002 auch eine Therapieoption für die fortgeschritteneren Stadien der Alzheimer-Demenz zur Verfügung. In kontrollierten klinischen Studien konnte die Wirksamkeit und Verträglichkeit bei Patienten mit mittelschwerer bis schwerer Alzheimer-Demenz der Memantin-Monotherapie und der Kombinationstherapie mit einem Cholinesterase-Inhibitor nachgewiesen werden [13, 15, 16]. Auch bei leichteren Formen der Alzheimer-Demenz konnte die Wirksamkeit von Memantin gezeigt werden [12]. In diesen Plazebo-kontrollierten Doppelblindstudien hat sich gezeigt, dass Memantin in den Bereichen Kognition, Alltagskompetenz und klinischer Gesamteindruck Plazebo signifikant überlegen war. Da in klinischen Studien aufgrund der strikten Ein- und Ausschlusskriterien nur stark selektierte Patientenkollektive untersucht werden, war das Ziel der hier diskutierten Anwendungsbeobachtung, die Wirksamkeit und Verträglichkeit von Memantin unter naturalistischen Bedingungen, das heißt bei einem heterogenen Patientenkollektiv in der täglichen Praxis zu untersuchen. Im Sinne der an eine Anwendungsbeobachtung zu stellenden Anforderung an qualitätssichernde Maßnahmen wurde neben den hierfür notwendigen Dokumentationsschemata ein mehrdimensionaler Fragebogen mit Selbst- und Fremdbeurteilungsmöglichkeit eingesetzt. Hierüber wurde die nach unterschiedlichen Aktivitäts- und Verhaltensbereichen geordnete Erfassung von angehörigenbezogenen Veränderungsdimensionen sichergestellt.
Patienten und Methode
In einer offenen, multizentrischen Anwendungsbeobachtung wurden Patienten mit einer Alzheimer-Demenz über sechs Monate mit 20 mg/d Memantin behandelt. Es nahmen hauptsächlich niedergelassene Ärzte teil (Allgemeinmediziner, Nervenärzte, Psychiater und Neurologen). Eine nach Diagnosegruppen orientierte Verteilung der untersuchten Patienten wurde nicht vorgenommen.
Insgesamt sollten 2000 Patienten, die an einer mittelschweren bis schweren Alzheimer-Demenz (ICD-10) litten, in die Anwendungsbeobachtung aufgenommen werden. Außer einer vom behandelnden Arzt nach klinischen Kriterien zu stellenden Demenzdiagnose wurden keine Vorgaben zur Auswahl der Patienten gemacht. Ausnahme war, dass die Patienten nicht gleichzeitig an einer klinischen Prüfung teilnehmen durften, oder eine Therapie mit Memantin sich als unverträglich erwiesen hatte. Die in der Fachinformation aufgeführten Gegenanzeigen und Vorsichtsmaßnahmen mussten beachtet werden.
Zu Beginn der Untersuchung wurden die demographischen Daten, die bisherige Therapie mit Antidementiva, Begleiterkrankungen und -medikation erfasst. Die Patienten wurden zu drei Zeitpunkten untersucht: Zur Eingangsuntersuchung und zur Beurteilung der Wirksamkeit nach drei und sechs Monaten wurden der Mini-Mental-Status-Test (MMST) und die Nurses’ Observation Scale for Geriatric Patients (NOSGER) verwendet. Neben dem Mini-Mental-Status-Test zur Prüfung der kognitiven Leistungsfähigkeit und der Nurses’ Observation Scale for Geriatric Patients zur Fremdeinschätzung der Alltagskompetenz wurde das Explorationsmodul Demenz (EMD) zur Eingangsuntersuchung und nach sechs Monaten eingesetzt. Das Explorationsmodul Demenz ist ein psychometrischer Fragebogen, bei dem anhand von 13 einfachen geschlossenen Fragen aus den Bereichen Kognition, Alltagsverhalten, Affektivität und Krankheitswahrnehmung sowohl eine Selbst- als auch eine Fremdeinschätzung der alltagsbezogenen Demenzbeeinträchtigungen und deren subjektiver Wahrnehmung abgegeben werden soll. Das Instrument ermöglicht eine Beurteilung von Gedächtnis- und anderen kognitiven Störungen sowie von Selbstständigkeit, Kommunikation, Stimmung und Antrieb. Die dimensionsspezifische Beurteilung erfolgte durch den Patienten selbst und durch die Bezugsperson.
Der klinische Gesamteindruck wurde durch den behandelnden Arzt auf einer dreistufigen Skala beurteilt (verbessert, stabilisiert, verschlechtert). Die Wirkung von Memantin auf die kognitiven Fähigkeiten und Alltagsfunktionen wurde anhand einer vierstufigen Skala bewertet (sehr gut, gut, mäßig, schlecht). In gleicher Weise wurde durch den Arzt die Verträglichkeit beurteilt. Zu jedem Untersuchungszeitpunkt wurden unerwünschte Ereignisse erfragt und gegebenenfalls dokumentiert. Die Dosierung von Memantin wurde nach drei und sechs Monaten erfasst. Bei vorzeitigem Therapieende wurden die Gründe für den Abbruch erfragt.
Die Auswertung dieser Anwendungsbeobachtung erfolgte hinsichtlich der Sicherheit und Verträglichkeit mit Methoden der deskriptiven Statistik. Die inferenzstatistische Überprüfung der Behandlungseffekte erfolgte mit parametrischen Tests. Für die Analyse des Hauptkollektivs wurden individuell fehlende Werte zu den Messzeitpunkten nach drei und sechs Monaten nicht berücksichtigt („observed-case population“).
Ergebnisse
In diese Beobachtungsstudie wurden insgesamt 1845 Patienten aufgenommen. Für die Wirksamkeitsanalyse konnten Daten von 1580 Patienten ausgewertet werden. 265 Patienten wurden aus der Wirksamkeitsanalyse ausgeschlossen. Bei 72 Patienten wurde keine Behandlung dokumentiert, für 60 Patienten lag keine Beurteilung nach drei oder sechs Monaten vor, 73 Patienten hatten einen MMST-Wert ≥27 und für 130 Patienten lag eine retrospektive Dokumentation vor.
Es wurden sowohl neu diagnostizierte als auch Patienten mit bereits bestehender Alzheimer-Demenz-Diagnose in die Anwendungsstudie aufgenommen (Tab. 1). Das Durchschnittsalter lag bei 76,3±8,7 Jahren. 58,2% der Patienten waren weiblich. 60,9% der Patienten waren bereits vorbehandelt. Unter Berücksichtigung von Mehrfachnennungen erhielten 24,9% Ginkgo-Extrakte, 20,1% Piracetam und 17,3% Cholinesterase-Hemmer. 21,6% der Patienten erhielten weiterhin ein Antidementivum. Da der Schwerpunkt dieser Anwendungsbeobachtung nicht in der Betrachtung der Wirksamkeit der Kombinationstherapie lag, wurden keine gesonderten Analysen der Kombinationstherapie durchgeführt.
Tab. 1. Patientencharakteristika
|
Geschlecht (weiblich) |
58,2% |
|
Alter [Jahre] (Mittelwert±SD) |
76,3±8,7 |
|
Größe [cm] (Mittelwert±SD) |
167,1±8,1 |
|
Gewicht [kg] (Mittelwert±SD) |
70,3±11,5 |
|
Bisherige Dauer der AD [Jahre] (Mittelwert±SD) |
2,4±1,9 |
|
Begleiterkrankungen* [%] |
|
|
MMST (Mini-Mental-Status-Test) zur Baseline (Mittelwert±SD), n=1496 |
15,4±5,65 |
*Mehrfachnennungen möglich
Neben der Alzheimer-Demenz litten 74,4% der Patienten an mindestens einer weiteren Begleiterkrankung. Die kardiovaskulären Erkrankungen standen dabei im Vordergrund (Tab. 1). Dementsprechend wurde bei 65,4% der Patienten eine Komedikation angegeben: 41,2% der Patienten erhielten Antihypertensiva. Darüber hinaus bestand die Komedikation aus Antidiabetika (13,4%), Antidepressiva (11,3%) und Neuroleptika (9,3%). Eine Änderung in der Komedikation wurde im Rahmen dieser Untersuchung nicht erfasst. Die Ergebnisse beim MMST (Mini-Mental-Status-Test) lagen zur Eingangsuntersuchung bei 15,4±5,7.
Die mittlere Erhaltungsdosis von Memantin lag nach drei Monaten bei 17,1±5,8 mg/d und nach sechs Monaten bei 17,3±5,8 mg/d. 185 Patienten brachen die Therapie vor Ende der sechsmonatigen Beobachtungsphase ab. Als Gründe wurden angegeben (Mehrfachnennungen möglich):
Wunsch des Patienten (3,4%)
Mangelnde Wirksamkeit (3,3%)
Unerwünschte Ereignisse (3,1%)
Andere Ursachen (2,4%)
Memantin führte auf allen untersuchten Ebenen (Kognition, Aktivitäten des täglichen Lebens und ärztliches Globalurteil) zu einer Besserung der Symptomatik. Der MMST-Wert verbesserte sich nach sechsmonatiger Therapie um 2,5±4,5 Punkte (n=1199, p<0,0001, Abb. 1).
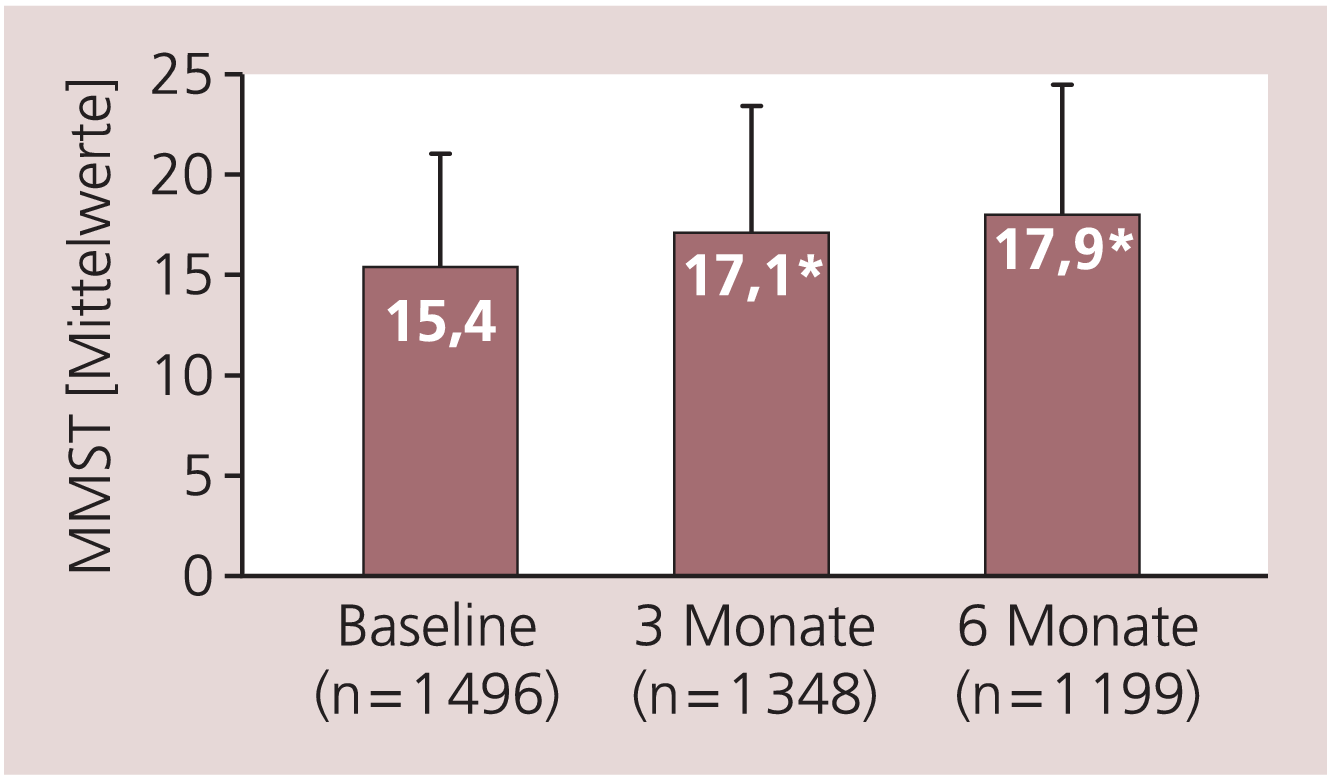
Abb. 1. Ergebnisse (Mittelwerte) des Mini-Mental-Status-Tests (MMST) zum Untersuchungsbeginn, nach drei und sechs Monaten (OC-Analyse) (*p<0,0001; t-Test)
In der Responder-Analyse konnte gezeigt werden, dass bei 68,2% der Patienten der MMST-Wert um mindestens einen Punkt zunahm. 17,0% der Patienten verbesserten sich um ein bis zwei Punkte, 34,4% um drei bis sechs Punkte und 16,8% um mehr als sechs Punkte. Eine Stabilisierung der kognitiven Kernsymptomatik zeigte sich bei 9,6% der Patienten (Abb. 2).
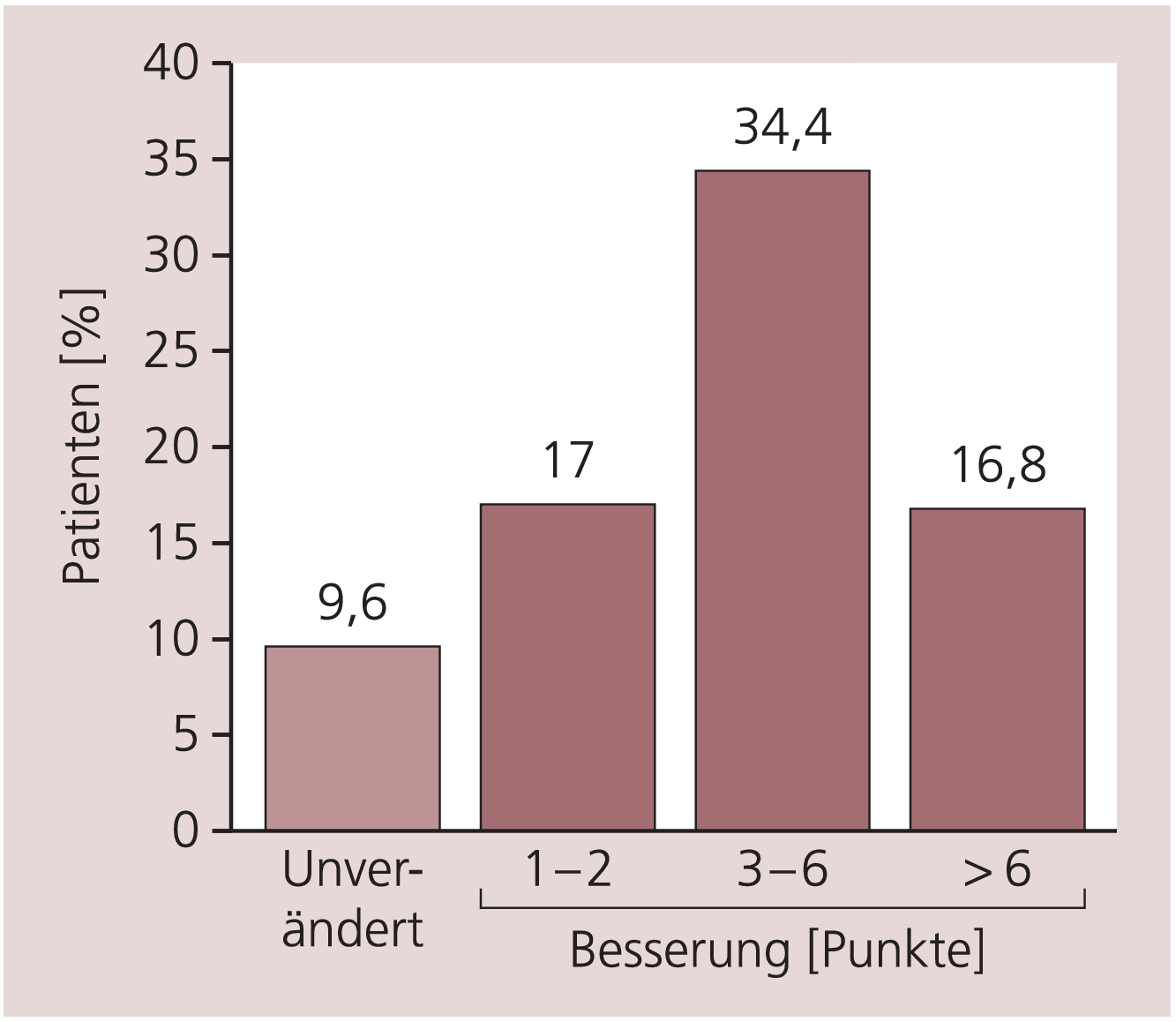
Abb. 2. Responder-Analyse: Patienten [%] mit einer Stabilisierung oder Verbesserung (1 bis ≥6 Punkte) im Mini-Mental-Status-Test (MMST) nach sechs Monaten Behandlung im Vergleich zur Ausgangsuntersuchung
Anmerkung: Standardabweichungen sind nicht berechnet worden
Bei der Nurses’ Observation Scale for Geriatric Patients konnte in allen sechs Dimensionen nach drei und sechs Monaten eine signifikante Verbesserung im Vergleich zum Ausgangswert beobachtet werden (Tab. 2).
Tab. 2. Verbesserung der Nurses’ Observation Scale for Geriatric Patients (NOSGER)-Items nach drei und sechs Monaten Behandlung (Abnahme = Verbesserung; IADL = Instrumental activities of daily living, ADL = Activities of daily living)
|
NOSGER-Item |
Mittlere Veränderung der NOSGER-Scores |
|
|
3 Monate |
6 Monate |
|
|
Gedächtnis |
–0,8±2,38 |
–1,1±2,92 |
|
IADL |
–0,6±2,41 |
–0,9±3,02 |
|
ADL |
–0,3±2,34 |
–0,6±2,86 |
|
Stimmung |
–1,1±2,76 |
–1,5±3,15 |
|
Sozialverhalten |
–0,8±2,60 |
–1,3±3,19 |
|
Störendes Verhalten |
–0,7±2,43 |
–1,2±2,79 |
Eine vergleichende Darstellung anhand der Medianveränderungen, die aus der Gesamtpunktzahl der im Explorationsmodul Demenz repräsentierten Einzeldimensionen errechnet wurden, zeigte eine sowohl in der Patienten- als auch in der Fremdeinschätzung durch die Angehörigen signifikante Veränderung der alltagsbezogenen Leistungseinschätzung sowohl für kognitive als auch für stimmungs- und verhaltensrelevante Bereiche.
Des Weiteren wurden sowohl für Mini-Mental-Status-Test als auch für Nurses’ Observation Scale for Geriatric Patients und Explorationsmodul Demenz Effektstärken über die Differenzen zwischen den unterschiedlichen Beobachtungszeitpunkten berechnet. Hierbei wurde die Differenz der Baseline-Daten zu den Ergebnissen der Zwischenmessung nach drei Monaten (Intervalleffekt für Nurses’ Observation Scale for Geriatric Patients und Mini-Mental-Status-Test) oder am Ende des Beobachtungszeitraums (Haupteffekt für Nurses’ Observation Scale for Geriatric Patients, Mini-Mental-Status-Test und Explorationsmodul Demenz) ins Verhältnis gesetzt. Für die Nurses’ Observation Scale for Geriatric Patients zeigten sich die deutlichsten Wirkungen bei „Stimmung“ und „störendem Verhalten“; im Mini-Mental-Status-Test trugen insbesondere „Orientierung“ und „Erinnerungsfähigkeit“ zur Wirkung bei. Im Explorationsmodul Demenz zeigte sich vor allem in der Dimension „Sozialverhalten“ sowohl in der Selbst- als auch in der Fremdeinschätzung die deutlichste Wirkung.
In der Gesamtbeurteilung durch den behandelnden Arzt wurde für 78,8% der Patienten eine Stabilisierung und eine Verbesserung der Symptomatik nach sechsmonatiger Therapie erreicht (Abb. 3). Bei der Beurteilung der kognitiven Leistungsfähigkeit nach sechsmonatiger Behandlung mit Memantin wurde für 37,6% der Patienten eine sehr gute oder gute Wirkung und für 40,9% eine immerhin noch mäßige Wirkung angegeben. Bei 16,2% der Patienten wurde sie als schlecht bewertet. Ähnliche Ergebnisse wurden bei der Beurteilung der Wirksamkeit auf die Alltagsaktivitäten erzielt. Bei 47,7% wurde diese als sehr gut bis gut, bei 32,7% noch als mäßig und bei 12,6% der Erkrankten als schlecht bewertet (Abb. 4).
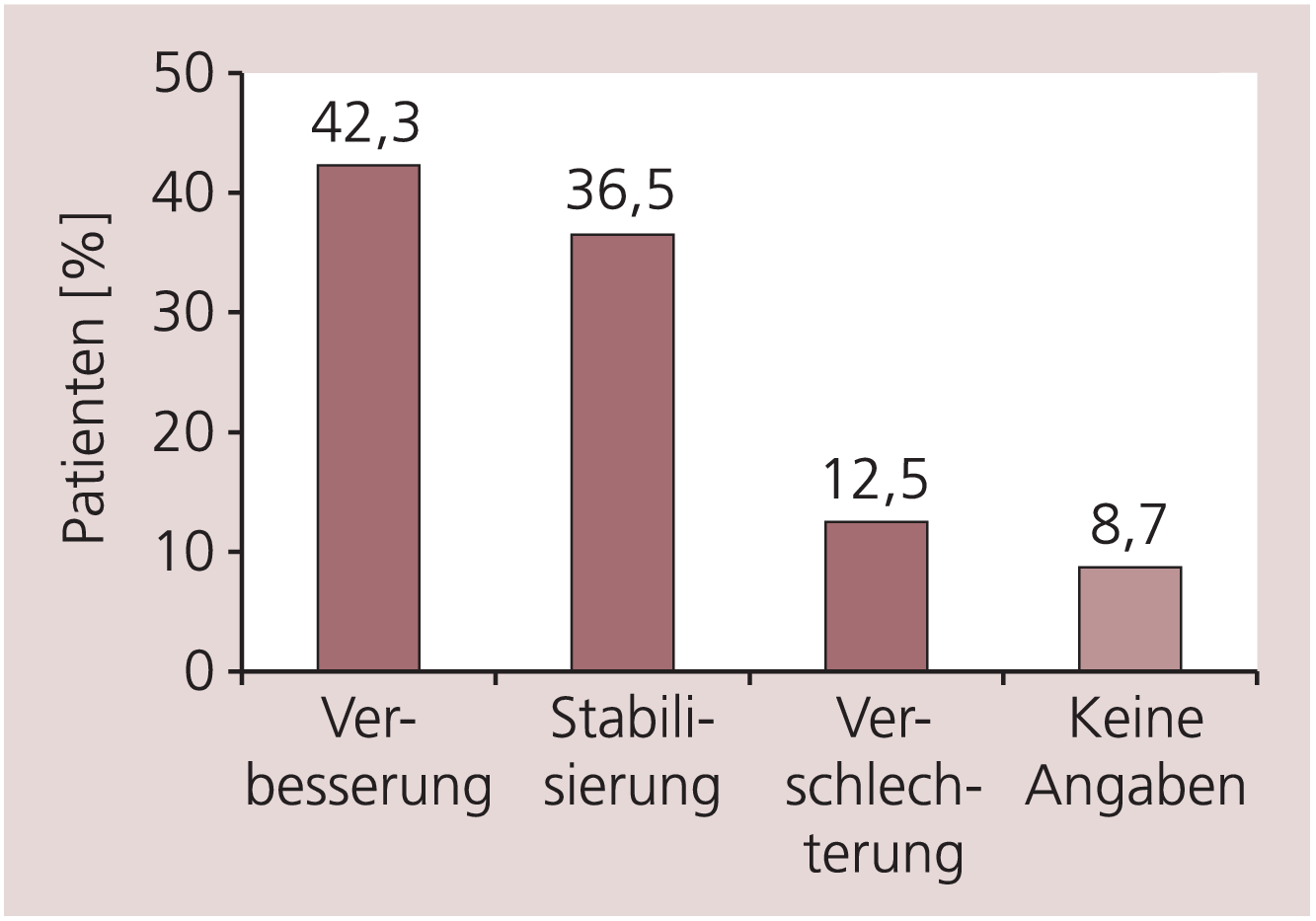
Abb. 3. Ergebnisse des klinischen Gesamturteils nach sechsmonatiger Behandlung
Anmerkung: Standardabweichungen sind nicht berechnet worden
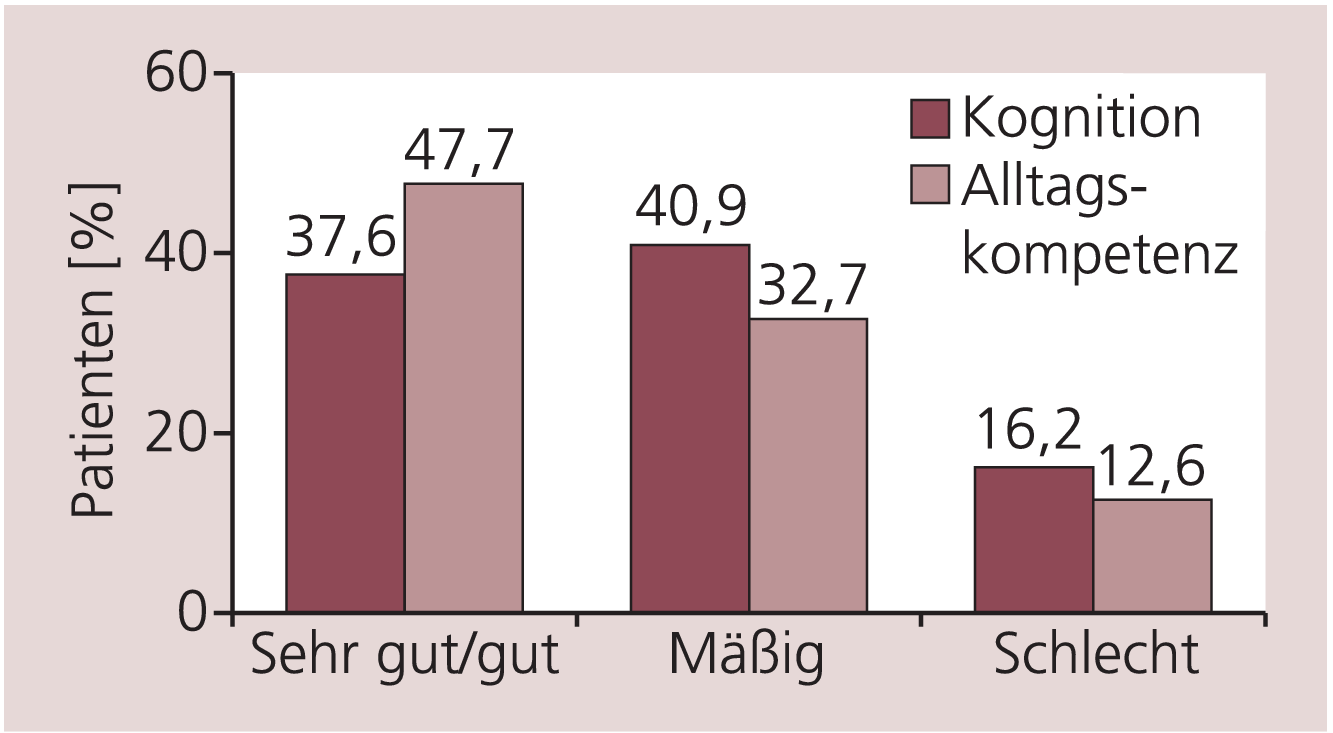
Abb. 4. Globale Beurteilung der Wirkung von Memantin auf die Kognition und Alltagsfunktionen nach sechsmonatiger Behandlung
Anmerkung: Standardabweichungen sind nicht berechnet worden
Bei 87 (4,7%) von 1845 Patienten trat mindestens ein unerwünschtes Ereignis auf. Insgesamt wurden 224 unerwünschte Ereignisse dokumentiert. Bei 58% der unerwünschten Ereignisse wurde kein Zusammenhang mit der Memantin-Behandlung gesehen. Die beobachteten Ereignisse zeigten keine besonderen Auffälligkeiten. Symptome aus dem psychiatrischen (1,8%) und neurologischen (1,7%) Bereich standen im Vordergrund. Alle anderen Organsysteme waren mit <1% betroffen. Die häufigsten unerwünschten Ereignisse (>0,2%) sind in Tabelle 3 aufgeführt. Als schwerwiegende unerwünschte Ereignisse wurden 2,7% klassifiziert, wobei der Großteil dieser Klassifizierungen auf eine Krankenhauseinweisung aufgrund einer Verschlechterung des Allgemeinzustands oder bestehender Begleiterkrankungen zurückzuführen war. Bei 87,8% der Patienten mit schwerwiegenden unerwünschten Ereignissen wurde kein Zusammenhang mit der Therapie gesehen.
Tab. 3. Anteil der Patienten [%] mit unerwünschten Ereignissen (aufgeführt sind die unerwünschten Ereignisse mit einer Inzidenz >0,2%)
|
Unerwünschtes Ereignis |
Patienten [%] |
|
Ruhelosigkeit |
0,5 |
|
Schwindel |
0,4 |
|
Pneumonie |
0,4 |
|
Verschlechterung der Demenz |
0,4 |
|
Verwirrtheit |
0,3 |
|
Zerebro-vaskuläre Ereignisse |
0,3 |
|
Herzinsuffizienz |
0,3 |
|
Aggressivität |
0,3 |
|
Dehydration |
0,3 |
|
Übelkeit |
0,2 |
|
Paranoia |
0,2 |
|
Erregung |
0,2 |
|
Harnwegsinfekte |
0,2 |
Während der Anwendungsbeobachtung verstarben 24 von 1848 Patienten (1,3%). Als häufigste Ursache wurden Herz-Kreislauf-Erkrankungen, Apoplex, Pneumonie und Verschlechterung des Allgemeinzustands oder Altersschwäche angegeben. Bei 23 Patienten waren anamnestisch Herz-Kreislauf-Erkrankungen, Diabetes mellitus, Arteriosklerose und/oder Zustand nach Apoplex dokumentiert. Bei keinem der Fälle wurde die Einnahme von Memantin als Ursache gesehen.
Die gute Verträglichkeit von Memantin spiegelt sich auch in der Globalbeurteilung durch den behandelnden Arzt wider: Bei 63% der Patienten wurde diese als sehr gut und bei 30% als gut bewertet.
Diskussion
In der hier vorliegenden Beobachtungsstudie konnte die Wirksamkeit und Verträglichkeit von Memantin an einem heterogenen Patientenkollektiv nachgewiesen werden.
Während die klinische Erprobung eines Arzneimittels an einer relativ geringen Zahl von Patienten durchgeführt wird, die zudem unter verschiedenen Aspekten für die klinische Prüfung besonders ausgewählt wurden, spiegeln die Ergebnisse von Anwendungsbeobachtungen die tägliche Praxis besser wider. Die Ein- und Ausschlusskriterien sind weiter gefasst und insofern „naturalistischer“. Damit können seltene oder sehr seltene unerwünschte Wirkungen, Wechselwirkungen oder andere Gefahren im Zusammenhang mit der Arzneimittelanwendung in Anwendungsbeobachtungen häufiger erkannt werden. Die Kenntnisse über Wirksamkeit, Sicherheit und Interaktionen sind zum Zeitpunkt ihrer erstmaligen Zulassung unvollständig. Da sich neue Erkenntnisse über die Sicherheit von Arzneimitteln auch noch lange Zeit nach ihrer Zulassung ergeben können und selbst bei hinlänglich bekannten Substanzen etwaige Wechselwirkungen auch von neuen Entwicklungen in der medizinischen Wissenschaft abhängen, erschien eine breit angelegte Studie mit einer repräsentativen Patientenstichprobe sinnvoll. Schließlich sieht das Arzneimittelgesetz der Bundesrepublik Deutschland vor, dass nach der Zulassung eines Arzneimittels die Erfahrungen bei seiner Anwendung im Sinne einer Pharmakovigilanz fortlaufend und systematisch gesammelt und ausgewertet werden.
Im Laufe der sechsmonatigen Behandlungsphase konnte bei den Patienten mit Alzheimer-Demenz eine Stabilisierung und Verbesserung im Mini-Mental-Status-Test dokumentiert werden. Am Ende der Beobachtungsphase hatte sich der MMST-Wert um 2,5±4,5 Punkte im Vergleich zum Ausgangswert signifikant verbessert. Eine Responder-Analyse zeigte darüber hinaus, dass sich 68% der Patienten im Mini-Mental-Status-Test verbesserten. Han et al. [9] konnten in einer Metaanalyse zeigen, dass bei unbehandelten Patienten der Punktwert im Mini-Mental-Status-Test jährlich um 3,3 abnimmt. Dem entgegen stieg der mittlere MMST-Wert in der hier diskutierten Untersuchung um 2,5 Punkte und deutet somit auf eine deutliche Verbesserung der kognitiven Symptome hin. Auch die Ergebnisse der Nurses’ Observation Scale for Geriatric Patients weisen auf eine Verbesserung des Gedächtnisses, der Alltagsaktivitäten und des Verhaltens hin. In den Bereichen Stimmung und Sozialverhalten war der Effekt am deutlichsten ausgeprägt und im Vergleich zum Ausgangswert statistisch signifikant. Darüber hinaus konnte dieser positive Effekt nach einem halben Jahr in den genannten Dimensionen sogar noch deutlicher dargestellt werden.
Damit konnte mit dem vorliegenden Therapieansatz ein vergleichbarer Effekt erzielt werden, wie er unter cholinerger Therapie dokumentiert ist [8].
Die mittleren Explorationsmodul Demenz-Scores zeigten nach der sechsmonatigen Beobachtungsphase sowohl für die Selbst- als auch für die Fremdbeurteilung einen leichten Rückgang, der als Abnahme der alltagsbezogenen Symptombelastung gewertet werden kann. Interessant erscheint hierbei, dass die zu beiden Messzeitpunkten von den Bezugspersonen a priori als stärker beeinträchtigt eingestuften Alltagsfunktionen am Ende des Beobachtungszeitraums in der Fremdbeurteilung ebenfalls eine deutlichere Symptombesserung erfuhren. Dies kann auf eine objektive Reduktion des Pflegeaufwands aufgrund der Interventionen zurückzuführen sein.
Die klinische Relevanz der Ergebnisse wurde anhand der Globalbeurteilungen bestätigt. Sowohl die Beurteilung des klinischen Gesamteindruckes als auch die der Wirksamkeit von Memantin auf die Kognition oder die Alltagsfunktionen zeigten deutlich, dass die im Mini-Mental-Status-Test, Nurses’ Observation Scale for Geriatric Patients und Explorationsmodul Demenz gemessenen Effekte auch für den behandelnden Arzt sichtbar waren.
In kontrollierten klinischen Studien über sechs Monate konnte gezeigt werden, dass es unter der Therapie mit Memantin zu einer Stabilisierung oder einer Verbesserung der Symptome kam [12, 13, 16]. Die hier diskutierte Anwendungsbeobachtung bestätigt, dass die in klinischen Studien gezeigten Effekte für den praktischen Alltag von Bedeutung sind. Diese sind jedoch bei Patienten mit fortgeschrittener Demenz nicht immer mit objektiven, an der kognitiven Leistungsfähigkeit orientierten Erhebungsinstrumenten darzustellen, da Bodeneffekte zu erwarten sind. Andererseits mag aus denselben Gründen eine Selbsteinschätzung etwaiger Defizite ebenfalls zu Verzerrungen führen. Tatsächlich zeigt sich gerade anhand der vorliegenden Explorationsmodul-Demenz-Ergebnisse, dass die subjektive Einschätzung seitens der Patienten und Angehörigen deutlich differieren kann. Umso wichtiger erscheint es bei weiter fortgeschrittenen Demenzen mit einer eingeschränkten Urteilsfähigkeit der Patienten, zur Darstellung eines Wirksamkeitsnachweises neben kognitiven auch verhaltensbezogene und insbesondere alltags- und pflegerelevante Beurteilungsdimensionen heranzuziehen.
Die Verträglichkeit einer antidementiven Therapie ist im Hinblick auf die Komorbidität der Patienten und der dadurch bedingten Komedikation besonders wichtig. 74,4% der in diese Beobachtungsstudie eingeschlossenen Patienten litten unter mindestens einer Begleiterkrankung, wobei Herz-Kreislauf-Erkrankungen mit 60,7% am häufigsten genannt wurden. Dementsprechend wurde bei 65,4% der Patienten eine Komedikation gegeben. Bei 4,7% der Patienten trat mindestens ein unerwünschtes Ereignis auf, was aufgrund des allgemeinen Gesundheitszustands der Patienten als gering zu werten ist. Keines der unerwünschten Ereignisse trat häufiger als 0,5% auf, wobei die auftretenden unerwünschten Ereignisse dem Spektrum der in klinischen Studien berichteten unerwünschten Ereignisse entsprechen, die Inzidenz jedoch deutlich geringer ist [7, 13]. Bei 1,3% der Patienten, die im Laufe dieser sechsmonatigen Anwendungsbeobachtung verstarben, lagen zu Beginn der Therapie anamnestisch Herz-Kreislauf-Erkrankungen, Diabetes mellitus, Arteriosklerose und/oder ein Apoplex vor, was der Häufigkeit in klinischen Studien [13] und der zu erwartenden Todesfälle aufgrund der Altersstruktur und der damit einhergehenden hohen Anzahl an Patienten, die zusätzlich mindestens eine weitere Erkrankung aufwiesen, entspricht [14].
Die Ergebnisse dieser Anwendungsbeobachtung haben gezeigt, dass die in klinischen Studien nachgewiesenen Effekte von Memantin auch im Praxisalltag erreicht werden können. Vergleicht man die Ergebnisse dieser Studie mit der von Hager et al. [8] publizierten Anwendungsbeobachtung, in der die Wirksamkeit von Donepezil bei Alzheimer-Demenz über einen Zeitraum von drei Monaten untersucht wurde, so zeigt sich, dass Memantin nach dreimonatiger Therapie eine ebenso gute Wirksamkeit aufweist wie Donepezil, sich jedoch durch ein günstigeres Verträglichkeitsprofil auszeichnet, welches auch über einen für Anwendungsbeobachtungen konventionellen Studienzeitraum hinaus und ohne Wirksamkeitsverlust aufrechterhalten wird.
Zusammengenommen zeigen die Ergebnisse der hier vorgestellten Anwendungsbeobachtung, dass Memantin aufgrund der guten Wirksamkeit, bei geringen Wechselwirkungen und guter Verträglichkeit, eine geeignete Therapieoption sowohl für kognitive als auch für nicht-kognitive Beeinträchtigungen bei mittelschwerer bis schwerer Alzheimer-Demenz darstellt. Die durch diese Intervention erzielten positiven Ergebnisse zeigen sich anhand realitätsnaher Erhebungsinstrumente und lassen sich in einem praxisrelevanten Behandlungsalltag darstellen.
Literatur
1. Bickel H. Demenzsyndrom und Alzheimer-Krankheit: Eine Schätzung des Krankenbestandes und der jährlichen Neuerkrankungen in Deutschland. Gesundheitswesen 2000;62:211–8.
2. Danysz W, Parsons CG, Möbius HJ, Stöffler A, et al. Neuroprotective and symptomatological action of memantine relevant for Alzheimer’s disease – A unified glutamatergic hypothesis on the mechanism of action. Neurotox Res 2000;2:85–97.
3. Danysz W, Parsons CG. The NMDA receptor antagonist memantine as a symptomatological and neuroprotective treatment for Alzheimer’s disease: preclinical evidence. Int J Geriatr Psychiatry 2003;18(Suppl 1):S23–32.
4. Davies KL, Maloney AJ. Selective loss of central cholinergic neurons in Alzheimer’s disease. Lancet 1976;2:1403.
5. Giacobini E. Cholinesterase inhibitors; from the calabar bean to Alzheimer therapy. In: Giacobini E (editor). Cholinesterase inhibitors. London: Martin Duniz, 2000:181–226.
6. Giacobini E. The cholinergic system in Alzheimer disease. Prog Brain Res 1990;84:321–2.
7. Graham SM, Jonas JM, Lee GS, Goetz MA, et al. Memantine is safe for short- and long-term treatment of dementia. 9th International Conference on Alzheimer’s Disease and Related Disorders (ICAD) 2004.
8. Hager K, Calabrese P, Frölich L, Göbel C, et al. An observational clinical study of the efficacy and tolerability of donepezil in the treatment of Alzheimer’s disease. Dement Geriatr Cogn Disorder 2003;15:189–98.
9. Han L, Cole M, Bellavance F, McCusker J, et al. Tracking cognitive decline in Alzheimer’s disease using the mini-mental state examination: A meta-analysis. Int Psychogeriatr 2000;12:231–47.
10. Kornhuber J, Wellern M, Schoppmeyer K, Riederer P. Amantadine and memantine are NMDA receptor antagonists with neuroprotective properties. J Neural Transm 1994;43:91–104.
11. Müller WE, Mutschler E, Riederer P. Noncompetitive NMDA receptor antagonists with fast open-channel blocking kinetics and strong voltage-dependency as potential therapeutic agents for Alzheimer’s dementia. Pharmacopsychiatry 1995;28:113–24.
12. Peskind ER, Potkin SG, Pomara N, Ott B, et al. Memantine monotherapy is effective and safe for the treatment of mild to moderate Alzheimer’s disease: a randomized controlled trial. 17th Collegium Internationale Neuro-Psychopharmacologicum (CINP), Paris, 20. bis 24. Juni 2004.
13. Reisberg B, Doody R, Stöffler A, Schmitt F, et al. Memantine in moderate-to-severe Alzheimer’s disease. N Eng J Med 2003;348:1333–41.
14. Statistisches Bundesamt. Todesursachen in Deutschland 2003. In: Statistisches Bundesamt 2005, Fachserie 12, Reihe 4.
15. Tariot P, Farlow MR, Grossberg GT, Graham SM, et al. Memantine treatment in patients with moderate to severe Alzheimer disease already receiving donepezil: a randomized controlled trial. JAMA 2004;291:317–24.
16. Winblad B, Poritis N. Memantine in severe dementia: Results of the 9M-best study (Benefit and efficacy in severely demented patients during treatment with memantine). Int J Geriatr Psychiatry 1999;14:135–46.
Priv.-Doz. Dr. Pasquale Calabrese, Neurologische Universitätsklinik Bochum, Bereich Neuropsychologie, In der Schornau 23–25, 44829 Bochum, E-Mail: Pasquale.Calabrese@rub.de
Dr. Ute Essner, Lundbeck GmbH, Scientific Unit, Karnapp 25, 21079 Hamburg
Prof. Dr. med. Hans Förstl, Klinikum rechts der Isar der TU München, Klinik und Poliklinik für Psychiatrie und Psychotherapie, Ismaninger Str. 22, 81675 München
Memantine in clinical practice – Results of an observational study
In a post-marketing surveillance study, the efficacy and tolerability of memantine (Ebixa®) was examined in patients with moderate to severe Alzheimer’s disease (AD). Patients were treated with memantine 20 mg/day for six months. Memantine’s efficacy was evaluated using the Mini-Mental-State Examination (MMSE), the Nurses’ Observation Scale for Geriatric Patients (NOSGER) and the Explorations Module Dementia (EMD) scales, as well as by a global assessment by the physician. After six months of open label treatment with memantine, patients’ cognitive function, ability to perform daily activities, and global performance have been clearly improved. Also, memantine showed an excellent tolerability profile. The results of this naturalistic study support the significant efficacy and tolerability of memantine that has been previously demonstrated in randomised, controlled clinical Alzheimer dementia trials.
Keywords: Alzheimer’s disease, memantine, observational study, NMDA receptor antagonist
Psychopharmakotherapie 2006; 13(02)
