Ullrich Wüllner, Bonn
Nach wie vor stellt Levodopa den Goldstandard für die symptomatische Therapie der sporadischen Parkinson-Krankheit (Parkinson’s disease, PD) dar. Vor allem in der Langzeit-Therapie zeigen sich jedoch Probleme: nach fünf Jahren kommt es bei etwa 50% der Patienten unter Levodopa-Monotherapie zum Auftreten von Wirkungsschwankungen und motorischen Komplikationen, deren Ursache zumindest teilweise, möglicherweise auch vollständig, in den stark schwankenden Plasmaspiegeln von Levodopa und der daraus resultierenden pulsatilen Stimulation der zentralen postsynaptischen Dopamin-Rezeptoren zu suchen ist [4, 12, 15]. Abhängig von der Plasmahalbwertszeit der Präparate und der Frequenz der Einnahme können durch Unterdosierung bei abklingenden Plasmaspiegeln End-of-Dose-Akinesien sowie durch Wirkstoffakkumulation bei erneuter Einnahme Peak-Dose-Dyskinesien auftreten; langfristig tritt der Bezug zu den Plasmaspiegeln in den Hintergrund und es ist zu vermuten, dass Freezing-Phänomene und dystone Störungen ganz überwiegend durch die durch pulsatile Stimulation der Dopamin-Rezeptoren gestörte postsynaptische dopaminerge Transmission verursacht werden [5, 8]. Experimentelle Untersuchungen belegen, dass durch kontinuierliche Zufuhr dopaminerger Medikamente – dies gilt sowohl für Levodopa wie für Dopaminagonisten – das Auftreten von Wirkungsschwankungen und motorischen Komplikationen vermindert wird, und bereits vorhandene Dyskinesien reduziert werden [1, 3, 10]. Ein weiterer wichtiger Mechanismus ist in der sekundär gestörten glutamatergen Transmission der striatalen Neuronen zu suchen [4, 9].
Wirkungsschwankungen und motorische Komplikationen können in der klinischen Praxis durch den Einsatz von Dopaminagonisten signifikant reduziert werden. Daher lautet die Empfehlung der Deutschen Gesellschaft für Neurologie für Patienten mit biologischem Alter von weniger als 70 Jahren, eine Monotherapie mit Dopaminagonisten anzustreben (Leitlinien der DGN: www.dgn.org). Für den frühen Einsatz dieser Substanzen spricht in erster Linie, dass motorische Spätkomplikationen seltener auftreten und dass die Levodopa-Dosis reduziert oder der Einsatz von Levodopa hinausgezögert werden kann. Zwar werden für Dopaminagonisten neuroprotektive Effekte diskutiert, doch ist weitgehend unklar, ob hierfür spezifische antioxidative Eigenschaften einzelner Substanzen verantwortlich sein könnten, ob es sich um einen Substanzklasseneffekt handelt, oder die Ergebnisse der bildgebenden (PET- bzw. SPECT-) Studien durch Sekundäreffekte beeinflusst sein könnten [6, 15, 18]. Seit langem ist umstritten, ob Levodopa selbst toxische Effekte haben könnte. Diese Frage konnte jedoch auch die eigens zu diesem Zweck aufgelegte ELLDOPA-Studie nicht abschließend klären. Unerwartet hatte sich bei dieser Untersuchung ein positiver Verlauf der Levodopa-behandelten Patienten gezeigt, der die Auswaschphase überdauerte [6]. Berücksichtigt man weiterhin die in mehreren Studien nachgewiesene bessere Lebensqualität der Levodopa-behandelten Patienten, so muss die Leitlinien-Empfehlung zur Behandlung mit Dopaminagonisten durchaus kritisch gesehen werden. Mit ähnlich guten wissenschaftlichen Argumenten kann für die ganz überwiegende Zahl von Patienten auch eine Kombinationstherapie mit Levodopa und Dopaminagonisten gefordert werden.
Die verschiedenen Dopaminagonisten unterscheiden sich in ihrer molekularen Struktur, Halbwertszeit und Rezeptor-Spezifität. Eine grundsätzliche Unterscheidung muss dabei zwischen Ergot- und Nicht-Ergot-Substanzen getroffen werden. Ergot-Alkaloide binden nicht nur an Dopamin-, sondern auch an Noradrenalin- und Serotonin-Rezeptoren, während die meisten Non-Ergot-Derivate sehr spezifisch an Dopamin-D2-, -D3- und teilweise auch -D4-Rezeptoren binden. Unklar ist gegenwärtig noch, ob die Ergot-Alkaloide tatsächlich in großem Umfang Herzklappenfibrosen verursachen können, wie es die kürzlich erschienene Arbeit von van Camp und Mitarbeitern vermuten lässt [17]. Der Pathomechanismus der unter Pergolid beobachteten fibrotischen Reaktionen ist unklar; für den vermuteten Effekt der Serotonin-Rezeptoraffinität von Pergolid fehlt bis jetzt eindeutige Evidenz.
Auch für die Dopaminagonisten gilt wie für jede Form der dopaminergen Therapie, dass grundsätzlich eine möglichst kontinuierliche Stimulation der Dopamin-Rezeptoren angestrebt werden sollte, da die pulsatile Stimulation von Dopamin-Rezeptoren – weitgehend unabhängig von der jeweiligen dopaminergen Substanz – entscheidend für die Entwicklung motorischer Komplikationen zu sein scheint [3]. Untersuchungen an Patienten belegen, dass die physiologische, kontinuierliche dopaminerge Stimulation das Auftreten motorischer Komplikation bei der Behandlung der Parkinson-Krankheit verhindert und teilweise sogar bereits eingetretene Dyskinesien bessern kann: Kontinuierliche duodenale Infusion von Levodopa reduziert Dyskinesien ebenso wie kontinuierliche subkutane Infusion der Dopaminagonisten Lisurid und Apomorphin; beide Verfahren sind jedoch mit invasiven Maßnahmen verbunden und sehr kostenintensiv [10, 13]. Eine Alternative hierzu könnten transdermale Behandlungsstrategien (Pflaster) darstellen, mit denen eine konstante Wirkstofffreisetzung und kontinuierliche Rezeptor-Stimulation möglich ist.
Die transdermale Applikation ist im Gegensatz zur oralen Verabreichung unabhängig von Mahlzeiten, Gastroparesen oder Resorptionsstörungen. Ein First-Pass-Effekt tritt nicht auf, die Applikation ist einfach, nicht invasiv, und fördert die Compliance der Patienten durch Einmaldosierung und die geringere Zahl der oral einzunehmenden Tabletten. Durch den fehlenden First-Pass-Effekt ist die Bioverfügbarkeit des Wirkstoffs höher und die Plasma-Spiegel bleiben stabil. Somit ist diese Applikationsform insbesondere auch für Patienten mit Schluckstörungen und kognitiven Defiziten geeignet.
Pharmakokinetik und -dynamik von Rotigotin
Rotigotin ist ein Non-Ergot-Dopaminagonist, der speziell für die transdermale Applikation entwickelt wurde. Rotigotin bindet vorwiegend an D3- und D2-, D4- und D5-Dopamin-Rezeptoren (Tab. 1), und könnte somit zusätzlich zur motorischen Aktivität auch stimmungsaufhellende und antidepressive Effekte entfalten. Das Pflaster, das in verschiedenen Größen (etwa 3x3 bis 6x6 cm) und damit verschiedenen Wirkstärken (4,5–18 mg) verfügbar sein wird, wird 1x täglich gewechselt. Der vorwiegend lipophile Wirkstoff wird aus einer Silikon-Träger-Matrix kontinuierlich freigesetzt und penetriert die Haut direkt trans- und intrazellulär und durch Follikel und ekkrine Schweißdrüsen (Abb. 1). Pharmakokinetische Untersuchungen haben eine lineare Beziehung zwischen Dosis und Plasmaspiegeln gezeigt.
Tab. 1. Rezeptoraffinität von Rotigotin
|
Selektivität |
Spezifität |
||||
|
D1 |
+ |
Agonist |
5-HT1A |
++ |
Agonist |
|
D2 |
++ |
Agonist |
5-HT2B |
– |
(Antagonist) |
|
D3 |
++++ |
Agonist |
α2B |
++ |
Antagonist |
|
D4 |
+++ |
Agonist |
α2C |
+ |
Antagonist |
|
D5 |
+++ |
Agonist |
|||
+: Ki >500 nmol/l; ++: Ki 50–500 nmol/l; +++: Ki 5–50 nmol/l; ++++: Ki 0,5–5 nmol/l
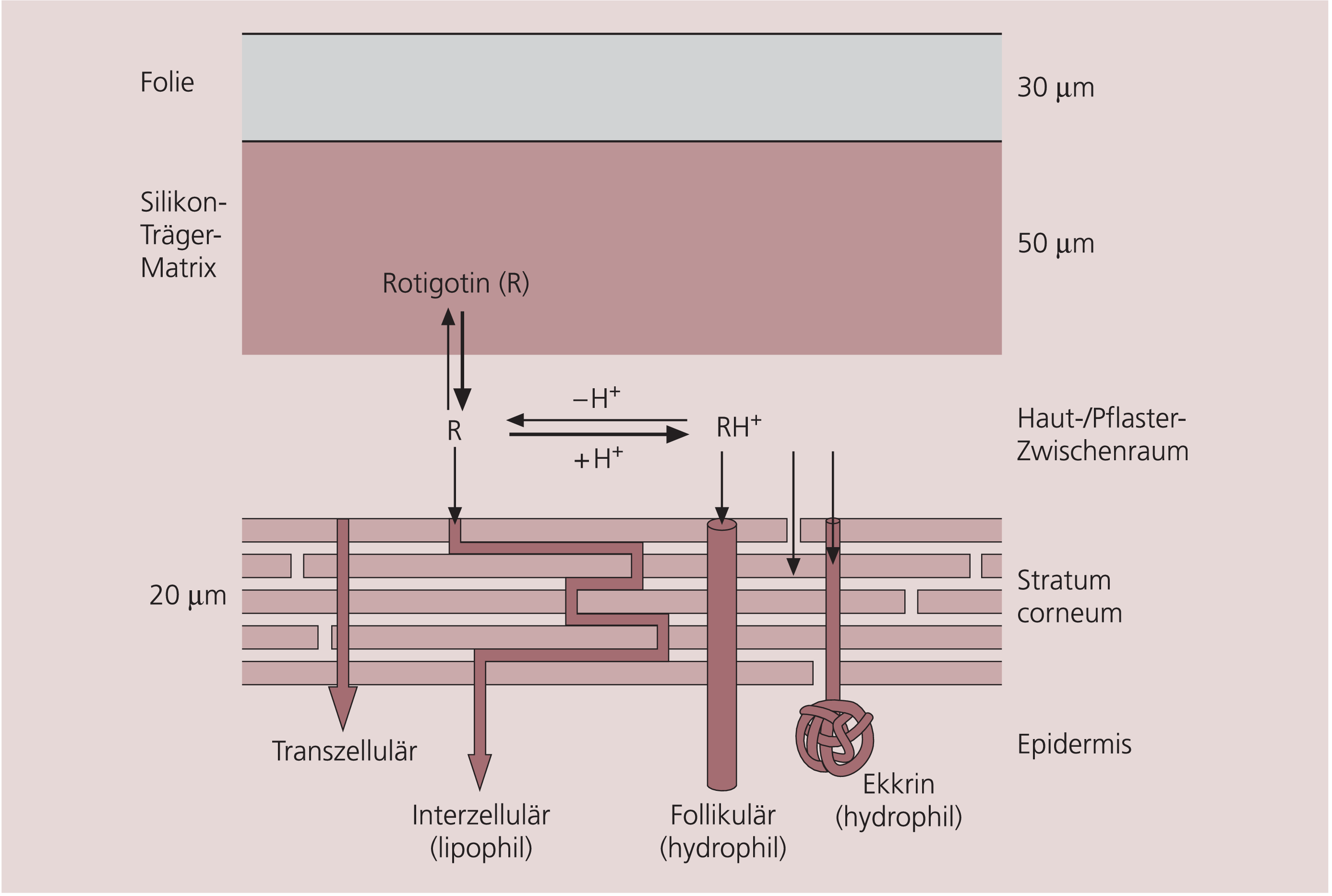
Abb. 1. Hautpenetration von Rotigotin
Rotigotin wird ganz überwiegend metabolisiert und renal und biliär eliminiert; die Halbwertszeit beträgt etwa 6 Stunden und durch die Formulierung der transdermal zu applizierenden Substanz in der Silikon-Träger-Matrix sind kontinuierliche Plasmaspiegel (Abb. 2) gewährleistet. Eine Akkumulation von Rotigotin ist bislang nicht beobachtet worden und durch Entfernen des Pflasters ist eine unkomplizierte und effiziente Therapie-Unterbrechung möglich.
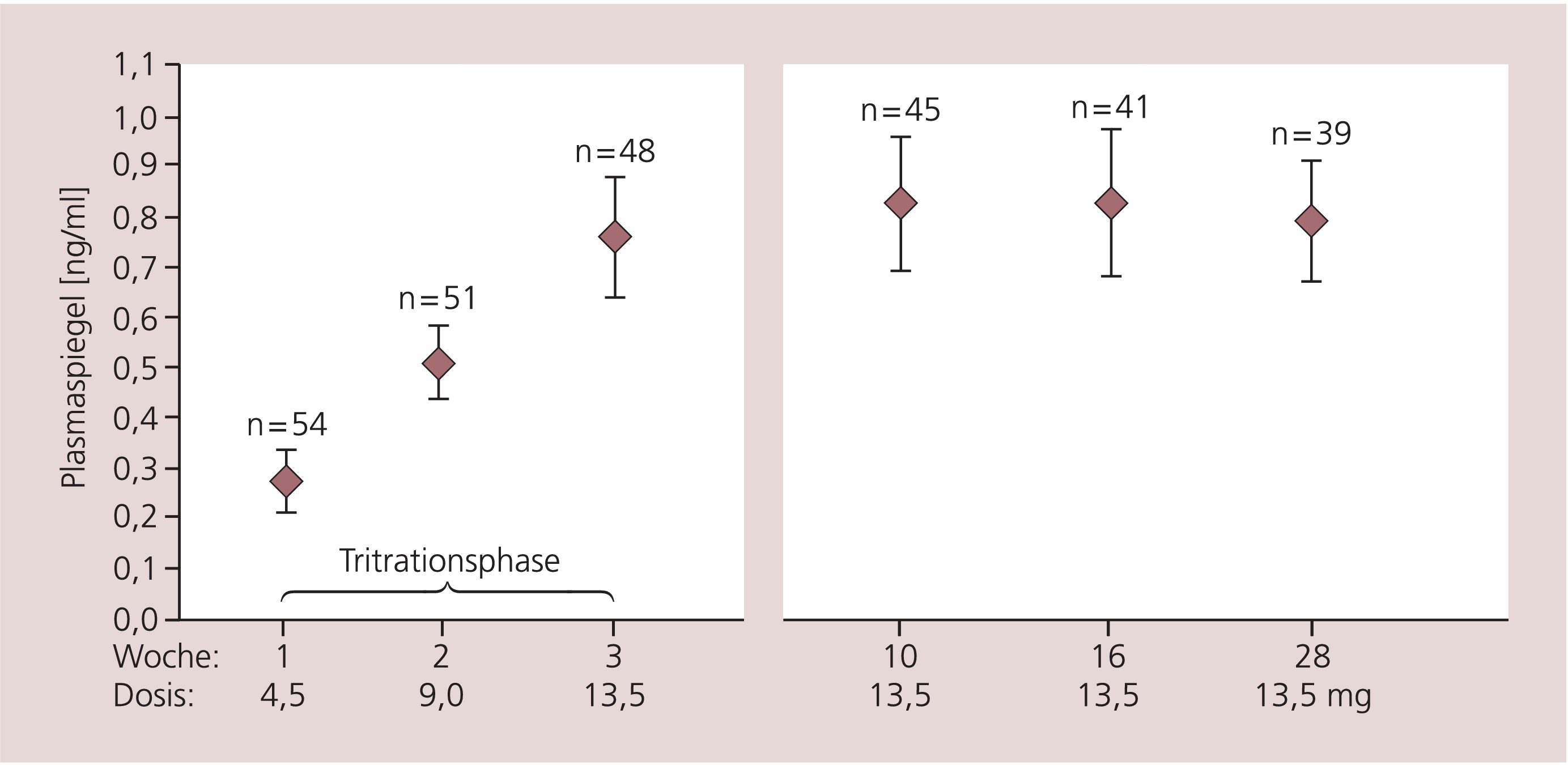
Abb. 2. Plasmaspiegel von Rotigotin nach transdermaler Applikation
Studienergebnisse
Wirksamkeit und Verträglichkeit von Rotigotin sind mittlerweile in einer Reihe von Phase-II- und -III-Studien, sowohl in der Monotherapie der frühen Parkinson-Krankheit, aber auch als ergänzende Therapie zusätzlich oder als Alternative zu Levodopa in späteren Krankheitsstadien untersucht worden. In einer der ersten randomisierten doppelblinden Studie an 242 Patienten mit Parkinson-Krankheit wurde die Substanz in Dosierungen von 4,5 bis 18 mg gegen Plazebo getestet. Dabei verbesserten sich die Messwerte für die Aktivitäten des täglichen Lebens und die motorischen Leistungen (UPDRS-II- und -III-Scores) bei den Dosierungen 13,5 und 18 mg signifikant gegenüber Plazebo (Abb. 3) bei vergleichbarem Nebenwirkungsprofil [14]. Erfreulich selten wurde über orthostatische Dysregulation oder Verwirrtheitszustände berichtet. In anderen Studien waren unerwünschte Nebenwirkungen unter der Behandlung mit Rotigotin mit denen anderer Dopaminagonisten vergleichbar; zu den häufigsten Nebenwirkungen zählten Übelkeit und Müdigkeit (38 vs. 15% bzw. 25 vs. 16%; gesamte „safety population“ vs. Plazebo) und überwiegend milde Hautreaktionen (37 vs. 14%; Tab. 2).
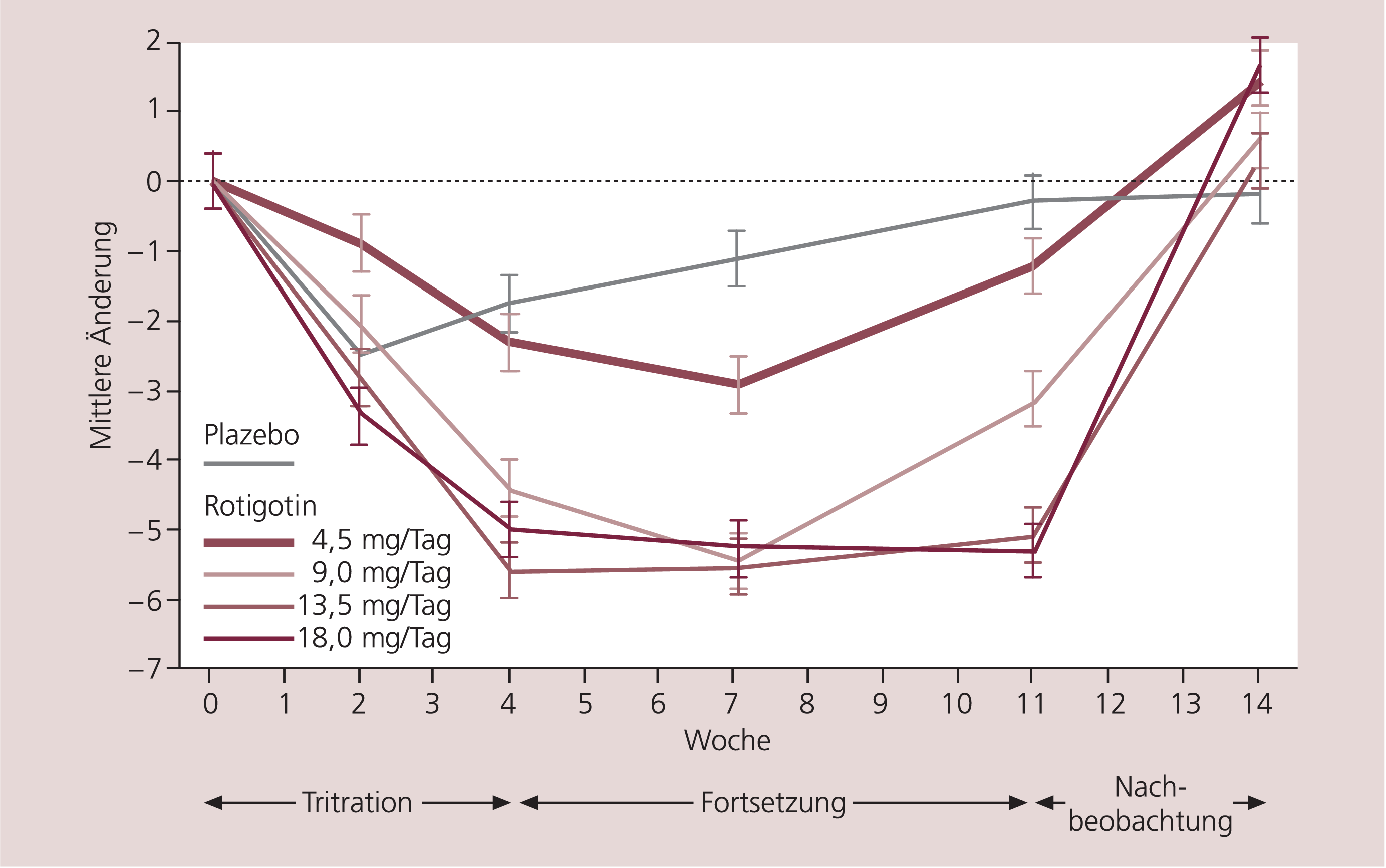
Abb. 3. Verbesserung der motorischen Funktionen und Aktivitäten des täglichen Lebens (UPDRS II + III)
Tab. 2. Nebenwirkungen
|
Rotigotin |
Plazebo |
|
|
Lokale Hautreaktion Deshalb Studie abgebrochen |
37%
|
14%
|
|
Übelkeit* |
38% |
15% |
|
Erbrechen |
13% |
2% |
|
Schläfrigkeit |
25% |
16% |
|
Schlaflosigkeit |
10% |
5% |
|
Benommenheit |
18% |
11% |
|
Kopfschmerzen |
14% |
10% |
|
Hypotension |
1% |
1% |
|
Halluzinationen |
2% |
1% |
*Einsatz von Domperidon war nicht erlaubt
In der Gesamtgruppe der bislang getesteten etwa 650 Patienten (Stand 08/05) kam es bei etwa 5% der Probanden zum Studienabbruch wegen Hautreaktionen. Die Häufigkeit von Hautreaktionen liegt damit in der Größenordnung anderer transdermal applizierbarer Pharmaka wie Fentanyl oder Nicotin [2, 7].
In einer vergleichenden Studie mit Parkinson-Patienten in fortgeschrittenem Stadium konnte ein deutliches Ansprechen mit Verbesserung der On-Zeit und Reduktion der Off-Zeit sowie eine Reduktion von Wirkungsschwankungen erzielt werden. In dieser Arbeit wurde eine kleine Gruppe von Patienten mit Wirkungsschwankungen und Dyskinesien über vier Wochen offen untersucht; Ziel war es Levodopa bei gleich bleibender Beweglichkeit einzusparen, dabei konnte im Mittel eine Reduktion der Levodopa-Dosis um 50% erzielt werden, bei gleichzeitiger Minderung der Off-Zeit bei 85% und Reduktion von Dyskinesien bei 70% der Patienten [16]. Nachdem in einer vorwiegend in Südafrika durchgeführten doppelblinden randomisierten Studie mit Rotigotin bei 274 Patienten mit fortgeschrittener Parkinson-Krankheit [11] eine ungewöhnlich gute Antwort auch der Plazebo-Gruppe beobachtet worden war, belegen die Daten einer jetzt in Nordamerika abgeschlossenen Studie, die kürzlich auf dem Kongress der EFNS vorgestellt wurde, eindeutig positive Wirkungen von Rotigotin auch bei dieser Patientengruppe [19].
Ausblick
Voraussichtlich im Frühjahr 2006 steht ein transdermal anwendbarer Dopaminagonist zur Verfügung, der sowohl in der Initialtherapie der Parkinson-Krankheit, aber auch in der Kombinationstherapie später Krankheitsstadien zur Anwendung kommen kann und, da unabhängig von Gastroparese oder Schluckstörungen, weitere Möglichkeiten, beispielsweise in der perioperativen Notfalltherapie und bei Patienten mit schlechter Compliance und kognitiven Defiziten verspricht.
Literatur
1. Baronti F, Mouradian MM, Davis TL, Giuffra M, et al. Continuous lisuride effects on central dopaminergic mechanisms in Parkinson’s disease. Ann Neurol 1992;32:776–81.
2. Bircher AJ, Howald H, Rufli T. Adverse skin reactions to nicotine in a transdermal therapeutic system. Contact Dermatitis 1991;25:230–6.
3. Blanchet PJ, Calon F, Martel JC, Bedard PJ, et al. Continuous administration decreases, pulsatile administration increases, behavioural sensitivity to a novel dopamine D2 agonist (U-91356A) in MPTP-exposed monkeys. J Pharmacol Exp Ther 1995;272:854–9.
4. Chase TN, Oh JD, Konitsiotis S. Antiparkinsonian and antidyskinetic activity of drugs targeting central glutamatergic mechanisms. J Neurol 2000;247(Suppl 2):II36–42.
5. Fabbrini G, Mouradian MM, Juncos JL, Schlegel J, et al. Motor fluctuations in Parkinson’s disease: central pathophysiological mechanisms. Ann Neurol 1988;24:366–78.
6. Fahn S, Oakes D, Shoulson I, Kieburtz K, et al.; Parkinson Study Group. Levodopa and the progression of Parkinson’s disease. N Engl J Med 2004;351:2498–508.
7. Hogan DJ, Maibach HI. Adverse dermatological reactions to transdermal drug delivery systems. J Am Acad Dermatol 1990;22;811–4.
8. Konitsiotis S, Blanchet PJ, Verhagen L, Lamers E, et al. AMPA receptor blockade improves levodopa-induced dyskinesia in MPTP monkeys. Neurology 2000;54:1589–95.
9. Löschmann PA, De Groote C, Smith L, Wüllner U, et al. Antiparkinsonian activity of Ro 25-6981, a NR2B subunit specific NMDA receptor antagonist, in animal models of Parkinson’s disease. Exp Neurol 2004;187:86–93.
10. Nilsson D, Nyholm D, Aquilonius SM. Duodenal levodopa infusion in Parkinson’s disease – long-term experience. Acta Neurol Scand 2001;104:343–8.
11. Quinn N. Rotigotin TDS (SPM962) – A multicenter, double-blind, randomized, placebo-controlled trial to assess the safety and efficacy of rotigotine TDS in patients with advanced Parkinson’s disease. Parkinsonism Relat Disord 2001;7(Suppl):P-TU-223.
12. Rascol O, Brooks DJ, Korczyn AD, De Deyn PP, et al. A five-year study of the insidence of dyskinesia in patients with early Parkinson’s disease who were treated with ropinirole or levodopa. 056 Study Group. N Engl J Med 2000;342:1484–91.
13. Stibe CM, Lees AJ, Kempster PA, Stern GM. Subcutaneous apomorphine in Parkinsonian on-off oscillations. Lancet 1988;1:403–6.
14. The Parkinson Study Group. A controlled trial of rotigotine monotherapy in early Parkinson’s disease. Arch Neurol 2003;60:1721–8.
15. The Parkinson Study Group. Pramipexole vs. levodopa as initial treatment for Parkinson disease: A randomized controlled trial. JAMA 2000;284:1931–8.
16. Verhagen Metman L, Gillespie M, Farmer C, Bibbiani F, et al. Continuous transdermal dopaminergic stimulation in advanced Parkinson’s disease. Clin Neuropharmacol 2001;24:163–9.
17. Van Camp G, Flamez A, Cosyns B, Weytjens C, et al. Treatment of Parkinson’s disease with pergolide and relation to restrictive valvular heart disease. Lancet 2004;363:1179–83.
18. Whone AL, Watts RL, Stoessl AJ, Davis M, et al.; REAL-PET Study Group. Slower progression of Parkinson’s disease with ropinirole versus levodopa: The REAL-PET study. Ann Neurol 2003;54:93–101.
19. LeWitt P, Chang FL, Fazzini E, Nausieda PA, et al. Rotigotine transdermal system in treatment of patients with advanced-stage Parkinson’s disease. EFNS 2005, Athen, 17. bis 20. September 2005.
Prof. Dr. med. Ullrich Wüllner, Klinik und Poliklinik für Neurologie, Universitätsklinikum Bonn, Sigmund-Freud-Str. 25, 53105 Bonn, E-Mail: Ullrich.Wuellner@ukb.uni-bonn.de
Transdermal rotigotine therapy in Parkinson‘s disease
Long-term therapy of Parkinson’s disease with the currently available drugs, especially the gold standard levodopa, is compromised by the occurrence of motor complications (end-of-dose-akinesia, freezing, dyskinesia). Pulsatile stimulation of dopamine-receptors represents a pathophysiologically important mechanism and the consequent use of dopamine agonists reduces the risk to develop motor complications.
Rotigotine is a non-ergot dopamine agonist, which was developed as a transdermally applicable compound. Formulated within a silicone-based patch, rotigotine provides constant plasma levels and stimulates dopamine-receptors continuously. Recent studies showed efficacy and few side effects, opening a new avenue for the treatment of Parkinson’s disease.
Keywords: Dopamine agonist, transdermal silicone-based patch, continuous receptor stimulation
Psychopharmakotherapie 2005; 12(06)
