Lutz Lachenmayer, Hamburg, und Peter Riederer, Würzburg
Rasagilin (N-Propargyl-1-[R]-aminoindan) ist ein selektiver irreversibler MAO-B-Hemmer der zweiten Generation. Die Spezifität der MAO-B-Hemmung ist in vitro und in vivo gut belegt; die MAO-B-Hemmung ist bis zu 100fach stärker als die MAO-A-Hemmung [6, 11, 15, 29]. Rasagilin hemmt die MAO-B 5- bis 10fach stärker als das bisher verfügbare Selegilin [29, 31].
Rasagilin wird im Gastrointestinaltrakt resorbiert und passiert rasch die Blut-Hirn-Schranke. Seine Bioverfügbarkeit beträgt etwa 36% und wird durch Mahlzeiten nicht beeinträchtigt. Wie Selegilin wird auch Rasagilin in der Leber metabolisiert. Bei Selegilin entstehen dabei Desmethyl-Selegilin und Amphetamin sowie Metamphetamin. Der Rasagilin-Metabolit ist Aminoindan, das keine vasoaktiven Effekte, wahrscheinlich aber neuroprotektive Potenzen hat [1, 25, 27].
Die kurze Halbwertszeit von Rasagilin (0,6–2 h) ist für die klinische Anwendung auch bei einmal täglicher Applikation ohne Bedeutung, da nach irreversibler Hemmung die Wiederherstellung der MAO-Aktivität von der Syntheserate des Enzyms bestimmt wird [24,30].
Die neuroprotektive Potenz von Rasagilin ist in verschiedenen In-vitro- und In-vivo-Modellen belegt (Übersicht bei [18, 31]). Rasagilin schützt vor der Toxizität von 6-Hydroxydopamin (6-OHDA; [3]) und Methylphenyltetrahydropyridin (MPTP; [16]) sowie vor der Glutamattoxizität in Kulturen hippokampaler Neuronen [12], vermindert das Ausmaß einer zerebralen und renalen Ischämie in der hypertensiven Ratte [9] und hat neuroprotektive Effekte gegen die Schädigung von zerebellären Körperzellen durch verschiedene Substanzen [4]. Der Rasagilin-Metabolit Aminoindan wirkt einer Neuroprotektion nicht entgegen (im Gegensatz zum Selegilin-Metaboliten Metamphetamin) und hat offenbar eigene neuroprotektive Eigenschaften [2].
Wirksamkeit von Rasagilin
Die symptomatische Wirksamkeit von Rasagilin ist für frühe und späte Stadien der Parkinson-Krankheit durch randomisierte Studien gut belegt (TEMPO-, PRESTO-, LARGO-Studie) [20–23].
Rasagilin in der Frühphase der Parkinson-Krankheit
In der TEMPO-Studie [20] wurden 404 Parkinson-Patienten mit knapp einjährigem Krankheitsverlauf, die noch keine dopaminerge Medikation benötigten, in drei Gruppen randomisiert (Plazebo, 1 mg/Tag Rasagilin, 2 mg/Tag Rasagilin). Nach einer Woche Eintitrierung (die 2-mg-Gruppe erhielt in der ersten Woche nur 1 mg/Tag Rasagilin) folgte eine Studienphase von 25 Wochen. Primäres Bewertungskriterium war die Änderung des UPDRS-Gesamtscores (Unified Parkinson’s disease rating scale). Nach 26 Wochen war der UPDRS-Gesamtwert in der 1-mg-Gruppe um 4,20 Punkte und in der 2-mg-Gruppe um 3,56 Punkte im Vergleich zu Plazebo verbessert (motorischer Subscore –2,71 bzw. –1,68; ADL-Subscore [Alltagsaktivitäten] –1,04 bzw. –1,22); zusätzlich hatten sich Parameter der Lebensqualität signifikant gebessert (–2,91 bzw. –2,74). Signifikante Wirkungsunterschiede zwischen der 1-mg- und 2-mg-Rasagilin-Dosis bestanden nicht.
Nach Auswertung der 6-Monats-Ergebnisse der TEMPO-Studie [20] wurden in einer zweiten Studienphase die Patienten der Plazebo-Gruppe für weitere 6 Monate mit 2 mg/Tag Rasagilin weiterbehandelt („delayed start“) [21]. Nach einem Jahr war der UPDRS-Gesamtwert in der Gruppe mit verzögertem Behandlungsbeginn (6 Monate Plazebo, dann 6 Monate 2 mg/Tag Rasagilin) um 2,29 Punkte schlechter im Vergleich zu der Gruppe, die von vornherein (12 Monate) 2 mg/Tag Rasagilin erhalten hatte (Abb. 1). In einer offenen Verlängerung der Studie waren die Vorteile einer frühen Behandlung mit Rasagilin auch nach 6,5 Jahren noch nachweisbar [14].
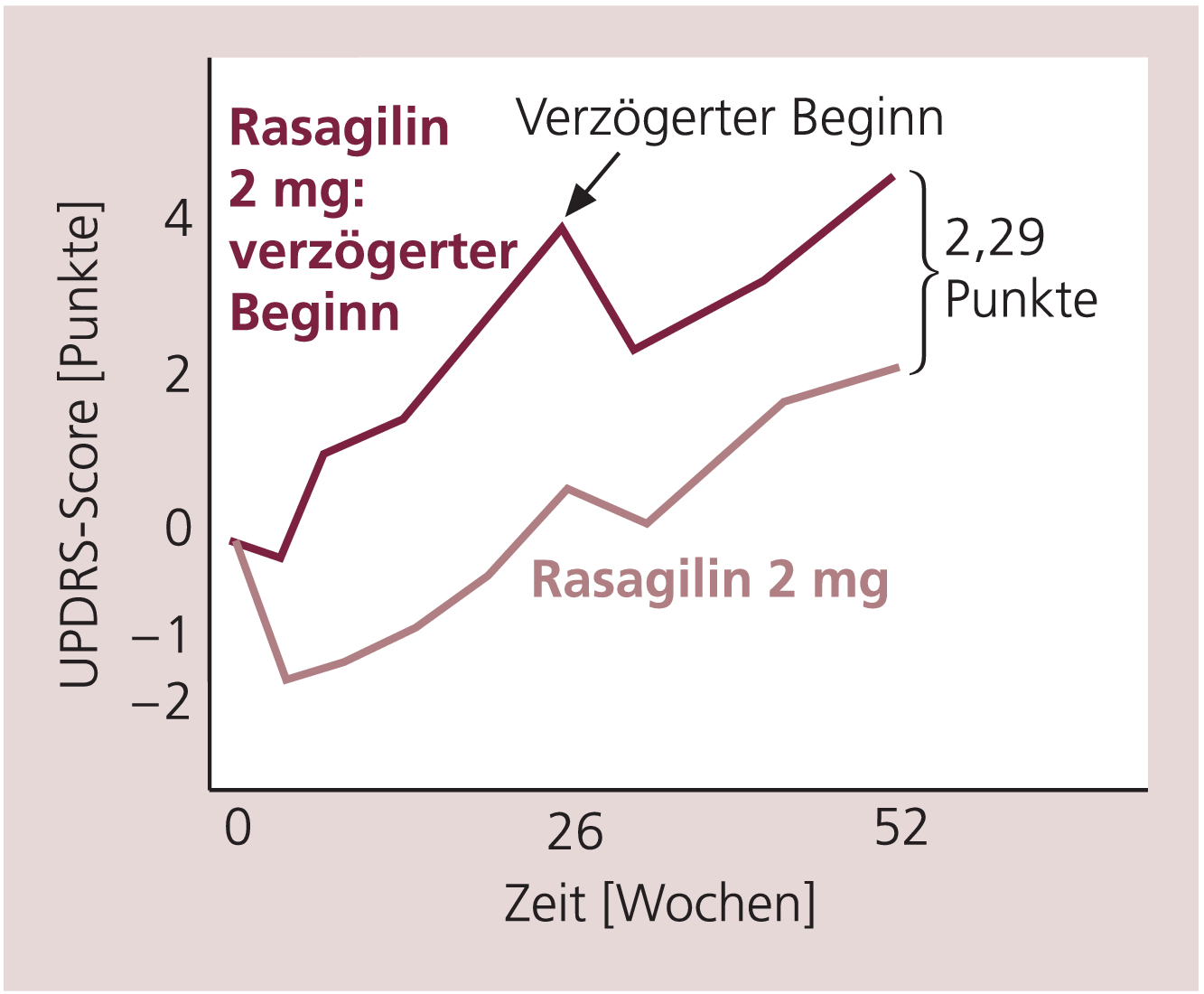
Abb. 1. TEMPO-Studie: Änderung des UPDRS-Scores unter 52-wöchiger Behandlung mit 2 mg/Tag Rasagilin oder bei verzögertem Behandlungsbeginn (26 Wochen Plazebo, danach 26 Wochen 2 mg/Tag Rasagilin). Die Gruppe mit verzögertem Behandlungsbeginn („delayed start“) ist nach 52 Wochen um 2,29 UPDRS-Punkte schlechter [mod. nach 21].
Im Falle eines ausschließlich symptomatischen Effekts von Rasagilin wäre zu erwarten, dass sich der UPDRS-Verlauf der „delayed start“-Gruppe bald an den der Gruppe angleichen würde, die von Anfang an mit 2 mg/Tag Rasagilin behandelt wurde. Die Tatsache, dass dies nicht der Fall war, weist auf krankheitsmodifizierende, möglicherweise neuroprotektive Effekte von Rasagilin hin. Weitere Belege für eine klinische Neuroprotektion durch Rasagilin werden von einer Langzeitstudie erwartet, die derzeit initiiert wird.
Rasagilin in späteren Phasen der Parkinson-Krankheit mit motorischen Komplikationen
In der PRESTO-Studie wurden 472 Parkinson-Patienten mit motorischen Komplikationen in drei Gruppen randomisiert (Plazebo, 0,5 mg/Tag Rasagilin, 1 mg/Tag Rasagilin) [22]. Die Patienten (Hoehn & Yahr II) hatten ein durchschnittliches Alter von 63 Jahren, eine Krankheitsdauer von etwa 9 Jahren und eine tägliche Off-Zeit von 6 Stunden. Bei Studienbeginn standen die Patienten unter einer Medikation von Levodopa, zusätzlich waren Dopamin-Agonisten, Entacapon und Amantadin, erlaubt (Tab. 1). Nach 26 Wochen ergab sich für beide Dosierungen von Rasagilin eine gegen Plazebo signifikante Verkürzung der Off-Zeit und korrespondierend eine Verlängerung der On-Zeit (Tab. 2 und Abb. 2). Die Besserung betraf alle motorischen Kardinalsymptome (Bradykinese, Rigor, Tremor) (Abb. 3) und Subscores der Lebensqualität (QoL social score mit 0,5 mg/Tag Rasagilin –1,77, mit 1 mg/Tag Rasagilin –1,42).
Tab. 1. PRESTO-Studie [22]: Medikation der Patienten bei Studienbeginn (Plazebo: n=159; 0,5 mg/Tag Rasagilin: n=164; 1 mg/Tag Rasagilin: n=149)
|
Plazebo |
0,5 mg/Tag Rasagilin |
1 mg/Tag Rasagilin |
|
|
Levodopa |
821 mg |
750 mg |
815 mg |
|
Dopamin-Agonist |
69,8% |
70,7% |
71,8% |
|
Entacapon |
40,9% |
33,5% |
36,2% |
|
Amantadin |
23,9% |
20,1% |
18,1% |
Tab. 2. PRESTO-Studie [22]: Änderung der On- und Off-Zeit nach 26 Wochen in den drei Studienarmen (Plazebo, 0,5 mg/Tag Rasagilin, 1 mg/Tag Rasagilin)
|
Plazebo |
0,5 mg/Tag Rasagilin |
1 mg/Tag Rasagilin |
|
|
Off-Zeit [h] |
–0,91 |
–1,41 |
–1,85 |
|
On-Zeit [h] |
+0,79 |
+1,19 |
+1,82 |
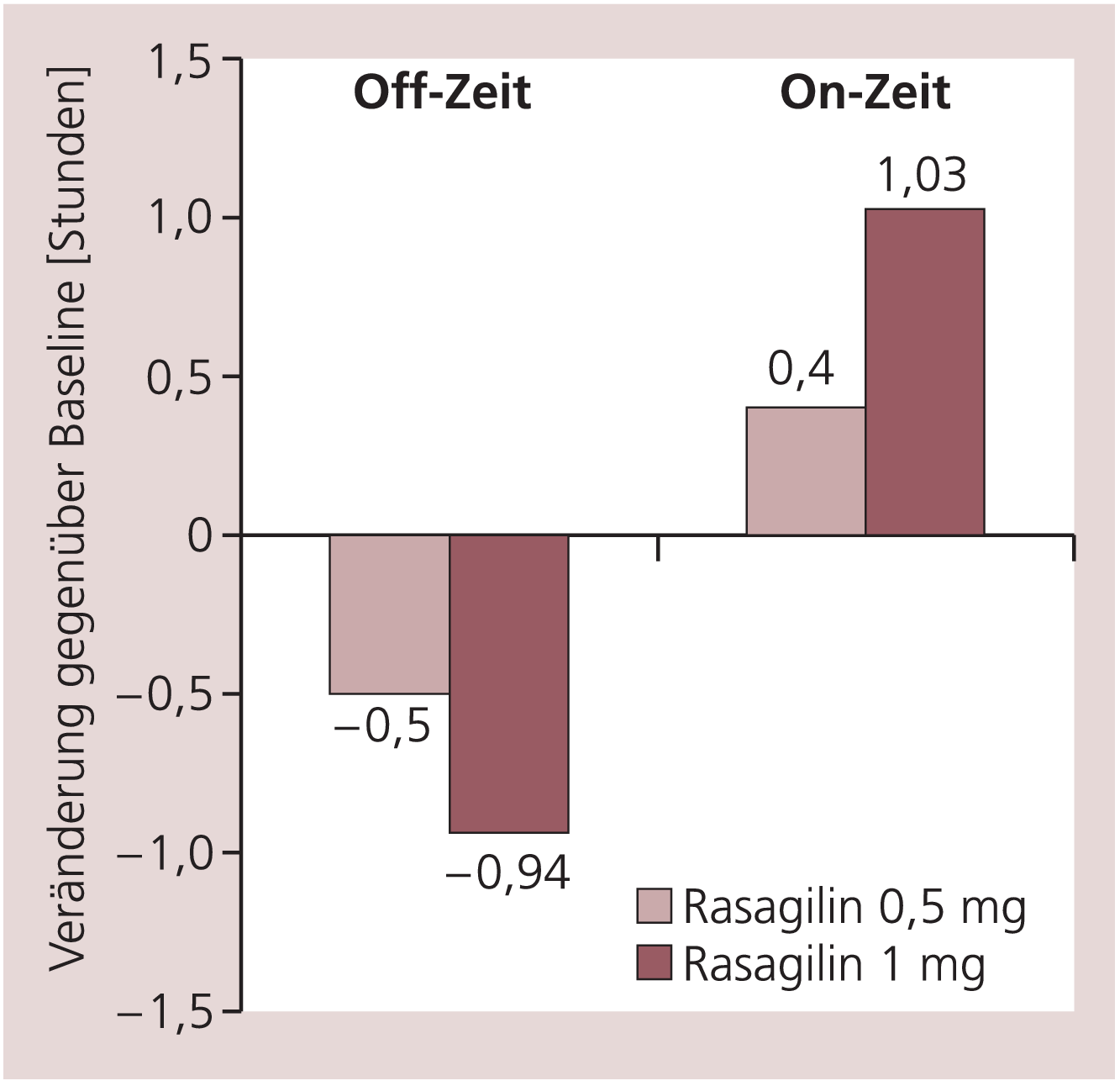
Abb. 2. PRESTO-Studie: Änderung der On- und Off-Zeit gegenüber Plazebo unter 0,5 bzw. 1 mg/Tag Rasagilin [mod. nach 22]
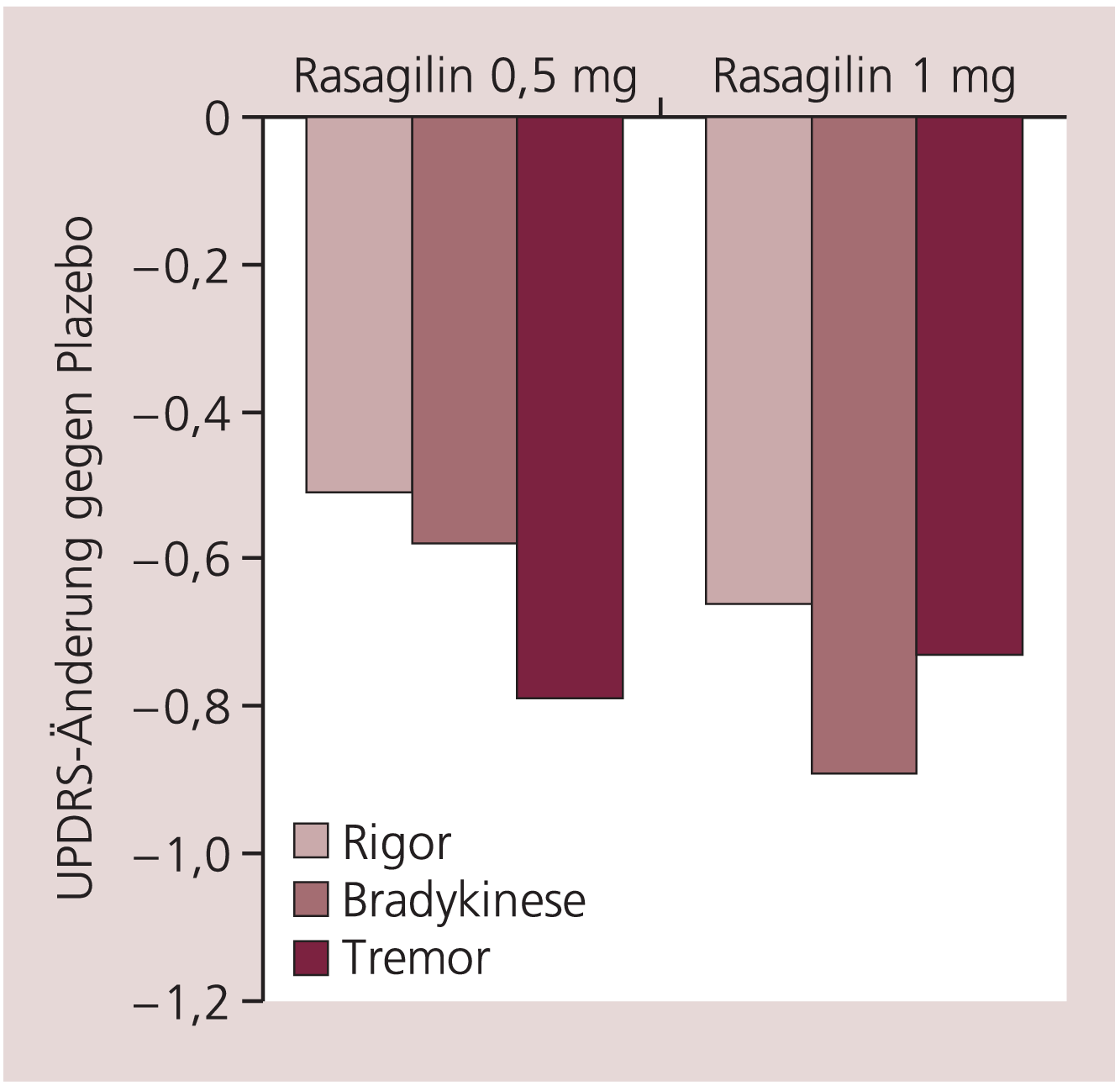
Abb. 3. PRESTO-Studie: Unter 0,5 und 1 mg/Tag Rasagilin Besserung aller motorischen Kardinalsymptome (Akinese, Rigor, Tremor) im Vergleich zu Plazebo [mod. nach 22]
Gegenstand der randomisierten, doppelblinden LARGO-Studie (Lasting effect in adjunct therapy with rasagiline given once daily) waren die Effekte einer MAO-B-Hemmung durch tägliche Einmalgabe von 1 mg Rasagilin oder einer Hemmung der Catechol-O-Methyltransferase (COMT) durch 200 mg Entacapon zu jeder Levodopa-Dosis im Vergleich mit Plazebo [23]. Die 18-Wochen-Studie umfasste 687 Patienten unter stabiler Levodopa-Dosis (Hoehn & Yahr II). Die mittlere tägliche Levodopa-Dosis lag bei etwa 700 mg (4,8 Einnahmeintervalle), etwa 60% der Patienten hatten zusätzlich einen Dopamin-Agonisten. Ausgeschlossen waren Selegilin und Tolcapon. Primäres Bewertungskriterium waren Veränderungen der täglichen Off-Zeit. Unter Rasagilin (Einmalgabe) und im selben Ausmaß unter Entacapon (200 mg zu jeder Levodopa-Dosis) wurde eine gegen Plazebo signifikante Reduktion der Off-Zeit und korrespondierend eine Verlängerung der On-Zeit beobachtet (Rasagilin: off –0,78 Stunden, on +0,86 Stunden; Entacapon off –0,80 Stunden, on +0,74 Stunden) (Abb. 4). Die Verbesserungen betrafen sowohl die On-Phase (Motorik) wie auch die Off-Phase (ADL) und waren funktionell relevant, was durch eine Verbesserung des klinischen Gesamteindrucks (CGI-Skala) belegt wird (Tab. 3).
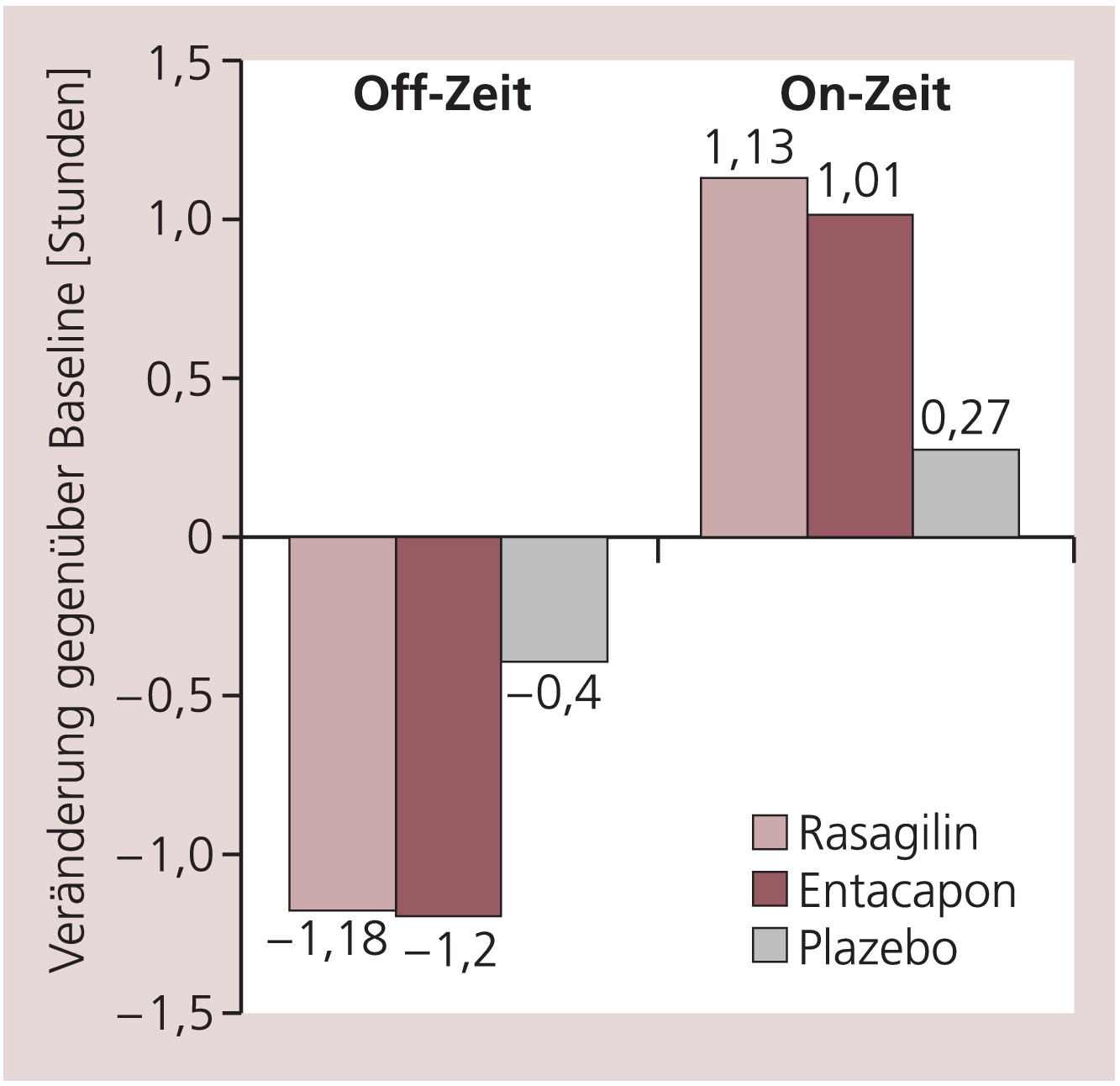
Abb. 4. LARGO-Studie: Änderung der On- und Off-Zeit gegenüber Baseline in den 3 Studienarmen (Plazebo, 1 mg Rasagilin 1-mal täglich, 200 mg Entacapon zu jeder Levodopa-Dosis) [mod. nach 23]
Tab. 3. LARGO-Studie: Änderung der sekundären UPDRS-Endpunkte (motor-on und ADL-off) und der Clinical-Global-Improvement-Skala gegen Plazebo unter Rasagilin und Entacapon; *p < 0,006, **p < 0,002, ***p < 0,001 vs. Plazebo [mod. nach 23]
|
Rasagilin |
Entacapon |
|
|
Motorische Funktion im „on“ |
–2,94 *** |
–2,73 *** |
|
ADL im „off“ |
–1,71 *** |
–1,38 * |
|
CGI (clinical global improvement) |
–0,86 *** |
–0,72 ** |
Sicherheit von Rasagilin
In den drei wichtigen kontrollierten Studien zu Rasagilin (TEMPO, PRESTO, LARGO) war die Zahl der Studienabbrüche in den Verum-Armen nicht signifikant unterschiedlich zu den Plazebo-Armen. Gastrointestinale Nebenwirkungen (Gewichtsverlust, Übelkeit, Anorexie) sind offenbar dosisabhängig (s. PRESTO-Studie) [22]. Insbesondere war in allen Studien die Häufigkeit von Schwindel, orthostatischer Hypotonie und von Verwirrtheit, Halluzinationen und Tagesmüdigkeit unter Rasagilin nicht häufiger als unter Plazebo [6, 10, 20–23]. Dies gilt allerdings nur bedingt für ältere Patienten (>65 Jahre), wenn Rasagilin in Kombination mit Levodopa gegeben wird [5, 13].
Sympathomimetische Nebenwirkungen („cheese effect“) sind unter der Dosierung von 1 mg/Tag Rasagilin nicht zu erwarten, der Blutdruckverlauf war in allen Studien unauffällig und nicht different zu Plazebo [20–23]. Einige Patienten der TEMPO- und PRESTO-Studie zeigten nach oraler Tyraminbelastung (75 bzw. 50 mg) keine Blutdruckveränderungen [19, 20].
Dyskinesien unter Rasagilin
In der PRESTO-Studie [22] verkürzte sich die Off-Zeit unter 0,5 mg/Tag Rasagilin um 0,5 Stunden, dabei traten keine Dyskinesien auf. Unter 1 mg/Tag Rasagilin betrug die Abnahme der Off-Zeit gegenüber Plazebo 0,94 Stunden, 32% der dadurch gewonnenen On-Zeit waren allerdings von Dyskinesien betroffen. Die Dyskinesien führten nicht zum Studienabbruch; in der täglichen Praxis kann man ihnen durch Reduktion der Levodopa-Dosis entgegenwirken. Die LARGO-Studie [23] zeigte, dass unter 1 mg/Tag Rasagilin nur ein sehr geringer Anteil der On-Zeit (0,23 Stunden) durch behindernde Dyskinesien belastet war ohne signifikante Unterschiede zur Entacapon- und Plazebo-Gruppe; die On-Zeit ohne Dyskinesien war in der Rasagilin- und Entacapon-Gruppe signifikant gegenüber Plazebo verlängert (Abb. 5).
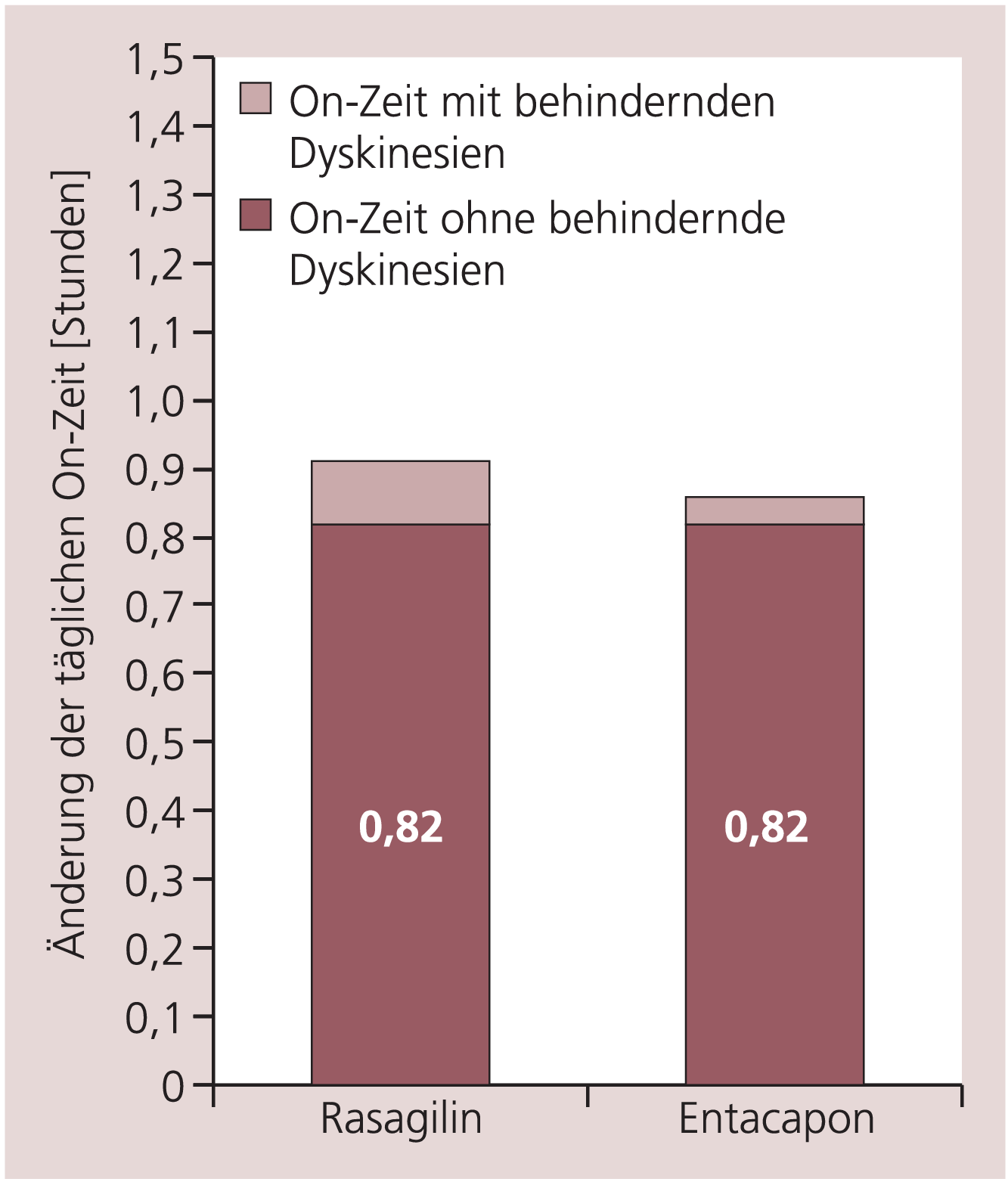
Abb. 5. LARGO-Studie: Änderung der täglichen On-Zeit mit und ohne behindernde Dyskinesien gegenüber Plazebo unter Rasagilin beziehungsweise Entacapon [mod. nach 23].
Vergleich mit anderen Hemmern der MAO-B
In Deutschland ist als MAO-B-Hemmer zur Behandlung der Parkinson-Krankheit neben Rasagilin seit längerem Selegilin zugelassen. Selegilin ist effektiv in der Monotherapie und in der Kombinationsbehandlung und kann den Zeitpunkt des Einsatzes von Levodopa verzögern; für eine Prävention von motorischen Komplikationen gibt es keine ausreichende Evidenz [25, 31]. Präklinische Hinweise auf eine neuroprotektive Wirkung von Selegilin konnten durch klinische Studien bisher nicht bestätigt werden [24].
Selegilin-Schmelztabletten („Zydis-Selegilin“, XiloparTM 1,25 mg) sind eine galenische Form von Selegilin, die den First-Pass-Effekt in der Leber umgeht und kaum amphetaminartige Metaboliten erzeugt. 1,25 mg der Substanz bewirken eine irreversible Hemmung der MAO-B, das Ausmaß der Hemmung und die klinische Wirkung entsprechen dem Effekt von 10 mg Selegilin als Tablette [7, 8]. In einer randomisierten, Plazebo-kontrollierten Doppelblindstudie konnte gezeigt werden, dass mit 1,25 mg/Tag die Off-Zeit nach 4 bis 6 Wochen um 9,9 Prozentpunkte (41,5% → 31,6%) und mit 2,5 mg/Tag nach 10 bis 12 Wochen um 13,2 Prozentpunkte (→ 28,3%) reduziert war. Die Off-Zeit war nach Woche 12 um 2,2 Stunden pro Tag reduziert (im Vergleich zu 0,6 Stunden in der Plazebo-Gruppe). Die On-Zeit ohne Dyskinesien war nach Woche 12 um 1,8 Stunden pro Tag verlängert [28]. Vergleichende klinische Studien zu den verschiedenen Hemmern der MAO-B liegen bisher noch nicht vor.
Indikationen für Rasagilin
Rasagilin ist zugelassen für die Behandlung des idiopathischen Parkinson-Syndroms in der Monotherapie und in der Kombinationstherapie bei Patienten mit motorischen Fluktuationen. Eine Monotherapie ist symptomatisch effektiv und kann den Zeitpunkt für die Notwendigkeit eines Einsatzes von dopaminergen Substanzen (Levodopa oder Dopamin-Agonist) hinauszögern. Ein Evidenz-basierter Vergleich der Wirksamkeit mit anderen MAO-Hemmern (Selegilin als Tablette oder Schmelztablette) ist derzeitig noch nicht möglich. Eine neuroprotektive Wirkung von Selegilin konnte bisher nicht durch klinische Studien belegt werden, ist aber aufgrund der präklinischen Daten zu erwarten [24]. Die ebenfalls günstigen präklinischen Befunde zu einer Neuroprotektion durch Rasagilin (s.o.) haben durch die TEMPO-Studie [21] eine erste klinische Bestätigung erfahren; weitere Untersuchungen sind aber erforderlich, um einen krankheitsmodifizierenden Effekt von Rasagilin zu bestätigen.
In der Kombinationsbehandlung (mit Levodopa oder Agonisten) ist Rasagilin signifikant wirksam und bewirkt eine Verlängerung der On-Zeit mit entsprechender Verkürzung der Off-Zeit. Dabei ist die Wirkung einer Einmalgabe von 1 mg/Tag Rasagilin dem Effekt eine COMT-Hemmung (durch 200 mg Entacapon zu jeder Levodopa-Dosis) vergleichbar. Bei der Behandlung von Wearing-off-Fluktuationen ist Rasagilin also eine Alternative zu Entacapon [17]. Es ist aber auch wahrscheinlich, dass man durch Kombination einer COMT-Hemmung (durch Entacapon) mit einer MAO-B-Hemmung (durch Rasagilin) einen zusätzlichen klinischen Effekt erreichen kann. Es wäre sehr wünschenswert, dies durch klinische Studien zu belegen. Ein günstiger Effekt auf die On-Zeit ist auch zu erwarten, wenn die Patienten mit einem Dopamin-Agonisten behandelt werden (etwa 60% der Patienten in der LARGO-Studie nahmen neben Levodopa auch einen Dopamin-Agonisten) [23].
In der täglichen Praxis sehen wir viele gut informierte Patienten, die bei der Erstdiagnose eines Parkinson-Syndroms mit der Einnahme einer dopaminergen Substanz zögern, weil sie befürchten, dadurch die Entwicklung eines Spätsyndroms mit motorischen Komplikationen zu beschleunigen. Für diese De-novo-Patienten ist eine Monotherapie mit Rasagilin in der ersten Krankheitsphase eine gute Alternative mit nachgewiesener symptomatischer Wirkung und der begründeten Option auf einen krankheitsmodifizierenden Effekt [26].
Literatur
1. Abassi ZA, Binah O, Youdim MBH. Cardiovascular activity of rasagiline, a selective and potent inhibitor of mitochondrial monoamine oxidase B: comparison with selegiline. Br J Pharmacol 2004;143:371–8.
2. Bar Am O, Amit T, Youdim MBH. Contrasting neuroprotective and neurotoxic actions of respective metabolites of anti-Parkinson drugs rasagiline and selegiline. Neurosci Lett 2004;355:169–72.
3. Blandini F, Armentero MT, Fancellu R, Blaugrund E, et al. Neuroprotective effect of rasagiline in a rodent model of Parkinson’s disease. Exp Neurol 2004;187:455–9.
4. Bonneh-Barkay D, Ziv N, Finberg JPM. Characterization of the neuroprotective activity of rasagiline in cerebellar granule cells. Neuropharmacology 2005;48:406–16.
5. Chen JJ, Berchou RC. Rasagiline, a selective, second-generation, irreversible inhibitor of monoamine oxidase type B, is effective in patients older and younger than 65 years of age with early-to-advanced Parkinson’s disease. Pharmacotherapy 2004;24:1448.
6. Chen JJ, Swope DM. Clinical pharmacology of rasagiline: a novel, second-generation propargylamine for the treatment of Parkinson disease. J Clin Pharmacol 2005;45:878–94.
7. Clarke A, Brewer F, Johnson ES, Mallard N, et al. A new formulation of selegiline: improved bioavailability and selectivity for MAO-B inhibition. J Neural Transm 2003;110:1241–55.
8. Clarke A, Johnson ES, Mallard N, Corn TH, et al. A new low-dose formulation of selegiline: clinical efficacy, patient preference and selectivity for MAO-B inhibition. J Neural Transm 2003;110:125771.
9. Eliash S, Speiser Z, Cohen S. Rasagiline and its (S) enantiomer increase survival and prevent stroke in salt-loaded stroke-prone spontaneously hypertensive rats. J Neural Transm 2001;108:909–23.
10. Elmer L, Parkinson study group. Rasagiline is effective and well tolerated in the treatment of Parkinson’s disease (PD) patients with levodopa-related motor fluctuations receiving other adjunctive therapy. Mov Disord 2005;20:S138.
11. Finberg JPM, Youdim MBH. Modification of blood pressure and nictitating membrane response to sympathetic amines by selective monoamine oxidase inhibitors, type A and type B in the cat. Br J Pharmacol 1985;85:541–6.
12. Finberg JPM, Lamersdorf I, Commissiong JW, Youdim MBH. Pharmacology and neuroprotective properties of rasagiline. J Neural Transm 1996;48:95–101.
13. Goetz CG, Schwid SR, Eberly SW, Oakes D, et al. Safety of rasagiline in elderly Parkinson’s disease (PD) patients. Mov Disord 2005;20:S81.
14. Hauser RA, Lew MF, Hurtig HI, Ondo WG, et al. Early treatment with rasagiline is more beneficial than delayed treatment start in the long-term treatment of Parkinson’s disease. Mov Disord 2005;20:S75, 16th International Congress on Parkinson’s Disease and Related Disorders, Berlin, 5.–9. Juni 2005 [Poster].
15. Hubalek F, Binda C, Li M, Herzig Y, et al. Inactivation of purified human recombinant monoamine oxidase A and B by rasagiline and its analogues. J Med Chem 2004;47:1760–6.
16. Kupsch A, Sautter J, Götz ME, Breithaupt W, et al. Monoamine oxidase-inhibition and MPTP-induced neurotoxicity in the non-human primate: comparison of rasagiline with selegiline. J Neural Transm 2001;108:985–1009.
17. Lachenmayer L, Fuchs G, Hueber R, Ludolph AC, et al. Aktuelle Therapieempfehlungen. Akt Neurol 2005;32(Suppl 3):S110–2.
18. Mandel S, Weinreb O, Amit T, Youdim MBH. Mechanism of neuroprotective action of the anti-Parkinson drug rasagiline and its derivatives. Brain Res Rev 2005;48:379–87.
19. Marcaida JA. Rasagiline does not promote tyramine pressor responses. Mov Disord 2005;20:S133.
20. Parkinson study group. A controlled trial of rasagiline in early Parkinson disease. Arch Neurol 2002;59:1937–43.
21. Parkinson study group. A controlled, randomized, delayed-start study of rasagiline in early Parkinson disease. Arch Neurol 2004;61:561–6.
22. Parkinson study group. A randomized placebo-controlled trial of rasagiline in levodopa-treated patients with Parkinson disease and motor fluctuations. The PRESTO study. Arch Neurol 2005;62:241–8.
23. Rascol O, Brooks DJ, Melamed E, Oertel W, et al. Rasagiline as an adjunct to levodopa in patients with Parkinson’s disease and motor fluctuations (LARGO, lasting effect in adjunct therapy with rasagiline given once daily, study): a randomized, double-blind, parallel-group trial. Lancet 2005;365:947–54.
24. Riederer P, Lachenmayer L. Selegiline’s neuroprotective capacity revisited. J Neural Transm 2003;110:1273–8.
25. Riederer P, Lachenmayer L, Laux G. Clinical applications of MAO-inhibitors. Curr Med Chem 2004;11:2033–43.
26. Schapira A, Bate G, Kirkpatrick P. Rasagiline. Nature Rev 2004;4:625–6.
27. Siddiqui MA, Plosker GL. Rasagiline. Drugs Aging 2005;22:83–91.
28. Waters CH, Sethi KD, Hauser RA, Molho E, et al. Zydis selegiline reduces off time in Parkinson’s disease patients with motor fluctuations: a 3-month, randomized, placebo-controlled study. Mov Disord 2004;19:426–34.
29. Youdim MBH, Gross A, Finberg JP. Rasagiline [N-propargyl-1R(+)-aminoindan], a selective and potent inhibitor of mitochondrial monoamine oxidase B. Br J Pharmacol 2001;132:500–6.
30. Youdim MBH, Tipton KF. Rat striatal monoamine oxidase-B inhibition by l-deprenyl and rasagiline: its relationship to 2-phenylethylamine-induced stereotypy and Parkinson’s disease. Parkinsonism Relat Disord 2002;8:247–53.
31. Youdim MBH, Riederer P (Hrsg). Monoamine oxidase A and B inhibitors in Parkinson’s disease. Im Druck.
Prof. Dr. Lutz Lachenmayer, Neurologische Abteilung, Klinikum Barmbek, Rübenkamp 148, 22307 Hamburg. E-Mail: Lutz.Lachenmayer@ak-barmbek.lbk-hh.de
Prof. Dr. Peter Riederer, Klinik and Poliklinik für Psychiatrie und Psychotherapie, Neurochemisches Labor, Füchsleinstr. 15, 97080 Würzburg, E-Mail: peter.riederer@mail.uni-wuerzburg.de
Rasagiline
Rasagiline (N-propargyl-1-[R]-aminoindane) is a new second-generation, selective, irreversible inhibitor of monoamine oxidase type B. Rasagiline (Azilect®) is approved in the EU for the treatment of Parkinson’s disease (monotherapy and adjunctive therapy in patients with motor fluctuations). The efficacy and safety of rasagiline is documented in randomized studies (monotherapy: TEMPO-study, adjunctive therapy: PRESTO-, LARGO-study). In early monotherapy of currently untreated patients rasagiline is symptomatically effective, can delay the need for dopaminergic therapy and may modify the course of the disease. In adjunctive therapy 1 mg rasagiline given once daily is as effective as entacapone (200 mg to each dose of levodopa) in decreasing off-time. Studies on a combination of COMT-inhibition (with entacapone) and MAO-B-inhibition (with rasagiline) are lacking. Evidence-based comparison with other inhibitors of MAO-B (selegiline, Zydis-selegiline) is currently not available.
Keywords: Rasagiline, idiopathic Parkinson syndrome, monotherapy, motor fluctuations, neuroprotection
Psychopharmakotherapie 2005; 12(06)
