Markus J. Schwarz, Ilja Spellmann, Anette Müller-Arends, Johanna Zach, Norbert Müller, Hans-Jürgen Möller und Michael Riedel, München
Das atypische Neuroleptikum Risperidon hat eine hohe Bindungsaffinität zum D2-Dopamin-Rezeptor und zu den 5-HT2-Serotonin-Rezeptoren und erwies sich in den vergangenen Jahren als sehr potentes Antipsychotikum sowohl gegen schizophrene Positiv- wie auch gegen Negativsymptomatik. Risperidon wird nach oraler Aufnahme fast vollständig absorbiert. Über das Cytochrom-P450-Enzym CYP2D6 erfolgt die Verstoffwechslung zum ebenfalls pharmakologisch aktiven Metaboliten 9-Hydroxyrisperidon. Zu einem geringeren Prozentsatz wird Risperidon auch über CYP3A4 verstoffwechselt. Gerade die Aktivität des CYP2D6 unterliegt deutlich interindividuellen Unterschieden, die auf Genpolymorphismen zurückzuführen sind. So ist bei etwa 8 % der europäischen Bevölkerung die CYP2D6-Aktivität deutlich herabgesetzt, während etwa 1 % der Bevölkerung ungewöhnlich aktive CYP2D6 besitzen. Bei normaler Verstoffwechslungsrate werden bereits etwa 24 Stunden nach Einnahme Steady-State-Spiegel von Risperidon erreicht; die Steady-State-Bedingungen von 9-Hydroxyrisperidon sind nach etwa fünf Tagen erreicht [16]. Da 9-Hydroxyrisperidon im ZNS ein sehr ähnliches Rezeptorbindungsprofil wie Risperidon selbst zeigt [18], wird die Summe aus Risperidon und 9-Hydroxyrisperidon als aktiver Anteil angegeben. Die Summe der Blutkonzentrationen kann entsprechend als aktiver Blutspiegel angegeben werden.
Gemäß Herstellerangaben sollte Risperidon in einer Dosierung von 4 bis 6 mg pro Tag verabreicht werden, doch zeigen Studien deutliche interindividuelle Unterschiede zwischen verabreichter Dosis und Blutspiegeln [2]. Einflussgrößen wie Alter oder Körpergewicht mögen diese Unterschiede ebenso begründen wie genetisch bedingte Variationen in der Metabolisierung [3, 7].
Die aktuellen Dosierungsempfehlungen berücksichtigen solche interindividuellen Unterschiede nicht. Deshalb ist es naheliegend, durch therapeutisches Drug-Monitoring von Risperidon und seinem aktiven Hauptmetaboliten die individuelle Bioverfügbarkeit zu überprüfen. Da ein direkter Zusammenhang zwischen Blutkonzentration und Rezeptorbindung im ZNS nachgewiesen werden konnte [18], wäre zudem ein ebenfalls direkter Zusammenhang zwischen Blutspiegeln und individuellem Ansprechen auf die Therapie oder dem Auftreten unerwünschter Arzneimittelwirkungen, insbesondere extrapyramidal-motorischer Nebenwirkungen, zu erwarten.
Wir untersuchten diese Fragestellung in einer prospektiven Studie, die in extenso anderweitig publiziert wird (Riedel et al., im Druck).
Methode
Wir führten eine sechswöchige Monotherapiestudie mit variabler Risperidon-Dosis an Patienten mit Schizophrenie durch.
Patienten
Die Diagnose wurde anhand der DSM-IV-Kriterien gestellt [1]. Vor Einschluss in die Studie wurden die Patienten über den Inhalt der Studie aufgeklärt und bestätigten schriftlich ihre Einwilligung. Ausschlusskriterien waren Alter unter 18 oder über 65 Jahren, schwerwiegende zusätzliche Erkrankungen, Auffälligkeiten in EKG oder EEG, mehr als 20 % von der Norm abweichende klinisch-chemische Laborwerte, positiver Befund im Urin-Drogentest, Substanzabusus, Hepatitis oder HIV-Infektion sowie Schwangerschaft.
An der Studie nahmen 82 Patienten (39 Frauen und 43 Männer) mit einem Durchschnittsalter von 36,2±12,9 Jahren teil. Das mittlere Erstmanifestationsalter lag bei 31,7±16,5 Jahren und die mittlere Erkrankungsdauer bei 6,7±8,7 Jahren. 53 Patienten litten an einer paranoid-halluzinatorischen Schizophrenie (DSM-IV 295.3), 12 an einer disorganisierten Schizophrenie (DSM-IV 295.1), 10 an einer schizoaffektiven Störung (295.7), 4 an einer undifferenzierten Schizophrenie (295.9) und 3 Patienten an einer schizophreniformen Störung (295.4).
Klinische Untersuchungen
Zu Beginn der Studie wurde jeder Patient eingehend medizinisch untersucht. Am Ende der dritten Woche sowie bei Studienende oder Studienabbruch wurde diese Untersuchung wiederholt. Einer Auswaschphase von zwei bis sieben Tagen folgte innerhalb einer Woche die langsame Aufdosierung mit Risperidon. Danach wurde bei Bedarf anhand der klinischen Symptomatik einmal pro Woche eine Dosisanpassung durchgeführt. Während der gesamten Zeit der Studie waren lediglich bis zu 4 mg/Tag Lorazepam, 15 mg/Tag Zolpidem und 6 mg/Tag Biperiden als Komedikation zugelassen.
In wöchentlichen Abständen wurden die Psychopathologie und die unerwünschten Arzneimittelwirkungen anhand der Positive and Negative Syndrome Scale (PANSS) [12], der Clinical Global Impressions Scale (CGI) [9], der Simpson and Angus Scale (SAS) [17] sowie der Barnes Akathisia Scale (BAS) [5] durch erfahrene Psychiater quantifiziert. Zudem wurde wöchentlich Blut zur nachträglichen Bestimmung der Arzneistoffspiegel abgenommen. Diese Bestimmungen wurden jedoch erst nach Ende der Studie durchgeführt, um die Dosierung nicht zu beeinflussen.
Bestimmung der Arzneistoffspiegel
Wie in einer anderen Publikation zu dieser Studie ausführlich dargestellt [15], wurden die Serumkonzentrationen von Risperidon und 9-Hydroxyrisperidon nach Flüssig-Flüssig-Extraktion per Hochdruckflüssigkeitschromatographie (HPLC) mit UV-Detektion nachgewiesen. Präzision und Interassayvarianz lagen für beide Analyte unter 5 %. Die Richtigkeit der Analyse wurde durch regelmäßige Teilnahme an Ringversuchen (Cardiff psychotropic drugs scheme) überprüft.
Statistik
Im Falle einer vorzeitigen Beendigung der Studie wurden durch LOCF (Last observation carried forward) die Werte der fehlenden Visiten durch die der letzten Visite ersetzt. LOCF wurde jedoch nur bei solchen Patienten angewandt, die wenigstens bis einschließlich der dritten Behandlungswoche an der Studie teilnahmen. Die Zielvariable war die Änderung der schizophrenen Symptomatik, erfasst durch die PANSS.
Generell wurden zum Ende der sechsten Behandlungswoche Therapieerfolg und -sicherheit festgestellt. Das Kriterium für das Ansprechen auf die Therapie (Responder) war eine mindestens 30%ige Reduktion des PANSS-Gesamtwerts. Die Summe aus Risperidon und 9-Hydroxyrisperidon wurde als aktiver Blutspiegel definiert. Um eventuelle interindividuelle Unterschiede während der Aufdosierungsphase auszuschließen, wurden die Blutspiegel der 5. Woche als Steady-State-Konzentration angenommen.
Um Patienten mit kurzer und langer Erkrankungsdauer voneinander zu unterscheiden, wurde ein Grenzwert von drei Jahren definiert. Um den Zusammenhang zwischen Blutspiegeln und Auftreten extrapyramidal-motorischer Nebenwirkungen (EPMS) zu untersuchen, wurde der Mittelwert der SAS als Grenzwert zur Unterscheidung zwischen stark und schwach ausgeprägten EPMS definiert.
Zum Vergleich zweier Variablen wurde der t-Test verwendet; Unterschiede im Behandlungsverlauf wurden mit ANOVA berechnet.
Ergebnisse
Dosis und Blutspiegel
Bei einer mittleren oralen Dosis von 4,3±0,9 mg/Tag lagen die aktiven Blutspiegel bei 41,6±26,6 ng/ml. Dabei zeigte sich eine positive lineare Korrelation zwischen Dosis und aktivem Blutspiegel (r=0,291, p=0,015) sowie zwischen den Serumkonzentrationen von Risperidon und 9-Hydroxyrisperidon (r=0,291; p=0,016).
Klinische Variablen
Der PANSS-Gesamtwert verringerte sich im Laufe der Risperidon-Behandlung von 85,4±19,4 (positiv: 20,5±6,3; negativ: 22,6±7,0; global: 42,3±11,0) auf 63,0±21,3 (positiv: 13,2±4,9; negativ: 18,0±7,1; global: 31,9±11,2) Punkte.
Wie in Abbildung 1 gezeigt, hatten Patienten, die mit weniger als 30 % Änderung ihres PANSS-Gesamtwerts schlecht auf die Behandlung ansprachen, deutlich höhere aktive Blutspiegel (49,9±30,7 ng/ml) als Responder (38,2±17,0 ng/ml; p=0,045), ohne dass jedoch die tägliche Dosis unterschiedlich war (p=0,601). Weder Alter (p=0,885) noch Gewicht (p=0,257) konnten die unterschiedlichen Blutspiegel erklären. Zudem unterschieden sich Nonresponder von Respondern nicht bezüglich der PANSS-Gesamtwerte bei Einschluss in die Studie (p=0,275). Patienten mit einer länger als drei Jahre währenden Erkrankungsdauer hatten deutlich höhere Blutspiegel (48,3±33,1 ng/ml) als jene mit kürzerer Erkrankungsdauer (35,5±17,8 ng/ml). Dieser Unterschied war nicht auf unterschiedliche Dosierungen zurückzuführen (p=0,039), allerdings war die Gruppe der länger erkrankten Patienten naturgemäß älter (40,1±12,2 Jahre vs. 31,9±12,3 Jahre; p=0,004).
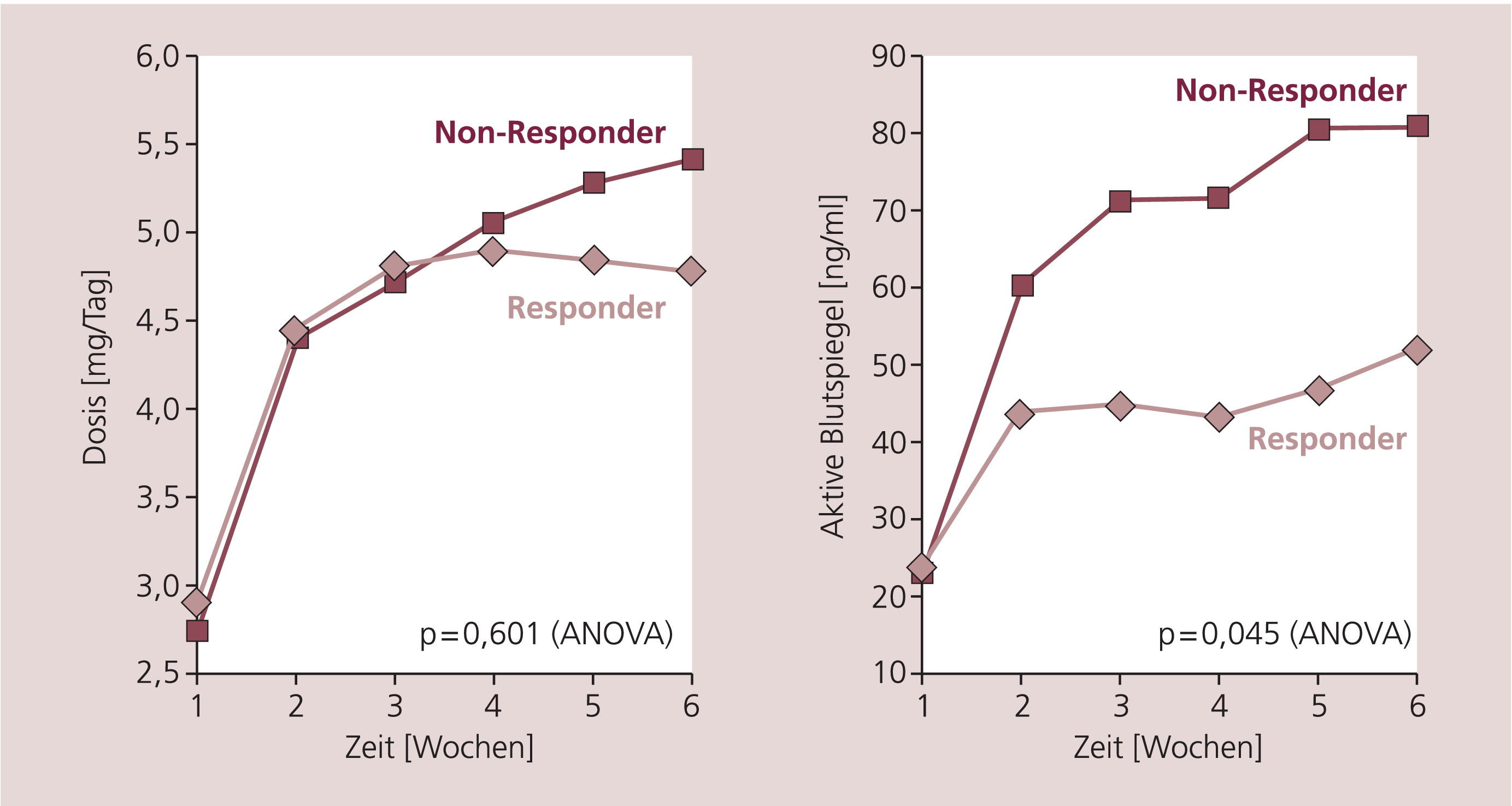
Abb. 1. Zusammenhang zwischen dem Ansprechen auf die Therapie, der täglichen Dosis und den aktiven Blutspiegeln. Nonresponder (weniger als 30% Reduktion der Symptomatik gemessen anhand der PANSS) wiesen bei gleicher Dosis deutlich höhere Blutspiegel auf als Responder.
Unerwünschte Arzneimittelwirkungen
Es zeigte sich keine direkte Korrelation zwischen den aktiven Blutspiegeln und dem Auftreten von EPMS, die anhand der SAS quantifiziert wurden (r=–0,040; p=0,722). Allerdings hatten Patienten, die zum Studienende EPMS aufwiesen (SAS ≥ 0,9), in der ersten Behandlungswoche deutlich höhere aktive Blutspiegel und eine höhere Dosis (jeweils p < 0,050). Höhere aktive Blutspiegel zu einem späteren Zeitpunkt standen jedoch nicht in Zusammenhang mit dem Auftreten von EPMS.
Diskussion
Das therapeutische Drug-Monitoring gewinnt an immer größerer Bedeutung [6]. Dies hat verschiedene Gründe: Zum einen stellt die Bestimmung der Blutspiegel von Wirkstoff und Metabolit ein hervorragendes Instrument dar, um individuelle Besonderheiten in der Verstoffwechslung des verabreichten Arzneistoffs nachzuweisen – unabhängig davon, ob diese Besonderheiten auf Arzneimittelinteraktionen an den abbauenden Leberenzymen beruhen oder ob eine genetische Disposition zu auffallend erhöhter oder verminderter Metabolisierungsrate besteht. Zum anderen wurde für verschiedene Psychopharmaka wie Risperidon der Zusammenhang zwischen Blutspiegeln und zentralnervöser Rezeptorbesetzung nachgewiesen [18]. Letzteres führte uns zu der hier dargestellten Studie, in der wir den möglichen Zusammenhang zwischen Blutspiegel und Arzneimittelwirkung untersuchten.
Tatsächlich konnten wir zeigen, dass die aktiven Blutspiegel von Risperidon und seinem pharmakologisch aktiven Metaboliten 9-Hydroxyrisperidon in Zusammenhang mit dem Ansprechen auf die Therapie sowie in Zusammenhang mit dem Auftreten extrapyramidal-motorischer Nebenwirkungen stehen.
Insgesamt war das Ansprechen auf die Therapie sehr gut und das Auftreten extrapyramidal-motorischer Nebenwirkungen war relativ gering. Dennoch fiel auf, dass Patienten, die am Ende der ersten Behandlungswoche eine höhere Dosis einnahmen und dadurch erhöhte aktive Blutspiegel hatten, gegen Ende der Studie vermehrt EPMS aufwiesen. Zu einem späteren Zeitpunkt bestand kein Zusammenhang mehr zwischen Dosis oder Blutspiegeln und EPMS. Ähnliche Befunde wurden bereits von Olesen und Kollegen beschrieben [14], doch existieren hierzu widersprüchliche Daten [10, 20].
Wie bereits von einer anderen Gruppe beschrieben [14], wiesen Patienten mit mehr als dreijähriger Dauer ihrer Erkrankung höhere aktive Blutspiegel auf, obwohl sie keine höhere Dosis erhielten. Dies mag am ehesten einen Alterseffekt darstellen und nicht genetisch bedingt sein, oder es mag auf direkten kumulativen pharmakologischen Effekten beruhen [21].
Überraschenderweise hatten jedoch unabhängig von Alter oder Körpergewicht Patienten, die schlechter auf die Therapie ansprachen, bei gleicher täglicher Dosis deutlich höhere aktive Blutspiegel. Eine Resorptionsstörung kann ausgeschlossen werden, denn andernfalls müsste man bei Nonrespondern verminderte Blutspiegel erwarten. Es bleibt deshalb zu spekulieren, ob möglicherweise eine (genetisch bedingt?) unterschiedliche Aktivität des P-Glykoproteins (P-gp) an der Blut-Hirn-Schranke für diesen Effekt verantwortlich ist. Das transmembranale P-gp ist ein Transportmolekül, das körperfremde Substanzen wie Pharmaka unter anderem über die Blut-Hirn-Schranke aus Körperkompartimenten transportiert. Sowohl Risperidon als auch 9-Hydroxyrisperidon wurden als P-gp-Substrate bestätigt [8]. Tierexperimentelle Daten weisen auf einen wichtigen Einfluss des P-gp auf die Aufnahme dieser beiden Substanzen ins Gehirn hin: Bei Mäusen mit defizientem P-gp an der Blut-Hirn-Schranke war das Verhältnis der Hirn-/Blut-Konzentrationen von Risperidon um das 12fache und für 9-Hydroxyrisperidon um das 29fache gesteigert [19].
In unserer Studie waren durchwegs die Blutkonzentrationen des Metaboliten höher als die der Muttersubstanz. Dies bestätigt Beobachtungen von Aravagiri und Kollegen [2] und legt nahe, dass die klinische Wirkung von Risperidon vorwiegend auf seinen Metaboliten zurückzuführen ist. Insofern nimmt Risperidon eher eine Sonderstellung unter den Psychopharmaka ein, da die klinische Bedeutung pharmakologisch aktiver Metaboliten meist deutlich geringer ausgeprägt ist [4]. Gerade aus diesem Grunde ist es wichtig, beim therapeutischen Drug-Monitoring (TDM) sowohl Risperidon als auch seinen aktiven Metaboliten zu bestimmen, wie auch in den Konsensus-Leitlinien der Expertengruppe TDM der Arbeitsgemeinschaft für Neuropsychopharmakologie und Pharmakopsychiatrie gefordert [6].
Zusammenfassend zeigte sich ein deutlicher Zusammenhang zwischen erhöhten aktiven Blutspiegeln und einem schlechteren Ansprechen auf die Therapie sowie einem erhöhten Risiko für EPMS; außerdem wiesen auch chronisch kranke Patienten höhere Blutspiegel auf. In Anbetracht dieser Befunde muss für den klinischen Alltag eine moderate Aufdosierung und insgesamt eine eher niedrige Dosierung sowie die regelmäßige Kontrolle der aktiven Blutspiegel empfohlen werden. Dies steht in Einklang mit dem aktuellen Trend, nicht mit Dosiseskalation, sondern mit niedrigen bis moderaten Dosierungen zu arbeiten [11, 13].
Literatur
1. American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders. Fourth edition, text revision. Washington, DC: American Psychiatric Association, 1994.
2. Aravagiri M., Marder SR, Nuechterlein KH, Gitlin MJ. Intra- and interindividual variations in steady-state plasma concentrations of risperidone and 9-hydroxyrisperidone in schizophrenic patients treated chronically with various doses of risperidone. Ther Drug Monit 2003;25:657–64.
3. Balant-Gorgia AE, Gex-Fabry M, Genet C, BalantLP. Therapeutic drug monitoring of risperidone using a new, rapid HPLC method: reappraisal of interindividual variability factors. Ther Drug Monit 1999;21:105–15.
4. Baldessarini RJ, Centorrino F, Flood JG, Volpicelli SA, et al. Tissue concentrations of clozapine and its metabolites in the rat. Neuropsychopharmacology 1993;9:117–24.
5. Barnes TR. A rating scale for drug-induced akathisia. Br J Psychiatry 1989;154:672–6.
6. Baumann P, Hiemke C, Ulrich S, Eckermann G, et al. The AGNP-TDM expert group consensus guidelines: therapeutic drug monitoring in psychiatry. Pharmacopsychiatry 2004;37:243–65.
7. Berecz R, LLerena A, de la RA, Gomez J, et al. Relationship between risperidone and 9-hydroxy-risperidone plasma concentrations and CYP2D6 enzyme activity in psychiatric patients. Pharmacopsychiatry 2002;35:231–4.
8. Boulton DW, DeVane CL, Liston HL, Markowitz JS. In vitro P-glycoprotein affinity for atypical and conventional antipsychotics. Life Sci 2002;71:163–9.
9. Guy W, Bunate RR. Clinical Global Impression. In: Guy W, Bunate RR (eds.) Manual for the ECDEU assessment battery. Bethesda: National Institute of Mental Health, 1970:12.1–12.6.
10. He H, Richardson JS. A pharmacological, pharmacokinetic and clinical overview of risperidone, a new antipsychotic that blocks serotonin 5-HT2 and dopamine D2 receptors. Int Clin Psychopharmacol 1995;10:19–30.
11. Huq ZU. A trial of low doses of risperidone in the treatment of patients with first-episode schizophrenia, schizophreniform disorder, or schizoaffective disorder. J Clin Psychopharmacol 2004;24:220–4.
12. Kay SR, Fiszbein A, Opler LA. The positive and negative syndrome scale (PANSS) for schizophrenia. Schizophr Bull 1987;13:261–76.
13. Lane HY, Chang YC, Chiu CC, Lee SH, et al. Fine-tuning risperidone dosage for acutely exacerbated schizophrenia: clinical determinants. Psychopharmacology (Berl) 2004;172:393–9.
14. Olesen OV, Licht RW, Thomsen E, Bruun T, et al. Serum concentrations and side effects in psychiatric patients during risperidone therapy. Ther Drug Monit 1998;20:380–4.
15. Riedel M, Schwarz MJ, Strassnig M, Spellmann I, et al. Risperidone plasma levels, clinical response and side-effects. Eur Arch Psychiatry Clin Neurosci. Im Druck. Epub Nov 2004.
16. Schatzberg AF, Nemeroff CB. Textbook of Psychopharmacology. Washington: The American Psychiatric Press, 1998.
17. Simpson GM, Angus JW. A rating scale for extrapyramidal side effects. Acta Psychiatr Scand 1970;212(Suppl):11–9.
18. van Beijsterveldt LE, Geerts RJ, Leysen JE, Megens AA, et al. Regional brain distribution of risperidone and its active metabolite 9-hydroxy-risperidone in the rat. Psychopharmacology (Berl) 1994;114:53–62.
19. Wang JS, Ruan Y, Taylor RM, Donovan JL, et al. The brain entry of risperidone and 9-hydroxyrisperidone is greatly limited by P-glycoprotein. Int J Neuropsychopharmacol 2004;7:415–9.
20. Yoshimura R, Ueda N, Nakamura J. Possible relationship between combined plasma concentrations of risperidone plus 9-hydroxyrisperidone and extrapyramidal symptoms. Neuropsychobiology 2001;44:129–33.
21. Zubenko GS, Sunderland T. Geriatric psychopharmacology: why does age matter? Harv Rev Psychiatry 2000;7:311–33.
Dr. med. Markus J. Schwarz, Dr. med. Ilja Spellmann, Dr. med. Anette Müller-Arends, Johanna Zach, Prof. Dr. med. Norbert Müller, Prof. Dr.med. Hans-Jürgen Möller, Dr. med. Michael Riedel, Klinik und Poliklinik für Psychiatrie und Psychotherapie, Ludwig-Maximilians-Universität München, Nussbaumstraße 7, 80336 München, E-Mail: Markus.Schwarz@med.uni-muenchen.de
Therapeutic drug monitoring of risperidone – clinical efficacy and side effects
There are only few data on the therapeutic drug monitoring of risperidone and its active metabolite 9-hydroxy-risperidone in relation to oral risperidone dose and clinical response. We thus prospectively investigated risperidone serum concentrations in relation to clinical efficacy and side-effects to determine their effect upon these parameters.
Risperidone monotherapy was administered to 82 schizophrenic patients in a 6-week open dose clinical trial. Weekly assessments included CGI and PANSS ratings to assess psychopathology, SAS to assess medication side effects, and blood samplings to quantify steady state plasma levels of risperidone and 9-OH-risperidone.
Mean oral dose of risperidone was 4.3±0.9 mg, while plasma levels of both risperidone and 9-OH-risperidone together (“active moiety”) were 41.6±26.6 ng/ml. Significant improvements in PANSS scales and the various subscales ensued. There was a positive linear correlation between active moiety plasma levels and dose (r=0.291, p=0.015) and between risperidone and 9-OH-risperidone levels (r=0.262; p=0.016). Nonresponders to pharmacotherapy (PANSS improvement <30%) showed significantly higher active moiety plasma levels (49.9±30.7 ng/ml) than responders (38.2±17.0 ng/ml; p=0.045) without significantly higher oral doses (p=0.601). Patients with longer illness duration (≥ 3 years) had significantly higher plasma drug levels than those with a shorter course (< 3 years; p=0.039). This may represent general ageing effects. Conversely, the observed higher plasma levels in nonresponders may derive from unaccounted genetic metabolism abnormalities or phase II metabolism disturbances.
Extrapyramidal side effects (EPS) and plasma levels were not correlated (r=0.028; p=.843), but higher plasma levels at week 2 predicted incidence of EPS (p < 0.050). Accordingly, patients initially receiving higher oral doses of risperidone were significantly more likely to respond with EPS in the trial course, which reaffirms the need for careful titration.
The high inter-individual variability in risperidone and 9-OH-risperidone metabolization and the relationship between clinical outcome and plasma levels warrants regular plasma level monitoring of both compounds to assess for the clinically relevant active moiety.
Keywords: Risperidone, metabolite, TDM, EPS, PANSS
Psychopharmakotherapie 2005; 12(04)
