Detlef Degner, Göttingen, Patrik Lukas Stephan, Eveline Jaquenoud-Sirot, Brugg (Schweiz), Roswitha Thilmann, Essen, Beate Schmidt, Berit Wenda, Jena, und Renate Grohmann, München
In Heft 3/04 der Psychopharmakotherapie [11] wurde auf das Thema lebertoxischer Wirkungen von Psychopharmaka erstmals im Rahmen der AMSP-Beiträge eingegangen. Im vorliegenden Beitrag soll mit drei weiteren Fällen die Problematik von möglichen additiven lebertoxischen Effekten bei Kombinationsbehandlungen sowie von Vorschädigungen durch Fettleber bei Adipositas dargestellt werden. Letzteres erscheint angesichts der zunehmenden Häufigkeit von Adipositas – bei psychiatrischen Patienten gerade in Folge medikamentenbedingter Gewichtszunahme – besonders bedeutsam.
Kasuistiken
Fall A
Eine 35-jährige Patientin mit einer schizoaffektiven Psychose musste wegen einer schweren psychotischen Symptomatik erstmalig psychiatrisch hospitalisiert werden. Bei Aufnahme bestand seit einigen Wochen eine Medikation mit Fluoxetin 40 mg/Tag und Alprazolam 2 mg/Tag. Die initial bestimmten Leberwerte lagen im Normbereich, anamnestisch fanden sich keine Hinweise für eine chronische Lebererkrankung oder einen Alkoholmissbrauch.
Fluoxetin wurde abgesetzt, Alprazolam innerhalb von drei Tagen ausgeschlichen. Im Verlauf erhielt die Patientin synchron Quetiapin (max. 800 mg/Tag) und Chlorprothixen (max. 150 mg/Tag). Darunter kam es zu einem Anstieg der Transaminasen (maximal bis zum Vierfachen des oberen Normwerts), geringgradig auch der alkalischen Phosphatase (AP, max. 116 U/l, Normbereich: bis 98 U/l) und der Gammaglutamyltransferase (γ-GT, max. 37 U/l, Normbereich: bis 32 U/l). Am Tage der maximalen Transaminasenwerte wurde zusätzlich erstmals Lorazepam gegeben.
In der Folge wurden Quetiapin und Lorazepam ausgeschlichen und Chlorprothixen abgesetzt mit schließlich vollständiger Normalisierung der Leberwerte. Die Patientin wurde mit einer Kombination aus Trazodon 200 mg/Tag und Escitalopram 20 mg/Tag entlassen.
Beurteilung. Auf Grund des Enzymverlaufs kann von einer transienten medikamentös-toxischen Leberschädigung zytolytischer Art ausgegangen werden. Ursächlich müssen angesichts des zeitlichen Verlaufs und positivem Dechallenge Quetiapin und Chlorprothixen in der Kombination als „wahrscheinliche“ Ursachen gemäß AMSP-Kriterien angeschuldigt werden. Für beide Substanzen sind Leberwerterhöhungen als unerwünschte Wirkung (UAW) bekannt. Im vorliegenden Fall ist von einem additiven Effekt auszugehen.
Fall B
Eine 68-jährige Patientin wurde wegen einer schweren depressiven Episode bei rezidivierender depressiven Störung (ICD-10 F33.2) stationär aufgenommen, bei insgesamt zwei stationären Voraufenthalten. Die Patientin war ambulant zuletzt mit Opipramol behandelt worden.
Vorbestehende Risikofaktoren für eine Leberfunktionsstörung waren eine Steatosis hepatis, eine Fettstoffwechselstörung sowie Übergewicht.
Die Laborbefunde bei stationärer Aufnahme (14.10.) lagen im Normbereich oder waren diskret erhöht (Tab. 1).
Tab. 1. Verlauf der Leberwerte bei Fall B (AP = alkalische Phosphatase, AST = Aspartataminotransaminase [GOT, Glutamat-Oxalacetat-Transaminase], ALT = Alaninaminotransferase [GPT, Glutamat-Pyruvat-Transaminase], γ-GT = Gammaglutamyltransferase; in Klammern Normbereiche)
|
Datum |
AP [U/l] |
AST [U/l] |
ALT [U/l] |
γ-GT [U/l] |
|
15.10.2003 |
67 |
38 |
50 |
27 |
|
05.11.2003 |
78 |
23 |
52 |
17 |
|
24.11.2003 |
86 |
43 |
302 |
200 |
|
01.12.2003 |
82 |
28 |
84 |
113 |
Weitere Befunde. Cholesterol 270 mg/dl (Normbereich: <200 mg/dl); HDL 38 mg/dl, LDL 197 mg/dl (LDL/HDL-Quotient 5,2); Triglyceride 213 mg/dl (Normbereich: <200 mg/dl); HbA1c 6,1 % (Normbereich: <6,05 %), bei Kontrolle 5,8 %.
Bei einer Körpergröße von 163 cm lag das Körpergewicht bei 75 kg (Body-Mass-Index [BMI] 29,4 kg/m2).
In der Ultraschalluntersuchung des Abdomens zeigten sich neben einer Aortensklerose eine Steatosis hepatis und eine Pankreas-Lipomatose.
Medikation. Die Patientin erhielt vom 16.10. bis 23.10. zunächst 15 mg/Tag, danach bis zum 24.11. 30 mg/Tag Mirtazapin. Diese Substanz wurde wegen der erhöhten Leberwerte am 25.11. abgesetzt.
Zusätzlich nahm sie seit dem 14.10. fortlaufend bis zur Entlassung 105 mg/Tag Chlorprothixen und vom 14.10. bis zum 17.11. 10 mg/Tag Zolpidem.
Beurteilung. Da sowohl Mirtazapin als auch Chlorprothixen prinzipiell eine Leberwerterhöhung verursachen können, war es problematisch, nach Absetzen von Mirtazapin und Erholung der Laborwerte Mirtazapin allein für die UAW anzuschuldigen. Deshalb wurde im Rahmen der AMSP-Erfassung die Kombination angeschuldigt, allerdings wurde das nicht abgesetzte Chlorprothixen mit einem „möglichen“ Zusammenhang, Mirtazapin als „wahrscheinliche“ Ursache eingeschätzt (definiert nach AMSP-Kriterien). Bei der Gesamtschau ist hervorzuheben, dass die Risikofaktoren Fettleber, Übergewicht und Fettstoffwechselstörung zu einer medikamentös-toxischen Reaktion disponieren und bei Patienten mit solchen Vorerkrankungen ein höheres Risiko von toxischen Leberreaktionen zu berücksichtigen ist.
Fall C
Eine 47-jährige Patientin wurde unter der Diagnose einer mittelgradigen depressiven Episode bei bipolarer affektiver Störung tagesklinisch behandelt. Zusätzlich bestanden eine Adipositas (aktueller BMI 26 kg/m2, anamnestisch Gewichtsabnahme in den letzten Jahren) sowie ein Turner-Syndrom, das mit einem Estrogen-Gestagen-Sequenzpräparat behandelt wurde. Ein Alkoholkonsum bestand nicht.
Bei Aufnahme (5.2.) zeigte sich unter einer länger bestehenden Olanzapin-Therapie (2,5 mg/Tag) eine leichte Erhöhung der Leberwerte, die nach Dosiserhöhung von Olanzapin auf 5 mg/Tag und Zugabe von Citalopram bis 40 mg/Tag deutlich progredient war (z.B. GLDH ca. 10fach des oberen Grenzwerts [5 U/l] innerhalb von 4 Wochen). Olanzapin wurde deswegen abgesetzt, wobei zunächst noch ein leichter weiterer Anstieg der Leberenzyme messbar war. Bei erneuter Kontrolle zehn Tage nach Absetzen von Olanzapin waren die Leberwerte rückläufig, jedoch insgesamt noch deutlich erhöht (z.B. GLDH 6- bis 7fach des oberen Grenzwerts), so dass auch Citalopram abgesetzt wurde. GLDH und AST normalisierten sich in der Folge innerhalb kurzer Zeit, ALT und γ-GT waren rückläufig (Abb. 1).
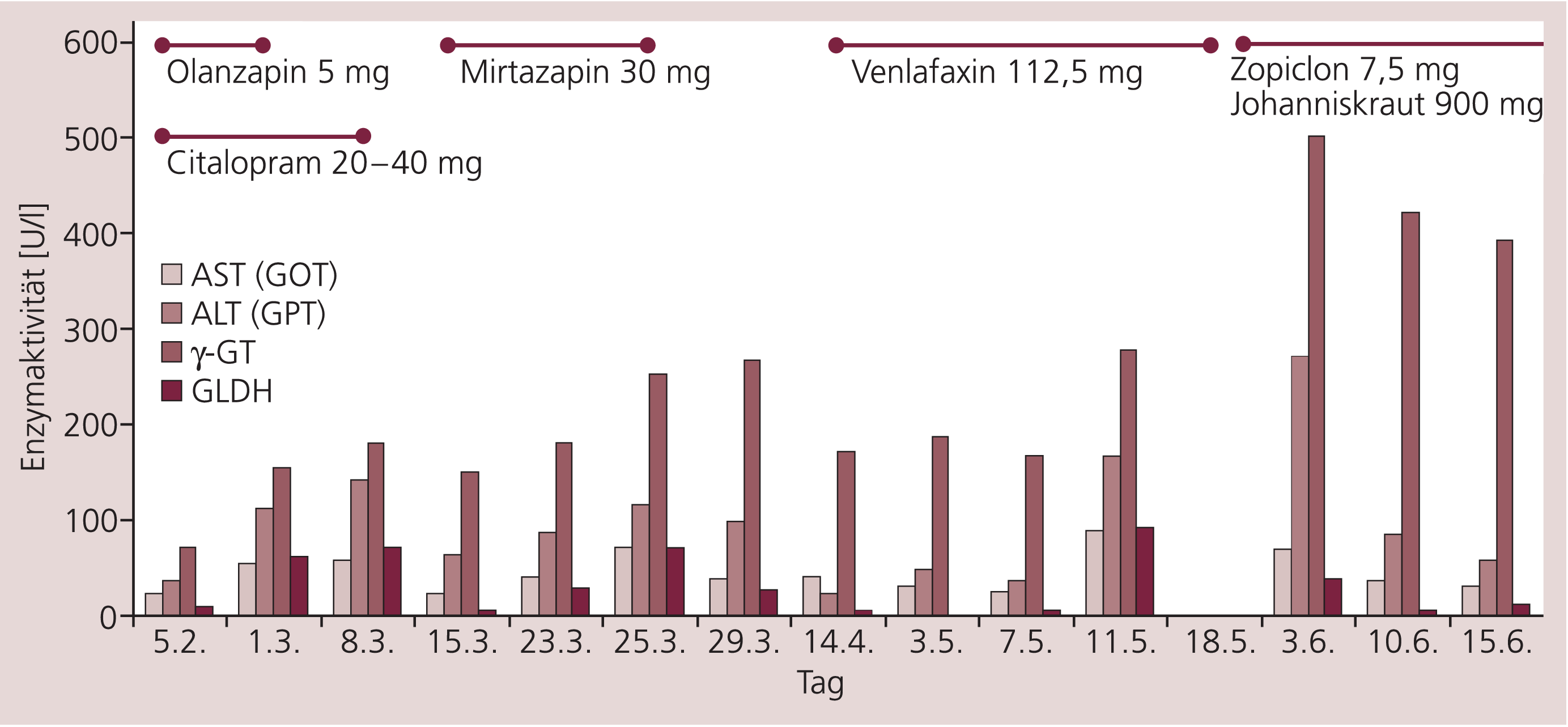
Abb. 1. Verlauf der Leberwerte bei Fall C (AST = Aspartataminotransaminase [GOT, Glutamat-Oxalacetat-Transaminase], ALT = Alaninaminotransferase [GPT, Glutamat-Pyruvat-Transaminase], γ-GT = Gammaglutamyltransferase, GLDH = Glutamatdehydrogenase)
Umstellungsversuche auf zunächst Mirtazapin und später Venlafaxin führten in beiden Fällen ebenfalls zu einer deutlichen, nach Absetzen jeweils rückläufigen Leberwerterhöhung (nach Venlafaxin verzögert unter Weiterbehandlung mit Johanniskraut, 900 mg/Tag und Zopiclon, 7,5 mg/Tag). Dies gab Anlass zu einer intensiveren hepatologischen Untersuchung der Patientin. Sonographisch fand sich eine Steatosis hepatis mit rarefizierter Gefäßstruktur. Eine autoimmune Lebererkrankung, eine chronische Virushepatitis oder eine Stoffwechselstörung wurden ausgeschlossen. Zusammenfassend wurde der Verdacht auf eine nichtalkoholische Fettleberhepatitis mit beginnendem Leberumbau gestellt und dies hauptsächlich auf die Adipositas zurückgeführt. Differenzialdiagnostisch wurde von internistischer Seite eine medikamentös-toxische Leberschädigung erwogen.
Beurteilung. Der dargestellte Verlauf zeigt, dass bei Patienten mit wiederholtem Anstieg von Leberenzymen unter unterschiedlichen Psychopharmaka unbedingt eine genauere hepatologische Diagnostik durchgeführt werden sollte, da eine vorbestehende Lebererkrankung anzunehmen ist. Auch in diesem Fall ist eine Adipositas offenbar wesentlich für die Lebervorschädigung, so dass bei Patienten mit Adipositas immer auch an eine Fettleber und damit eine besondere Vulnerabilität der Leber gedacht werden muss. Wie der Fall bestätigt, ist unter diesen Umständen ein pathologischer Anstieg von Leberenzymen wahrscheinlich auch unter anderen Psychopharmaka als den bisher verabreichten zu erwarten, so dass eine medikamentöse Therapie deshalb ganz besonders abzuwägen ist.
Diskussion
Schädigungen der Leber können medikamentös-toxisch direkt die Hepatozyten (Nekrose, Steatose) oder die duktalen Zellen der Gallenwege (Cholestase) betreffen oder immunologisch induziert sein (Hypersensitivitätsreaktion).
Bei den Antidepressiva besitzen trizyklische Substanzen gegenüber selektiven Serotonin-Wiederaufnahmehemmern (SSRI) ein erhöhtes hepatotoxisches Risiko [4, 10]. Im AMSP-Projekt [5] waren ausgeprägte Leberenzymanstiege unter trizyklischen Antidepressiva mit einer Inzidenz von 0,16 % die zweithäufigste UAW-Art; unter Mirtazapin waren sie bei insgesamt 4750 überwachten Patienten die häufigste UAW. In einer englischen Studie wurden bei 13554 Patienten, die mit Mirtazapin behandelt wurden, 12 Fälle mit einer deutlich erhöhten Leberenzymaktivität dokumentiert [3]. Kasuistisch wurden zwei Patientinnen mit Mirtazapin-induziertem protrahiertem Ikterus beschrieben [8].
Bei den Antipsychotika besitzen vor allem trizyklische Substanzen ein erhöhtes lebertoxisches Risiko. Isolierte Leberwerterhöhungen wurden unter Phenothiazinen bis zu 20 %, toxische Hepatitiden unter Phenothiazinen zwischen 0,1 und 1 %, unter Haloperidol bei 0,002 % beobachtet [6].
Bei den atypischen Antipsychotika wurden besonders unter Clozapin (transient) erhöhte Leberwerte beobachtet [6]. In einer prospektiven Studie verglichen Hummer und Mitarbeiter [9] insgesamt 238 Patienten, die entweder Clozapin oder Haloperidol erhielten. Bei 37,3 % der Patienten in der Clozapin-Gruppe, gegenüber 16,6 % in der Haloperidol-Gruppe, zeigte sich ein Anstieg der Leberfunktionswerte über das 2fache des oberen Referenzwerts. Im Rahmen des AMSP-Systems wurden unter Clozapin bei 15414 überwachten Patienten 14 Fälle, unter Olanzapin bei 9231 überwachten Patienten sogar 17 UAW-Fälle mit massiven Leberenzym-Anstiegen beobachtet [2].
Über schwere hepatische UAW unter den modernen Atypika liegen mehrere kasuistische Darstellungen vor. El Hajj und Mitarbeiter [7] berichteten von einem tödlich verlaufenden Leberversagen unter Quetiapin, Raz et al. [12] von einer schweren toxischen Hepatitis im Rahmen eines Hypersensitivitäts-Syndroms 60 Tage nach Beginn einer Olanzapin-Medikation, Benazzi [1] von schweren Funktionsstörungen der Leber unter Risperidon.
Die vorliegenden Fälle des AMSP-Projekts zeigen, dass sowohl bei verschiedenen älteren Substanzen (Chlorprothixen) als auch bei neueren Antidepressiva (Citalopram, Mirtazapin, Venlafaxin) und Antipsychotika (Olanzapin, Quetiapin) mit lebertoxischen Effekten gerechnet werden muss. Dabei waren in den hier vorgestellten Kasuistiken die Leberwerte nach Reduktion beziehungsweise Absetzen erfreulicherweise jeweils rückläufig und es kam zu keinen schwerwiegenden Komplikationen.
Literatur
1. Benazzi F. Risperidone-induced hepatotoxicity. Pharmacopsychiatry 1998;31:241.
2. Bender S, Grohmann R, Kropp S, et al. Severe adverse drug reactions in psychiatric inpatients treated with neuroleptics. Pharmacopsychiatry 2004;37(Suppl 1):46–53.
3. Biswas PN, Wilton LV, Shakir SV. The pharmacovigilance of mirtazapine: results of a prescription monitoring study on 13554 patients in England. J Psychopharmacol 2003;1:121–6.
4. Carvajal GP, Garcia D, Sandoz SA, et al. Hepatotoxicity associated with the new antidepressants. J Clin Psychiatry 2002;63:135–7.
5. Degner D, Grohmann R, Kropp S, et al. Severe adverse drug reactions of antidepressants: results from the German multicenter drug surveillance program AMSP. Pharmacopsychiatry 2004;37(Suppl 1):39–45.
6. Dumortier G, Cabaret W, Stamtiadis L, et al. Hepatic tolerance of atypical antipsychotic drugs. Encephale 2002;28:542–51.
7. El Hajj I, Sharara A, Rockey DC. Subfulminant liver failure associated with quetiapine. J Gastroenterol Hepatol 2004;16:1415–8.
8. Hui CK, Yuen MF, Wong WM, et al. Mirtazapine induced hepatoxicity. J Clin Gastroenterology 2002;35:270–1.
9. Hummer M, Kurz M, Kurzthaler I, et al. Hepatotoxicity of clozapine. J Clin Psychopharmacol 1997;17:314–7.
10. Lucena MI, Carvajal A, Andrade RJ, et al. Antidepressant-induced hepatotoxicity. Expert Opin Drug Saf 2003;2:249–62.
11. Rüther E, Grohmann R, Degner D. Lebertoxische unerwünschte Arzneimittelwirkungen unter Psychopharmaka. Psychopharmakotherapie 2004;11:132.
12. Raz A, Berman R, Eilam O, et al. A case report of olanzapine-induced hypersensitivity syndrome. Am J Med Sci 2001;321:156–8.
Dr. med. Detlef Degner (Korrespondenzautor), Klinik für Psychiatrie und Psychotherapie der Georg-August-Universität Göttingen, von-Siebold-Str. 5, 37075 Göttingen, E-Mail: ddegner@gwdg.de
Dr. med. Patrik Lukas Stephan, Dr. Eveline Jaquenoud-Sirot, Psychiatrische Klinik Königsfelden, Psychiatrische Dienste des Kantons Aargau, Postfach 298, 5201 Brugg, Schweiz
Dr. Roswitha Thilmann, Kliniken Essen-Mitte, Evangelische Huyssens-Stiftung, Abteilung für Psychiatrie, Henricistr. 92, 45136 Essen
Dr. Beate Schmidt, Dr. Berit Wenda, Klinikum der Friedrich-Schiller-Universität Jena, Klinik für Psychiatrie, Philosophenweg 3, 07740 Jena
Dr. Renate Grohmann, Klinik für Psychiatrie der Ludwig-Maximilians-Universität München, Nussbaumstr. 7, 80336 München
Psychopharmakotherapie 2005; 12(03)
