Alexander Brunnauer, Elisabeth Geiger, Wasserburg, Gerd Laux, Wasserburg und München, Thomas Glaser, Leverkusen, Michael Soyka und Hans-Jürgen Möller, München
Schizophrene Erkrankungen gehen meist mit Störungen der Informationsverarbeitung einher, die bereits in Prodromalphasen der Erkrankung zu sehen sind [1, 14] und oft trotz Remission der psychopathologischen Symptomatik bestehen bleiben [10, 13, 15]. Bei den Betroffenen können sie zu Beeinträchtigungen in weiten Bereichen des alltäglichen Lebens führen [11, 26].
Vor dem Hintergrund steigender Mobilitätsanforderungen und Mobilitätsbedürfnisse sind Fragen zur Medikamentensicherheit in der klinischen Praxis von besonderer Bedeutung. Die epidemiologische Datenlage zu Unfallrisiken von psychiatrischen Patienten unter Psychopharmakotherapie ist jedoch dünn und von methodischen Problemen gekennzeichnet. Insgesamt scheinen psychisch kranke Patienten weniger häufig als Gesunde aktiv am Straßenverkehr teilzunehmen, bei gleichzeitig erhöhtem Risiko in einen Unfall verwickelt zu werden [7, 8, 27].
Atypika haben im Vergleich zu konventionellen Neuroleptika Vorteile bezüglich psychomotorischer und kognitiver Leistungen [12, 18, 22]. Systematische Studien zu Auswirkungen psychotroper Medikation auf psychomotorische und kognitive Funktionen in klinischen Populationen existieren jedoch nur vereinzelt. Bezogen auf die Frage der Verkehrssicherheit stellt sich die Datenlage als noch unbefriedigender dar [2, 19, 20]. Die meisten Untersuchungen zu dieser Thematik wurden an gesunden Probanden unter Einmaldosierungen durchgeführt und sind somit nur begrenzt auf klinische Alltagsbedingungen übertragbar. Nur in wenigen Studien wurde der Frage der Verkehrssicherheit bei stationär behandelten Patienten nachgegangen. In diesen Untersuchungen konnte gezeigt werden, dass ein Großteil der Patienten mit schizophrenen Erkrankungen kurz vor Entlassung aus der stationären Behandlung und unter pharmakologischen Steady-State-Bedingungen, deutliche Einbußen im Bereich der psychomotorischen Leistungsfähigkeit aufweisen [3, 9, 16, 25]. Darüber hinaus belegen diese Untersuchungen einen Vorteil von Atypika gegenüber konventionellen Neuroleptika in Bezug auf die psychomotorische Leistungsfähigkeit.
Von verschiedenen Autoren wird Flupentixol (Fluanxol®) auf Grund des Rezeptorbindungsprofils sowie der klinischen Wirksamkeit, als partiell atypisches Antipsychotikum bezeichnet [23, 24]. In der vorliegenden Studie wurde folgenden Fragen nachgegangen:
Unterscheidet sich die psychomotorische Leistungsfähigkeit von Patienten, die mit Flupentixol behandelt werden, von Patienten unter Haloperidol (z. B. Haldol®)?
Zeigen Patienten, die mit Flupentixol behandelt werden, vergleichbare Leistungen in den untersuchten Bereichen, wie Patienten, die mit dem atypischen Antipsychotikum Risperidon (Risperdal®) behandelt werden?
Gemäß den Begutachtungs-Leitlinien zur Kraftfahrereignung [21] wurden folgende Funktionsbereiche untersucht:
- Optische Orientierung
- Aufmerksamkeit
- Konzentrationsfähigkeit
- Reaktionsfähigkeit
- Belastbarkeit
Zudem hatten die Patienten verschiedene Risikosimulationen in einem Fahrsimulator zu absolvieren.
Patienten und Methoden
In die Stichprobe eingeschlossen wurden 47 schizophrene Patienten im Alter zwischen 21 und 60 Jahren, davon 17 Frauen und 30 Männer.
Alle Personen wurden unter pharmakologischen Steady-State-Bedingungen und unter antipsychotischer Monotherapie untersucht und befanden sich zum Zeitpunkt der Testung in der letzten stationären Behandlungswoche. Die einzig erlaubte Begleitmedikation war Biperiden (z.B. Akineton®) bei Anzeichen von extrapyramidal-motorischen Nebenwirkungen. 16 Patienten erhielten Flupentixol (5,5 mg ± 3,1 mg), 15 Risperidon (4,1 mg ± 1,6 mg) und 16 Patienten Haloperidol (6,3 mg ± 4,1 mg).
Die Klassifizierung erfolgte nach der Internationalen Klassifikation psychischer Erkrankungen (ICD-10).
Psychometrische Verfahren
Nach schriftlicher Einverständniserklärung zur Teilnahme an der Studie erfolgte am Untersuchungstag eine Einschätzung der aktuellen psychopathologischen Symptomatik anhand von CGI (Clinical Global Impression Scale) und BPRS (Brief Psychiatric Rating Scale) durch den jeweils behandelnden ärztlichen Kollegen. Zudem wurde das Ausmaß extrapyramidal-motorischer Nebenwirkungen mit der EPS-Skala (Extrapyramidale-Symptom-Skala) quantifiziert.
Psychomotorische Leistungsfähigkeit
Zur Erhebung der psychomotorischen Leistungsparameter kamen das computergestützte Act & React Testsystem – ART 90 (Kuratorium f. Verkehrssicherheit) sowie das Wiener Testsystem – WTS (Fa. Schuhfried) zum Einsatz. In einer Reihe von verkehrspsychologischen Untersuchungen wurde die hohe Reliabilität und Validität dieser Messinstrumente bestätigt [4, 5, 17]. In Anlehnung an die Fahrerlaubnisverordnung (FeV) wurden die Funktionsbereiche optische Orientierung, Aufmerksamkeit, Konzentrationsfähigkeit, Reaktionsfähigkeit und Belastbarkeit untersucht und anhand der dort festgelegten Grenzwertdefinition beurteilt. Die visuelle Orientierungsleistung wurde mit dem Tachistoskoptest (TT15) gemessen. Beim TT15 müssen zu tachistoskopisch (0,75 s) vorgegebenem Bildmaterial mit typischen Verkehrssituationen Multiple-Choice-Fragen beantwortet werden.
Reaktionsfähigkeit und Belastbarkeit wurden mit dem Reaktions- und Stresstoleranztest RST3 erfasst. In drei vom Interstimulusintervall (ISI) her unterschiedlichen Subtests (ISI-Phase-I = 1,58 s; Phase-II = 0,95 s und Phase-III = 1,07 s) werden jeweils 180 Farb-, Ton- und Lichtstimuli präsentiert; auf diese ist mit Fußpedalen, Farb- und Ton-Reaktionstasten zu reagieren.
Die Leistungsbereiche Aufmerksamkeit und Konzentration wurden mit zwei Subtests untersucht. Der Vigilanztest (VIGIL) erfordert die Aufrechterhaltung der Aufmerksamkeit unter Monotoniebedingungen: Über einen Zeitraum von 25 Minuten sind auf einer Kreisbahn Unregelmäßigkeiten in einer Bewegungsabfolge zu erkennen. Es werden 100 kritische Reize ausgegeben, auf die mit Tastendruck zu reagieren ist. Aspekte der Konzentrationsfähigkeit wurden mit dem Aufmerksamkeitsflexibilitätstest (FAT) gemessen: Das Reizmaterial besteht aus einfachen Zeichen, deren Identität der Patient zu beurteilen hat. Der Test dauert etwa sieben Minuten.
Fahrsimulator
Der Fahrtrainer FT-SR 200 ist ein statischer Fahrsimulator mit verschiedenen Realbildaufnahmen von Verkehrssituationen. Der Patient sitzt in einem Original-Autocockpit vor einem Monitor. Informationen über Lenkbewegung, Bremsbetätigung und Geschwindigkeit werden über einen Computer aufgezeichnet. Verschiedene Risiko- und Übungssimulationen können vom Versuchsleiter eingespielt werden, auf die der Patient reagieren muss. Die Simulation wird ergänzt durch akustische Effekte, wie Motorengeräusche.
Um sich mit der Bedienung des Fahrsimulators vertraut zu machen, mussten die Patienten in einer Eingewöhnungsphase eine etwa fünf Minuten dauernde, simulierte Überlandfahrt mit unterschiedlichen Geschwindigkeitsanforderungen absolvieren. Hieran schloss sich die Untersuchungsphase mit vier verschiedenen Risikosimulationen an. Als kritische Variable ging die Anzahl an Unfällen in die Auswertung ein.
Statistische Analyse
Die inferenzstatistische Analyse erfolgte mittels χ2- und Mann-Whitney-U-Test sowie multivariaten Verfahren, unter Berücksichtigung der Medikation, des Alters und des Schweregrads der Erkrankung als Kovariate. Die Berechnung erfolgte mit dem Statistikprogramm SPSS (Version 10.0).
Ergebnisse
Da sich die Medikamentengruppen signifikant bezüglich der Altersverteilung, des BPRS-Summenscore und der Dosierung unterschieden (Tab. 1), wurden die nachfolgenden multivariaten Analysen unter Berücksichtigung dieser Variablen als Kovariaten berechnet.
Tab. 1. Soziodemographische und klinische Daten (* = p < 0,05; Standardabweichung in Klammern; n.s. = nicht signifikant)
|
Flupentixol |
Risperidon |
Haloperidol |
Statistische Signifikanz* |
|
|
Alter [Jahre] |
32,6 (11,4) |
33,9 (9,9) |
42,3 (8,5) |
Flupentixol < Haloperidol |
|
Geschlecht (männlich/weiblich) |
9/7 |
11/4 |
10/6 |
n. s. |
|
Ausbildung [Jahre] |
10,3 (1,1) |
11,3 (2,6) |
11,6 (2,9) |
n. s. |
|
Führerscheinbesitz [Jahre] |
16,1 (11,9) |
16,2 (10,5) |
23,8 (7,9) |
n. s. |
|
Diagnose |
||||
|
– Paranoide Schizophrenie (F20.0) |
8 |
12 |
15 |
– |
|
– Hebephrene Schizophrenie (F20.1) |
4 |
– |
– |
– |
|
– Undifferenzierte Schizophrenie (F20.3) |
1 |
1 |
– |
– |
|
– Akute polymorphe psychotische Störung mit Symptomen einer Schizophrenie (F23.1) |
3 |
1 |
1 |
– |
|
– Schizoaffektive Störung (F25.0) |
– |
1 |
– |
– |
|
Chlorpromazin-Äquivalente [mg] |
275,0 (154,9) |
206,6 (82,1) |
315,9 (158,0) |
Risperidon < Haloperidol |
|
Komedikation (Biperiden) [n] |
1 |
– |
3 |
– |
|
CGI |
5,3 (0,7) |
4,8 (0,9) |
5,6 (0,7) |
Risperidon < Haloperidol |
|
BPRS |
49,6 (31,2) |
31,0 (16,3) |
52,8 (10,6) |
Flupentixol > Risperidon |
|
EPS-Skala |
0,4 (0,3) |
0,6 (0,4) |
0,5 (0,4) |
n. s. |
Globaler Fahrtauglichkeitsscore
In einem ersten Analyseschritt wurde gemäß den Begutachtungs-Leitlinien zur Kraftfahrereignung ein Testergebnis mit einem altersunabhängigen Prozentrangwert < 16 als auffällig gewertet. Legt man diese Grenzwertdefinition zu Grunde, erfüllen lediglich 28 % der schizophrenen Patienten die Leistungskriterien zum Führen von Kraftfahrzeugen der Gruppe 1 (< 3,5 t).
Die Einzelvergleiche mittels Mann-Whitney-U-Test ergaben einen statistisch signifikanten Unterschied in der globalen Fahrtauglichkeitsmessung zwischen den mit Haloperidol und Risperidon behandelten Patienten (p < 0,05; z = –1,94). Zusätzlich wurde in Anlehnung an Grabe et al. [9] eine Einteilung anhand der Globalanalyse vorgenommen in:
„Moderate Beeinträchtigung”, das heißt, in bis zu 40 % der Testvariablen wurde ein Prozentrang <16 erzielt
„Schwerwiegende Beeinträchtigungen” – in mehr als 40 % der kritischen Parameter wurde der kritische Schwellenwert unterschritten
Dieser Einteilung liegt die Überlegung zu Grunde, dass die Kriteriumsbeurteilung keine Informationen über Leistungen über dem Prozentrang 16 enthält. Es ist davon auszugehen, dass in der Gruppe der moderat beeinträchtigten Patienten Leistungseinbußen bis zu einem gewissen Grad kompensiert werden können und in diesen Fällen somit eine individuelle Beratung erforderlich ist. Abbildung 1 fasst die Ergebnisse der Kriteriumsbeurteilung in den einzelnen Behandlungsgruppen zusammen.
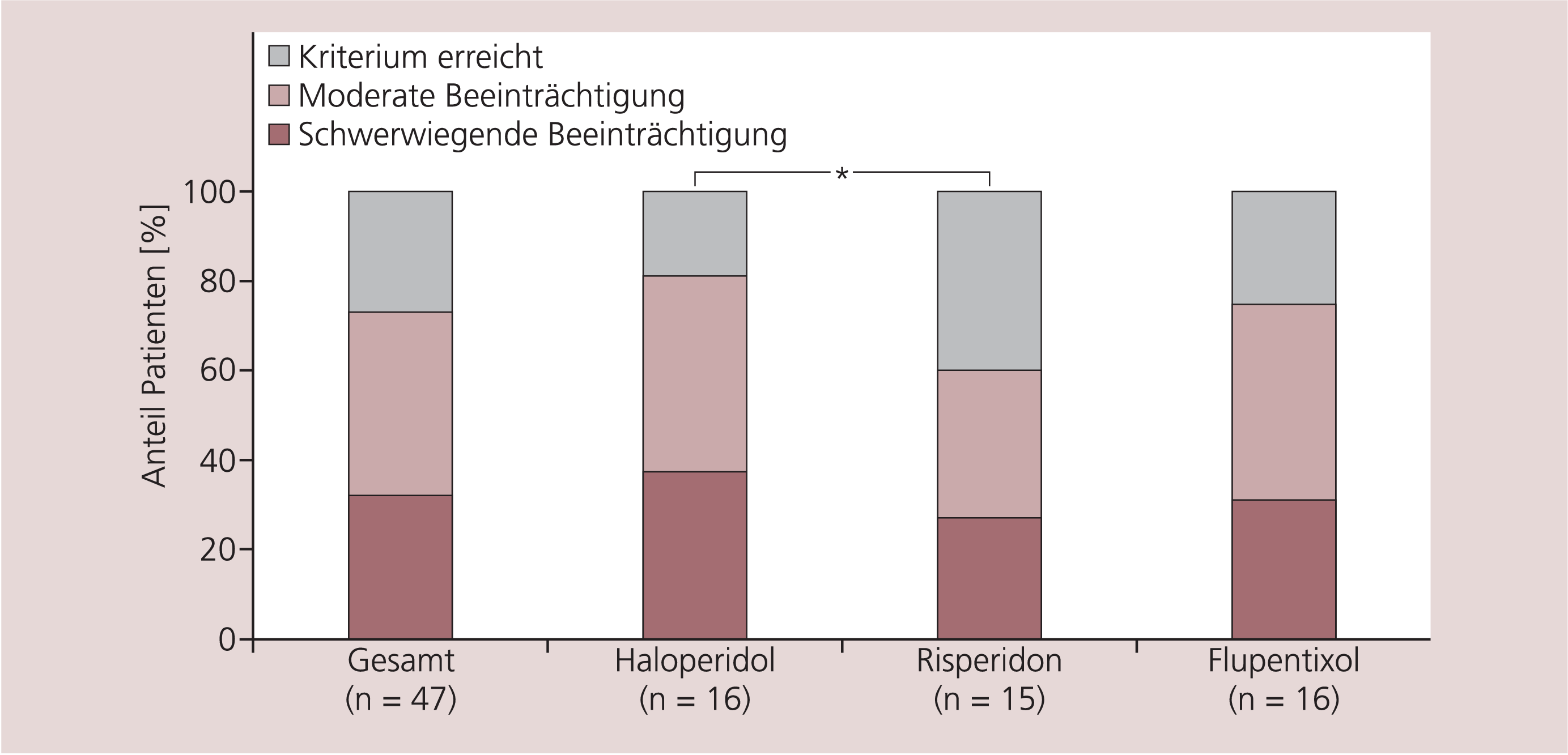
Abb. 1. Ergebnisse der globalen Fahrtüchtigkeitsbeurteilung (*p < 0,05)
Psychomotorische Leistungsparameter
Um Gruppenunterschiede in den einzelnen Testparametern zu objektivieren wurden die Daten mittels multivariater Kovarianzanalyse analysiert. Patienten, die mit Risperidon oder Haloperidol behandelt wurden, unterschieden sich signifikant in den Leistungsparametern. Die übrigen Gruppenvergleiche ergaben keine statistisch bedeutsamen Unterschiede (Tab. 2).
Tab. 2. Ergebnisse der Leistungsuntersuchung (Standardabweichung in Klammern; *=multivariate Analyse mit den Kovariaten Alter, BPRS und Chlorpromazin-Äquivalente
|
Flupentixol |
Risperidon |
Haloperidol (n = 16) |
Zwischengruppeneffekte* Analyse |
|
|
Verkehrsspezifischer tachistoskopischer Test (TT15) |
Flupentixol vs. Haloperidol F1,31 = 0,51 Risperidon vs. Haloperidol F1,30 = 2,49 Flupentixol vs. Risperidon F1,30 = 0,44 n. s. |
|||
|
Richtige |
31,1 (3,4) |
31,2 (3,3) |
30,8 (3,9) |
|
|
Aufmerksamkeitsflexibilitätstest (FAT) |
||||
|
Fehler [%] |
4,5 (2,8) |
4,1 (2,8) |
6,7 (7,2) |
|
|
Vigilanztest (VIGIL) |
||||
|
Summenscore |
3,1 (2,3) |
2,6 (1,7) |
3,5 (2,3) |
|
|
Reaktions- u. Stresstoleranztest (RST3) |
||||
|
Langsame Phase (Phase 1) |
||||
|
Auslasser |
4,3 (5,9) |
2,4 (3,5) |
7,5 (6,9) |
|
|
Verzögerte |
6,6 (5,5) |
7,6 (9,7) |
9,9 (9,1) |
|
|
Schnelle Phase (Phase 2) |
||||
|
Auslasser |
43,1 (26,7) |
43,4 (30,6) |
48,9 (29,0) |
|
|
Verzögerte |
60,7 (24,6) |
57,5 (24,7) |
63,1 (21,9) |
|
|
Moderate Phase (Phase 3) |
||||
|
Auslasser |
19,3 (19,1) |
25,1 (28,5) |
27,3 (26,7) |
|
|
Verzögerte |
41,3 (24,9) |
37,0 (27,2) |
42,4 (28,7) |
|
Die nachfolgend durchgeführten univariaten F-Tests bestätigten diesen Trend. Mit Risperidon behandelte Patienten zeigten im Vergleich zu den mit Haloperidol behandelten ein besseres Leistungsniveau im Bereich der Reaktionsfähigkeit und Belastbarkeit (RST3 Phase 2 Verzögerte: F1,30 = 3,95, p = 0,05; RST3 Phase 3 Auslasser: F1,30 = 6,78, p = 0,01; RST3 Phase 3 Verzögerte: F1,30 = 3,97, p = 0,05).
Fahrsimulator
Die Ergebnisse der Fahrsimulation, bei der verschiedene riskante Verkehrssituationen bewältigt werden mussten, sind in Abbildung 2 dargestellt.
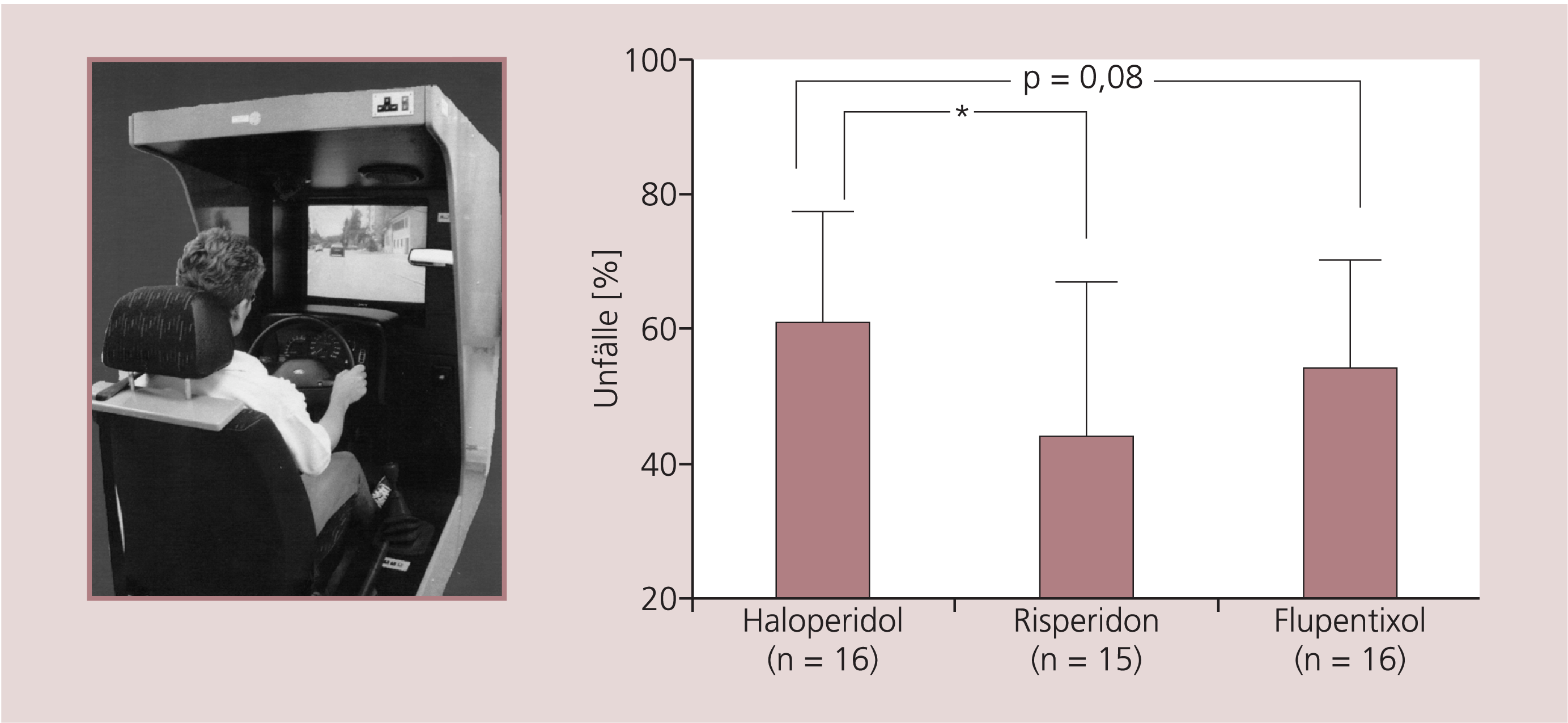
Abb. 2. Ergebnisse der Fahrsimulation
Die besten Ergebnisse erzielten Patienten mit Risperidon mit einer prozentualen Unfallhäufigkeit von 44 % in der Simulation, das niedrigste Leistungsniveau zeigte sich bei den mit Haloperidol behandelten Patienten (61 % Unfallhäufigkeit). Die Berechnung des Korrelationskoeffizienten zwischen den Ergebnissen der Fahrsimulation und dem globalen Fahrtauglichkeitsscore weisen auf signifikante Zusammenhänge hin (r = –0,58; p < 0,01). Die paarweisen Vergleiche mittels Mann-Whitney-U-Test ergaben signifikante Unterschiede in der Risikosimulation zwischen der Gruppe, die mit Risperidon oder Haloperidol behandelt wurden (p = 0,03; z = –2,02). Zudem weist die Analyse auf Unterschiede beim Vergleich von Flupentixol mit Haloperidol hin (p = 0,08; z = –1,42).
Diskussion
Bei einem hohen Prozentsatz der kurz vor Entlassung aus stationärer Behandlung stehenden schizophrenen Patienten ließen sich erhebliche Beeinträchtigungen der psychomotorischen Leistungsfähigkeit und somit der Fahrtüchtigkeit beobachten. Lediglich 28 % der Patienten erreichten die vom Gesetzgeber geforderten Leistungskriterien zum Führen eines Kraftfahrzeugs < 3,5 t.
Die Ergebnisse der vorliegenden Studie stehen im Einklang mit vergleichbaren Untersuchungen, die unter pharmakologischen Steady-State-Bedingungen, bei weitgehend remittierten schizophrenen Patienten, eine eingeschränkte Fahrtüchtigkeit objektivieren konnten [3, 9, 16, 25]. In der Gruppe der mit Haloperidol behandelten Patienten erreichten 19 % diese Mindestanforderungen, unter Flupentixol 25 % und unter Risperidon 40 %. Bei etwa 40 % der schizophrenen Patienten, die als moderat beeinträchtigt klassifiziert wurden, erscheint unter Berücksichtigung von Kompensationsfaktoren eine individuelle Beurteilung der Fahrtüchtigkeit gerechtfertigt. Je nach Medikamentengruppe ist bei etwa 23 % bis 38 % der Patienten von schwerwiegenden Einbußen auszugehen, deren Kompensation in Bezug auf die Fahrtüchtigkeit eher fragwürdig erscheint.
Atypische Antipsychotika wirken sich im Behandlungsverlauf meist günstiger auf psychomotorische und kognitive Funktionen aus, als konventionelle Neuroleptika. Dies vor allem auf Grund der geringeren extrapyramidal-motorischen Nebenwirkungen [22]. Eine Normalisierung attentionaler oder kognitiver Funktionen wird jedoch meist nicht erreicht [12, 18]. Patienten unter Flupentixol unterschieden sich in der vorliegenden Untersuchung in den Leistungsdaten und den Ergebnissen der Fahrsimulation nicht signifikant von denen, die mit Risperidon behandelt wurden. Gegenüber Haloperidol erzielten sie am Fahrsimulator ein tendenziell besseres Ergebnis. Die deskriptive Analyse über die verschiedenen Datenebenen hinweg weist darauf hin, dass die mit Flupentixol behandelten Patienten beim Vergleich mit Risperidon und Haloperidol eine Zwischenstellung einnehmen. Dieses Ergebnis lässt sich mit klinischen Untersuchungen zur Verkehrssicherheit in Einklang bringen, die belegen, dass Flupentixol innerhalb der Typika eine Sonderstellung einnimmt [3, 6].
Natürlich gibt es Einschränkungen bei der Interpretation der Ergebnisse, die in der Natur des Untersuchungsdesigns liegen. Ursächliche Aussagen zu pharmakologischen Wirkungen können im Rahmen dieser Untersuchung nicht getroffen werden. Eine randomisierte Zuteilung zu den Behandlungsgruppen erfolgte nicht. Zudem wurden nur Patienten in die Studie eingeschlossen, bei denen davon auszugehen war, dass sie eine etwa 120 Minuten dauernde Untersuchungseinheit bewältigen können. Somit ist ein Selektionsbias nicht auszuschließen. Auf der anderen Seite kann die Stärke dieser Studie in dem klinisch relevanten Untersuchungsdesign gesehen werden. Die Patienten standen kurz vor Entlassung aus der stationären Behandlung und unter einer nach klinischen Gesichtspunkten ausgewählten pharmakologischen Behandlung. Die Frage der Fahrtüchtigkeit war somit für die meisten Patienten von hoher Relevanz. Viele kontrollierte Studien werden meist in hoch selektierten Stichproben durchgeführt, deren Ergebnisse nur auf eine kleine Subgruppe von Patienten übertragbar sind.
Wer als Arzt oder Psychologe über die Sicherheit seiner Patienten nachdenkt, wird unweigerlich auch zu Fragen der Verkehrssicherheit Stellung nehmen müssen, was sowohl auf Seiten des Patienten als auch des Behandelnden meist mit großer Unsicherheit und Skepsis verbunden ist. Der Mobilität von Patienten kommt ein hoher Stellenwert zu, hängt hiervon doch oft der Erfolg beruflich-psychosozialer Wiedereingliederungsmaßnahmen und somit auch die Compliance des Patienten ab. Die informelle Abklärung der Fahrtüchtigkeit im Rahmen der stationären Behandlung kann auf Grund der hohen Relevanz dieser Thematik ein wichtiger Schritt zur Erarbeitung eines Störungsbewusstseins beim Patienten sein. Natürlich kann eine Beurteilung der Fahrtüchtigkeit nicht ausschließlich auf Basis der psychomotorischen Leistungsfähigkeit erfolgen. Die große interindividuelle Variabilität von Testleistungen schizophrener Patienten weist auf die Notwendigkeit einer individuellen Beurteilung hin. Fahrerfahrung oder Persönlichkeitsfaktoren nehmen als mögliche Kompensationsfaktoren bei Einschränkungen der Leistungsfähigkeit eine wichtige Stellung ein. Neben ausreichendem Wissen über die vorliegende Erkrankung und Mängel, sind Selbstbeobachtung, Verhaltenssteuerung und angemessene Verhaltensumstellung von zentraler Bedeutung. Bei der Behandlung von Patienten sollte die Wahl der psychotropen Medikation auch unter dem Aspekt der Verkehrs- und Alltagssicherheit erfolgen.
Diese Studie wurde mit finanziellen Mitteln der Fa. Bayer Vital GmbH unterstützt.
Danksagung
Wir danken Frau Michaela Wende und Frau Heidemarie Riedl für ihre Mitarbeit bei diesem Projekt.
Literatur
1. Bilder RM, Goldmann RS, Robinson D, Reiter G, et al. Neuropsychology of first-episode schizophrenia: initial characterization and clinical correlates. Am J Psychiatry 2000;157:549–59.
2. Brunnauer A, Laux G, Geiger E. Fahrtüchtigkeit und psychische Erkrankung. Z Neuropsychol 2004;15:209–18.
3. Brunnauer A, Laux G, Geiger E, Möller HJ. The impact of antipsychotics on psychomotor performance with regards to car driving skills. J Clin Psychopharmacol 2004;24:155–60.
4. Bukasa B, Christ R, Pocorny-Seliger E, Smuc M, et al. Validitätsüberprüfung verkehrspsychologischer Leistungstests für die Fahreignungsbegutachtung. Z Verkehrssicherheit 2003;49:191–7.
5. Bukasa B, Kisser R, Wenninger U. Computergestützte Leistungsdiagnostik bei verkehrspsychologischen Eignungsuntersuchungen. Diagnostica 1990;36:148–65.
6. Classen W, Laux G. Sensorimotor and cognitive performance of schizophrenic inpatients treated with haloperidol, flupenthixol, or clozapine. Pharmacopsychiatry 1988;21:295–7.
7. Edlund MJ, Conrad C, Morris P. Accidents among schizophrenic outpatients. Compr Psychiatry 1989;30:522–6.
8. Eelkema RC, Bronssean J, Koshnick R, McGee M. A statistical study on the relationship between mental illness and traffic accidents. Am J Public Health 1970;60:459–69.
9. Grabe HJ, Wolf T, Grätz S, Laux G. The influence of clozapine and typical neuroleptics on information processing of the central nervous system under clinical conditions in schizophrenic disorders: Implications for fitness to drive. Neuropsychobiology 1999;40:196–201.
10. Grawe RW, Levander S. Neuropsychological impairments in patients with schizophrenia: stability and prediction of outcome. Acta Psychiatr Scand 2001;104(Suppl 408):60–4.
11. Green MF. What are the functional consequences of neuropsychological deficits in schizophrenia? Am J Psychiatry 1996;153:321–30.
12. Green MF. Recent studies on the neurocognitive effects of second-generation antipsychotic medication. Curr Opin Psychiatry 2002;15:25–9.
13. Heaton RK, Gladsjo JK, Palmer BW, Kuck J, et al. Stability and course of neuropsychological deficits in schizophrenia. Arch Gen Psychiatry 2001;58:24–32.
14. Ho BC, Alicata D, Ward J, et al. Untreated initial psychosis: relation to cognitive deficits and brain morphology in first episode schizophrenia. Am J Psychiatry 2003;160:142–8.
15. Hoff AL, Kremen WS. Neuropsychology in schizophrenia: An update. Curr Opin Psychiatry 2003;16:149–55.
16. Kagerer S, Winter C, Möller HJ, Soyka M. Effects of haloperidol and atypical neuroleptics on psychomotor performance and driving ability in schizophrenic patients. Results from an experimental study. Neuropsychobiology 2003;47:212–8.
17. Karner T, Biehl B. Über die Zusammenhänge verschiedener Versionen von Leistungstests im Rahmen der verkehrspsychologischen Diagnostik. Z Verkehrssicherheit 2001;42:53–63.
18. Keefe RSE, Silva SG, Perkins DO, Liebermann JA. The effects of atypical antipsychotic drugs on neurocognitive impairment in schizophrenia: A review and meta-analysis. Schizophr Bull 1999;25:201–22.
19. Laux G. Psychomotorische Leistungsparameter und deren Beeinflussung während der Langzeitbehandlung unter besonderer Berücksichtigung von Fahrtauglichkeitsaspekten. In: Möller HJ, Staab H (Hrsg). Langzeitbehandlung mit Psychopharmaka. Stuttgart: Thieme Verlag, 1995:56–71.
20. Laux G. Psychische Störungen und Fahrtauglichkeit. Eine Übersicht. Der Nervenarzt 2002;73:231–8.
21. Lewrenz H. Begutachtungs-Leitlinien zur Kraftfahrereignung. Bremerhaven: Wirtschaftsverlag, 2000.
22. Meltzer HY, McGurk SR. The effects of clozapine, risperidone, and olanzapine on cognitive function in schizophrenia. Schizophr Bull 1999;25:233–55.
23. Messer T, Glaser T, Schmauß M. Therapeutischer Stellenwert von Flupentixol und Flupentixoldecanoat zur Therapie schizophrener Erkrankungen. Psychopharmakotherapie 2003;10:141–50.
24. Philipp M, Lesch OM, Schmauß M, Dose M, et al. Vergleichbare Wirksamkeit von Flupentixol und Risperidon auf schizophrene Negativsymptomatik. Psychiatr Prax 2003;30(Suppl 2):S94–6.
25. Soyka M, Winter C, Kagerer S, Brunnauer A et al. Effects of haloperidol and risperidone on psychomotor performance relevant to driving ability in schizophrenic patients compared to healthy controls. J Psychiatr Res 2005;39:101–8.
26. Vellignan DI, Bow-Thomas C, Mahurin RK, Miller AL, et al. Do specific neurocognitive deficits predict specific domains of community function in schizophrenia? J Nerv Ment Dis 2000;188:518–24.
27. Waller JA. Chronic medical conditions and traffic safety: a review of the California experience. N Engl J Med 1965;273:1413–20.
Dr. rer. nat. Dipl.-Psych. Alexander Brunnauer, Dipl.-Psych. Elisabeth Geiger, Prof. Dr. med. Dipl.-Psych. Gerd Laux, Bezirksklinikum Gabersee, Fachkrankenhaus für Psychiatrie, Psychotherapie, Psychosomatische Medizin und Neurologie, 83512 Wasserburg a. Inn, E-Mail: Brunnauer.Alexander@gabersee.de Prof. Dr. med. Michael Soyka, Prof. Dr. med. Hans-Jürgen Möller, Psychiatrische Universitätsklinik, Ludwig-Maximilians-Universität, 80336 München Dr. rer. nat. Thomas Glaser, Bayer Vital GmbH, Pharma Medizin, 51368 Leverkusen
Psychopharmakotherapie 2005; 12(03)
